2. 吉林省现代中药工程研究中心有限公司, 吉林 长春 130012
2. Jilin Modern Chinese Medicine Engineering and Research Center Co., Ltd., Changchun 130012, China
五味子糖浆为中国药品标准中药成方制剂第二册收载的品种,是由单味五味子经渗漉制成流浸膏后,加入到单糖浆中而制成的糖浆剂,具有收敛固涩、益气生津、补肾宁心之效[1-2]。临床上用于治疗久咳虚喘、梦遗滑精、遗尿尿频、久泻不止、自汗、盗汗、津伤口渴、气短脉虚、内热消渴、心悸失眠等症[3]。
五味子Schisandrae Fructus(SF)为木兰科(Magnoliaceae)五味子属Schisandra Michx.植物五味子Schisandra chinensis (Turcz.) Baill.的干燥成熟果实,习称北五味子。其有效成分主要包括五味子醇甲、五味子酯甲、五味子甲素、五味子乙素等成分,具有广泛的药理作用[4-8]。北五味子主要产于东北三省及内蒙古地区,由于野生资源逐年下降,产区已进行人工种植[9]。目前市售的五味子有野五味子、北五味子和南五味子等。而北五味子的药用价值高于其他品种,加之外观相似,价格悬殊等,市场上以次充好现象十分普遍。有研究表明,东北地区的辽宁、吉林、黑龙江3省的五味子药材中木脂素成分的量均有较大差异,且很多市售五味子药材中五味子醇甲的量均低于《中国药典》2015年版质量标准[10-11]。不同品质的五味子药材生产出的糖浆制品,品质也各不相同,因此建立原料药材和成品的质控方法势在必行。
中药指纹图谱是一种多指标的质控方法,可比较全面地反映制剂中的化学成分信息,现已日益成为国内外广泛采用的中药质量评价模式[12-15]。本研究采用HPLC指纹图谱法对长白山地区的五味子药材、五味子糖浆中间体及成品进行质控研究,并进行相关性分析,从药材-中间体-成品全过程控制五味子糖浆的产品质量,完善该制剂的质量评价体系,以保证该药的质量和临床疗效稳定。
1 仪器与材料Agilent 1200型液相色谱仪及紫外检测器,美国Agilent公司;Uitimate 3000型液相色谱仪及紫外检测器,美国戴安公司;Mettler ME204E双量程电子天平,梅特勒-托利多仪器有限公司。
对照品五味子醇甲(批号110857-201412,质量分数99.46%)、五味子酯甲(批号111529-200604,质量分数95.3%)、五味子甲素(批号110764-201312,质量分数99.6%)、五味子乙素(批号110765-201311,质量分数98.8%)均购自中国食品药品检定研究院。乙腈为美国Fisher,水为娃哈哈纯净水。
10批长白山地区五味子药材编号为Y1~Y10,由吉林农业大学中药材学院张连学教授鉴定为木兰科五味子属植物五味子Schisandra chinensis (Turcz.) Baill.的干燥成熟果实;由10批药材分别制备成对应的五味子糖浆中间体及成品,所得10批五味子糖浆中间体及成品编号及批号见表 1,均由吉林天力泰药业有限公司提供。
|
|
表 1 样品编号及批号 Table 1 Sample number and batch number |
2 方法与结果 2.1 色谱条件
色谱柱为ACE5-C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-水,梯度洗脱:0~20 min,40%~55%乙腈;20~35 min,55%~60%乙腈;35~44 min,60%~65%乙腈;44~50 min,65%~75%乙腈;50~60 min,75%乙腈;柱温30 ℃;检测波长218 nm;体积流量1.0 mL/min;进样量10 μL。
2.2 对照品溶液的制备精密称定五味子醇甲、五味子酯甲、五味子甲素、五味子乙素的对照品适量,加甲醇制成含五味子醇甲57.68 μg/mL、五味子酯甲58.72 μg/mL、五味子甲素55.36 μg/mL、五味子乙素56.08 μg/mL的混合对照品溶液。
2.3 供试品溶液的制备 2.3.1 五味子药材溶液的制备分别精密称取长白山产地不同批次药材粉末(过3号筛)0.5 g于具塞锥形瓶中,精密加入25 mL甲醇,称质量,超声提取30 min,放置室温,补足减失质量,滤过,取续滤液,即得。
2.3.2 五味子糖浆成品及中间体供试品溶液的制备分别精密量取不同批次五味子糖浆成品10 mL、中间体5 mL于分液漏斗中,成品精密加入10 mL水,中间体精密加入5 mL水,混匀,用正己烷振摇3次,成品每次20 mL,中间体每次10 mL,合并正己烷液,回收溶剂至干,残渣用甲醇使溶解,转移至10 mL量瓶中,定容至刻度,摇匀,滤过,取续滤液,即得。
2.4 方法学考察 2.4.1 精密度试验取Y3样品,按“2.3.1”项下方法制备,连续进样6次,记录色谱图。计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰的相对保留时间的RSD在1%以内,相对峰面积的RSD在5%以内,表明仪器精密度良好。
2.4.2 重复性试验取Y3样品,按“2.3.1”项下方法制备供试品溶液6份,记录色谱图。计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰的相对保留时间的RSD在1%以内,相对峰面积的RSD在5%以内,表明仪器方法重复性良好。
2.4.3 稳定性试验取Y3样品1份,按“2.3.1”项下方法制备,分别在0、2、4、6、8、10、12、16、20、24 h按“2.1”项下色谱条件测定,记录色谱图。计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰的相对保留时间的RSD在1%以内,相对峰面积的RSD在5%以内,表明供试品溶液在24 h内稳定。
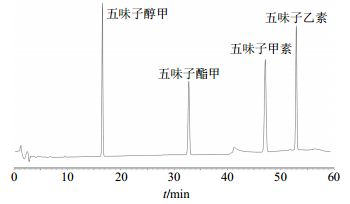
2.5 指纹图谱的研究 2.5.1 参照峰的选择[16-17]按照“2.1”项色谱方法分离混合对照品,由图 1可见五味子醇甲、五味子酯甲、五味子甲素、五味子乙素的峰型分离效果较好,作为五味子糖浆原药材、中间体、成品研究的参照峰。
|
图 1 混合对照品的HPLC色谱图 Fig.1 HPLC of mixed reference substances |
2.5.2 五味子药材指纹图谱的建立
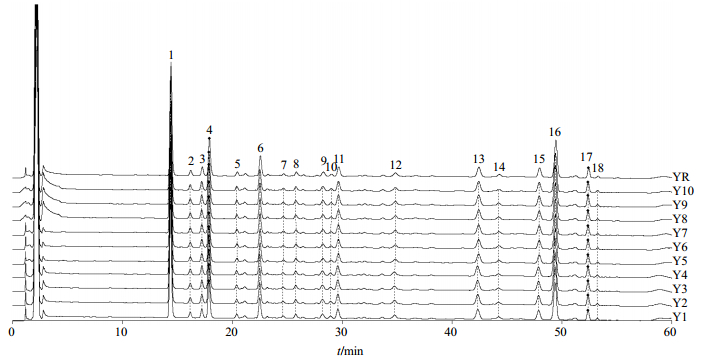
取10批长白山不同产地的药材按“2.3.1”项下方法制备供试品溶液。精密吸取5 μL,注入液相色谱仪,按“2.1”项下色谱条件进行测定,得到10批次五味子药材的HPLC指纹图谱。由图 2可知,共确定18个色谱峰为五味子药材的指纹图谱共有峰,且共有峰的峰面积占总峰面积的90%以上。通过与混合对照品对比分析,确定1号峰为五味子醇甲,11号峰为五味子酯甲,13号峰为五味子甲素,16号峰为五味子乙素。
|
1-五味子醇甲11-五味子酯甲13-五味子甲素16-五味子乙素,下同 1-schisandrin 11-schisantherin A 13-deoxyschizandrin 16-schisandrin B, same as below 图 2 五味子药材指纹图谱及对照指纹图谱(YR) Fig.2 Fingerprint and control fingerprint (YR) of SF |
采用国家药典委员会“中药色谱指纹图谱相似度评价系统(2004A)”对所得的HPLC指纹图谱全谱进行相似度分析,其相似度均达到0.998以上(表 2)。说明长白山产地五味子药材质量及成分稳定,以其作为制备五味子糖浆制剂的原料,可以保证制剂的药效稳定性。
|
|
表 2 五味子药材指纹图谱相似度 Table 2 Similarity of fingerprints of SF |
2.5.3 五味子糖浆成品及中间体指纹图谱的建立
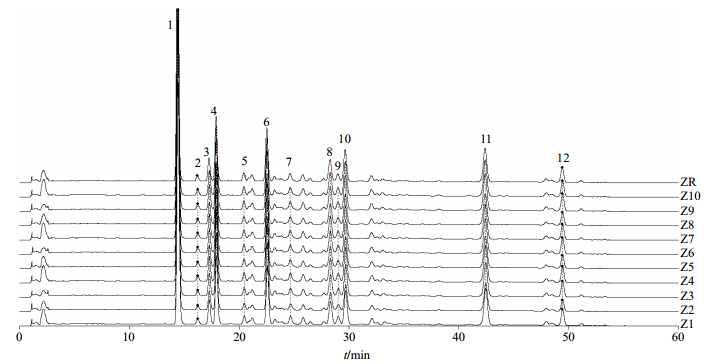
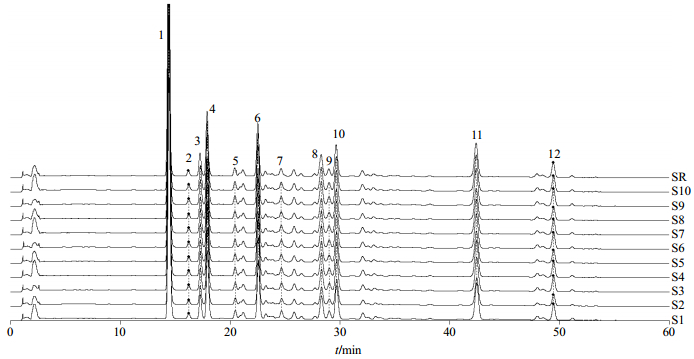
分别取10批成品及中间体按“2.3.2”项下制备供试品溶液。分别精密吸取成品10 μL,中间体5 μL注入液相色谱仪,按“2.1”项下色谱条件进行测定,得到10批次五味子糖浆成品和中间体的HPLC指纹图谱。由图 3、4可知,五味子糖浆中间体及成品分别含有12个共有色谱峰,且共有峰的峰面积占总峰面积的90%以上。通过与混合对照品对比分析,确定五味子糖浆中间体和成品的指纹图谱中的1号峰为五味子醇甲、9号峰为五味子酯甲、11号峰为五味子甲素、12号峰为五味子乙素。
|
图 3 五味子糖浆中间体指纹图谱及对照指纹图谱(ZR) Fig.3 Fingerprint and control fingerprint (ZR) of intermediates of Wuweizi Syrup |
|
图 4 五味子糖浆成品指纹图谱及对照指纹图谱(SR) Fig.4 Fingerprint and control fingerprint (SR) of finished products of Wuweizi Syrup |
采用国家药典委员会“中药色谱指纹图谱相似度评价系统(2004A)”对所得的HPLC指纹图谱全谱进行相似度分析,其中间体及成品的相似度均在0.998以上(表 3、4),相对保留时间及相对峰面积的RSD差异不明显,说明不同批次的中间体及成品的化学成分具有较好的一致性及稳定性。
|
|
表 3 五味子糖浆中间体指纹图谱相似度 Table 3 Similarity of fingerprints of intermediate of Wuweizi Syrup |
|
|
表 4 五味子糖浆成品指纹图谱相似度 Table 4 Similarity of fingerprints of finished products of Wuweizi Syrup |
2.6 五味子糖浆原药材-中间体-成品指纹图谱的相关性分析 2.6.1 色谱条件
同“2.1”项下色谱条件。混合对照品溶液色谱图见图 1。
2.6.2 对照品溶液的制备精密称取五味子醇甲、五味子酯甲、五味子甲素、五味子乙素各7 mg,置量瓶中,各加甲醇定容至25 mL。制成质量浓度均为0.28 mg/mL的对照品母液。再各取5 mL与量瓶中,加甲醇定容至25 mL,稀释成质量浓度为0.056 mg/mL的混合对照品溶液,即得。
2.6.3 供试品溶液的制备同“2.3”项下制备方法。
2.6.4 线性关系的考察精密量取2、4、6、8、10 mL混合对照品于10 mL量瓶中,加甲醇至刻度,分别吸取5 μL,注入液相色谱仪,测定,以进样质量浓度为横坐标(X),峰面积积分值为纵坐标(Y)绘制标准曲线,得回归方程分别为五味子醇甲Y=530.66 X-0.032 8,R2=0.999 9;五味子酯甲Y=380.29 X+0.038 6,R2=0.999 5;五味子甲素Y=597.91 X-0.442 5,R2=0.998 7;五味子乙素Y=547.22 X+0.015 6,R2=0.999 5。结果五味子醇甲、五味子酯甲、五味子甲素、五味子乙素分别在5.768~57.68、5.872~58.72、5.536~55.36、5.608~56.08 μg/mL呈良好的线性关系。
2.6.5 精密度试验取同一供试品(Y3)溶液连续进样6次,以峰面积计算各指标成分的RSD,分别为五味子醇甲0.73%、五味子酯甲0.79%、五味子甲素1.03%、五味子乙素1.11%。
2.6.6 稳定性试验取同一供试品(Y3)溶液,分别于0、2、4、6、10、18、24 h注入液相色谱仪中,以峰面积计算各指标成分的RSD,分别为五味子醇甲0.53%、五味子酯甲1.09%、五味子甲素0.91%、五味子乙素0.75%,结果表明供试品溶液中各成分在24 h稳定性良好。
2.6.7 重复性试验取同一供试品(Y3)0.5 g,精密称量,按照“2.3”项下方法,平行制备6份,以峰面积计算各指标成分的RSD,分别为五味子醇甲0.31%、五味子酯甲0.79%、五味子甲素0.67%、五味子乙素1.01%,结果表明本方法重复性良好。
2.6.8 回收率试验取同一供试品(Y3)0.25 g,精密称定6份,分别置于具塞锥形瓶中,精密量取“2.6.2”项下混合对照品溶液5 mL置于以上6份样品中,再精密加入甲醇20 mL,摇匀,称质量,超声提取30 min,放置室温,补足减失质量,滤过,取续滤液5 μL注入液相色谱中,测定计算回收率。结果五味子醇甲、五味子酯甲、五味子甲素、五味子乙素回收率分别为99.78%、101.34%、98.17%、102.96%,RSD分别为0.43%、0.97%、1.09%、1.02%。
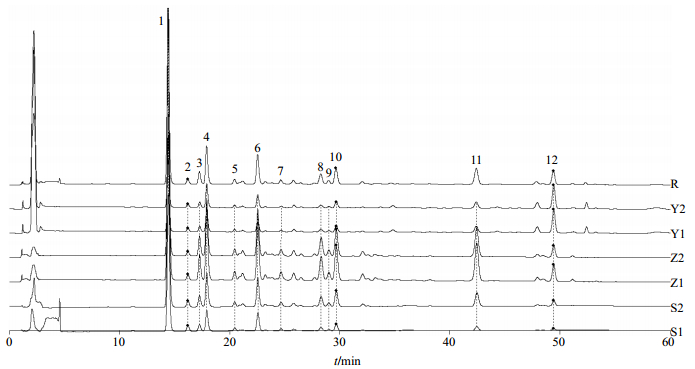
2.6.9 相似度分析分别各取2批药材(Y1、Y2)、中间体(Z1、Z2)及成品(S1、S2)按照拟定的方法绘制HPLC图谱,并采用相似度评价软件评价三者图谱的相似度。由图 5可知,药材、中间体、成品共有12个共有峰,对比参照峰图谱确定1号峰为五味子醇甲、9号峰为五味子酯甲、11号峰为五味子甲素、12号峰为五味子乙素。通过相似度研究分析(表 5),药材与中间体及成品的相似度在0.88~0.92,相关性较好。由此得证药材中主要成分均在
|
图 5 药材-中间体-成品图谱和对照指纹图谱(R) Fig.5 Fingerprint and control fingerprint (R) of SF-intermediate-finshed product |
|
|
表 5 药材-中间体-成品指纹图谱相似度 Table 5 Similarity of fingerprints of SF-intermediate-finished products |
中间体及成品中体现,同时中间体与成品的特征峰在药材中也找到追溯。
2.6.10 主要成分定量变化分析由表 6可见,中间体及成品中五味子醇甲、五味子酯甲、五味子甲素、五味子乙素的量基本稳定,但相对于原料药材其量相对较小,原因可能与该制剂提取工艺有关。因此进一步改进和优化提取生产工艺,使药材在提取工艺中能提取出更多主要成分,是今后研究的重点。
|
|
表 6 主要成分定量结果分析 Table 6 Principal component analysis |
3 讨论
本研究前期曾考察了Ultimmate XB-C18色谱柱(250 mm×4.6 mm,5 μm)、TopsilTM-C18色谱柱(250 mm×4.6 mm,5 μm)和ACE5-C18色谱柱(250mm×4.6 mm,5 μm),甲醇-水流动相系统、乙腈-水流动相,分析药材、中间体、成品三者的液相色谱图的分离效果,最终选定ACE5-C18柱、乙腈-水为流动相系统的分离度好,稳定性好。同时,本研究考察了正己烷、氯仿、醋酸乙酯萃取成品及中间体的提取效果,甲醇和乙醇的超声、回流对药材的提取效果,比较分析认为用正己烷萃取3次得到的中间体及成品的色谱峰面积、甲醇超声提取药材得到的样品的液相色谱峰的峰面积可以达到峰值。通过一系列的前期实验最终确定选用ACE5-C18柱、乙腈-水流动相、正己烷3次萃取中间体及成品、甲醇超声提取药材的分析条件能使五味子糖浆药材、中间体、成品的液相色谱峰的分离效果达到最佳,便于建立指纹图谱方法。
本研究首次建立了五味子糖浆从药材至中间体、成品的全方位的指纹图谱,确定了长白山地区的五味子药材相似度较高。由其生产的糖浆中间体和成品的相似度较高、稳定性良好,三者的相关性好,为生产出安全、药效稳定的五味子糖浆制品提供了科学依据,为企业大生产建立质量标准提供数据支撑。
| [1] | 中华人民共和国卫生部药品标准中药成方制剂(第二册)[S].1998. |
| [2] | 中国药典[S].一部.2015. |
| [3] | 张朝民, 黄海欣, 张玉洁. 五味子糖浆质量研究标准[J]. 中国实验方剂学杂志 , 2005, 11 (6) :18–19. |
| [4] | 李伟, 刘亚丽, 宋永贵, 等. UPLC-Q-TOF-MSE结合OPLS-DA模式快速鉴定南、北五味子化学成分与识别差异标志物[J]. 中草药 , 2015, 46 (15) :2212–2218. |
| [5] | 王丽薇. 北五味子的化学成分[J]. 杭州师范学院学报:自然科学版 , 2007, 6 (5) :363–365. |
| [6] | 高慧, 佟鑫, 裴启洋, 等. 五味子"生熟异用"之补肾阳作用[J]. 中草药 , 2014, 45 (13) :1889–1893. |
| [7] | Tran M H, Min K N, Byung S M, et al. Acetylcholinesterase inibitory effect of lignans isolated from Schizandra chinensis[J]. Arch Pharm Res , 2007, 30 (6) :685–686. DOI:10.1007/BF02977628 |
| [8] | 史琳, 王志成, 冯叙桥. 五味子化学成分及药理作用的研究进展[J]. 药物评价研究 , 2011, 34 (3) :208–212. |
| [9] | 胥克章. 北五味子GAP基地的栽培及管理技术[J]. 农业与技术 , 2006, 26 (2) :126–128. |
| [10] | Zhu M, Chen X S, Wang K X. Variation of the lignan content of Schisandra chinensis (Turcz.) Baill.and Schisandra sphenanthera Rehd.et Wils[J]. Chromatographia , 2007, 66 (1) :125–127. |
| [11] | Deng X X, Chen X H, Cheng W M, et al. Simultaneous LC-MS Quantification of 15 lignans in Schisandra chinensis (Turcz.) Baill.Fruit[J]. Chromatographia , 2008, 67 (7) :559–566. |
| [12] | 苏瑞, 金敏婷, 许鑫, 等. 黑龙江产万寿菊花醇提物的指纹图谱研究[J]. 中草药 , 2012, 43 (7) :1324–1327. |
| [13] | 秦昆明, 方前波, 蔡宝昌, 等. 指纹图谱技术在方剂现代研究中的应用现状[J]. 世界科学技术-中医药现代化 , 2009, 11 (2) :287–293. |
| [14] | 于敏, 王雪, 焦安妮, 等. 五味子咀嚼片的HPLC-DAD指纹图谱研究[J]. 中草药 , 2015, 46 (16) :2413–2416. |
| [15] | 李倩, 罗祖良, 杨小丽. 中药质量控制方法研究述评[J]. 中医学报 , 2012, 27 (4) :448–451. |
| [16] | 谭春梅, 黄琴伟, 张文婷, 等. 五味子和南五味子的HPLC指纹图谱研究[J]. 中国现代应用药学杂志 , 2008, 25 (6) :514–517. |
| [17] | 李晓亮, 易进海, 刘云华, 等. 南五味子、五味子HPLC指纹图谱研究和木脂素成分测定[J]. 中成药 , 2011, 33 (6) :920–924. |
 2016, Vol. 47
2016, Vol. 47


