2. 北京市食品环境与健康工程技术研究中心, 北京 100081 ;
3. 陕西师范大学生命科学学院, 陕西 西安 710091
2. Beijing Engineering Research Center of Food Environment and Public Health, Minzu University of China, Beijing 100081, China ;
3. College of Life Science, Shaanxi Normal University, Xi'an 710091, China
小花八角Illicium micranthum Dunn是木兰科(Magnoliaceae)八角属Illicium Linn. 植物,为多年生灌木或小乔木,广泛分布于我国西南民族地区[1]。其根、树皮、叶和果实可入药;树皮外用可治风湿骨痛、跌打损伤;其果实入药有祛风解表、行气止痛、止吐泻之效,可治感冒风寒、呕吐腹泻、胸腹气痛等症。小花八角用作傣药,有毒,药用时需注意用量;煮水可作杀虫农药[1-3]。韭菜迟眼蕈蚊Bradysia odoriphaga Yang and Zhang,俗称韭蛆,以7科超过30种植物为食,是影响我国北方韭菜产量的主要害虫[4]。韭蛆的生活习性导致其防治管理方法主要是运用一类化学合成农药进行灌根处理,该方法给环境带来农药残留等影响。因此,发展新型、高效、环境友好型的杀虫剂十分必要[5-6]。本课题组前期已从小花八角果实和枝叶中有抗氧化活性的提取物中分离得到了23个化合物[7-8]。为进一步深入研究该植物的化学成分,寻找新型杀虫农药先导化合物,本实验采用现代色谱分离技术,对其枝叶进行了系统化学成分研究,从甲醇提取物的醋酸乙酯萃取部位中分离得到了5个化合物,分别鉴定为 (-)-(1R*,4S*)-1-羟甲基-2-烯基- 4-异丙基-1,4-环己二醇 [(-)-(1R,4S)-1- (hydroxymethyl)-4-isopropylcyclohex-2-ene-1,4-diol,1]、(1R,2R,4R)-1-甲基-4-异丙基-1,2,4-环己三醇 [(1R,2R,4R)-1-methyl-4-(1-methylethyl)-1,2,4-cyclohexanetriol,2]、4-羟基胡椒酮(4-hydroxypiperitone,3)、乳香醇C(olibanumol C,4)、α,α-二甲基-4-羟甲基苯甲醇(α,α-dimethyl-4-hydroxymethylbenzyl alcohol,5)。其中,化合物1为新化合物,命名为小花八角素A,化合物2~5为首次从该植物中分离得到。对化合物2进行了韭菜迟眼蕈蚊幼虫的毒杀活性测试,实验结果显示其作用48 h后的LD50值为30.4 mg/L,72 h后的LD50值为22.5 mg/L。
1 仪器与材料DRX 500、AVANCE 600核磁共振波谱仪(德国布鲁克公司);BT224S电子天平(北京赛多利斯仪器系统有限公司);Anton Paar MCP 200 Analytical Automatic Polarimeter旋光仪(奥地利安东帕公司);Nicolet IS5 FT-IR(KBr)红外光谱仪(美国赛默飞世尔科技公司);Agilent 6890N-5975质谱仪(美国安捷伦科技有限公司);Agilent HPLC-QTOF/MS 6520高分辨质谱仪(美国安捷伦科技有限公司);薄层色谱硅胶(GF254)和柱色谱硅胶(100~200目、200~300目)均购自青岛海洋化工有限公司;Sephadex LH-20为Pharmacia公司生产;氘代试剂为北京大学大北公司产品;水为蒸馏水;其他试剂均为分析纯,北京化工厂生产。
小花八角枝叶于2011年10月采于云南省澜沧县,由中国科学院昆明植物研究所李锡文研究员鉴定为小花八角Illicium micranthum Dunn的枝叶,标本(201110103)保存于中央民族大学生命与环境科学学院。
2 提取与分离干燥的小花八角枝叶500.0 g,粉碎,甲醇室温提取3次,每次7 d,合并提取液,减压浓缩,得棕色的总浸膏50.0 g。将总浸膏加入适量蒸馏水混悬,依次用石油醚、醋酸乙酯萃取,浓缩,得到相应的萃取物。醋酸乙酯萃取物15.0 g,拌以等量硅胶(100~200目),经硅胶柱色谱(200~300目),以石油醚-丙酮(30∶1→0∶1)为洗脱剂梯度洗脱,得Fr. 1~9。Fr. 5(石油醚-丙酮5∶1)经反复硅胶柱色谱并结合Sephadex LH-20(氯仿-甲醇1∶1)凝胶柱色谱得到化合物2(5.0 mg)、3(2.0 mg)。Fr. 6(石油醚-丙酮3∶1)经反复硅胶柱色谱并结合Sephadex LH-20凝胶柱色谱(氯仿-甲醇1∶1)得到化合物1(1.5 mg)、4(2.5 mg)、5(1.5 mg)。
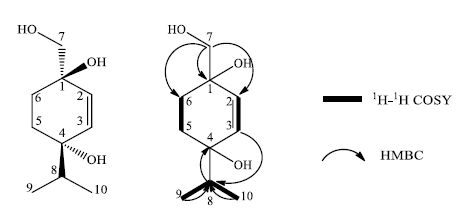
3 结构鉴定化合物1:无色油状物,薄层展开后三氯化锑显色剂显淡黄色。HR-ESI-MS m/z: 209.114 7 [M+Na]+(计算值209.114 8)给出分子式C10H18O3 (c 0.1,MeOH)。IR谱提示含有羟基(3 384 cm-1)和双键(1 666 cm-1)。1H-NMR (600 MHz,CD3COCD3) 谱(表 1)中可见2个双键氢信号δH 5.70 (1H,d,J = 12.0 Hz,H-2)、5.66 (1H,d,J = 12.0 Hz,H-3);1对连氧亚甲基信号δH 3.40 (1H,dd,J = 5.4,10.8 Hz,H-7a)、3.34 (1H,dd,J = 6.0,10.8 H z,H-7b) 提示存在1个羟甲基;1组异丙基信号δH 1.69 (1H,m,H-8)、0.94 (3H,d,J = 7.2 Hz,H-10)、0.88 (3H,d,J = 6.6 Hz,H-9)。1H-1H COSY谱中,有3组相关信号(图 1)。
|
|
表 1 化合物1的1H-NMR和13C-NMR数据 Table 1 1H-NMR and 13C-NMR data for compound 1 |
|
图 1 化合物1的结构及主要1H-1H COSY和HMBC相关 Fig.1 Structure and key 1H-1H COSY and HMBC correlations of compound 1 |
13C-NMR (150 MHz,CD3COCD3) 谱(表 1)和DEPT谱显示化合物1含有10个碳信号,包括1组双键碳信号δC 136.1 (C-3)、132.1 (C-2);1个连氧亚甲基碳信号δC 70.5 (C-7);1组异丙基碳信号δC38.3 (C-8)、18.0 (C-9)、17.0 (C-10);2个连氧季碳信号δC 71.8 (C-4)、69.9 (C-1)。结合一维NMR信息,初步推断可能是1个薄荷烷型单萜。HMBC谱中H-7a (δH 3.40)、H-7b (δH 3.34) 与C-1 (δC 69.9) 远程相关,H-8 (δH 1.69) 与C-4 (δC 71.8) 远程相关,确定连氧亚甲基连在C-1上,异丙基连在C-4上。通过HSQC和HMBC图谱,对化合物1的NMR数据进行了归属,确证了其平面结构。查阅文献发现化合物1与(-)-(1R*,4S*)-1,4-dihydroxy-p-menth-2- ene[9]的1H-NMR和13C-NMR数据非常相似,二者差异仅在于化合物1中7位上的1个H被-OH取代,而且NOESY谱中有H-7a与H-5a、H-2相关信号,H-3与H-8相关信号,提示C-1和C-4的羟基应该处于相反的方向,这种伸展方向与文献化合物的相对构型一致。进一步对比比旋光度数值,发现二者均让偏振光左旋为负值。综上推测化合物1与已知化合物的相对构型一致,确定其结构式为 (-)-(1R,4S)-1-羟甲基-2-烯基-4-异丙基-1,4-环己二醇,经SciFinder检索核实,为1个未见报道的薄荷烷单萜,命名为小花八角素A。
化合物2:无色油状物,C10H20O3,ESI-MS m/z: 189.1 [M+H]+,薄层展开后三氯化锑显色剂显淡黄色。1H-NMR (600 MHz,MeOD) δ: 3.50 (1H,brs,H-2),1.94 (1H,m,H-3b),1.90 (1H,m,H-6b),1.78 (1H,m,H-5b),1.59 (1H,m,H-3a),1.56 (1H,m,H-8),1.44 (1H,m,H-5a),1.39 (1H,m,H-6a),1.23 (3H,s,
7-CH3),0.91 (3H,brs,10-CH3),0.90 (3H,brs,9-CH3);13C-NMR (150 MHz,MeOD) δ: 75.79 (C-4),75.74 (C-2),72.09 (C-1),39.05 (C-8),34.86 (C-3),30.42 (C-6),30.32 (C-5),27.13 (C-7),17.27 (C-10),17.18 (C-9)。以上数据与文献报道一致[10],故鉴定化合物2为 (1R,2R,4R)-1-甲基-4-异丙基-1,2,4-环己三醇。
化合物3:无色油状物,C10H16O2,ESI-MS m/z: 169.1 [M+H]+,薄层展开后三氯化锑显色剂显淡黄色。1H-NMR (600 MHz,CD3COCD3) δ: 5.80 (1H,s,H-2),2.35 (1H,m,H-4b),2.28 (1H,m,H-4a),2.01 (3H,s,10-CH3),1.75 (1H,m,H-7),1.60 (1H,m,H-5b),1.36 (1H,m,H-5a),0.85 (3H,d,J = 6.6 Hz,9-CH3),0.74 (3H,d,J = 6.6 Hz,8-CH3);13C-NMR (150 MHz,CD3COCD3) δ: 201.63 (C-1),161.58 (C-3),122.56 (C-2),76.60 (C-6),32.94 (C-4),31.09 (C-5),30.41 (C-7),23.32 (C-10),15.95 (C-9),15.56 (C-8)。以上数据与文献报道一致[11],故鉴定化合物3为4-羟基胡椒酮。
化合物4:无色油状物,C10H18O2,ESI-MS m/z: 171.1 [M+H]+,薄层展开后三氯化锑显色剂显淡黄色。1H-NMR (600 MHz,CD3COCD3) δ: 5.51 (1H,s,H-2),3.91 (2H,d,J = 6.6 Hz,H-7),2.18 (1H,m,H-6b),2.14 (1H,m,H-3b),1.97 (1H,m,H-6a),1.91 (1H,m,H-3a),1.65 (1H,m,H-5b),1.64 (1H,m,H-8),1.50 (1H,m,H-5a),0.93 (3H,d,J = 7.2 Hz,10-CH3),0.91 (3H,d,J = 7.2 Hz,9-CH3);13C-NMR (150 MHz,CD3COCD3) δ: 138.55 (C-1),119.64 (C-2),71.75 (C-4),66.71 (C-7),37.56 (C-8),35.31 (C-3),31.87 (C-5),23.48 (C-6),17.25 (C-9),17.19 (C-10)。以上数据与文献报道一致[12],故鉴定化合物4为乳香醇C。
化合物5:无色油状物,C10H14O2,ESI-MS m/z: 167.1 [M+H]+,薄层展开后三氯化锑显色剂显淡黄色。1H-NMR (600 MHz,CD3COCD3) δ: 7.48 (2H,d,J = 8.4 Hz,H-2,6),7.29 (2H,d,J = 7.8 Hz,H-3,5),4.59 (2H,s,H-7),1.48 (6H,s,9,10-CH3);13C-NMR (150 MHz,CD3COCD3) δ: 150.01 (C-1),141.08 (C-4),127.07 (C-3,5),125.26 (C-2,6),71.95 (C-8),64.61 (C-7),32.49 (C-9,10)。以上数据与文献报道一致[13],故鉴定化合物5为α,α-二甲基-4-羟甲基苯甲醇。
4 杀虫活性研究杀虫活性参照文献报道[14]采用触杀胃毒联合毒力方法,测试化合物2对4龄韭菜迟眼蕈蚊幼虫的半数致死量(LD50)。
结果表明,将化合物2质量浓度设定在100.0 mg/L,韭菜迟眼蕈蚊幼虫48 h后死亡率大于50%。表 2中显示化合物2对韭菜迟眼蕈蚊幼虫有明显的毒杀活性,且随质量浓度的升高而增强。运用SPSS 19.0软件上的Probit模型对化合物毒力活性测定数据进行统计分析[15],化合物2在48 h后的LD50值为30.4 mg/L;72 h后的LD50值为22.5 mg/L。
|
|
表 2 化合物2对4龄韭菜迟眼蕈蚊幼虫的毒杀活性 Table 2 Insecticidal activities data of compound 2 on four age-stage larvae of B. odoriphaga |
天然薄荷烷型单萜是广泛存在于药用植物的一类功效化学成分,但测试从小花八角中所得单萜的杀虫活性尚属首次报道。上述测试结果显示,单萜化合物2对韭菜迟眼蕈蚊幼虫有毒杀活性,其48、72 h的LD50的测试结果值均小于50 mg/L,可能是小花八角中一种重要的、具有杀虫活性的化合物。
| [1] | 中国科学院昆明植物所. 云南植物志(第11卷)[M]. 北京: 科学出版社, 2000 . |
| [2] | 林祁. 八角属药用植物资源[J]. 中草药 , 2002, 33 (7) :654–657. |
| [3] | 贾敏如, 李星炜. 中国民族药志要[M]. 北京: 中国医药科技出版社, 2005 . |
| [4] | Li W X, Yang Y T, Xie W Q, et al. Effects of temperature on the age-stage, two-sex life table of Bradysia odoriphaga (Diptera:Sciaridae)[J]. J Econ Entomol , 2015, 108 (1) :126–134. DOI:10.1093/jee/tou011 |
| [5] | 张兴, 李广泽, 马志卿, 等. 试论"农药无公害化"[J]. 西北农林科技大学学报:自然科学版 , 2002, 30 (3) :130–137. |
| [6] | 何军, 马志卿, 张兴. 植物源农药概述[J]. 西北农林科技大学学报:自然科学版 , 2006, 34 (9) :79–86. |
| [7] | Liu T T, Wu H B, Wang W S, et al. A new illicinolide from leaves of Illicium micranthum Dunn[J]. Nat Prod Res , 2014, 28 (19) :1598–1601. DOI:10.1080/14786419.2014.927875 |
| [8] | 刘婷婷, 武海波, 陈艳艳, 等. 小花八角果实抗氧化活性部位化学成分研究[J]. 中草药 , 2014, 45 (5) :611–614. |
| [9] | Ahmed A. Highly oxygenated monoterpenes from Chenopodium ambrosioides[J]. J Nat Prod , 2000, 63 (7) :989–991. DOI:10.1021/np990376u |
| [10] | Nagamatsu R, Mitsuhashi S, Shigetomi K, et al. Cleavage of α-dicarbonyl compounds by terpene hydroperoxide[J]. Biosci Biotech Bioch , 2012, 76 (10) :1904–1908. DOI:10.1271/bbb.120378 |
| [11] | Pooter H L D, Buyck L F D, Schamp N M. The volatiles of Calamintha nepeta subsp[J]. Phytochemistry , 1986, 25 (3) :691–694. DOI:10.1016/0031-9422(86)88025-6 |
| [12] | Yoshikawa M, Morikawa T, Oominami H, et al. Absolute stereostructures of olibanumols A, B, C, H, I, and J from olibanum, gum-resin of Boswellia carterii, and inhibitors of nitric oxide production in lipopolysaccharide-activated mouse peritoneal macrophages[J]. Chem Pharm Bull , 2009, 57 (9) :957–964. DOI:10.1248/cpb.57.957 |
| [13] | Yun B S, Lee I K, Kim J P, et al. Lipid peroxidation inhibitory activity of some constituents isolated from the stem bark of Eucalyptus globulus[J]. Arch Pharm Res , 2000, 23 (2) :147–150. DOI:10.1007/BF02975503 |
| [14] | Zhang P, Liu F, Mu W, et al. Life table study of the effects of sublethal concentrations of thiamethoxam on Bradysia odoriphaga Yang and Zhang[J]. Pestic Biochem Phys , 2014, 111 :31–37. DOI:10.1016/j.pestbp.2014.04.003 |
| [15] | 武怀恒, 万鹏, 黄民松. 毒力回归计算方法及相应软件使用介绍[J]. 安徽农业科学 , 2014, 42 (27) :9335–9338. |
 2016, Vol. 47
2016, Vol. 47


