2. 天津药物研究院, 天津 300193
2. Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
野菊Chrysanthemum indicum L. 为菊科植物野菊花的干燥地上部分,我国除新疆外均有分布,全草入药,具有清热解毒的功效,可用于治疗流行性感冒、脑脊髓膜炎、毒蛇咬伤等[1]。其干燥头状花序是我国一种传统中药,现代药理学研究表明其具有抗炎[2]、免疫调节[3]、抗焦虑[4]、抑菌和抗病毒[5]等多种作用,毒理试验表明其主要入药部位野菊花是一种低毒且可长期安全使用的中药[6]。随着现代中药色谱分离方法不断发展,野菊的化学成分研究逐渐深入,主要含黄酮类、苯丙素类、萜类和多糖等化学成分。中药市场上以假乱真、以次充好的现象时有发生,且由于采收花期、产地、加工炮制方法等因素也会造成野菊质量参差不齐,而《中国药典》2010年版[7]中只收载野菊花,且单以蒙花苷作为薄层和定量测定指标,故有必要加强中药野菊的质量控制研究。基于此,本文对野菊的化学成分及质量评价研究进展进行综述,为野菊资源的进一步开发利用提供理论依据。 1 化学成分 1.1 黄酮类
黄酮类成分是野菊清热解毒的主要药效组分[8],人们对野菊化学成分的认识和研究也多以黄酮类为主,早在1942年相关学者就从野菊花中分离出黄酮类成分木犀黄酮苷[9]。Feng等[10]对野菊干燥头状花 序水提取物采用多种色谱方法进行分离,得到蒙花苷等13种物质;沈一形等[11]从野菊全草植物中分离得到木犀草素等4种物质。迄今为止,相关学者利用各种色谱分离技术和光谱鉴定技术从野菊中已分离鉴定出的黄酮类物质达40余种,主要有黄酮(1~30)、黄酮醇(31~37)、二氢黄酮(38~40)及查耳酮类物质(41),且多为C-7,3′,4′位取代。化合物结构式和名称见图 1和表 1。
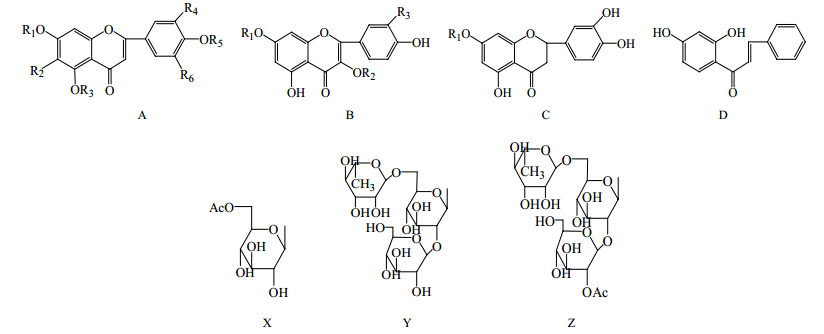 | 图 1 野菊中黄酮类化合物母核 (A、B、C)、取代基(X、Y、Z)及2′,4′-二羟基查耳酮 (D)的化学结构Fig.1 Nucleus structures (A,B,and C),substituents (X,Y,and Z) of flavonoids,and 2′,4′-dihydroxychalcone (D) in C. indicum |
| 表 1 野菊中的主要黄酮类化合物 Table 1 Main flavonoids in C. indicum |
酚酸类成分是野菊除黄酮类之外发挥清热解毒功效的另一主要药效组分[8],目前分离得到16种酚酸类物质。苯丙素类成分为野菊酚酸类物质的主要成分,野菊中含有以绿原酸和咖啡酰奎尼酸类成分为主的多种苯丙素类成分(42~52),化合物53~57为无苯丙素结构的酚酸类成分。孙昱等[21]首次从野菊花分离得到具有心血管活性的3,5-二咖啡酰奎尼酸等多种咖啡酰奎尼酸类化合物,苯丙素类及其他酚酸类成分名称及结构见表 2和图 2。
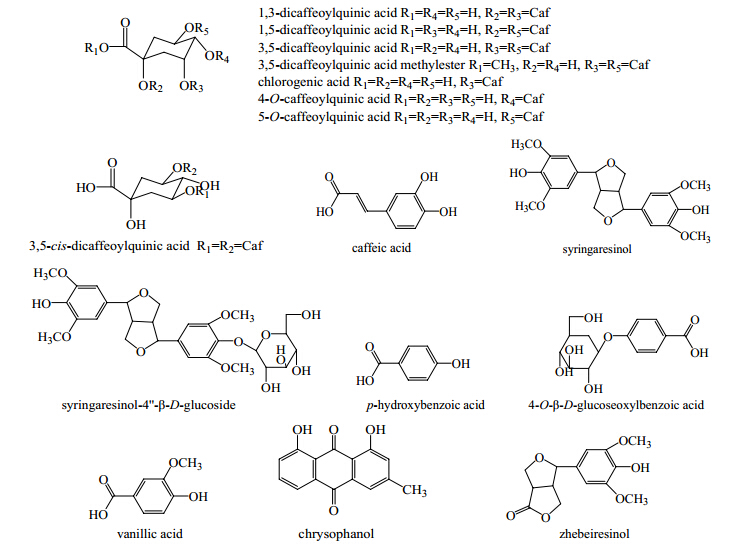 | 图 2 野菊中苯丙素类化合物及其他酚酸类的化学结构 (A、B、C)、取代基(X、Y、Z)及2′,4′-二羟基查耳酮 (D)的化学结构Fig.2 Chemical structures of phenylpropanoids and other phenolic acid compounds in C. indicum |
| 表 2 野菊中的苯丙素及酚酸类成分 Table 2 Phenylpropanoids and phenolic acid constituents from C. indicum |
野菊挥发油类成分主要为单萜、倍半萜及其含氧衍生物、三萜及脂肪族化合物等,其中倍半萜类成分较多,目前已从该植物中分离得到的倍半萜类化合物达40种(化合物58~97),其中非挥发性的萜类主要为野菊花内酯、野菊花醇、野菊花三醇等[25]。野菊花中的萜类成分具有保肝作用[26]。Yu等[27]从野菊花蕾的甲醇提取物中分离得到kikkanol A等3种新的桉烷型倍半萜类成分,药理实验显示其具有醛糖还原酶抑制活性;Zhou等[28]从野菊干燥头状花序的乙醇提取物中分离得到一种新的倍半萜二聚体disesquiterpenoid B和2种新的倍半萜类成分。野菊中的倍半萜类成分见表 3和图 3。
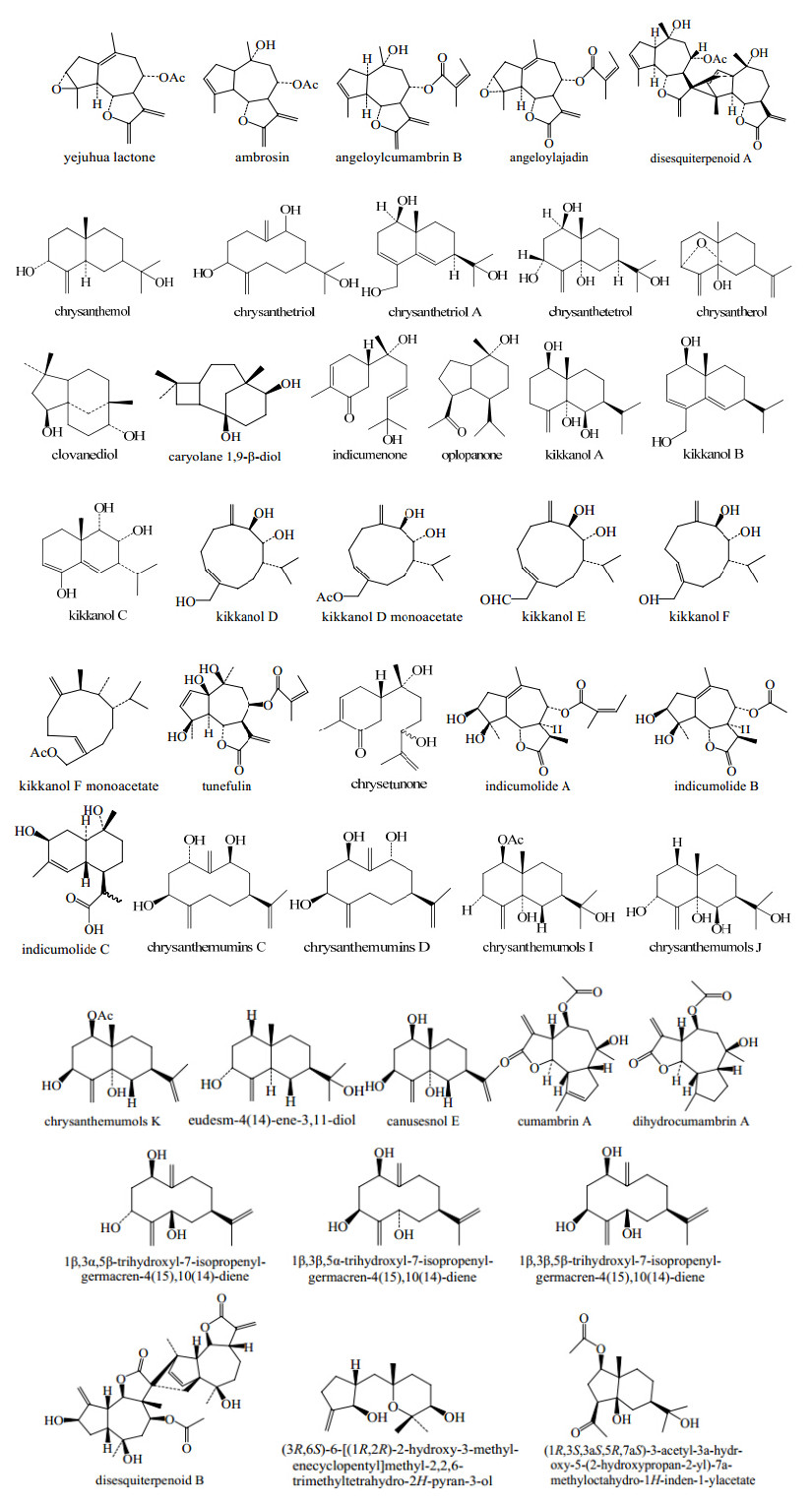 | 图 3 野菊中倍半萜类的化学结构Fig.3 Chemical structures of sesquiterpenes in C. indicum |
| 表 3 野菊中的倍半萜类成分 Table 3 Sesquiterpenes constituents from C. indicum |
野菊中还存在一类具有螺缩酮结构的特殊的烃类物质(98~100),相关学者从野菊花中分离得到2种成分具有2个五元环的物质[27],并从野菊花蕾中分离得到1种具有1个五元环和1个六元环的物质[42]。野菊花中的螺缩酮烃类成分见表 4和图 4。
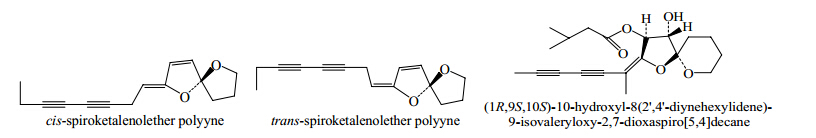 | 图 4 野菊中螺缩酮烃类化合物的化学结构Fig.4 Chemical structures of spiperone alkene in C. indicum |
| 表 4 野菊中的螺缩酮烃类成分 Table 4 Spiperone alkene constituents from C.indicum |
多糖也是野菊花主要活性成分之一,其可以清除活性氧自由基而表现出抗氧化作用[43]和抗肿瘤作用[44]。金红英等[45]采用水提醇沉法从野菊花中分离得到一种中性多糖,经结构鉴定是由D-甘露糖、D-葡萄糖、D-半乳糖等组成。此外,野菊花尚含有β-谷甾醇、β-胡萝卜素、色素、山嵛酸甘油酯、丁香脂素、鹅掌秋碱、鞣质、蛋白质、氨基酸、维生素A和B1以及铜、铁、锌、锡等人体必需微量元素。 2 质量评价研究
中药的质量评价是中医药研究的难点和热点,由于野菊化学成分复杂,传统的评价方法无法反映中药材质量的优劣,所以利用现代分析仪器,已成为现行中药质量控制的基本模式[46]。 2.1 毛细管电泳-电化学检测法(CE-ED)
毛细管电泳法(CE)法具有分离效率高、溶剂和样品消耗少等优点,是野菊黄酮类、有机酚酸类等成分定量评价中的一种可靠方法。电化学检测法 (ED)对电活性物质具有高的选择性和灵敏度。有学者以微碳圆盘电极为工作电极,建立了CE-ED测定野菊花中黄酮类化合物的方法,刺槐素、槲皮素、木樨草素3种黄酮类化合物在16 min内完全分离[47]。野菊中某些多酚类成分也可利用CE-ED法进行分析,程宏英等[48]同时分离并测定了野菊中木犀草素、槲皮素等5种多酚的量,所选体系对木犀草素和槲皮素有很好的分离效果。采用P/ACE MDQ毛细管电泳系统联合二极管阵列检测器(DAD),可建立野菊干燥头状花序中蒙花苷、山柰酚等9种黄酮类化合物的毛细管电泳分析方法,实验结果表明该法测定野菊花中黄酮类化合物简便、准确,分离效率高[49]。 2.2 红外吸收光谱法
红外吸收光谱法突出的特点是具有高度的特征性,不同产地野菊花由于其所含黄酮类成分的种类 及其量的不同,在二阶导数光谱及二维相关红外光谱中均存在显著差异[50]。采用傅里叶变换红外光谱技术对野菊花不同炮制品进行研究,结果表明红花不同炮制品的红外光谱有着许多共同的特征,而 由于各种成分量的不同也导致其红外光谱存在差异[51]。刘承萍[52]运用傅里叶变换红外光谱仪扫描,结果显示二阶导数图谱能较好地区分直观分析上较为相似的野菊花红外吸收光谱。利用红外光谱的宏观指纹特性,对野菊花不同溶剂提取物的红外光谱图和二阶导数红外光谱图进行整体分析可知,野菊花石油醚提取物主含长链脂肪酸(酯)、不饱和酮以及小分子萜类等低极性化合物,醋酸乙酯提取物主 含萜类和黄酮类化合物,无水乙醇提取物主含黄酮及黄酮苷类化合物,95%乙醇提取物主含黄酮苷类化合物,去离子水提取物主含多糖及鞣质类等大极性成分[53]。 2.3 高效液相色谱法(HPLC)
HPLC以分离效能高、分析速度快、选择性高等优势,且操作简单、重复性好、稳定可靠,已成为中药定性或定量等质量评价领域中的主流技术[54]。此外,制备型高效液相色谱(pHPLC)和超高效液相色谱法(UPLC)在野菊质量评价中也有应用。 2.3.1 HPLC定量测定研究
《中国药典》2010年版中野菊花项下是以蒙花苷作为其质量控制指标[7],但目前市售的野菊花药材多是炒制后晒干制成,其中蒙花苷的量低于直接晒干的炮制品,因此单以蒙花苷量的高低评价野菊花质量的优劣是否可行尚需进一步探讨。查付琼等[55]提出将蒙花苷和绿原酸的定量测定作为鉴别野菊花真伪的依据。野菊花中化学成分的定量研究多以有机溶剂提取,而传统中药临床以水煎液用药,故有学者建立了HPLC法同时测定野菊花水煎液中蒙花苷、绿原酸等7种药效成分的量,发现不同产地野菊花水煎液中各成分的量差异较大[8]。仰铁锤等[56]通过对野菊中蒙花苷的定量测定发现不同花期和不同炮制品中蒙花苷的量存在差异,其中花苞期和炒制后的量最高。 2.3.2 HPLC指纹图谱研究
近年来相关学者多采用RP-HPLC指纹图谱技术对市售、不同产地或不同种野菊进行质量评价研究,多采用一定比例的甲醇加热回流提取,以蒙花苷等主要黄酮类成分作为对照品,以326 nm或334 nm作为检测波长,乙腈-磷酸水梯度洗脱的方法,所得到的图谱指纹性强,各色谱峰达到基线分离[57,58,59,60]。敬应春等[59]在所建立的HPLC指纹图谱基础上,结合相似度、花型以及蒙花苷量间的对应关系而提出一种新的质控模式。张金杰等[60]对14批野菊花样品进行测定,标定15个共有峰,归属了8个黄酮类成分,首次建立了野菊花黄酮类物质指纹图谱,可用于野菊黄酮类成分的质量控制。 2.3.3 pHPLC
在中药质量控制研究中,化学对照品是保证研究深入开展的一个重要前提。陈晓辉等[61]对野菊中黄酮类成分进行分离研究,使用pHPLC进行分离纯化,建立了蒙花苷、绿原酸、咖啡酸化学对照品的制备工艺,质量分数均为99%以上。pHPLC已成为制备野菊等天然植物药化学对照品的重要手段。 2.3.4 UPLC
与HPLC技术相比,UPLC在灵敏度、分析效率和峰容量等方面都有很大的提高,采用UPLC技术,以乙腈-0.1%磷酸水为流动相可实现野菊中蒙花苷和绿原酸成分的同时测定,结果显示亳州产野菊中蒙花苷的量相对较高,焦作产野菊中地绿原酸的量相对较高。陈宁等[62]采用UPLC技术,在12 min内得到15批野菊花药材UPLC特征性指纹图谱,为全面有效地评价野菊花质量提供科学依据。 2.4 气相色谱-质谱联用法(GC-MS)
GC-MS将气相色谱分离能力强和质谱鉴别能力强的优点有机结合,在野菊花的质量评价中,GC- MS法主要用于其挥发油成分的质量分析。对进口和国产野菊花采用GC-MS对比分析发现其主要成分分别为α-蒎烯、1,8-桉树脑和樟脑、吉玛烯等[63,64,65]。新鲜野菊花与阴干、冻干野菊花的挥发性成分也存在差异,但均以黄酮类为主要成分[66]。李晓波等[67]对中国不同产地的野菊花样品通过GC-MS法分析鉴定出169种挥发性物质,主要为1,8-桉叶素和樟脑等成分。
此外,野菊茎叶部位也含有大量挥发性成分,刘晓丹等[68]利用GC-MS法对野菊茎叶部位挥发油进行分析,发现2-(亚-2,4-己二炔基)-1,6-二氧螺[4,4]壬-3-烯的量高达17.93%,且为野菊茎叶部位所特有的挥发性成分。除水蒸气蒸馏与超临界萃取法[69]外,超声辅助提取、顶空固相微萃取与GC-MS联用技术在野菊中樟脑和冰片等挥发油成分分析中也有应用[70,71,72]。此外,衍生化气相色谱法可用于野菊多糖组成的分析,陆颖等[73]研究发现野菊多糖均由葡萄糖、鼠李糖、甘露糖等5~6种单糖组成。 2.5 火焰原子吸收光谱法与电感耦合等离子体发射光谱法
野菊中含有丰富的矿物元素,相关学者采用火焰原子吸收光谱法测定发现野菊中Se、Mn、Ca等元素量相对较高[74,75]。申海进等[76]用火焰原子吸收分光光度计测定其铅和铜的量,结果显示2种提取物作为食品抗氧化剂使用是安全的。应用电感耦合等离子体发射光谱(ICP-AES)技术,Cui等[77]测定并分析了野菊根、茎、叶、花不同器官矿质元素量、累积量和比例,明确了野菊不同部位矿质元素差异,并为野菊的合理施肥提供了新的科学依据。此外,相关学者采用ICP-AES法测定野菊不同部位元素的量并进行主成分分析,结果显示野菊花中元素的量呈现特征性上下起伏的波动折线元素谱[78]。 2.6 分子生物技术
野菊在不同地理居群个体形态差异较大,有学者从形态学和分子标记(ISSR、SRAP)两方面对11份不同居群野菊进行遗传多样性分析,发现其遗传变异与地理分布相关性并不明显,可能由遗传基因基础所决定[79]。Fang等[80]利用化学及生物分析技术评价36种野生野菊种群的遗传变异和组织学特征,发现不同种群间基因分化程度和生物活性物质的量显著不同。相关学者通过利用叶绿体DNA转移T-F序列来研究野菊的种群地理模式,发现相邻的分布区扩大以及基因流动是形成当今野菊种群分布状态的主要原因[81]。 3 展望
建立完善的质量评价体系,揭示中药疗效的本质特征是中药现代化发展的核心问题。建立在中药成分系统研究基础上的指纹图谱研究可以为中药质量评价提供一定的参考依据,但是药理活性研究才能更好地体现中药质量,因此可以将药动学研究与代谢组学相结合来进行代谢指纹图谱研究,将药效物质基础研究与现代分析手段相结合,更好地体现野菊花质量控制的科学性。
野菊花色泽金黄,可药食两用,饮用时芳香甘醇,还可降压减肥,加之人们对于生活质量的要求意识不断增强,越来越多的人把目光转向来自于天然的功能性食品,因此应加大野菊花保健饮料、香料或食品添加剂的研制,具有较好的市场前景。
我国野菊花资源丰富,每年都可再生,现今野菊花茎叶尚未被开发利用,任其掉落腐烂而造成资源浪费,所以对野菊花及其茎叶的综合开发就显得十分重要。
| [1] | 丁宝章, 王遂义. 河南植物志 [M]. 郑州: 河南省科学技术出版社, 1997. |
| [2] | Su J Y, Tan L R, Lai P, et al. Experimental study on anti-inflammatory activity of a TCM recipe consisting of the supercritical fluid CO2 extract of Chrysanthemum indicum, Patchouli oil and Zedoary turmeric Oil in vivo [J]. J Technopharmacol, 2012, 141(2): 608-614. |
| [3] | Kim J E, Jun S, Song M J, et al. The extract of Chrysanthemum indicum Linne inhibits EBV LMP1-induced NF-kappa B activation and the viability of EBV-transformed lymphoblastoid cell lines [J]. Food Chem Toxicol, 2012, 50(5): 1524-1528. |
| [4] | Hong S, Kwon S H, Kim M J, et al. Anxiolytic-like effects of Chrysanthemum indicum aqueous extract in mice: Possible involvement of GABA (A) receptors and 5-HT1A receptors [J]. Biomol Therap, 2012, 20(4): 413-417. |
| [5] | 任爱农, 王志刚, 卢振初, 等. 野菊花抑菌和抗病毒作用实验研究 [J]. 药物生物技术, 1999, 6(4): 241-244. |
| [6] | 宋立人, 洪 恂, 丁旭亮, 等. 现代中药学大辞典 [M]. 北京: 人民卫生出版社, 2001. |
| [7] | 中国药典 [S]. 一部. 2010. |
| [8] | 吴明侠, 王晶娟, 张贵君. 野菊花水煎剂中七种药效组分的含量测定 [J]. 中成药, 2011, 33(2): 300-304. |
| [9] | Rao P S. Occurrence of luteolin in the flowers of Chrysanthemum indicum [J]. Proc Indian Acad Sci, 1942, 15(A): 123-125. |
| [10] | 冯子明, 杨桠楠, 姜建双, 等. 野菊花的化学成分 [J]. 中国中药杂志, 2010, 35(24): 3302-3305. |
| [11] | 沈一形, 权丽辉, 关 玲, 等. 北野菊黄酮类成分研究 [J]. 药学学报, 1997, 32(6): 451-454. |
| [12] | 高美华, 李 华, 张 莉, 等. 野菊花化学成分的研究 [J]. 中药材, 2008, 31(8): 682-684. |
| [13] | 周洪雷. 野菊花化学成分及总黄酮提取工艺研究 [D]. 山东: 山东中医药大学, 2009. |
| [14] | 周虹云, 吴长顺, 程存归. 野菊花化学成分研究 [J]. 中国现代应用药学, 2013, 30(1): 31-35. |
| [15] | 张金杰, 陈宇峰, 颜 鸣, 等. 野菊花中的黄酮类化学成分 [J]. 医药导报, 2013, 32(1): 15-18. |
| [16] | 李青杰. 野菊花的化学成分研究 [J]. 临床合理用药, 2011, 4(9A): 65-66. |
| [17] | 汤毅, 高美华, 姚美村. 野菊花黄酮类成分研究[J]. 中药材, 2009, 32(10): 1532-1534. |
| [18] | Hisashi M, Toshio M, Masayuki Y. Medicinal flowers. IV. Absolute stereostuctures of two new flavanone glycosides and a phenylbutanoid glycoside from the flowers of Chrysanthemum indicum L.: Their inhibitory activities for rat lens aldose reductase [J]. Chem Pharm Bull, 2002, 50(7): 972-975. |
| [19] | 陈 凯, 屈亚楠. 野菊花活性成分及应用的研究进展 [J]. 安徽化工, 2014, 40(1): 10-13. |
| [20] | 冯子明. 野菊花化学成分及生物活性研究 [D]. 北京: 北京协和医学院, 2009. |
| [21] | 孙 昱, 马晓斌, 刘建勋. 野菊花心血管活性部位化学成分的研究 [J]. 中国中药杂志, 2012, 37(1): 61-65. |
| [22] | 王锦越, 陈东, 梁丽娟,等. 野菊花的化学成分研究 [J]. 中国中药杂志, 2010, 35(6): 718-720. |
| [23] | Chatterjee A, Sarkar S, Saha S. Acacetin-7-O-β-D- galactopyranoside from Chrysanthemum indicum [J]. Phytochemitry, 1981, 20(7): 1760-1761. |
| [24] | 张 聪, 秦民坚, 王 玉. 野菊花的化学成分 [J]. 药学与临床研究, 2009, 17(1): 39-41. |
| [25] | 汪国鹏. 野菊花有效组分的鉴定特征研究 [D]. 北京: 北京中医药大学, 2009. |
| [26] | 李国栋, 陈园园, 王 盼, 等. 野菊花中萜类和黄酮类化合物保肝作用研究 [J]. 中草药, 2013, 44(24): 3510-3514. |
| [27] | Yu D Q, Xie F Z. A new sesquiterpene from Chrysanthemum indicum [J]. Chin Chem Lett, 1993, 4(10): 893-894. |
| [28] | Zhou J, Wang J S, Zhang Y, et al. Disesquiterpenoid and sesquiterpenes from the flos of Chrysanthemum indicum [J]. Chem Pharm Bull, 2012, 60(8): 1067-1071. |
| [29] | Mladenova K, Tsankova E, Stoianova I B. Sesquiterpene lactones from Chrysanthemum indicum [J]. Planta Med, 1985, 51(3): 284-285. |
| [30] | 中国医学科学院药物研究所. 中草药现代研究 (第2卷) [M]. 北京: 北京医科大学中国协和医科大学联合出版社, 1996. |
| [31] | Mladenova K, Tsankova E, Dinh V H. New sesquiterpenoids from Chryanthemum indicum var. tuneful [J]. Planta Med, 1988, 54(6): 553-555. |
| [32] | 于德泉, 谢凤指. 野菊花化学成分的研究 [J]. 药学学报, 1987, 22(11): 837-840. |
| [33] | 汪国鹏. 野菊花有效组分的鉴定特征研究 [D]. 北京: 北京中医药大学, 2006. |
| [34] | 于德泉, 谢凤指, 贺文义, 等. 用二维核磁共振技术研究野菊花三醇的结构 [J]. 药学学报, 1992, 27(3): 191-196. |
| [35] | Yoshikawa M, Morikawa T, Murakami T, et al. Medicinal flowers. I. Aldose reductase inhibitors and three new eudesmane-type Sesquiterpenes, kikkanolsA, B, C, from the flowers of Chryanthemum indicum L. [J]. Chem Pharm Bull, 1999, 47(3): 340-345. |
| [36] | Liu L L, Wang R, Yang J L, et al. Five New Sesquiterpenoids from Chrysanthemum indicum [J]. Chin J Chem, 2012, 30(6): 1255-1260. |
| [37] | 周炳南. 野菊花化学成分研究 [A]//中法天然产物化学学术讨论会论文集 [C]. 上海: 《上海文化年鉴》编纂委员会, 1986. |
| [38] | 陈乃泽, 徐佩娟. 野菊花内酯的结构鉴定 [J]. 药学学报, 1987, 22(1): 67-69. |
| [39] | Mladenova K, Tsankova E, Stoianova I B. A new bisabolane ketodiol from Chryanthemum indicum [J]. Planta Med, 1987, 53(12): 118-119. |
| [40] | Yoshikawa M, Morikawa T, Toguchidal I, et al. Medicinal flowers. II. Inhibitors of nitric oxide production and absolute stereostructures of five new germacrane-type sesquiterpenes, kikkanols D, D monoacetate, E, F, and F monoacetate from the flowers of Chrysanthemum indicum L. [J]. Chem Pharm Bull, 2000, 45(8): 651-656. |
| [41] | Wang J S, Zhou J, Kong L Y. Three new germacrane-type sesquiterpene stereoisomers from the flowers of Chrysanthemum indicum [J]. Fitoterapia, 2012, 83(21): 1675-1679. |
| [42] | Cheng W M, You T P, Li T P. A new compound from the bud of Chrysanthemum indicum L. [J]. Chin Chem Lett, 2005, 10(16): 1341-1342. |
| [43] | 李贵荣. 野菊花多糖的提取及其对活性氧自由基的清除作用 [J]. 中国公共卫生, 2002, 18(3): 269-270. |
| [44] | 范灵婧, 倪鑫炎, 吴纯洁, 等. 菊花多糖的结构特征及其对NF-κB和肿瘤细胞的活性研究 [J]. 中草药, 2013, 44(17): 2364-2371. |
| [45] | 金红英, 施松善, 王顺春, 等. 野菊花中性多糖CIP-C的分离纯化及结构解析. [J]. 高等学校化学学报, 2012, 33(4): 755-760. |
| [46] | 陶燕蓉, 陈 曦. 中药质量评价技术的国内外研究现状及分析 [J]. 中药与临床, 2011(2): 59-61. |
| [47] | 徐雪琴, 余丽双, 陈国南. 毛细管电泳-电化学检测测定野菊花中的黄酮类化合物 [J]. 福州大学学报, 2008, 36(6): 884-887. |
| [48] | 程宏英, 曹玉华. 毛细管电泳法研究菊花、野菊及及其复方药中的多元酚 [J]. 苏州科技学院学报, 2009, 26(3): 37-41. |
| [49] | 吴婷妮, 李 俊, 刘长柱, 等. 毛细管电泳法检测野菊花中的黄酮类化合物 [J]. 安徽医科大学学报, 2012, 47(6): 734-737. |
| [50] | 吴明侠, 王晶娟, 张贵君, 等. 不同产地野菊花中蒙花苷含量和红外光谱的对比 [J]. 中国实验方剂学杂志, 2010, 16(14): 54-57. |
| [51] | 吴明侠, 王晶娟, 张贵君, 等. 野菊花药材不同炮制品的红外鉴别研究 [J]. 时珍国医国药, 2011, 22(1): 211-212. |
| [52] | 刘承萍. 野菊花药材稳定性与药材质量评建 [D]. 广州: 广州中医药大学硕士学位论文, 2011. |
| [53] | Zhang Y L, Xia Y, Tsogt, et al. Study on different extracts of Chrysanthemum indicum by fourier transform infrared spectroscopy [J]. Spectrosc Spectral Anal, 2012, 32(12): 3225-3228. |
| [54] | 赵 超, 李会军, 陈 君, 等. 中药复杂成分解析与质量评价的研究进展 [J]. 中国药科大学学报, 2012, 43(3): 283-288. |
| [55] | 查付琼, 胡林峰, 吴金伟, 等. HPLC法鉴别野菊花真伪的研究 [J]. 安徽农业科学, 2011, 39(10): 5765-5766. |
| [56] | 仰铁锤, 韩正洲, 陈贝贝, 等. 不同花期及不同炮制的野菊花中蒙花苷含量测定 [A]//2012海峡两岸暨CSNR全国第十届中药及天然药物资源学术研讨会 [C]. 兰州: 中药及天然药物资源学术委员会, 2012. |
| [57] | 刘 菲. 野菊花质量控制方法研究 [D]. 沈阳: 沈阳药科大学, 2009. |
| [58] | 刘婷娜, 朱恩圆, 侴桂新, 等. 野菊花高效液相色谱指纹图谱及质量评价方法的建立 [J]. 时珍国医国药, 2009, 20(4): 823-825. |
| [59] | 敬应春, 郭美兰, 蔡国琴, 等. 野菊花反相高效液相色谱指纹图谱的建立及品质评价 [J]. 国际药学研究杂志, 2012, 39(3): 246-250. |
| [60] | 张金杰, 吕文文, 翁远超, 等. 野菊花中黄酮类成分的抗菌活性及指纹图谱 [J]. 国际药学研究杂志, 2013, 40(6): 807-812. |
| [61] | 陈晓辉, 谭晓杰, 田中克佳, 等. 制备型高效液相色谱在中药野菊花化学成分分离中的应用 [J]. 药品评价, 2004, 1(5): 359-361. |
| [62] | 陈 宁, 韩永成, 刘 伟, 等. 野菊花的UPLC指纹图谱研究 [J]. 中国实验方剂学杂志, 2014, 20(3): 83-85. |
| [63] | Chang K M, Kim G H. Comparative chemical composition of domestic and imported Chrysanthemum indicum L. flower oils [J]. Food Sci Biotechnol, 2009, 18(5): 1288-1292. |
| [64] | Wu L Y, Gao H Z, Wang X L, et al. Analysis of chemical composition of Chrysanthemum indicum flowers by GC/MS and HPLC [J]. J Med Plants Res, 2010, 4(5): 421-426. |
| [65] | Chang K M, Choi E M, Kim G H. Chemical constituents of Chrysanthemum indicum L. flower oil and effect on osteoblastic MC3T3-E1 cells [J]. Food Sci Biotechnol, 2010, 19(3): 815-819. |
| [66] | Choi H S, Kim G H. Volatile flavor composition of Gamguk (Chrysanthemum indicum) flower essential oils [J]. Food Sci Biotechnol, 2011, 20(2): 319-325. |
| [67] | 李晓波. 四川野菊花挥发油化学成分GC-MS 联用分析 [J]. 海峡药学, 2010, 22(8): 50-52 |
| [68] | 刘晓丹, 刘存芳, 赖普辉, 等. 野菊花茎叶挥发油的化学成分及其对植物病原真菌抑制作用 [J]. 食品工业科技, 2013, 24(34): 98-104. |
| [69] | 周 欣, 莫彬彬, 赵 超, 等. 野菊花二氧化碳超临界萃取物的化学成分研究 [J]. 中国药学杂志, 2012, 37(3): 170-172. |
| [70] | Ye Q, Deng C H. Determination of camphor and borneol in Flos Chrysanthemi Incidi by UAE and GC-FID [J]. J Chromatogr Sci, 2009, 47(4): 287-290. |
| [71] | Deng C H, Mao Y, Yao N, et al. Development of microwave-assisted extraction followed by headspace solid-phase microextraction and gas chromatography- mass spectrometry for quantification of camphor and borneol in Flos Chrysanthemi Indici [J]. Anal Chim Acta, 2006, 575(1): 1250-125. |
| [72] | Shen S, Sha Y E, Deng C H, et al. Quality assessment of Flos Chrysanthemi Incidi from different growing areas in China by solid-phase-microextraction-gas chromatography- mass spectrometry [J]. J Chromatogr A, 2004, 1047(2): 281-287. |
| [73] | 陆 颖, 任爱农, 李厚兵, 等. 野菊花多糖的分离纯化及化学组成研究 [J]. 中国实验方剂学杂志, 2013, 19(1): 139-143. |
| [74] | 王淑荣, 焦锁囤. 火焰原子吸收光谱法测定陕西秦岭不同地域野菊花中的微量元素 [J]. 光谱实验室, 2013, 30(1): 325-328. |
| [75] | Cheng C G, Li D T, Liu X H, et al. Comparative study on trace elements in Flos Chrysanthemum and Flos Chrysanthemum Incidii [J]. Spectrosc Spectral Anal, 2006, 26(1): 156-158. |
| [76] | 申海进, 郭巧生, 邵清松. 野菊花及其提取物中有害元素及农药残留的测定 [J]. 食品工业科技, 2013, 34(3): 93-96. |
| [77] | Cui X S, Guo Y H. Analysis of mineral elements in different organs of Chrysanthemum indicum L. based on ICP-AES [J]. Spectrosc Spectral Anal, 2012, 32(10): 2828-2830. |
| [78] | 房海灵, 郭巧生, 邵清松. 野菊花中元素分布特征及相关性和主成分分析 [J]. 中国中药杂志, 2010, 35(18): 2432-2436. |
| [79] | 张鲜艳, 张 飞, 陈发棣, 等. 12份不同地理居群野菊的遗传多样性分析 [J]. 南京农业大学学报, 2011, 34(3): 48-54. |
| [80] | Fang H L, Guo Q S, Shen H J, et al. Genetic diversity evaluation of Chrysanthemum indicum L. by medicinal compounds and molecular biology tools [J]. Biochem Syst Ecol, 2012, (41): 26-34. |
| [81] | Fang H L, Guo Q S, Shen H J, et al. Phylogeography of Chrysanthemum indicum L. (Compositae) in China based on trn L-F sequences [J]. Biochem Syst Ecol, 2010, 38(6): 1204-1211. |
 2015, Vol. 46
2015, Vol. 46


