2. 成都中医药大学, 四川 成都 610072;
3. 第三军医大学大坪医院野战外科研究所 药剂科, 重庆 400042;
4. 太极集团有限公司, 重庆 401147
2. Chengdu University of Traditional Chinese Medicine, Chengdu 610072, China;
3. Department of Pharmacy, Daping Hospital and Research Institute of Surgery of the Third Military Medical University, Chongqing 400042, China;
4. Taiji Group Co., Ltd., Chongqing 401147, China
黄连为毛茛科(Ranunculaceae)黄连属Coptis Salisb.植物黄连Coptis chinensis Franch.、三角叶黄连Coptis deltoidea C. Y. Cheng et Hsiao或云连Coptis teeta Wall. 的加工品[1],据文献报道,其化学成分主要为生物碱类物质[2]。黄连的广泛利用与其所含各种生物碱的药理作用有密切的关系,且研究表明,黄连的药理作用并不是某单一生物碱作用的结果,如黄连中小檗碱具有较强的抗炎作用,但是黄连水提液的最低抑菌能力要强于小檗碱,说明黄连中含有其他抗菌或对抗菌有协同作用的成分[3, 4]。所以,只有对其主要的多个生物碱(如小檗碱、黄连碱、非洲防己碱、表小檗碱、巴马汀等)的质量分数进行全面控制,才能保证药材的质量。但对照品来源限制了多个生物碱的含量控制。有研究者提出了一测多评的多指标质控模式[5],即在多指标质量控制时,利用中药有效成分内在函数关系和比例关系,以药材中对照品廉价易得的典型成分为内标,建立该成分与其他成分间的相对校正因子,再通过校正因子同步计算出其他成分的量。在方法实施时,可在只有一个对照品的情况下,实现这些成分的同步测定,并成功应用于薄荷,五味子,白芷、丹参、赤芍、淫羊藿、连翘、黄芩、黄连、人参和枳实等药材的质量控制[6, 7, 8, 9, 10],以及热毒宁注射液、复方丹参、清开灵注射液等中成药的质量控制[11, 12, 13]。其中黄连药材的一测多评方法被《中国药典》2010年版采用[1],但只对其中4种生物碱进行了控制。同时测定黄连中6种生物碱更有利于黄连药材质量的控制[14, 15]。本研究采用一测多评的方法同时检测黄连中6种生物碱的量,相较于《中国药典》方法增加指标成分的种类,不受对照品来源的限制,更有利于黄连及其炮制品的质量控制。
1 仪器与试药高效液相色谱仪(Waters 2695-2998,Agilent 1200S,岛津LC-20A);KQ5200型超声波清洗器(昆山市超声仪器有限公司);CPA225D型电子天平(十万分之一,德国赛多利斯公司);BS224S型电子天平(万分之一,德国赛多利斯公司)。
对照品盐酸巴马汀(批号110732-200506)、盐酸小檗碱(批号110713-200609)由中国食品药品检定研究院提供;对照品盐酸药根碱(质量分数96.17%)、盐酸非洲防己碱(质量分数96.41%)、盐酸表小檗碱(质量分数90.38%)、盐酸黄连碱(质量分数91.92%)由重庆市中药研究院药化室提供;乙腈为色谱纯,其余试剂均为分析纯。
黄连 Coptidis Rhizoma药材(批号2008004、080803、080805、080804、2008005、20120905、080810、2008008、2008007、2008006),黄连饮片Coptidis Rhizoma decoction pieces(批号20080501、0808003、080802、080801、0801101、0809021、0803180、060401、2008007、0801005、08031801、080101),酒黄连Coptidis Rhizoma stir-fried with wine(批号071224、080301、080301、071124、080805、080301、08032101、080401、080804、20081001),萸黄连Coptidis Rhizoma stir-fried with Evodiae Fructus(批号20080301、080313、071201、080301、080805、080301、08032101、20080401、080804、20081001),姜黄连Coptidis Rhizoma Stir-fried with ginger juice(批号080301、080313、080804、08032101、071130、080401、080301、080803、080805、20081001),以上药材及炮制品均由太极集团有限公司提供;云连Coptis teeta Wall.和三角叶黄连Coptis deltoidea C. Y. Cheng et Hsiao(雅连)自采,各3批,以上药材均由江西中医药大学钟国跃研究员鉴定。
2 方法与结果 2.1 一测多评方法学考察 2.1.1 对照品溶液的配制精密称取盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱各适量,用50%乙腈制成含有11.13 μg/mL盐酸药根碱、15.2 μg/mL非洲防己碱、52.77 μg/mL盐酸表小檗碱、100.93 μg/mL盐酸黄连碱、75.32 μg/mL盐酸巴马汀、284.2 μg/mL盐酸小檗碱的混合对照品溶液。
2.1.2 供试品溶液的制备取药材粉末约0.2 g,精密称定,置具塞锥形瓶中,精密加入50%乙腈-盐酸(100∶1)50 mL,密塞,称定质量,超声处理30 min,放冷,再称定质量,用50%乙腈-盐酸(100∶1)补足减失的质量,摇匀,滤过,精密量取续滤液2 mL,置10 mL量瓶中,加各溶剂至刻度,摇匀,滤过,取续滤液即得。
2.1.3 色谱条件色谱柱为Gemini-NX C18(250 mm×4.6 mm,5 μm);流动相为乙腈-0.25 mol/L乙酸铵和8 mmol/L十二烷基硫酸钠(SDS)水溶液(氨水调节pH值为9.3)(36∶64);柱温35 ℃;体积流量1 mL/min;检测波长270 nm;进样量10 μL。上述色谱条件下,盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱分离良好,各组分的理论塔板数均>7 500。色谱图见图 1。
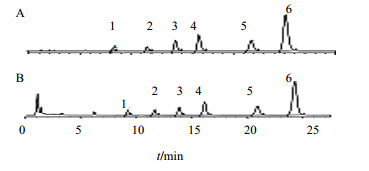 |
1-盐酸药根碱 2-盐酸非洲防己碱 3-盐酸表小檗碱 4-盐酸黄连碱 5-盐酸巴马汀 6-盐酸小檗碱 1-jatrorrhizine hydrochloride 2-columbamine hydrochloride 3-epiberberine hydrochloride 4-coptisine hydrochloride 5-palmatine hydrochloride 6-berberine hydrochloride 图 1 混合对照品 (A) 和黄连样品 (B) 的HPLC图谱 Fig.1 HPLC of reference substances (A) and Coptidis Rhizoma sample (B) |
将混合对照品溶液依次稀释2、4、8、16、32、160倍,精密吸取混合对照品溶液及其稀释液各10 μL进样。以进样量对峰面积积分值进行线性回归处理,得盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的回归直线方程及线性范围。结果见表 1。
| 表 1 6种生物碱的线性关系及线性范围 Table 1 Linear relationship and range of six alkaloids |
取盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱混合对照品溶液,各重复进样6次,测得盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱平均峰面积的RSD依次为0.59%、0.37%、0.44%、0.20%、0.28%、0.14%。表明有较好的精密度。
2.1.6 重复性试验取同一批次的样品6份,照上述制定的方法制备供试品溶液和进行HPLC测定,测得盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的平均质量分数依次为0.50%、0.45%、1.13%、2.38%、1.68%、7.20%,RSD依次为1.00%、0.91%、0.76%、0.49%、0.69%、0.36%。表明该法重复性良好。
2.1.7 稳定性试验取同一供试品溶液,分别于0、2、4、8、12、24 h测定峰面积,结果盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的RSD依次为0.81%、0.96%、0.57%、0.40%、0.43%、0.15%。说明供试品溶液在24 h内稳定。
2.1.8 加样回收率试验精密称取适量已测定的黄连药材粉末约0.1 g,精密称定,共6份,加入混合对照品溶液适量,按供试品制备方法制备样品进行HPLC测定,计算回收率。结果盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的平均回收率依次为99.65%、98.59%、98.49%、98.66%、98.64%、98.63%,RSD依次为0.03%、0.15%、0.21%、0.12%、0.28%、0.23%。
2.2 相对校正因子的确定 2.2.1 相对校正因子计算以盐酸小檗碱为内标(S),分别计算盐酸小檗碱(berberine hydrochloride,B)对盐酸药根碱(jatrorrhizine hydrochloride,J)、盐酸非洲防己碱(columbamine hydrochloride,C1)、盐酸表小檗碱(epiberberine hydrochloride,E)、盐酸黄连碱(coptisine hydrochloride,C2)、盐酸巴马汀(palmatine hydrochloride,P)的相对校正因子(fs/k),结果见表 2。
| 表 2 黄连生物碱fs/k的测定结果 Table 2 Determination of fs/k of alkaloid in Coptidis Rhizoma |
考察了3种高效液相色谱系统:Waters 2695-2998、岛津LC-20A和Agilent 1200S型高效液相色谱仪和3种色谱柱:Gemini-NX C18(250 mm×4.6 mm,5 μm),XtimateTM C18(250 mm×4.6 mm,5 μm),BETASIL C18(250 mm×4.6 mm,5 μm)并进行了不同实验室的考察,盐酸小檗碱对盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀的fs/k均基本一致,RSD小于2%,其结果比较稳定可靠。结果见表 3。
| 表 3 相对校正因子重现性考察 Table 3 Reproducibility of relative correction factor |
利用相对保留值(rk/s)定性,测得盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的rk/s结果见表 4,RSD≤5%,表明利用rk/s进行峰的定位可行。
| 表 4 不同仪器和色谱柱测得的rk/s Table 4 rk/s determined by different instruments and columns |
rk/s=tR(k)/tR(s)
k为待测组分,s为对照物
2.3 一测多评法和外标法的比较取各批次黄连及其炮制品样品粉末,按照供试品溶液的制备方法制备样品,分别注入液相色谱仪,测定样品中盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱含量;并运用小檗碱对药根碱、非洲防己碱、表小檗碱、黄连碱、巴马汀的相对校正因子计算药根碱、非洲防己碱、表小檗碱、黄连碱、巴马汀的量,各批次每个样品测定3次,取均值,再计算各类型黄连及其炮制品的总平均值。将一测多评与外标法得到的量值进行比较,2种方法所得值的偏差都在3%以内,由此说明一测多评法用于黄连药材及炮制品的多成分质量评价研究是可行的,结果见表 5。
| 表 5 黄连及其炮制品一测多评法与外标法测得生物碱量的比较 Table 5 Determinatin of Coptidis Rhizoma by QAMS and ESM |
黄连供试品制备方法中对溶媒种类进行了考察,文献中黄连的提取溶媒多用甲醇或甲醇-盐酸,在黄连质量标准研究中,发现50%乙腈对生物碱的溶解度较大,因此,对比了甲醇与50%乙腈做溶媒对黄连中主要生物碱质量分数的影响,结果表明50%乙腈-盐酸(100∶1)为提取溶剂时6种生物碱质量分数较高。
《中国药典》2010年版一部对黄连制定了4种生物碱的量限度,但文献已有关于黄连中5种或5种以上生物碱HPLC法同时测定的报道,其中包括木兰花碱、Groenlandicine、药根碱、非洲防己碱等;多成分测定符合中药多成分的特点,有利于中药质量控制的整体性和客观性。因此,本课题组考察了流动相系统,建立了分离度及对称因子都较好且稳定的6种生物碱测定的HPLC方法;在对其检测波长的选择上,参考文献和PDA检测器主要生物碱的紫外吸收图谱,6种生物碱在270 nm及345 nm处均有最大吸收,但考虑到木兰碱在345 nm下无吸收,而在270 nm下,出峰数量较多且基线稳定;因此,检测波长定为270 nm。
为防止上述各项测定结果出现远离均数的极端值,分别采用统计方法中的格拉布斯(Grubbs)检验法和狄克逊(Dixon)检验法对黄连6种生物碱量的最大值和最小值进行检验,舍去可疑值;并采用各生物碱均值的20%下限制定其质量分数限度,黄连及其炮制品的不合格数据基本集中于同一来源的药材,其量差异与药材的产地和炮制习惯有关。
雅连和云连中生物碱成分的量与味连相比差异较大,其药根碱量较高,约为味连中药根碱量的2倍;但其非洲防己碱、表小檗碱、巴马汀量较味连低;黄连碱量与味连一致。故在确定黄连生物碱限度时,未将二者计算在内,单独列出,加以区分。
本研究6种生物碱的测定方法,与《中国药典》2010年版一部黄连的测定方法相比,符合中药多成分的特点,有利于中药质量控制的整体性和客观性,更符合中药质量控制方法的要求,对黄连及其相关产品的质量控制具有重要意义。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 崔学军. 黄连及其有效成分的药理研究进展 [J]. 中国药师, 2006, 9(5): 469-470. |
| [3] | 李 娜, 陈琴华. 黄连-小檗碱的药理作用研究概况 [J]. 中国临床医药研究杂志, 2006, 159: 28-30. |
| [4] | Li R, Niu Y B, Dou Z Y. Comparative study for pharmacological action of Corydalis Rhizoma before and after processing [J]. Chin Herb Med, 2015, 7(3): 247-254. |
| [5] | 王智民, 高慧敏, 付雪涛, 等. “一测多评”法中药质量评价模式方法学研究 [J]. 中国中药杂志, 2006, 31(23): 1925-1928. |
| [6] | 贺凤成, 李守信, 赵志全, 等. 一测多评法测定五味子中4种木脂素类成分的含量 [J]. 药学学报, 2012, 47(7): 930-933. |
| [7] | 朱晶晶, 王智民, 匡艳辉, 等. 一测多评法同步测定人参和三七药材中多种人参皂苷的含量 [J]. 药学学报, 2008, 43(12): 1211-1216. |
| [8] | 徐晶晶, 徐 超, 刘 斌. 一测多评法测定薄荷药材中4种黄酮苷的含量 [J]. 中国药学杂志, 2014, 49(3): 234-239. |
| [9] | 宋永贵, 张武岗, 刘岩庭, 等. 一测多评法同时测定预知子中4种三萜皂苷 [J]. 中草药, 2012, 43(7): 1418-1421. |
| [10] | 陈建维, 刘 圆, 刘晟楠, 等. 一测多评法测定枳实中4种黄酮类成分 [J]. 中草药, 2015, 46(9): 1374-1377. |
| [11] | 张亚非, 王 雪, 毕宇安, 等. 一测多评法测定热毒宁注射液中9种成分 [J]. 中草药, 2013, 44(22): 3162-3169. |
| [12] | 张 倩, 张加余, 董鲁艳, 等. 一测多评法测定清开灵注射液中的绿原酸类成分 [J]. 中成药, 2014, 36(4): 768-772. |
| [13] | 吴 笛, 叶秋雄, 李楚源. 一测多评法测定复方丹参片中5种酚酸类成分的含量 [J]. 中国新药杂志, 2013, 22(18): 2130-2135. |
| [14] | 彭 福, 瞿显友, 钟国跃, 等. HPLC法测定黄连不同部位中6个生物碱 [J]. 中草药, 2014, 45(4): 509-512. |
| [15] | 阳 勇, 李铁刚, 朱晶晶, 等. HPLC法测定黄连药材及其炮制品中主要生物碱的含量 [J]. 中成药, 2010, 32(9): 1540-1544. |
 2016, Vol. 47
2016, Vol. 47


