龙脷叶是大戟科(Euphorbiaceae)守宫木属Sauropus Bl. 植物龙脷叶Sauropus rostratus Miq. 的叶,具有清热润肺、化痰止咳之功效。现代药理研究表明,龙脷叶具有抗过敏、抑菌、抗炎镇痛等药理活性[1-2],龙脷叶与其他药物配伍可用于治疗间质性肺炎、急性支气管炎[3-4],其主要成分为生物碱、三萜、黄酮类等[5-9],龙脷叶原产越南,我国引入栽培,主要分布在广东、广西、福建等地,是广西壮医常用解毒药,壮语称为Mbawoinxlungz(蒙凛垄),壮医认为其具有通气道、谷道,润肺止咳,滑肠通便之功效[10],民间用于治疗肺热咳喘痰多、口干、便秘等疾病。目前,国内外对龙脷叶活性成分研究很少。本实验从龙脷叶75%乙醇提取物中分离得到19个化合物,分别鉴定为正三十烷醇(n-triacontanol,1)、2,4-二叔丁基苯酚(2,4-di-tert-butylphenol,2)、β-谷甾醇(β-sitosterol,3)、胡萝卜苷(daucosterol,4)、3,6-anhydro-2-deoxy-D-arabino-hexono-l,4-lactone(5)、烟酰胺(niacinamide,6)、东莨菪亭(scopoletin,7)、3β- hydroxy-fernane-26α,28-dimethyl-13(18)-en-oic acid(8)、2R,3R,5S-trihydroxy-6R-nonadecyltetra-hydropyran-4-one(9)、大黄素(emodin,10)、原儿茶酸(protocatechuic acid,11)、2,3-dideoxy-D-erythro-hex-2-enono-1,4-lactone(12)、咖啡酸(caffeic acid,13)、3-乙酰氧基咖啡酸(3-acetrlc-affeic acid,14)、槲皮素(quercetin,15)、D-半乳糖(D-galactose,16)、甘露醇(mannitol,17)、橙黄胡椒酰胺(aurantiamide acetate,18)、山柰酚(kaempferol,19)。其中化合物8为新化合物,命名为龙脷叶酸。化合物2、5~14、16~18均为首次从该属植物中分离得到。
1 仪器与材料Waters Autospec Premier 776质谱仪(Waters公司,美国);Bruker Drx-800 MHz、Bruker Drx-500 MHz、Bruker AV-400 MHz核磁共振仪(Bruker公司,瑞士);TD电子分析天平(德国赛多利斯公司),XT4-100A控温型显微熔点测定仪(北京科仪电光仪器厂);Agilent 1100高效液相色谱仪(安捷伦公司,美国);RE-52C旋转蒸发仪(巩义予华仪器有限责任公司);柱色谱硅胶(100~200、200~300目),聚酰胺粉(30~60、80~100目,国药集团化学试剂有限公司);大孔吸附树脂(华东理工大学华昌聚合物有限公司);Sephadex LH-20(pharmacia公司,美国);MCI GEL CHP20P聚苯乙烯型反相树脂(日本三菱化学公司),所有试剂均为分析纯,购自国药集团化学试剂有限公司。
龙脷叶药材2014年3月购于广西玉林银丰中药港,经广西中医药大学壮医药学院韦松基教授鉴定为大戟科守宫木属植物龙脷叶Sauropus rostratus Miq. 的叶。标本(DYB45-GXZYC0061-2008)存放于广西中医药大学中药化学教研室。
2 提取与分离龙脷叶粗粉9 kg,用75%乙醇进行渗漉,得乙醇总提取物浸膏约2 200 g。采用系统溶剂法进行部位分离,得石油醚部位浸膏约100 g;醋酸乙酯部位浸膏150 g;正丁醇部位浸膏400 g;水部位1 000 g。
取石油醚部位浸膏80 g,经石油醚-醋酸乙酯(80∶1、50∶1、30∶1、15∶1、7∶1、2∶1)系统硅胶柱色谱分离。其中石油醚-醋酸乙酯(15∶1)洗脱流分经氯仿-甲醇(50∶1)洗脱得到化合物1(20 mg);7∶1洗脱流分经硅胶柱色谱分离得到化合物2(4 mg)、3(6 mg)。石油醚-醋酸乙酯(2∶1)洗脱部分经重结晶得到化合物4(10 mg)。取醋酸乙酯部位浸膏85 g,经氯仿-甲醇系统硅胶柱色谱、凝胶柱色谱分离,得到化合物5(8 mg)、6(11 mg)、7(13 mg)、8(5 mg)、9(4.0 mg)、10(2 mg)、11(3.2 mg)、12(5 mg)、13(5 mg)、14(16 mg)、15(10 mg)。取正丁醇部位浸膏100 g,D101大孔吸附树脂柱色谱进行分离,水-乙醇(30%、60%、90%)梯度洗脱,经小孔吸附树脂柱色谱、凝胶柱色谱分离,重结晶,得到化合物16(3 mg)、17(4 mg)、18(6 mg),经聚酰胺柱色谱分离,得到化合物19(6 mg)。
3 结构鉴定化合物1:白色片状结晶(石油醚),mp 87~88 ℃,与正三十烷醇对照品共薄层,在3种不同的展开系统中Rf值相同,与正三十烷醇对照品混合熔点不下降,故鉴定化合物1为正三十烷醇。
化合物2:白色粉末(丙酮),mp 51~53 ℃。EI-MS m/z: 206 [M]+。分子式为C14H22O。1H-NMR (500 MHz,C5D5N) δ: 7.39 (1H,d,J = 2.4 Hz,H-3),7.16 (1H,dd,J = 8.5,2.4 Hz,H-5),7.07 (1H,d,J = 8.5 Hz,H-6),1.47 (9H,s,7-CH3),1.22 (9H,s,8-CH3);13C- NMR (125 MHz,C5D5N) δ: 148.3 (C-1),139.0 (C-2),125.0 (C-3),147.8 (C-4),124.7 (C-5),119.6 (C-6),34.6 (C-7),35.2 (C-8),30.3 (7-CH3),31.3 (8-CH3)。以上光谱数据与文献报道[11-12]基本一致,故鉴定化合物2为2,4-二叔丁基苯酚。
化合物3:无色透明针状结晶(氯仿),Liebermann-Burchard反应阳性,与β-谷甾醇对照品共薄层,在3种不同的展开系统中比较,Rf值完全一致,且显色相同;与β-谷甾醇对照品混合熔点不下降,故鉴定化合物3为β-谷甾醇。
化合物4:白色粉末(甲醇),mp 286~287 ℃,与胡萝卜苷对照品共薄层,在3种不同的展开系统中Rf值相同,且显色相同,与胡萝卜苷对照品混合熔点不下降,故鉴定化合物4为胡萝卜苷。
化合物5:透明针状结晶(醋酸乙酯),mp 97~98 ℃。EI-MS m/z: 144 [M]+,分子式为C6H8O4。1H-NMR (400 MHz,CD3COCD3) δ: 4.94 (1H,t,J = 4.9 Hz,H-4),4.75 (1H,ddd,J = 6.6,5.0,1.5 Hz,H-3),2.93 (1H,m,H-2α),3.88 (1H,dd,J = 8.9,6.1 Hz,H-6β),3.59 (1H,dd,J = 8.8,7.2 Hz,H-6α),2.45 (1H,dd,J = 18.5,1.4 Hz,H-2β);13C-NMR (100 MHz,CD3COCD3) δ: 176.4 (C-1),37.0 (C-2),77.7 (C-3),83.6 (C-4),71.5 (C-5),72.4 (C-6)。以上数据与文献报道[13]基本一致,故鉴定化合物5为3,6-anhydro-2-deoxy-D-arabino-hexono-l,4-lactone。
化合物6:黄色针状结晶(氯仿),mp 129~130 ℃。EI-MS m/z: 122 [M]+,分子式为C6H6N2O。1H-NMR (500 MHz,C5D5N) δ: 9.69 (1H,s,H-2),8.73 (1H,d,J = 8.0 Hz,H-6) 8.53 (1H,d,J = 8.0 Hz,H-4),7.32 (1H,dd,J = 7.3,5.0 Hz,H-5);13C-NMR (125 MHz,C5D5N) δ: 151.7 (C-2),131.2 (C-3),137.4 (C-4),123.4 (C-5),153.3 (C-6)。以上数据与文献报道[14]基本一致,故鉴定化合物6为烟酰胺。
化合物7:浅黄色针状结晶(氯仿),mp 203~204 ℃。EI-MS m/z: 192 [M]+。分子式为C10H8O4。1H-NMR (800 MHz,CDCl3) δ: 7.59 (1H,d,J = 9.4 Hz,H-4),6.91 (1H,s,H-8),6.26 (1H,d,J = 9.4 Hz,H-3),6.12 (1H,s,OH),6.84 (1H,s,H-5),3.95 (3H,s,-OCH3);13C-NMR (200 MHz,CDCl3) δ: 161.54 (C-2),111.6 (C-3),144.1 (C-4),113.5 (C-5),143.4 (C-6),150.3 (C-7),103.3 (C-8),150.3 (C-9),107.6 (C-10),56.5 (OCH3)。以上数据与文献报道[15]基本一致,故鉴定化合物7为东莨菪亭。
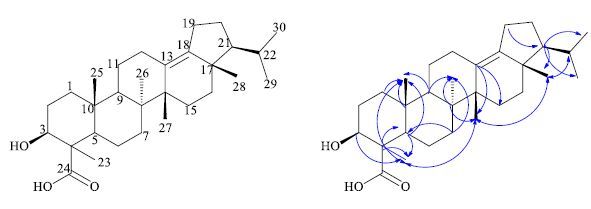
化合物8:白色粉末(丙酮),氯仿-浓硫酸反应呈阳性。HR-EI-MS m/z: 456.359 5 [M]+,分子式C30H48O3(理论值456.360 3)。1H-NMR (800 MHz,CD3COCD3) 显示7个甲基信号,分别为δ 0.81,0.91,0.94,0.96,1.03,1.10,1.40,符合三萜化合物的氢谱特征。13C-NMR (200 MHz,CD3COCD3)谱显示30个碳信号,分别为7个甲基,10个亚甲基,5个次甲基,8个季碳。其中δ 78.2为连氧的次甲基,δ 179.5为羧基,δ 131.9,142.3为1个4取代双键的碳信号。此外无其他不饱和碳信号,结合其不饱和度分析,应为五环三萜类化合物。以上数据与文献报道[16]相似,推测可能为该类型的五环三萜化合物。通过HMQC和HMBC谱分析可知H-27 (δ 1.10) 和C-13 (δ 131.9) 相关,H-28 (δ 0.81) 和C-18 (δ 142.3)、C-17 (δ 43.0) 相关,H-23 (δ 1.40) 与C-3 (δ 78.2)、C-4 (δ 50.3)、C-24 (δ 179.6) 相关,H-25 (δ 0.94) 与C-1 (δ 37.7)、C-10 (δ 37.7) 相关。由ROESY谱可看出H-28 (δ 0.81) 与H-22 (δ 0.88) 相关,可知两者均为β构型。对比文献报道[16]可知,当3-OH为α构型时,C-5的化学位移为44左右,当3-OH为β构型时形成了分子内氢键,使得C-5向低场位移,该化合物C-5的化学位移为51.7,可推断3-OH为β构型。因此确定化合物8的结构为3β-hydroxy-26α,27β-arbor-13(18)-ene-24-carboxylic acid(图 1)。其13C-NMR谱和1 H-NMR谱数据归属见表 1。
|
图 1 化合物8的化学结构和主要的HMBC (    |
|
|
表 1 化合物8的1H-NMR和13C-NMR谱数据 Table 1 1H-NMR and 13C-NMR data of compound 8 |
化合物9:白色片状结晶(甲醇),mp 118~120 ℃。EI-MS m/z: 414 [M]+,415 [M+H]+,385,368,284,分子式为C24H46O5。1H-NMR (800 MHz,CD3OD) δ: 4.54 (1H,d,J = 5.7 Hz,H-2),4.34 (1H,d,J = 5.7 Hz,H-3),4.21 (1H,d,J = 3.3 Hz,H-5),3.72 (1H,dt,J = 8.6,3.3 Hz,H-6),1.52 (2H,m,H-1′),1.48 (1H,m,H-2′a),1.21~1.33 (33H,m,H-2′b,H-3′~18′),0.86 (3H,t,J = 7.1 Hz,H-19′);13C-NMR (200 MHz,CD3OD) δ: 71.6 (C-2),69.2 (C-3),178.8 (C-4),90.2 (C-5),70.4 (C-6),34.4 (C-1′),27.0 (C-2′),30.5~30.9 (C-3′~16′),33.1 (C-17′),23.9 (C-18′),14.8 (C-19′)。以上数据与文献报道[17]基本一致,故鉴定化合物9为2R,3R,5S- trihydroxy-6R-nonadecyltetrahydropyran-4-one。
化合物10:橙红色针状结晶(甲醇),mp 253~257 ℃,Bornstrager反应呈阳性。推测为蒽醌类化合物,与大黄素对照品共薄层,在3种不同的展开系统中Rf值相同,荧光下橙红色单斑,故鉴定化合物10为大黄素。
化合物11:白色粉末(甲醇),mp 200~202 ℃,荧光显蓝色。三氯化铁反应,溶液呈墨绿色,推测为酚类化合物,与原儿茶酸对照品共薄层,在3种不同的展开系统中Rf值相同,故鉴定化合物11为原儿茶酸。
化合物12:透明针状结晶(氯仿),mp 89~90 ℃。EI-MS m/z: 144 [M]+,分子式为C6H8O4。1H-NMR (500 MHz,C5D5N) δ: 8.02 (1H,dd,J = 5.8,1.5 Hz,H-2),6.31 (1H,dd,J = 5.8,2.0 Hz,H-3),5.60~4.81 (1H,m,5-OH),4.42~4.28 (1H,m,H-4),4.24~4.11 (1H,m,H-5),3.59 (2H,d,J = 1.2 Hz,H-6);13C-NMR (125 MHz,C5D5N): 173.9 (C-1),122.0 (C-2),156.5 (C-3),85.1 (C-4),72.7 (C-5),64.0 (C-6)。以上数据与文献报道[18]基本一致,故鉴定化合物12为2,3-dideoxy-D-erythro-hex-2-enono-1,4-lactone。
化合物13:淡黄色粉末(甲醇),mp 223~225 ℃,荧光显淡蓝色。三氯化铁反应,溶液呈墨绿色,推测为酚类化合物,与咖啡酸标准品共薄层,在3种不同的展开系统中Rf值相同,故鉴定化合物13为咖啡酸。
化合物14:黄色针状结晶(甲醇),与3-乙酰氧基咖啡酸对照品共薄层,荧光下为黄色,在3种不同的展开系统中Rf值均相同,故鉴定化合物14为3-乙酰氧基咖啡酸。
化合物15:黄色粉末(甲醇),mp 313~314 ℃,与槲皮素对照品共薄层,在紫外下显黄色单斑,在3种不同的展开系统中Rf值相同,故鉴定化合物15为槲皮素。
化合物16:白色粉末(水),mp 165~166 ℃,α-萘酚浓硫酸反应呈阳性。与D-半乳糖对照品共薄层,显色剂为苯胺-邻苯二甲酸,100 ℃左右加热数分钟,呈深红色单斑。在3种不同的展开系统中Rf值相同,故鉴定化合物16为D-半乳糖。
化合物17:白色粉末(水),mp 167~168 ℃,与甘露醇对照品共薄层,在3种不同的展开系统中Rf值相同,故鉴定化合物17为甘露醇。
化合物18:白色针状结晶(甲醇),mp 188~189 ℃,碘化汞钾试剂反应有黄色沉淀,碘化铋钾反应有棕黄色沉淀。EI-MS m/z: 444 [M]+,分子式为C27H28N2O4。1H-NMR (800 MHz,CD3COCD3) δ: 7.82 (2H,d,J = 7.3 Hz,H-16,16′),7.52 (1H,t,J = 7.4 Hz,H-18),7.45 (2H,t,J = 7.7 Hz,H-17,17′),7.30 (1H,m,H-13),7.28 (2H,m,H-12,12′),7.24 (2H,m,H-11,11′),7.15 (2H,d,J = 8.0 Hz,H-9,9′),7.11 (2H,d,J = 7.5 Hz,H-8,8′),4.78 (1H,m,H-5),4.33 (1H,m,H-2),2.80 (2H,m,H-3),2.03 (3H,s,H-CH3);13C-NMR (200 MHz,CD3COCD3) δ: 65.0 (C-1),50.7 (C-2),38.0 (C-3),171.0 (C-4),55.9 (C-5),38.4 (C-6),139.1 (C-7),130.2 (C-8,8′),129.2 (C-9,9′),139.0 (C-11),129.3 (C-12,12′),130.3 (C-13,13′),127.4 (C-14),127.2 (C-16,16′),128.2 (C-17,17′),132.2 (C-18),167.4 (C-19),20.9 (-CH3CO),171.7 (-CH3CO)。以上数据与文献报道[19-20]基本一致,鉴定化合物18为橙黄胡椒酰胺。
化合物19:黄色针状结晶(甲醇),mp 276~278 ℃,磷钼酸显蓝色,盐酸-镁粉反应呈阳性。与山柰酚对照品共薄层,在3种不同的展开系统中荧光下为黄色单斑,且Rf值相同,故鉴定化合物19为山柰酚。
| [1] | 林慧, 林斌. 龙利叶抗过敏作用的实验研究[J]. 海峡药学 , 2011, 23 (4) :23–24. |
| [2] | 张国熙, 叶锡洪, 林胜英, 等. 千龙合剂对小鼠肺炎双球菌的药效学研究[J]. 新中医 , 2002, 32 (4) :35–36. |
| [3] | 邓汉华, 邓景云, 孔令深, 等. 千龙汤治疗间质性肺炎62例[J]. 新中医 , 1999, 31 (11) :42. |
| [4] | 史筱冰, 赵不潜, 潘俊辉, 等. 天龙茶治疗急性支气管炎的临床观察[J]. 现代临床医学生物工程学杂志 , 1997, 3 (2) :126. |
| [5] | Wang P H, Lee S S. Active chemical constituents from Sauropus androgynus[J]. J Chin Chem Soc , 1997, 7 (44) :145–149. |
| [6] | Rao S N, Vasanth S, Pattabhi V. Lup-1,20(29)-dien-3-one, a tripenoid from Agyneia bacciformis[J]. Acta Cryst , 2004, 60 (6) :1092–1093. |
| [7] | 林宏凤, 黎瑞珍, 吴清权. 五指山特色蔬菜守宫木、马齿苋中水分粗脂肪含量的测定[J]. 琼州学报 , 2009, 16 (2) :57–59. |
| [8] | 周聪, 赵敏, 罗金辉, 等. 树仔菜生长过程中镉元素的生物循环规律研究[J]. 安徽农业科学 , 2011, 39 (33) :20378–20380. |
| [9] | 杨暹, 郭巨先. 华南主要野生蔬菜的基本营养成分及营养价值[J]. 食品科学 , 2002, 23 (11) :121–125. |
| [10] | 广西壮族自治区壮药质量标准[S]. 2008. |
| [11] | 华会明, 李铣, 邢素娥, 等. 柳穿鱼化学成分的研究[J]. 中国药学杂志 , 2005, 40 (9) :653–656. |
| [12] | 俎成立, 顾谦群, 方玉春. 海鞘中一种酚类衍生物的分离与结构鉴定[J]. 青岛海洋大学学报 , 1999, 29 (1) :53–56. |
| [13] | Vekemans J A J M, Dapperens C W M, Claessen R, et al. Vitamin C and isovitamin C derived chemistry. 4. Synthesis of some novel furanone chirons[J]. J Org Chem , 1999, 55 :5336–5344. |
| [14] | 高巍, 杨柳, 李慧慧, 等. 杯鞘石斛的化学成分研究[J]. 中国现代中药 , 2015, 17 (4) :311–314. |
| [15] | 谢红刚, 张宏武, 张江, 等. 羊耳菊的化学成分[J]. 中国天然药物 , 2007, 5 (3) :193–196. |
| [16] | Ahmed B, Al-Howiriny T A, Mossa J S. Crotalic and emarginellic acids:Two triterpenes from Crotalaria emarginella and anti-inflammatory and anti-hepatotoxic activity of crotalic acid[J]. Phytochemistry , 2006, 67 :956–964. DOI:10.1016/j.phytochem.2006.02.019 |
| [17] | Sotanaphun U, Lipipun V, Bavovada R. Constituents of the pericarp of Glyptopetalum sclerocarpum[J]. Fitoterapia , 2004, 75 :606–608. DOI:10.1016/j.fitote.2004.04.012 |
| [18] | Vekemans J A J M, Franken G A M, Dapperens C W M, et al. Vitamin C and isovitamin C derived chemistry. 3. Chiral butenolides via efficient 2,3-didehydroxylations of L-gulono-, D-mannono-, and D-ribono-1,4-lactones[J]. J Org Chem , 1988, 53 :627–633. DOI:10.1021/jo00238a028 |
| [19] | 汤俊, TewtrakulS, 王峥涛, 等. 蚬壳花椒茎中的橙黄胡椒酰胺[J]. J Chin Pharm Sci , 2003, 12 (4) :231–233. |
| [20] | 赵伟杰, 郭永沺, 手塚康弘, 等. 乌苏里藜芦中橙黄胡椒酰胺的分离鉴定[J]. 中国中药杂志 , 1998, 23 (1) :41–42. |
 2016, Vol. 47
2016, Vol. 47


