2. 贵州医科大学药学院, 贵州 贵阳 550004;
3. 民族药与中药开发应用教育部工程研究中心/国家苗药工程技术研究中心, 贵州 贵阳 550004
2. School of Pharmacy, Guizhou Medical University, Guiyang 550004, China;
3. Engineering Research Center for the Development and Application of Ethnic Medicine and TCM, Ministry of Education/National Engineering Research Center of Miao's Medicines, Guiyang 550004, China
艾纳香为菊科艾纳香属植物艾纳香Blumea balsamifera L. DC. 的新鲜或干燥地上部分,别名冰片艾、大风艾等,广泛生长于广西、贵州等地,是黎、瑶、苗等少数民族常用药,具有祛风除湿、温中止泻等功效,可用于风湿痹痛、跌扑伤痛等症的治疗[1],为制备艾片的原料[2]。艾粉是艾纳香的叶和嫰枝经水蒸气蒸馏而得,是提取艾片的中间体,也是重要的医药工业原料[3]。艾纳香油是精制艾粉过程中压榨粗升华物而得的油,为贵州一种重要民族药材,用于制备金喉健喷雾剂、咽立爽口含滴丸等民族药制剂[4]。
色谱-质谱法是集色谱分离与质谱鉴别于一体的综合的、整体的鉴定手段,可用于鉴定药物的真伪及评价药材质量的均一性和稳定性[5-7],指纹图谱分析方法也常作为中药质量控制的辅助手段,用于评价中药材以及中药制剂半成品质量的真实性、优良性和稳定性[8-9]。为控制艾纳香、艾粉和艾纳香油质量和产品批次间一致性,本研究对艾纳香、艾粉和艾纳香油进行了系统的GC-MS指纹图谱研究,建立了可用于三者鉴别及质量控制的方法。
1 仪器与材料Agilent 7890A-5975C气相色谱质谱联用仪(美国Agilent公司);VF-5MS毛细管柱(30 m×250 μm×0.25 μm);EL204型电子天平(梅特勒-托利多仪器上海有限公司);KQ-3000DE型数控超声波清洗器(昆山市超声仪器有限公司);CHROMAP 1.5指纹图谱系统解决方案软件(珠海科曼中药研究有限公司)。
艾纳香(BB)、艾粉和艾纳香油(BBO)均由贵州省望谟县平宇中药材种植农民专业合作社提供,具体信息见表 1,其中编号S2~S11的艾纳香药材为对应编号艾粉及艾纳香油的原料药材。艾纳香药材由贵州医科大学药用植物学与生药学教研室龙庆德副教授鉴定为菊科植物艾纳香Blumea balsamifera L. DC. 的干燥全草。乙醚(国药集团化学试剂有限公司,分析纯,批号20140509)。
|
|
表 1 艾纳香药材、艾粉、艾纳香油来源 Table 1 Sources of BB,Aifen,and BBO |
2 方法与结果 2.1 GC-MS条件
色谱柱为VF-5MS毛细管柱(30 m×250 μm,0.25 μm);升温程序为初始温度40 ℃,保持5 min,以10 ℃/min升至50 ℃,以2 ℃/min升至100 ℃,以4 ℃/min升至160 ℃,以10 ℃/min升至260 ℃保持2 min,再以50 ℃/min升至310 ℃,保持1min;进样口温度250 ℃;载气为高纯氦气;体积流量1 mL/min;进样量1 μL;分流比20∶1;电子轰击(EI)离子源,电子能量70 eV;离子源温度230 ℃;四级杆温度150 ℃;传输线温度280 ℃;溶剂延迟3 min;TIC模式,质量范围m/z 10~550。
2.2 供试品溶液的制备 2.2.1 艾纳香供试品溶液的制备取艾纳香粉末1 g,精密称定,置于25 mL具塞锥形瓶中,加入15 mL乙醚,称定质量,用封口膜密封,浸泡过夜,超声10 min,用乙醚补足减失的质量,滤过,取续滤液,即得。
2.2.2 艾粉供试品溶液的制备取艾粉50 mg,精密称定,置于5 mL量瓶中,加乙醚稀释至刻度,摇匀,即得。
2.2.3 艾纳香油供试品溶液制备取艾纳香油50 mg,精密称定,置于5 mL量瓶中,加乙醚稀释至刻度,摇匀,即得。
2.3 方法学考察 2.3.1 精密度试验取同一艾粉供试品溶液(S3,批号F20151210-2),按“2.1”项下色谱条件连续进样6次,记录其色谱图,结果各共有峰峰面积RSD为1.11%~2.98%,表明仪器精密度良好。
2.3.2 重复性试验取同一编号艾粉样品(S3,批号F20151210-2)50 mg 6份,按“2.2.2”项下方法平行处理得供试品溶液,按“2.1”项下条件分别进样测定,记录其色谱图,结果各共有峰峰面积RSD为0.91%~2.94%,表明该方法重复性良好。
2.3.3 稳定性试验取同一艾粉供试品溶液(S3,批号F20151210-2)按“2.1”项下条件,分别于0、2、4、6、8、10、12、24 h进样测定,记录其色谱图,结果各共有峰峰面积RSD为0.65%~2.96%,表明供试品溶液在24 h内稳定性较好。
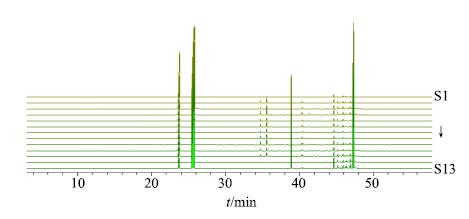
2.4 指纹图谱的建立与分析 2.4.1 指纹图谱的建立分别取艾纳香、艾粉、艾纳香油供试品溶液按“2.1”项下条件进样测定,得到13批次艾纳香、13批次艾粉和13批次艾纳香油GC-MS指纹图谱,见图 1~3。

|
图 1 13批次艾纳香药材GC-MS指纹图谱 Fig.1 GC-MSfingerprints of 13 batches of BB |
|
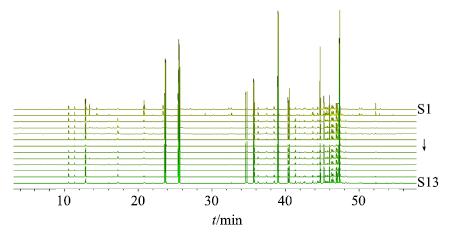
图 2 13批艾粉GC-MS指纹图谱 Fig.2 GC-MSfingerprints of 13 batches of Aifen |
|
图 3 13批艾纳香油GC-MS指纹图谱 Fig.3 GC-MSfingerprints of 13 batches of BBO |
2.4.2 共有峰的标定及鉴定
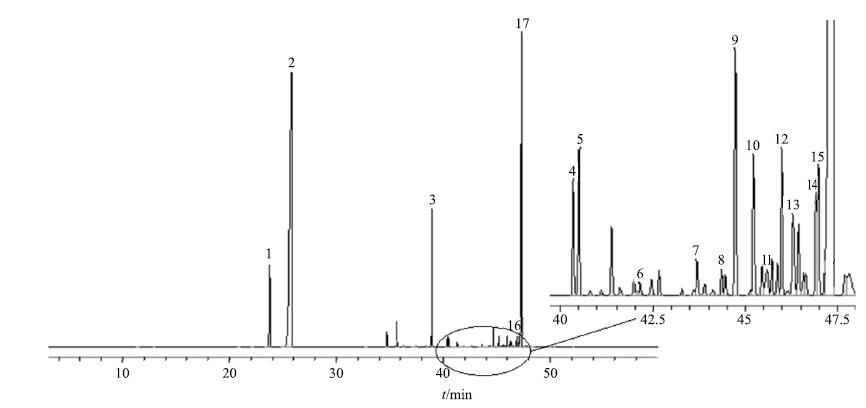
采用CHROMAP 1.5指纹图谱系统解决方案软件,以编号为S3的艾纳香样品色谱图为参照图谱,得到了13批次艾纳香药材共有模式图谱,标示40个共有指纹峰,见图 4;以编号为S3的艾粉样品色谱图为参照图谱,得到了13批次艾粉共有模式图谱,标示17个共有指纹峰,见图 5;以编号为S3的艾纳香油样品色谱图为参照图谱,得到了13批次艾纳香油共有模式图谱,标示31个共有指纹峰,见图 6。

|
图 4 13批次艾纳香药材GC-MS共有指纹图谱 Fig.4 GC-MScommonfingerprints of 13 batches of BB |
|
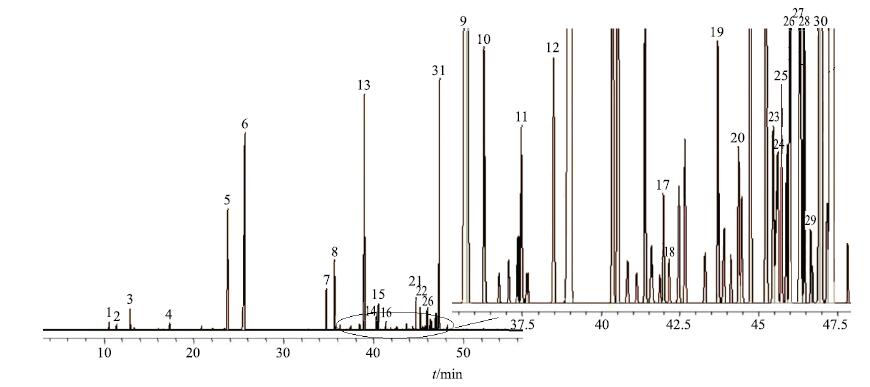
图 5 13批次艾粉GC-MS共有指纹图谱 Fig.5 GC-MScommonfingerprints of 13 batches of Aifen |
|
图 6 13批次艾纳香油GC-MS共有指纹图谱 Fig.6 GC-MScommonfingerprints of 13 batches of BBO |
将各共有指纹峰在NIST11标准谱库进行检索分析,结合相关文献报道[10-16]鉴定了艾纳香药材40个共有指纹峰、艾粉13个共有指纹峰、艾纳香油25个共有指纹峰化学成分;将确认的各共有指纹峰进行峰面积归一化计算,得到13批次样品中各成分平均相对质量分数,结果见表 2。
|
|
表 2 艾纳香药材、艾粉、艾纳香油共有峰化学成分及平均相对质量分数 Table 2 Common peaks constituents and average realtive mass fraction of BB,Aifen,and BBO |
2.4.3 相似度分析
采用CHROMAP 1.5指纹图谱系统解决方案软件,分别将13批次艾纳香、艾粉、艾纳香油样品指纹图谱与其共有模式图谱进行比较,以反映指纹图谱特征变量上变化模式的夹角余弦法计算相似度[17-21],结果见表 3。
|
|
表 3 13批次艾纳香药材、艾粉、艾纳香油GC-MS指纹图谱相似 Table 3 Similarity evalution of GC-MS fingerprints of 13 batches of BB,Aifen,and BBO |
2.5 指纹图谱相关性分析
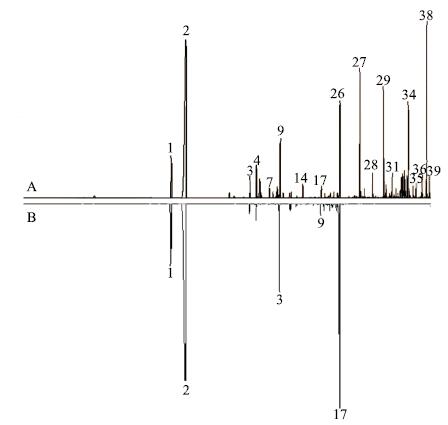
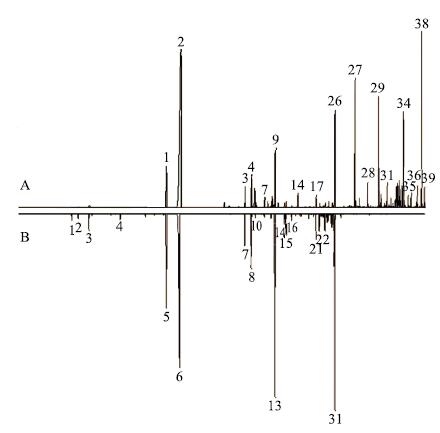
将艾纳香药材共有指纹图谱分别与艾粉、艾纳香油共有指纹图谱比较,见图 7、8,可以看出艾粉、艾纳香油各指纹峰在艾纳香药材中基本可以追溯,通过指纹图谱测定结果看出,艾纳香药材的共有峰40个,艾粉共有峰17个,艾纳香油共有峰31个,且鉴定艾粉的13个化合物、艾纳香油的25个化合物均可在艾纳香中得到追踪。对有溯源关系的艾纳香药材和艾粉、艾纳香油分析发现相关性也较好,由此可见,艾粉、艾纳香油与艾纳香药材有良好相关性。
|
图 7 艾纳香药材共有指纹图谱 (A) 与艾粉共有指纹图谱 (B) 镜像图 Fig.7 Mirror image of BB (A) and Aifen (B) common fingerprints |
|
图 8 艾纳香药材共有指纹图谱 (A) 与艾纳香油共有指纹图谱 (B) 镜像图 Fig.8 Mirror image of BB (A) and BBO (B) common fingerprints |
3 讨论
本实验对不同升温程序、分流比、载气体积流量等GC-MS条件进行了考察优化,最终选定“2.1”项下GC-MS条件进行指纹图谱分析。在该色谱条件下,艾纳香、艾粉、艾纳香油的信息量丰富且各色谱峰得到较好分离,故选定该条件作为GC-MS条件。
从相似度评价结果可看出,同一产地艾纳香药材的指纹图谱有一定差异,但提取物艾粉和艾纳香油指纹图谱相似度均在0.90以上,说明尽管原料药材之间存在一定差距,而提取物则相对较为稳定且不同批次产品差异较小,表明生产工艺稳定可靠,提取物艾粉和艾纳香油的质量稳定可控。
本研究运用GC-MS对艾纳香、艾粉、艾纳香油进行系统的指纹图谱研究,既从整体上全面反映其信息,又对部分化学成分进行分析,该方法可作为有效的分析手段用于三者鉴别及质量控制。
| [1] | 贵州省中药材、民族药材质量标准[S]. 2003. |
| [2] | 中国药典[S]. 一部. 2015. |
| [3] | 韦睿斌, 庞玉新, 杨全, 等. 艾纳香黄酮类化学成分研究进展[J]. 广东药学院学报, 2014, 30(1):123–127. |
| [4] | 易琼, 王玉坤, 王鲁. 艾纳香油药理学作用评价[J]. 黑龙江畜牧兽医, 2016, 21(16):149–151. |
| [5] | 方雯雯, 成守玲, 陈培胜, 等. 白芷药材-饮片-提取物及配方颗粒的HPLC特征图谱相关性研究[J]. 中草药, 2016, 47(18):3211–3214. |
| [6] | 陈晓水, 侯宏卫, 边照阳, 等. 气相色谱-串联质谱(GC-MS/MS)的应用研究进展[J]. 质谱学报, 2013, 34(5):308–320. |
| [7] | 董自亮, 夏芳, 官柳, 等. 华盖散制剂-药材谱峰匹配指纹图谱研究[J]. 中草药, 2016, 47(3):425–429. |
| [8] | 雍思曼. 中药指纹图谱研究进展及展望[J]. 东方食疗与保健, 2016(3):112. |
| [9] | 佟志军, 魏晓雨, 王美慧, 等. 五味子糖浆原药材、中间体及成品的HPLC指纹图谱相关性研究[J]. 中草药, 2016, 47(17):3032–3038. |
| [10] | 朱廷春. 艾纳香乙酸乙酯萃取部位的化学成分研究[D]. 桂林:广西师范大学, 2007. |
| [11] | 周欣, 杨小生, 赵超. 艾纳香挥发油化学成分的气相色谱-质谱分析[J]. 分析测试学报, 2001, 20(5):76–77. |
| [12] | Bhuiyan M N I, Chowdhury J U, Begum J. Chemical components in volatile oil from Blumea Balsamifera (L.) DC[J]. Bangladesh J Bot, 2009, 38(1): 107–109. |
| [13] | 赵金华, 康晖, 姚光辉, 等. 艾纳香化学成分研究[J]. 中草药, 2007, 38(3):350–352. |
| [14] | 王远辉, 王洪新, 田洪芸, 等. HS-SPME与GC-MS联用分析不同季节艾纳香叶香气成分[J]. 食品科学, 2012, 33(12):97–105. |
| [15] | 夏嬿, 李祥, 陈建伟. 不同提取方法对艾纳香挥发油化学组成的影响及其体外抗氧化活性[J]. 中成药, 2014, 36(10):2221–2224. |
| [16] | 韦睿斌, 庞玉新, 杨全, 等. 艾纳香黄酮类化学成分研究进展[J]. 广东药学院学报, 2014, 30(1):123–127. |
| [17] | 王龙星, 肖红斌, 梁鑫淼, 等. 一种评价中药色谱指纹谱相似性的新方法:向量夹角法[J]. 药学学报, 2002, 37(9):713–717. |
| [18] | 王玺, 王文宇, 张克荣, 等. 中药HPLC指纹图谱相似性研究的探讨[J]. 沈阳药科大学学报, 2003, 20(5):360–366. |
| [19] | 王莉, 程孟春, 肖红斌, 等. 天麻液相色谱指纹图谱研究[J]. 中草药, 2006, 37(9):1402–1405. |
| [20] | 李春来, 李俊松, 刘丹, 等. 赭石炮制品X射线衍射分析及指纹图谱的建立[J]. 中草药, 2011, 42(4):701–703. |
| [21] | 张海红, 王树, 薛贵平. 四季三黄片制剂-药材谱峰匹配指纹图谱研究[J]. 中草药, 2014, 45(21):3087–3091. |
 2017, Vol. 48
2017, Vol. 48


