光叶丁公藤Erycibe schmidtii Craib为旋花科(Convolvulaceae)丁公藤属Erycibe Roxb.植物[1]。其藤茎部分是中药丁公藤的药源之一,具有祛风除湿、消肿止痛的功效,用于治疗风湿痹痛、半身不遂、跌扑肿痛[2]。目前,关于光叶丁公藤化学成分研究只有宋蔚等[3]从中分离出了7个化合物,分别为十六碳酸、β-谷甾醇、绿原酸、东莨菪素、胡萝卜苷、东莨菪素-7-葡萄糖苷及1个水溶性生物碱丁公藤丙素。为了进一步阐明光叶丁公藤的药效物质基础,并为其质量控制和开发利用提供依据,本实验对其化学成分进行了研究,从中分离得到12个化合物,分别鉴定为咖啡酸(caffeic acid,1)、N-反式-对羟基苯乙基阿魏酰胺(N-trans-p-hydroxyphenethylferolamine,2)、绿原酸(chlorogenic acid,3)、绿原酸甲酯(chlorogenic acid methyl ester,4)、4-O-咖啡酰基奎宁酸(4-O-caffeoylquinic acid,5)、4-O-咖啡酰基奎宁酸甲酯(4-O-caffeoylquinic acid methyl ester,6)、4,5-Ocaffeoylquinic acid methyl ester,8)、3,5-O-双咖啡酰基奎宁酸(3,5-di-O-caffeoylquinic acid,9)、3,5-O-双咖啡酰基奎宁酸甲酯(3,5-di-O-caffeoylquinic acid methyl ester,10)、3,4-O-双咖啡酰基奎宁酸(3,4-di-O-caffeoyl-quinic acid,11)、3,4-O-双咖啡酰基奎宁酸甲酯(3,4-di-O-caffeoylquinic acid methyl ester,12)。化合物5~7、9、11、12为首次从该属植物中分离得到,化合物1、2、4~12为首次从该植物中分离得到。抗炎活性筛选结果表明:化合物1和2对RAW 264.7细胞释放NO显示出一定的抑制活性。
1 仪器和材料Bruker Avance 400核磁共振波谱仪(德国Bruker公司);Bruker Daltonics BioTOF-Q质谱仪(德国Bruker公司);高效液相色谱仪(上海伍丰科学仪器有限公司);薄层色谱硅胶板GF254(60型)和柱色谱硅胶(200~300目)购于青岛海洋化工厂;葡聚糖凝胶Sephadex LH-20(40~70 μm,GE Healthcare Bio-Sciences AB公司);反相硅胶(ODS,50 μm,YMC公司);D101大孔树脂(成都科龙化工试剂厂);其他试剂均为分析或色谱纯。
光叶丁公藤藤茎于2013年8月采自广西桂林,由中国科学院成都生物研究所彭玉兰副研究员鉴定为旋花科丁公藤属植物光叶丁公藤Erycibe schmidtii Craib藤茎,标本(ES201301)保存在成都医学院科研实验中心。
2 提取分离光叶丁公藤藤茎20.0 kg,粉碎,用60.0 kg 95%乙醇室温浸提3次,每次7 d,减压浓缩得到浸膏,分散于5.0 L水中,依次用等体积石油醚、醋酸乙酯和正丁醇萃取3次,分别得到石油醚层(150.0 g)、醋酸乙酯层(200.0 g)和正丁醇层(500.0 g)。
醋酸乙酯层经反相硅胶柱色谱,水和20%、30%、40%、100%甲醇进行梯度洗脱,经TLC检测合并,得到B1(58.0 g)、B2(61.5 g)、B3(49.5 g)、B4(31.0 g)4段。B1段(取4.8 g)过SephadexLH-20柱(甲醇),TLC分析后合并为B11(1.5 g)和B12(2.0 g)2部分,其中B12(2.0 g)以40%甲醇水(含0.3%甲酸)为流动相,进行HPLC制备得到化合物9(40.0 mg)。B2段(取3.6 g)过Sephadex LH-20柱(甲醇),经TLC分析后合并,分为7个部分B21、B22、B23、B24、B25、B26、B27,其中B27(0.6 g)以30%甲醇水(含0.3%甲酸)为流动相,进行HPLC制备得到化合物3(35.0mg)。B3段(取0.2g)经硅胶柱色谱,氯仿-甲醇(20∶1→8∶1)洗脱,得到化合物2(87.0 mg)。B3段(另取2.3 g)以45%甲醇水(含0.2%甲酸)为流动相,进行HPLC分段制备,分为B31、B32、B33 3个部分,其中,B31为化合物4(6.0mg);B32(25.0mg)进一步用40%甲醇水进行HPLC制备,得到化合物7(11.0mg);B33(0.8g)用30%乙腈(含0.15%甲酸)HPLC制备,得到化合物11(0.4 g)和12(35.0 mg)。B4段(取5.0 g)用45%甲醇水(含0.1%甲酸)进行HPLC制备,得到化合物8(0.2g)和10(0.2g)。
正丁醇层经大孔吸附树脂柱,甲醇-水(20%→100%)进行梯度洗脱,经TLC检测合并得到C1(150.0 g)和C2(170.0 g)2个部分。C1部分(取2.5 g)用24%甲醇(含0.3%乙酸)进行HPLC制备,得到化合物1(84.0 mg)、3(0.3 g)和5(90.0 mg)。C2部分(取8.0 g)过Sephadex LH-20柱(甲醇),TLC分析后合并为C21(2.5 g)、C22(0.4 g)2段。C21段经硅胶柱色谱,氯仿-甲醇(20∶1→4∶1)进行梯度洗脱,TLC检测合并,分为2部分C211和C212,其中,C212部分(0.4 g)用34%甲醇水进行HPLC制备,得到化合物4(65.0 mg)和6(17.5 mg)。
3 结构鉴定化合物1:棕色粉末(甲醇)。1H-NMR(400 MHz,DMSO-d6)δ: 6.18(1H,d,J=15.6 Hz,H-8),6.78(1H,d,J=7.2Hz,H-5),6.95(1H,d,J=7.2 Hz,H-6),7.03(1H,brs,H-2),7.40(1H,d,J=15.6 Hz,H-7);13C-NMR(100 MHz,DMSO-d6)δ: 115.1(C-8),116.0(C-2),116.2(C-5),121.5(C-6),126.2(C-1),144.7(C-7),146.1(C-3),148.6(C-4),168.6(C-9)。通过波谱数据分析,并与文献数据对照[4],将该化合物鉴定为咖啡酸。
化合物2:白色无定形粉末(氯仿)。ESI-MS m/z: 336 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ: 2.76(2H,t,J=7.6 Hz,H-7′),3.48(2H,t,J=7.2 Hz,H-8′),3.87(3H,s,OCH3),6.42(1H,d,J=16.0 Hz,H-8),6.74(2H,d,J=8.4 Hz,H-3′,5′),6.81(1H,d,J=8.0 Hz,H-5),7.02(1H,d,J=8.4 Hz,H-6),7.06(2H,d,J=8.4 Hz,H-2′,6′),7.11(1H,brs,H-2),7.45(1H,d,J=15.6 Hz,H-7);13C-NMR(100 MHz,CD3OD)δ:34.5(C-7′),41.1(C-8′),55.0(OCH3),110.2(C-2),115.0(C-3′,5′),115.1(C-8),117.4(C-5),121.2(C-6),126.9(C-1′),129.4(C-1),129.9(C-2′,6′),140.4(C-7),147.8(C-4),148.4(C-3),155.5(C-4′),167.8(C-9)。通过波谱数据分析,并与文献数据对照[5],将该化合物鉴定为N-反式-对羟基苯乙基阿魏酰胺。
化合物3:淡黄色粉末(甲醇)。ESI-MS m/z: 377 [M+Na]+。1H-NMR(400 MHz,DMSO-d6)δ: 1.82~2.03(4H,m,H-2,6),3.57(1H,m,H-3),3.94(1H,m,H-4),5.08(1H,m,H-5),6.16(1H,d,J=16.0 Hz,H-8′),6.78(1H,d,J=8.0 Hz,H-5′),7.00(1H,d,J=8.0 Hz,H-6′),7.04(1H,d,J=1.2 Hz,H-2′),7.43(1H,d,J=16.0 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[6],将该化合物鉴定为绿原酸。
| 表 1 化合物3~12的碳谱数据 (100 MHz) Table 1 13C-NMR (100 MHz) data of compounds 3—12 |
化合物4:白色粉末(甲醇)。1H-NMR(400 MHz,DMSO-d6)δ: 1.77~2.11(4H,m,H-2,6),3.57(3H,s,OCH3),3.76(1H,m,H-3),3.87(1H,m,H-4),5.02(1H,m,H-5),6.11(1H,d,J=16.0 Hz,H-8′),6.77(1H,d,J=8.0 Hz,H-5′),6.98(1H,d,J=7.6 Hz,H-6′),7.03(1H,brs,H-2′),7.38(1H,d,J=15.9 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[7],将该化合物鉴定为绿原酸甲酯。
化合物5:淡黄色粉末(甲醇)。ESI-MS m/z: 377 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 1.85~2.00(4H,m,H-2,6),4.00(1H,m,H-3),4.12(1H,m,H-5),4.70(1H,d,J=6.0 Hz,H-4),6.28(1H,d,J=16.0 Hz,H-8′),6.78(1H,d,J=7.6 Hz,H-5′),7.01(1H,d,J=7.6 Hz,H-6′),7.06(1H,brs,H-2′),7.51(1H,d,J=16.0 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[6],将该化合物鉴定为4-O-咖啡酰基奎宁酸。
化合物6:淡黄色粉末(甲醇)。1H-NMR(400 MHz,DMSO-d6)δ: 1.83~2.08(4H,m,H-2,6),3.62(3H,s,OCH3),3.97(1H,m,H-3),4.09(1H,m,H-5),4.73(1H,dd,J=6.8,2.8 Hz,H-4),6.27(1H,d,J=16.0Hz,H-8′),6.76(1H,d,J=8.0 Hz,H-5′),7.00(1H,d,J=8.0Hz,H-6′),7.05(1H,brs,H-2′),7.50(1H,d,J=16.0 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[8],将该化合物鉴定为4-O-咖啡酰基奎宁酸甲酯。
化合物7:淡黄色粉末(甲醇)。ESI-MS m/z: 539 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 1.95~2.15(4H,m,H-2,6),4.19(1H,m,H-3),4.98(1H,m,H-4),5.37(1H,m,H-5),6.18(1H,d,J=16.0 Hz,H-8″),6.25(1H,d,J=15.6 Hz,H-8′),6.75(2H,d,J=8.0 Hz,H-5′,5″),6.97(2H,d,J=8.0 Hz,H-6′,6″),7.05(2H,s,H-2′,2″),7.45(1H,d,J=15.6 Hz,H-7″),7.47(1H,d,J=16.0 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[9],将该化合物鉴定为4,5-O-双咖啡酰基奎宁酸。
化合物8:微黄色粉末(甲醇)。ESI-MS m/z: 553 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 1.90~2.26(4H,m,H-2,6),3.60(3H,s,OCH3),4.15(1H,m,H-3),4.97(1H,dd,J=2.8,6.4 Hz,H-4),5.28(1H,m,H-5),6.14(1H,d,J=15.6 Hz,H-8″),6.27(1H,d,J=16.0 Hz,H-8′),6.77(2H,d,J=7.2 Hz,H-5′,5″),7.00(2H,d,J=8.6Hz,H-6′,6″),7.05(2H,d,J=4.4 Hz,H-2′,2″),7.42(1H,d,J=15.6 Hz,H-7″),7.51(1H,d,J=15.6 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[10],将该化合物鉴定为4,5-O-双咖啡酰基奎宁酸甲酯。
化合物9:微黄色粉末(甲醇)。ESI-MS m/z: 539 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 2.18~2.34(4H,m,H-2,6),4.00(1H,dd,J=8.8,7.2 Hz,H-4),5.41(1H,m,H-3),5.46(1H,m,H-5),6.28(1H,d,J=16.0 Hz,H-8″),6.37(1H,d,J=16.0 Hz,H-8′),6.80(2H,d,J=8.0 Hz,H-5′,5″),6.99(2H,m,H-6′,6″),7.09(2H,brs,H-2′,2″),7.59(1H,d,J=16.0 Hz,H-7″),7.63(1H,d,J=16.0 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[7],将该化合物鉴定为3,5-O-双咖啡酰基奎宁酸。
化合物10:微黄色粉末(甲醇)。ESI-MS m/z: 553 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 2.00~2.23(4H,m,H-2,6),3.60(3H,s,OCH3),3.86(1H,m,H-4),5.09(1H,m,H-3),5.19(1H,m,H-5),6.14(1H,d,J=15.6 Hz,H-8″),6.27(1H,d,J=16.0 Hz,H-8′),6.80(2H,d,J=7.6 Hz,H-5′,5″),7.02(2H,d,J=7.6 Hz,H-6′,6″),7.06(2H,brs,H-2′,2″),7.43(1H,d,J=15.6 Hz,H-7″),7.50(1H,d,J=15.6Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[10],将该化合物鉴定为3,5-O-双咖啡酰基奎宁酸甲酯。
化合物11:微黄色粉末(甲醇)。ESI-MS m/z: 539 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 1.92~2.16(4H,m,H-2,6),4.18(1H,m,H-4),4.97(1H,m,H-5),5.39(1H,m,H-3),6.15(1H,d,J=16.0 Hz,H-8″),6.25(1H,d,J=15.6 Hz,H-8′),6.77(2H,d,J=8.0 Hz,H-5′,5″),6.98(2H,d,J=8.0 Hz,H-6′,6″),7.03(2H,brs,H-2′,2″),7.44(1H,d,J=15.6 Hz,H-7″),7.50(1H,d,J=16.0 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[11],将该化合物鉴定为3,4-O-双咖啡酰基奎宁酸。
化合物12:淡黄色粉末(甲醇)。ESI-MS m/z: 553 [M+Na]+。1H-NMR(400MHz,DMSO-d6)δ: 1.96~2.21(4H,m,H-2,6),3.63(3H,s,OCH3),4.05(1H,m,H-5),4.98(1H,m,H-4),5.40(1H,m,H-3),6.18(1H,d,J=15.6 Hz,H-8″),6.27(1H,d,J=15.6 Hz,H-8′),6.76(2H,d,J=8.1 Hz,H-5′,5″),6.97(2H,dd,J=8.1,2.1 Hz,H-6′,6″),7.05(2H,d,J=2.1 Hz,H-2′,2″),7.44(1H,d,J=15.2 Hz,H-7″),7.47(1H,d,J=15.2 Hz,H-7′);13C-NMR数据见表 1。通过波谱数据分析,并与文献数据对照[12],将该化合物鉴定为3,4-O-双咖啡酰基奎宁酸甲酯。
4 抗炎活性本实验利用NO相对生成率法对量较多的化合物1~3、5~6、8、10和11进行抗炎活性检测,结果见图 1。将2×105个/mL RAW 264.7细胞悬液接种于48孔培养板上,每孔加入0.5 mL细胞悬液,每组设置3个复孔,置于培养箱中培养。待培养板中细胞贴壁后,各实验组分别加入1μL受试药物(终质量浓度10μg/mL),阳性对照组加入1 μLNF-κB抑制剂BAY 11-7802(简写为BAY,10 μmol/L),模型组与空白组加入1 μL DMSO,孵育2 h后各孔内加入1 μL脂多糖(LPS,终质量浓度0.5 μg/mL),空白组不予处理。培养24 h后吸取培养液上清至酶标板中,加入等体积的Griess试剂,室温条件下反应10 min,然后测定540 nm波长处的吸光度(A)值,绘制标准曲线,根据相应标准曲线计算样品质量浓度,以模型组NO生成量作为100%,最后计算出NO的相对生成率。
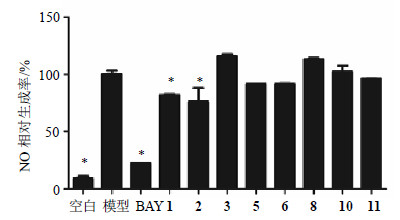 | 图 1 各化合物的NO相对生成率Fig.1 Relative yield of NO for each compound |
该结果显示,化合物1和2对RAW264.7细胞释放NO显示出一定的抑制活性,其余化合物的NO相对生成率均大于80%,提示其对RAW264.7细胞释放NO无明显的抑制作用。
| [1] | 中国医学科学院药物研究所. 中药志[M]. 北京:人民卫生出版社, 1994. |
| [2] | 中国药典[S]. 一部. 2010. |
| [3] | 宋蔚, 金蓉鸾, 刘继华. 光叶丁公藤化学成分的研究[J]. 中国中药杂志, 1997, 22(6):359-360. |
| [4] | 李岗, 仙云霞, 王晓, 等. 皂角刺化学成分及其抗肿瘤活性研究[J]. 中草药, 2015, 46(19):2846-2850. |
| [5] | 宋爽, 杨亚军, 李义秀, 等. 毛叶丁公藤化学成分研究[A]//第十届全国中药和天然药物学术研讨会论文集[C]. 北京:中国药学会, 2010. |
| [6] | 刘俊霞, 侯微, 窦凤鸣, 等. 五味子藤茎正丁醇部位化学成分研究[J]. 中草药, 2015, 46(13):1878-1882. |
| [7] | Peng L Y, Mei S X, Jiang B, et al. Constituents from Lonicera japonica[J]. Fitoterapia, 2000, 71(6):713-715. |
| [8] | 张卫东, 陈万生, 孔德云, 等. 中药灯盏细辛中酚酸类化合物的结构与活性研究[J]. 中国药学杂志, 2002, 37(8):579-581. |
| [9] | 汤丹, 李会军, 钱正明, 等. 黄褐毛忍冬花蕾咖啡酰奎宁酸类成分研究[J]. 中国药学杂志, 2007, 42(20):1537-1539. |
| [10] | 刘健. 丁公藤的化学成分及生物活性研究[D]. 北京:中国医学科学院中国协和医科大学, 2007. |
| [11] | 王永霞, 王恩, 尚靖, 等. 驱虫斑鸠菊中咖啡酰基奎宁酸类化学成分[J]. 中国中药杂志, 2012, 37(11):1590-1592. |
| [12] | 胡扬帆, 吴楚材. 灰毡毛忍冬藤化学成分研究[J]. 中药材, 2012, 35(1):66-69. |
 2016, Vol. 47
2016, Vol. 47


