2. 天津药物研究院, 天津 300193
2. Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
黄芪Astragali Radix是临床应用广泛的补益要药,据有记载黄芪炮制的108部历代炮制文献统计,黄芪炮制的主要传统方法是蜜炙、盐炙、酒炙和炒制[1, 2]。现行《中国药典》2015年版收载有黄芪、(蜜)炙黄芪2种规格的饮片。现代有关比较黄芪加工炮制前后化学成分差异性的文献报道较少,且相关报道多围绕黄芪生品和蜜炙品,相关指标化学成分也比较单一。而盐炙和酒炙黄芪确有无法替代的功效,故有必要对黄芪炮制前后的成分变化进行细致深入地研究[1]。
本实验选取蒙古黄芪Astragalus membranaceus (Fisch.) Bge. var. mongholicus (Bge.) Hsiao的药用部位根作为原药材,制备成生饮片及炮制饮片,系统进行了原药材、生饮片及其炒制品、蜜炙品、酒炙品和盐炙品中黄芪甲苷、毛蕊异黄酮苷和芒柄花素、总多糖、总黄酮和总皂苷的量差异性研究。
1 仪器与材料Agilent1100高效液相色谱仪,蒸发光散射检测器Alltech ELSD 2000ES,Agilent Technologies,Germany;Dionex液相系统,四元梯度泵,UV1601检测器,变色龙工作站;UV1601分光光度计,日本岛津;BP2IID型电子天平,十万分之一,德国SartorinS公司;AB204-N电子分析天平,Mettler Toledo。
黄芪甲苷(批号110781-200613,质量分数≥98%)、毛蕊异黄酮苷(批号111920-201102,质量分数97.1%)、芒柄花素(批号111703-201204,质量分数≥98%)、无水D-葡萄糖(批号0833-9501,质量分数≥98%)均购于中国食品药品检定研究院。蒙古黄芪药材,蒙古巴盟市乌拉特前旗朝阳镇农户种植,由天津药物研究院张铁军研究员鉴定为豆科黄芪属植物蒙古黄芪Astragalus membranaceus (Fisch.) Bge. var. mongholicus (Bge.) Hsiao的干燥根,批号H8。黄芪生饮片、炒制品、蜜炙品、酒炙品、盐炙品均自制;乙腈(色谱纯),娃哈哈纯净水,其余试剂均为分析纯。
2 方法与结果 2.1 炮制方法参照各省《中药饮片炮制规范》以及《医院中药饮片管理规范实施手册》进行制备,通过L9(34) 正交试验,得到优化炮制工艺如下。
2.1.1 黄芪生饮片的制备取蒙古黄芪药材净制后,用温水(30~40 ℃)浸泡5 min,取出,覆盖温麻布润透软化2 h,切制成椭圆形厚片,厚度2~3 mm。烘箱60 ℃鼓风干燥,备用。
2.1.2 黄芪炒制品的制备炒锅置电磁炉上,文火(120 ℃)加热,倒入“2.1.1”项制备的生饮片,160 ℃翻炒至药材表面显微黄色,透出香气,出锅后及时摊晾,备用。
2.1.3 黄芪蜜炙品的制备取炼熟蜂蜜加入适量开水稀释,开水量为熟蜜量的1/3,得到稀炼蜜。取“2.1.1”项制备的生饮片,加入质量分数为25%稀炼蜜,搅拌均匀,闷润2.0 h,用文火约110 ℃翻炒至外表皮色泽加深,呈淡棕黄色,略有光泽,具蜜香气、略带黏性而以不黏手为度,取出,摊晾,备用。
2.1.4 黄芪酒炙品的制备取“2.1.1”项制备的生饮片,黄芪饮片与黄酒用量(W/V)为10∶1,将黄酒均匀喷淋在黄芪片上,搅拌均匀,闷润2.0 h,用文火80 ℃翻炒至表面显微黄色,取出,摊晾,备用。
2.1.5 黄芪盐炙品的制备取食用盐制成20%盐水,另取“2.1.1”项制备的生饮片,加上述盐水拌匀(食用盐用量为2%),闷润1 h,用文火(120 ℃)加热翻炒至显微黄色。有香气逸出时,取出,摊晾,备用。
2.2 炮制前后黄芪甲苷的量差异性研究[3] 2.2.1 色谱条件Dikma C18色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈-水(32∶68);柱温35 ℃;体积流量1 mL/min;蒸发光散射检测:撞击器关(Impactor off);漂移管温度100 ℃;载气体积流量2.0 L/min;理论板数按黄芪甲苷峰计算应不低于4 000。
2.2.2 对照品溶液的制备精密称取黄芪甲苷对照品适量,加甲醇制成质量浓度为506.4 μg/mL的对照品溶液。
2.2.3 供试品溶液的制备取各种黄芪样品中粉约4 g,精密称定,按照《中国药典》2015年版黄芪项下黄芪甲苷的定量测定方法制备。
2.2.4 样品测定分别精密吸取对照品溶液10、20 μL,各供试品溶液20 μL,注入液相色谱仪,测定,按照《中国药典》2015年版黄芪项下黄芪甲苷定量测定方法,以外标两点法对数方程计算,得对数方程y=1.092 4 x+2.602 6,HPLC色谱图见图 1,测定结果见表 1。结果显示,炮制后,黄芪甲苷的量由高到低为原药材>生饮片>蜜炙品>酒炙品>盐炙品>炒制品。
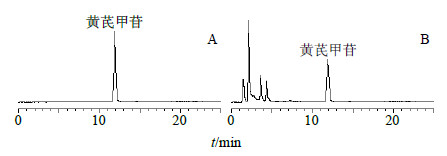 | 图 1 黄芪甲苷对照品 (A) 和蒙古黄芪原药材 (B) 的HPLC图 Fig.1 HPLC of astragaloside IV (A) and medical material of A. membranaceus var. mongholicus (B) |
| 表 1 蒙古黄芪原药材、生饮片及其炮制品中黄芪甲苷定量测定结果 Table 1 Quantitative determination of astragaloside IV in medicinal material,raw decoction pieces,and processed product of A. membranaceus var. mongholicus |
Dikma C18色谱柱(250 mm×4.6 mm,5 μm);检测波长260 nm;柱温30 ℃;体积流量1 mL/min;流动相为乙腈-0.2%甲酸水溶液,梯度洗脱程序:0~20 min,20%~40%乙腈;20~35 min,40%乙腈。
2.3.2 对照品溶液的制备精密称取毛蕊异黄酮苷、芒柄花素对照品适量,加甲醇制成含毛蕊异黄酮苷60.3 μg/mL、芒柄花素16.32 μg/mL的混合对照品溶液。
2.3.3 供试品溶液的制备取各种黄芪样品粉末(过4号筛)约1 g,精密称定,置100 mL圆底烧瓶中,精密加入甲醇50 mL,称定质量,加热回流4 h,放冷,再称定质量,甲醇补足减失的质量,摇匀,滤过,精密量取滤液25 mL,回收溶剂至干,残渣加甲醇溶解,转移至5 mL量瓶中,加甲醇稀释至刻度,摇匀,0.45 μm微孔滤膜滤过,备用。
2.3.4 线性关系考察分别精密吸取“2.3.2”项下制备的混合对照品溶液2、5、10、15、18、20 μL,注入液相色谱仪。以进样量为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,得回归方程为毛蕊异黄酮苷Y=3.544 X-69.908,r=0.999 9,表明毛蕊异黄酮苷进样量在120.6~1 206.0 μg呈良好的线性关系;芒柄花素Y=6.254 X-26.612,r=0.999 8,表明芒柄花素进样量在32.64~326.4 μg呈良好的线性关系。
2.3.5 精密度试验取混合对照品溶液,按“2.3.1”项下色谱条件连续进样6次,测定毛蕊异黄酮苷和芒柄花素的峰面积,计算毛蕊异黄酮苷峰面积RSD为0.34%,芒柄花素峰面积RSD为0.81%,表明仪器精密度良好。
2.3.6 稳定性试验取蒙古黄芪原药材(批号H8)按“2.3.3”项下方法制成供试品溶液,按“2.3.1”项下色谱条件分别在0、4、8、14、20、24 h测定,结果显示,毛蕊异黄酮苷峰面积RSD为0.99%,芒柄花素峰面积RSD为1.05%,表明供试品溶液在24 h内稳定。
2.3.7 重复性试验取蒙古黄芪原药材(批号H8)6份,精密称定,按“2.3.3”项下方法制备供试品溶液并测定,结果毛蕊异黄酮苷平均质量分数为1.192 mg/g,RSD为2.40%;芒柄花素平均质量分数为142.2 μg/g,RSD为2.74%。
2.3.8 加样回收率试验取批号H8蒙古黄芪原药材6份,每份约0.5 g,精密称定,置100 mL圆底烧瓶中,分别精密加入1 mL毛蕊异黄酮苷对照品溶液(质量浓度为0.594 mg/mL)、1 mL芒柄花素对照品溶液(质量浓度为72.2 μg/mL),置100 mL圆底烧瓶中,精密加入甲醇48 mL,按“2.3.3”项下方法制成供试品溶液,按“2.3.1”项下方法测定,按照《中国药典》2015年版9101药品质量标准分析方法验证指导原则,采用外标法计算其质量分数及加样回收率,记录样品和对照品中毛蕊异黄酮苷和芒柄花素峰面积,计算回收率。结果毛蕊异黄酮葡糖苷的平均回收率为99.57%,RSD为1.85%,芒柄花素的平均回收率为99.26%,RSD为2.11%。
2.3.9 样品测定结果取上述蒙古黄芪原药材、生饮片及其各种炮制样品,按“2.3.3”项下方法制备供试品溶液并测定,HPLC色谱图见图 2,测定结果见表 2。结果显示,炮制后,毛蕊异黄酮苷和芒柄花素的量由高到低为原药材>生饮片>酒炙品>盐炙品>蜜炙品>炒制品。
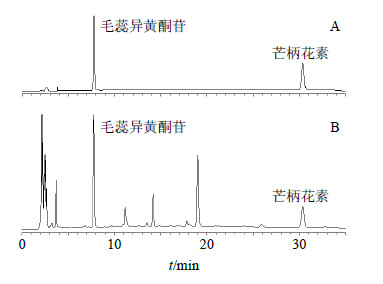 | 图 2 混合对照品 (A) 和蒙古黄芪原药材 (B) HPLC图 Fig.2 HPLC of mixed reference substances (A) and crude drug of Astragalus Radix (B) |
| 表 2 蒙古黄芪原药材、生饮片及其炮制品中毛蕊异黄酮苷和芒柄花素的定量测定结果 Table 2 Determination of calycosin-7-O-β-D-glucopyranoside and formononetin of medicinal material,raw decoction pieces,and processed products from A. membranaceus var. mongholicus |
精密称取无水D-葡萄糖对照品适量,加甲醇制成质量浓度为404.8 μg/mL的对照品溶液。
2.4.2 供试品溶液的制备取各样品粉末(过4号筛)约3 g,精密称定,置索氏提取器中,用80%乙醇索氏回流提取2 h,残渣挥干溶剂后,加水100 mL回流提取2次,每次1.5 h,滤过置200 mL量瓶中,加水稀释至刻度,摇匀,精密量取5 mL,加乙醇50 mL超声处理10 min,离心,取沉淀挥干溶剂,加水溶解至10 mL量瓶中,稀释至刻度,0.45 μm微孔滤膜滤过,精密量取滤液1 mL,置10 mL具塞干燥试管中,备用。
2.4.3 显色及测定分别精密量取D-葡萄糖对照品溶液0.5、1.0 mL和各供试品溶液1.0 mL,精密加入蒸馏水至总体积1.0 mL,加入5%苯酚溶液1.0 mL,混匀,迅速加入浓硫酸5.0 mL,摇匀,100 ℃水浴加热15 min,取出,冰浴中冷却15 min,于490 nm测定吸光度(A)值。
2.4.4 线性关系考察分别精密量取“2.4.1”项下制备的D-葡萄糖对照品溶液1.0、2.0、2.5、3.0、4.0、5.0 mL置5 mL量瓶中,加水稀释至刻度,摇匀。分别精密量取1.0 mL,按“2.4.3”项下方法测定A值。以进样量为横坐标(X),A值为纵坐标(Y),绘制标准曲线,得回归方程为Y=0.001 4 X-0.018 4,r=0.999 7,说明D-葡萄糖进样质量在80.96~404.80 μg呈良好的线性关系。
2.4.5 样品测定结果取上述蒙古黄芪原药材、生饮片及其各种炮制样品,按“2.4.2”项下方法制备供试品溶液,按“2.4.3”项下方法测定,应用外标两点法计算多糖质量分数。结果见表 3。结果显示,炮制后,多糖的量由高到低为原药材>生饮片>酒炙品>盐炙品>蜜炙品>炒制品。
| 表 3 蒙古黄芪原药材、生饮片及其炮制品中多糖的定量测定结果 Table 3 Quantitative determination of polysaccharides of medicinal material,raw decoction pieces,and processed products from A. membranaceus var. mongholicus |
精密称取毛蕊异黄酮苷对照品适量,加80%乙醇制成质量浓度为401.6 μg/mL的对照品溶液。
2.5.2 供试品溶液的制备取各样品粉末(过4号筛)约2 g,精密称定,置索氏提取器中,用60~90 ℃石油醚索氏回流脱脂4 h,残渣挥干溶剂后,加80%乙醇40 mL回流提取2次,每次1.5 h,滤过置200 mL量瓶中,加80%乙醇至刻度,摇匀。精密吸取5 mL至10 mL量瓶中,加80%稀释至刻度,摇匀,0.45 μm微孔滤膜滤过,备用。
2.5.3 显色及测定精密量取毛蕊异黄酮苷对照品溶液1.0 mL和样品溶液1.0 mL,置10 mL量瓶中,加入5%亚硝酸钠溶液0.3 mL,放置6 min,加入10%硝酸铝溶液0.3 mL,放置6 min,加入4%氢氧化钠溶液4.0 mL,加水至刻度,混匀,于510 nm测定A值。
2.5.4 线性关系考察分别精密量取“2.5.1”项下制备的毛蕊异黄酮苷对照品溶液1.0、2.0、2.5、3.0、4.0、5.0 mL置5 mL量瓶中,加水稀释至刻度,摇匀。分别精密量取1.0 mL,按“2.5.3”项下方法测定A值。以进样质量为横坐标(X),A值为纵坐标(Y),绘制标准曲线,得回归方程为Y=0.015 9 X+0.007 7,r=0.999 8,说明毛蕊异黄酮苷进样质量在8.032~40.160 μg呈良好的线性关系。
2.5.5 样品测定取上述蒙古黄芪原药材、生饮片及其各种炮制样品,按“2.5.2”项下方法制备供试品溶液,按“2.5.3”项下方法测定,应用外标法计算总黄酮质量分数。结果见表 4。结果显示炮制后,总黄酮量由高到低为原药材>酒炙品>生饮片>盐炙品>蜜炙品>炒制品。
| 表 4 蒙古黄芪原药材、生饮片及其炮制品中总黄酮的定量测定结果 Table 4 Determination of total flavonoids of medical material,raw decoction pieces and processed products from A. membranaceus var. mongholicus |
精密称取黄芪甲苷对照品适量,加甲醇制成质量浓度为350.4 μg/mL的对照品溶液。
2.6.2 供试品溶液的制备取黄芪样品中粉约1 g,精密称定,置索氏提取器中,用60~90 ℃石油醚索氏回流脱脂4 h,残渣挥干溶剂后,加乙醇100 mL回流提取2次,每次2 h,提取液减压回收溶剂至干,残渣加热水20 mL使溶解,用水饱和的正丁醇振摇提取4次,每次30 mL,合并正丁醇液,用氨试液充分洗涤2次,每次30 mL,弃去氨液,正丁醇液蒸干,残渣用甲醇溶解并转移至10 mL量瓶中,加甲醇至刻度,摇匀,即得。
2.6.3 显色及测定分别精密量取黄芪甲苷对照品溶液1.0 mL和样品溶液1.0 mL,水浴蒸干,精密加入5%香草醛-冰醋酸溶液0.2 mL和高氯酸0.8 mL,混匀,至70 ℃水浴加热15 min,取出,冷水中冷却5 min,于580 nm测定A值。
2.6.4 线性关系考察分别精密量取“2.6.1”项下制备的黄芪甲苷对照品溶液1.0、2.0、2.5、3.0、4.0、5.0 mL置5 mL量瓶中,加甲醇稀释至刻度,摇匀。分别精密量取1.0 mL,按“2.6.3”项下方法测定A值。以进样质量为横坐标(X),A值为纵坐标(Y),绘制标准曲线,得回归方程为Y=0.003 1 X-0.161 9,r=0.999 8,说明黄芪甲苷进样量在70.08~350.40 μg呈良好的线性关系。
2.6.5 样品测定结果取上述蒙古黄芪原药材、生饮片及其各种炮制样品,按“2.6.2”项下方法制备供试品溶液,按“2.6.3”项下方法测定,应用外标法计算总皂苷质量分数。结果见表 5。结果显示,炮制后,总皂苷的量由高到低为原药材>蜜炙品>生饮片>酒炙品>盐炙品>炒制品。
| 表 5 蒙古黄芪原药材、生饮片及其炮制品中总皂苷的定量测定结果 Table 5 Determination of total saponins of medical material,raw decoction pieces,and processed products from A. membranaceus var. mongholicus |
黄芪炮制方法为实验室自建,是参考《中国药典》《中药大辞典》《中华药海》《中草药炮制规范》《全国中草药汇编》及全国各省市《中药材炮制规范》等文献,建立L9(34) 因素水平表优化而成。蜜炙黄芪可以增其补中益气之功兼能健脾温肺润燥,在临床上应用尤为广泛。依据上述规范确定药材与炼蜜比例为4∶1,炒制状态为不黏手,对其他未确定因数炼蜜加开水的比例、闷润时间和炒制温度进行考察;酒炙黄芪可以应用于肢体麻木、关节痹痛,对因素黄酒用量、闷润时间、炮制温度进行考察;盐炙黄芪可补肾益气,对因素食盐用量、闷润时间、炒制温度进行考察;以黄芪甲苷量和传统外观质量为评价指标,优化得到最优炮制工艺。
通过系统比较原药材、生饮片及其炮制品中总皂苷及其代表性成分黄芪甲苷、总黄酮及其代表性成分毛蕊异黄酮苷、芒柄花素与总多糖的量,可以看出:炮制品中这些成分量降低最多,可能由于直接受热,一部分成分变性所致。有文献报道[9]高温对黄芪甲苷具破坏作用。蜜炙品中黄芪甲苷的量降低最少,且总皂苷的量略微升高,可能由于其用蜜水闷润,黏度较大,炒制过程中对黄芪甲苷等皂苷类成分起到了保护作用。另有文献报道[10]皂苷类成分加热可能发生糖键断裂致总量增加。酒炙品和盐炙品中毛蕊异黄酮苷、芒柄花素与总多糖的量降低较少,且总黄酮的量略微升高,可能由于辅料在药材表面的附着以及不同程度地渗入药材组织内部,起到一定的保护作用。另推测在加热条件下不同辅料加入可能使黄酮类成分发生变化[11]。因此认为温度和辅料保护可能对炮制过程中多种成分量的变化起主导作用。
| [1] | 徐丽莉, 袁久林. 黄芪炮制历史沿革及现代研究思路[J]. 中华中医药学刊, 2011, 29(9):2071-2073. |
| [2] | 周倩, 孙立立, 张乐林. 黄芪炮制历史沿革研究[J]. 中成药, 2014, 36(1):157-159. |
| [3] | 中国药典[S]. 一部. 2015. |
| [4] | 孙玉萍, 龚苏晓, 曹煌, 等. 不同加工方法的蒙古黄芪药材中毛蕊异黄酮苷和芒柄花素定量分析[J]. 中草药, 2015, 46(11):1678-1681. |
| [5] | 龚苏晓, 高展, 张铁军, 等. 微波辅助提取黄芪多糖及含量测定[J]. 时珍国医国药, 2008, 19(4):784-786. |
| [6] | 李春红, 田吉, 何兵, 等. 紫外分光光度法测定黄芪总黄酮的含量[J]. 重庆医科大学学报, 2011, 36(8):954-956. |
| [7] | 房树标, 李艳彦, 刘必旺, 等. 紫外分光光度法测定蒙古黄芪中总黄酮的含量[J]. 中国药物与临床, 2007, 7(12):899-901. |
| [8] | 郑美蓉, 陈鑫, 牟宗涛, 等. 紫外分光光度法测定不同产地黄芪中总皂苷含量[J]. 吉林医药学院学报, 2009, 30(2):80-81. |
| [9] | 尹丽华, 杨中林, 张红飞, 等. 不同产地、不同炮制品中黄芪中黄芪甲苷的含量差异研究[J]. 中成药, 2005, 27(9):1044-1046. |
| [10] | 刘星堦. 黄芪蜜炙方法的历史沿革及效用的探讨[J]. 中国中药杂志, 1993, 18(2):87-89. |
| [11] | 宋肖炜, 李清, 叶静, 等. 黄芪不同炮制品中黄酮类成分的含量比较[J]. 中国实验方剂学杂志, 2013, 19(9):85-88. |
 2016, Vol. 47
2016, Vol. 47


