詹淑玉, 朱琦峰, 徐宏祥, 傅应华 . UPLC-MS/MS法快速测定减肥类中成药及保健食品中非法添加15种化学药的研究[J]. 中草药, 2016, 47(17): 3023-3031.

ZHAN Shu-yu, ZHU Qi-feng, XU Hong-xiang, FU Ying-hua . Rapid determination of 15 chemical drugs illegally added into slimming Chinese patent medicines and health foods by UPLC-MS/MS[J]. Chinese Traditional and Herbal Drugs, 2016, 47(17): 3023-3031 .

UPLC-MS/MS法快速测定减肥类中成药及保健食品中非法添加15种化学药的研究
1. 嘉兴学院医学院, 浙江 嘉兴 314001
;
2. 嘉兴市食品药品检验检测院, 浙江 嘉兴 314050
收稿日期: 2016-03-26
基金项目: 浙江省公益性技术应用研究计划资助项目(2013C37103);“十二五”浙江省高校重点学科(药理学)项目的资助
摘要:
目的
建立一种快速、准确检测减肥类中成药及保健食品中非法添加15种化学药的方法。
方法
采用UPLC-MS/MS法,以Waters Acquity BEH-C18柱(100 mm×2.1 mm,1.7 μm)为色谱柱,以0.1%甲酸甲醇溶液(A)-0.1%甲酸水溶液(B)为流动相,梯度洗脱:0~3 min,33%~45% A;3~5 min,45%~55% A;5~7 min,55%~70% A;7~9 min,70%~80% A;9~10 min,80%~90% A;10~11 min,90%~33% A;11~13 min,33% A;体积流量0.2 mL/min;柱温40℃。选择ESI离子源、正离子扫描、多反应监测(MRM)模式测定15种临床常用的化学减肥药,通过比较MRM通道中样品峰与对照品峰的分子离子峰、二级碎片离子峰、色谱保留时间等信息确定添加的化学药物,并根据外标法以质谱峰面积计算添加药物的准确量。
结果
在上述色谱及质谱条件下,硫酸特布他林、盐酸麻黄碱、茶碱、咖啡因、多索茶碱、盐酸克仑特罗、盐酸妥洛特罗、盐酸班布特罗、盐酸芬氟拉明、呋塞米、吲达帕胺、酚酞、盐酸西布曲明、盐酸N-单去甲基西布曲明、盐酸N, N-双去甲基西布曲明等15种化学药物的分离良好,方法检测限(LOD)均在0.1~5.0 ng/g,定量限(LOQ)均在0.3~15.0 ng/g,标准加样回收率均在91.8%~110.8%。在86批样品(包括胶囊、颗粒剂等不同基质类型)中检出74批添加了化学药,阳性率为86.0%,样品中主要检出盐酸西布曲明(39批)、呋塞米(20批)、酚酞(23批)、茶碱(1批)、咖啡因(15批),其中检出2种的22批,3种的1批。相较而言,未明确标示生产厂家的产品中非法添加更严重。
结论
方法简便、准确,灵敏度高,可作为减肥类中成药及保健食品中非法添加15种化学药的定性定量方法。
关键词:
UPLC-MS/MS
化学药物
中成药
保健食品
非法添加
硫酸特布他林
盐酸麻黄碱
茶碱
咖啡因
多索茶碱
盐酸克仑特罗
盐酸妥洛特罗
盐酸班布特罗
盐酸芬氟拉明
呋塞米
吲达帕胺
酚酞
盐酸西布曲明
盐酸N-单去甲基西布曲明
盐酸N, N-双去甲基西布曲明
Rapid determination of 15 chemical drugs illegally added into slimming Chinese patent medicines and health foods by UPLC-MS/MS
ZHAN Shu-yu1
,
ZHU Qi-feng1,
XU Hong-xiang2,
FU Ying-hua1

1. Medical College of Jiaxing University, Jiaxing 314001, China
;
2. Jiaxing Institute for Food and Drug Control, Jiaxing 314050, China
Abstract:
Objective
To establish a rapid and accurate method for the determination of 15 chemical drugs which were illegally added into the slimming Chinese patent medicines (CPM) and health foods.
Methods
The UPLC-MS/MS method was adopted. The samples were extracted with methanol by ultrasonic processing and separated on a Waters Acquity BEH C18 column (100 mm×2.1 mm, 1.7 μm) with 0.1% formic acid methanol (A)-0.1% formic acid water (B) as mobile phase by gradient elution (0-3 min, 33%-45% A; 3-5 min, 45%-55% A; 5-7 min, 55%-70% A; 7-9 min, 70%-80% A; 9-10 min, 80%-90% A; 10-11 min, 90%-33% A; 11-13 min, 33% A at a flow rate of 0.2 mL/min, and the column temperature was 40℃. A positive-ion (ESI+) source and an MRM mode were used to separate and quantitatively determine 15 chemical drugs. The obtained molecular ions, fragment ions, and retention time for MRM channels were used to identify the 15 kinds of drugs by comparison with those of reference substances. The obtained peak areas were used to determine the accurate contents of chemical drugs in CPM and the health foods.
Results
A good resolution of 15 kinds of chemical drugs, including terbutaline hydrochloride, ephedrine hydrochloride, theophylline, caffeine, doxofylline, clenbuterol hydrochloride, tulobuterol hydrochloride, bambuterol hydrochloride, fenfluramine hydrochloride, furosemide, indapamide, phenolphthalein, sibutramine hydrochloride, N-demethylated sibutramine hydrochloride, and hydrochloric acid N, N-dinor sibutraminel, was obtained under this UPLC and MS/MS condition. The limits of qualitation and quantitation were in the range of 0.1-5.0 ng/g and 0.3-15.0 ng/g. The standard addition recoveries were in the range of 91.8%-110.8%. In the 86 batches of samples (including capsules, granules, and other different matrix types) were detected in the 74 batches of added chemicals, the positive rate was 86.0%. Sibutramine hydrochloride (39 batches), furosemide (20 batches), phenolphthalein (23 batches), theophylline (1 batch), and caffeine (15 batches) were checked out in the samples, 22 batches of which two kinds were checked out, one batch of which three kinds were checked out. By contrast, the products which were not clearly marked manufacturer illegally added more seriously.
Conclusion
The method is simple, accurate, and highly sensitive, which can be used for the determination of illegally added chemical drugs in slimming CPM and health foods.
Key words:
UPLC-MS/MS
chemical drugs
Chinese patent medicines
health foods
illegally added
terbutaline hydrochloride
ephedrine hydrochloride
theophylline
caffeine
doxofylline
clenbuterol hydrochloride
tulobuterol hydrochloride
bambuterol hydrochloride
fenfluramine hydrochloride
furosemide
indapamide
phenolphthalein
sibutramine hydrochloride
N-demethylated sibutramine hydrochloride
hydrochloric acid N, N-dinor sibutraminel
随着人们生活水平的不断提高,因饮食高脂肪、高蛋白导致肥胖的人越来越多,肥胖导致的心脑血管疾病对人们的健康构成了极大的危险,因此,人们想通过药物来进行减肥。近年来,市场上标示各种减肥功能的中成药和保健食品越来越多。用于减肥类的化学药物主要有:食欲抑制剂,代表性药物有盐酸芬氟拉明(FH)和盐酸西布曲明(SH),前者不良反应易引起成瘾性、肺部高血压等,后者不良反应易引精神、心律失常等。国家已经明令禁止使用这两种药物。增加消耗能量的药物,一类是中枢兴奋药如盐酸麻黄碱(EH)、茶碱、咖啡因等,此类药物容易产生焦虑、兴奋、失眠等不良反应;另一类为人工合成的β肾上腺素兴备剂,如盐酸克仑特罗(CH,俗称瘦肉精)、盐酸妥洛特罗(TH)和盐酸班布特罗(BH)等,此类药物使用过量会引起中毒症状。泻药,如酚酞等,可使血糖升高,血钾降低,长期使用可引起药物的依赖性。利尿药,如呋塞米、吲达帕胺等,该类药物会导致脱水、肾功能损害,严重时造成休克。
目前减肥类中药及保健食品中添加化学药物问题比较突出[1],2010年国家食品药品监督管理局颁布了针对减肥类中成药及保健食品中非法添加化学药的国家药品监督管理局药品食药监办许[2010]114号文附件2“减肥类保健食品违法添加药物的检测方法”,适用于减肥类中成药及保健食品中非法添加SH等5种化学药品的筛查和验证。该方法中,采用TLC法快速筛查,HPLC法定性检查,HPLC-MS法定性验证,操作繁琐费时。文献报道方法主要是HPLC-MS/MS法[2-15]。
本实验选择了4大类15种化学减肥药作为目标物,采用UPLC-MS/MS方法,以多离子反应监测(MRM)为测定模式,建立了多通道实时定性和定量检测减肥类中成药及保健食品中非法添加化学药的方法,在10 min内可同时准确检测出胶囊剂、颗粒剂2种剂型中违法添加的15种化学减肥药,大大提高了检测效率,结果满意。
1 仪器与材料 Acquity UPLC型超高效液相色谱仪、Quattro Premiere XE型三重四极杆串联质谱仪、电喷雾离子化源(ESI)、MassLynx数据处理系统,美国Waters公司;Mili-Q超纯水器,美国密理搏公司;Sartorius BP211D型电子天平,赛多利斯科学仪器(北京)有限公司;KQ-500E型超声提取仪,上海波龙电子有限公司。
对照品硫酸特布他林(TS,批号100273-201202,质量分数99.8%)、EH(批号171241-201007,质量分数99.7%)、茶碱(批号100121-201104,质量分数100.0%)、咖啡因(批号171215-201010,质量分数100.0%)、多索茶碱(批号100625-200301,质量分数100.0%)、CH(批号100072-200402,质量分数100.0%)、TH(批号100472-200401,质量分数100.0%)、BH(101009-200701,质量分数100.0%)、FH(批号100073-200002,质量分数100.0%)、呋塞米(批号100544-200501,质量分数100.0%)、吲达帕胺(批号100257-200903,质量分数99.7%)、酚酞(批号100091-199601,质量分数100.0%)、SH(批号100624-200401,质量分数100.0%)、盐酸N-单去甲基西布曲明(NDSH,批号520002-201301,质量分数98.8%)、盐酸N, N-双去甲基西布曲明(NNDSH,批号520001-201301,质量分数98.9%)均购自中国食品药品检定研究院。以上对照品均供定量测定用。实测样品主要为市、县食药监局及公安办案抽检的样品,部分样品通过网络、微信平台购买。典型样品如阿娇魔鬼组合胶囊(小鬼魔鬼组合)、魔鬼瘦身胶囊、院线溶脂胶囊、老中医百年秘方纯中药瘦身胶囊、纯中药瘦身小丸子、瘦身丸(强效型、早)等。甲醇(德国Merck公司)、甲酸(美国Tedia公司)均为色谱纯,其余试剂均为国产分析纯,水为超纯水。
2 方法与结果
2.1 UPLC色谱条件 色谱柱为Waters Acquity BEH-C18(100 mm×2.1 mm,1.7 μm)柱,流动相为0.1%甲酸甲醇溶液(A)-0.1%甲酸水溶液(B),梯度洗脱:0~3 min,33%~45% A;3~5 min,45%~55% A;5~7 min,55%~70% A;7~9 min,70%~80% A;9~10 min,80%~90% A;10~11 min,90%~33% A;11~13 min,32% A;体积流量0.2 mL/min;柱温为40 ℃;进样量5 μL。
2.2 MS/MS质谱条件 毛细管电压:3.0 kV;二级锥孔电压(Extractor):3 V;六级杆透镜电压(RF Len):0 V;离子源温度:110 ℃;脱溶剂气温度(Desolvation Temp):350 ℃;脱溶剂气体积流量:600 L/h;锥孔反吹气体积流量:50 L/h;碰撞气压力0.31 Pa;选择多反应监测模式(MRM)采集碎片离子信号。因药物数量多,化学性质差异大,为提高检测灵敏度和定量准确性,按色谱峰流出时间将15种化学药分为4组,分别对各时间段内流出物质的定性和定量离子进行质谱扫描,各物质的色谱保留时间、准分子离子峰、主要子离子碎片峰及其质谱数据采集参数见表 1。
表 1(Table 1)
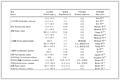
表 1 15种减肥类化学药物的质谱采集参数
Table 1 LC-MS/MS parameters for 15 chemical drugs used for slimming
| tR/min |
药品成分 |
电离模式 |
母离子(m/z) |
定量离子(m/z) |
定性离子(m/z) |
锥孔电压/V |
碰撞能量/eV |
| 1.25 |
TS |
ES+ |
226.0 |
151.8 |
169.8 |
24 |
16,12 |
| 1.90 |
EH |
ES+ |
165.8 |
147.7 |
132.7 |
20 |
20,12 |
| 1.98 |
茶碱 |
ES+ |
180.8 |
123.7 |
95.7 |
32 |
18,22 |
| 2.29 |
咖啡因 |
ES+ |
194.9 |
137.8 |
109.8 |
32 |
18,24 |
| 2.74 |
多索茶碱 |
ES+ |
266.8 |
180.9 |
123.9 |
34 |
20,32 |
| 2.96 |
CH |
ES+ |
276.8 |
202.6 |
258.8 |
22 |
18,12 |
| 3.74 |
TH |
ES+ |
227.9 |
153.7 |
171.8 |
24 |
16,12 |
| 4.02 |
BH |
ES+ |
368.0 |
294.0 |
312.0 |
28 |
20,16 |
| 5.18 |
FH |
ES+ |
231.7 |
158.5 |
186.6 |
32 |
22,14 |
| 6.02 |
呋塞米 |
ES+ |
330.9 |
80.7 |
— |
11 |
14,— |
| 6.26 |
吲达帕胺 |
ES+ |
365.9 |
131.7 |
116.7 |
22 |
16,26 |
| 6.96 |
酚酞 |
ES+ |
318.9 |
224.9 |
196.9 |
26 |
22,32 |
| 8.14 |
SH |
ES+ |
280.0 |
138.7 |
124.7 |
22 |
14,24 |
| 8.45 |
NDSH |
ES+ |
266.0 |
124.6 |
138.6 |
23 |
22,15 |
| 8.69 |
NNDSH |
ES+ |
251.9 |
124.6 |
138.6 |
20 |
19,10 |
|
表 1 15种减肥类化学药物的质谱采集参数
Table 1 LC-MS/MS parameters for 15 chemical drugs used for slimming
|
2.3 溶液的制备
2.3.1 对照品溶液 精密称取上述15种对照品各10 mg,分别置于10 mL棕色量瓶中,加甲醇适量超声溶解,放冷,用甲醇稀释至刻度,制成质量浓度均为1 mg/mL的对照品储备液。精密量取2 mL,用50%甲醇水(含0.1%甲酸)定容至100 mL,摇匀,再精密量取1 mL,用50%甲醇水(含0.1%甲酸)定容至100 mL,摇匀,得质量浓度均为200 ng/mL的混合对照品溶液。其中多个对照品与盐酸成盐,定量计算以盐酸盐计。
2.3.2 供试品溶液 取胶囊剂样品的内容物和颗粒剂各适量,分别置于研钵中,研磨均匀成粉末状,分别精密称取0.5 g,置50 mL量瓶中,加甲醇溶液约40 mL,超声处理15 min,放冷至室温,加甲醇稀释至刻度,摇匀后初滤,经0.22 μm微孔滤膜滤过,用50%甲醇水溶液(含0.1%甲酸)按比例逐步稀释成与对照品溶液质量浓度相近的溶液,作为供试品溶液。
2.3.3 阴性样品溶液 取胶囊剂(威莱斯牌芦荟胶囊、绿瘦牌奥赛青胶囊)、颗粒剂(威莱斯牌左旋肉碱绿茶减肥颗粒)2种剂型具有代表性的阴性样品,按上述方法分别制成胶囊剂、颗粒剂的空白基质,分别称取1.0 g,置于50 mL量瓶中与供试品溶液同法制备2种剂型的阴性样品溶液。
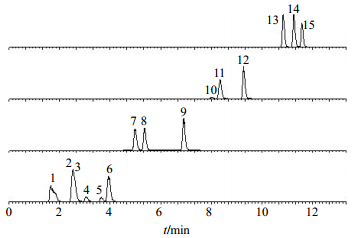
2.4 15种减肥类化学药的色谱及质谱特性 按照“2.1”和“2.2”项下色谱和质谱条件进样,分别测定了15种化学药的一组定性离子和一组定量离子,其中呋塞米为一组定量离子,共安排29个离子监测通道。为了保证定量分析的准确性,要求对色谱流出峰质谱定量满足采集15个点以上。为此,本方法将整个色谱分离时间(10 min)分成4个MRM采集时间段,可以确保各物质均有足够的质谱扫描采集点。各质谱采集时间段的MRM总离子流图见图 1。由图 1可知,由于化合物数量较多,第1时间段内有EH、茶碱色谱峰之间未分离开;其余采集时间段内各物质的色谱峰均完全分离。由图 2可知,在MRM模式下,保留时间相近的EH、茶碱能达到完全分离,各通道之间无明显干扰。
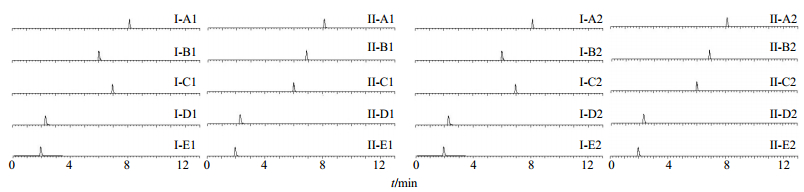
2.5 方法专属性考察 取“2.3.3”项下2种阴性样品溶液各5 μL,按“2.1”和“2.2”项下色谱、质谱条件进样测定,所得到的2种剂型阴性样品溶液的TIC和MRM色谱图,均未见有干扰15种目标化学药成分的色谱峰。结果显示,上述2种剂型中所含的中药成分均不干扰目标物的测定,方法专属性强。
2.6 线性范围考察与检测限(LOD)和定量限(LOQ)试验 精密量取“2.3.1”项下制备的对照品储备液,根据各物质离子化效率的不同,分别用50%甲醇水溶液(含0.1%甲酸)定量稀释成含CH、TS、EH、BH、FH、TH、吲达帕胺、SH、NDSH、NNDSH质量浓度均为5、10、25、50、125、250、500 ng/mL;多索茶碱、咖啡因、茶碱、酚酞质量浓度均为10、25、50、125、250、500、1 000 ng/mL;呋塞米质量浓度为25、50、125、250、500、1 000 ng/mL的混合对照品溶液。按“2.1”和“2.2”项下色谱、质谱条件进样测定,以各化学药的定量监测离子对的色谱峰峰面积为纵坐标(Y),对应的进样质量浓度为横坐标(X)绘制标准曲线,进行线性回归得线性方程和相关系数见表 2。结果表明15种化学药在各自的质量浓度范围内(5~500、10~1 000、25~1 000 ng/mL)与色谱峰峰面积均呈良好线性关系,r均在0.992 9~0.999 9。
表 2(Table 2)

表 2 15种化学药物的线性方程、相关系数、回收率及LOD、LOQ
Table 2 Linear equation, r, recovery and LOD, LOQ for 15 chemical drugs
| 药品成分 |
线性方程 |
r |
线性范围/(ng∙mL−1) |
LOD/(ng∙g−1) |
LOQ/(ng∙g−1) |
RSD/% |
平均回收率/% |
| 进样精密度 |
稳定性 |
回收率 |
| TS |
Y=4 007.9 X+10 102.3 |
0.999 6 |
5~500 |
0.8 |
2.5 |
4.2 |
4.6 |
6.1 |
93.6~105.2 |
| EH |
Y=4 600.9 X+15 645.8 |
0.992 9 |
5~500 |
0.9 |
2.8 |
2.6 |
3.2 |
4.8 |
96.7~106.7 |
| 茶碱 |
Y=455.9 X+3 102.4 |
0.999 5 |
10~1 000 |
2.0 |
6.0 |
3.0 |
3.3 |
5.0 |
94.2~103.0 |
| 咖啡因 |
Y=566.8 X+1 324.3 |
0.999 4 |
10~1 000 |
2.0 |
6.0 |
4.3 |
4.5 |
5.6 |
92.8~105.8 |
| 多索茶碱 |
Y=411.8 X+3 371.7 |
0.999 6 |
10~1 000 |
2.0 |
6.0 |
3.1 |
3.7 |
3.9 |
91.8~106.3 |
| CH |
Y=2 158.9 X+12 948.9 |
0.998 8 |
5~500 |
0.5 |
1.5 |
3.8 |
4.5 |
4.6 |
99.0~106.9 |
| TH |
Y=5 860.8 X+13 915.4 |
0.999 1 |
5~500 |
1.0 |
3.0 |
3.6 |
3.9 |
4.8 |
95.8~108.5 |
| BH |
Y=5 813.9 X+11 154.6 |
0.999 4 |
5~500 |
0.1 |
0.3 |
2.3 |
2.9 |
4.3 |
97.6~107.8 |
| FH |
Y=7 875.9 X-19 223.9 |
0.999 9 |
5~500 |
0.7 |
2.0 |
7.4 |
5.6 |
6.7 |
95.8~105.4 |
| 呋塞米 |
Y=35.86 X-920.6 |
0.995 8 |
25~1 000 |
5.0 |
15.0 |
4.5 |
5.0 |
5.6 |
96.4~110.8 |
| 吲达帕胺 |
Y=498.4 X+54.8 |
0.999 5 |
5~500 |
1.0 |
3.0 |
2.5 |
3.6 |
4.5 |
95.7~108.5 |
| 酚酞 |
Y=565.0 X+9 076.5 |
0.997 1 |
10~1 000 |
1.5 |
5.0 |
2.3 |
2.8 |
3.6 |
94.2~109.4 |
| SH |
Y=2 428.3 X+9 990.0 |
0.999 7 |
5~500 |
0.3 |
0.9 |
1.9 |
1.9 |
3.0 |
96.3~105.8 |
| NDSH |
Y=4 320.0 X+9 545.5 |
0.999 8 |
5~500 |
0.3 |
0.9 |
2.0 |
2.8 |
4.1 |
95.5~105.2 |
| NNDSH |
Y=2 658.4 X-6 716.9 |
0.999 9 |
5~500 |
0.5 |
1.5 |
3.9 |
4.6 |
5.8 |
97.2~105.9 |
|
表 2 15种化学药物的线性方程、相关系数、回收率及LOD、LOQ
Table 2 Linear equation, r, recovery and LOD, LOQ for 15 chemical drugs
|
取阴性样品(威莱斯牌芦荟胶囊、绿瘦牌奥赛青胶囊),按1.0 mg/g的添加量加入经适当稀释的混合对照品溶液,进样,以信噪比为3时计算各化学药的LOD和信噪比为10时的LOQ,结果见表 2,LOQ均在15.0 ng/g以下,表明方法具有较高的灵敏度,完全能满足非法添加化学药的检测要求。
2.7 进样精密度试验 取各成分质量浓度均为200 ng/mL混合对照品液5 μL,按“2.1”和“2.2”项下色谱和质谱条件进样测定,连续测定6次,计算上述15种化学药定量离子对质谱峰面积的RSD在1.9%~7.4%,见表 2。表明该方法的精密度良好。
2.8 重复性试验 取阴性样品(威莱斯牌芦荟胶囊、绿瘦牌奥赛青胶囊,取内容物研磨均匀,按1∶1混合)共6份,分别精密加入对照品储备液适量,使含各化学药质量分数均为1.0 mg/g,按“2.3.2”项下方法进行提取后,按“2.1”和“2.2”项下色谱、质谱条件进样测定,计算各成分质量分数及RSD。结果TS、EH、茶碱、咖啡因、多索茶碱、CH、TH、BH、FH、呋塞米、吲达帕胺、酚酞、SH、NDSH、NNDSH的平均质量分数分别为1.05、0.94、1.03、0.97、1.06、1.04、1.07、0.93、0.99、1.07、1.04、0.96、1.05、1.06、1.08 mg/g,RSD分别为4.2%、3.8%、5.2%、5.1%、3.7%、3.3%、3.9%、2.7%、5.6%、4.1%、3.6%、3.5%、4.6%、5.0%、3.1%。表明该方法重复性较好。
2.9 溶液稳定性试验 取“2.8”项下一份供试品溶液(各化学药质量浓度均为200 ng/mL),分别在配制后于0、2、4、6、8、12 h依法测定。根据上述15种化学药的定量离子对色谱峰面积计算RSD(表 2),结果RSD均在1.9%~5.6%,表明供试品溶液在12 h内稳定。
2.10 加样回收率与日内、日间精密度试验 精密称取不含15种化学药的阴性胶囊样品(威莱斯牌芦荟胶囊、绿瘦牌奥赛青胶囊)、颗粒剂(威莱斯牌左旋肉碱绿茶减肥颗粒)的空白基质各9份,每份称取0.5 g,分别置于100 mL量瓶中,加入混合对照品溶液各适量,同“2.3.2”项下方法制备供试品溶液,按照各化学药物的质谱响应,将15种化学药分为3组,其中CH、BH、FH、TH、SH、NDSH、NNDSH进行(2.0、3.0、4.0)mg/g,EH、TS、咖啡因、吲达帕胺、酚酞进行(3.0、4.0、5.0)mg/g,茶碱、呋塞米、多索茶碱进行(4.0、5.0、6.0)mg/g 3个添加水平的回收率试验。结果见表 2。从表 2可见,15种化学药的标准加样回收率,各质量浓度的回收率均在80%~120%,达到比较满意的结果。
日内精密度和日间精密度均采用添加水平为2.0 mg/g的空白样品(威莱斯牌芦荟胶囊、绿瘦牌奥赛青胶囊),按“2.3.2”项下方法进行提取后,按“2.1”和“2.2”项下色谱、质谱条件进样测定,日内精密度由重复试验6次测定得到,日间精密度由连续3 d重复取样测定得到。结果,日内精密度RSD控制在2.8%~5.8%;日间精密度RSD控制在3.5%~6.3%。表明方法精密度良好。
2.11 样品测定 本研究收集减肥类中成药及保健食品共86个样品,取各样品,按“2.3.2”项下方法制备供试品溶液,按“2.1”和“2.2”项下色谱、质谱条件分别进样测定,另取“2.3.1”项下200 ng/mL的混合对照品溶液同法测定作对照。根据定量监测离子对的色谱峰面积,采用外标法计算样品中各添加化学药的量,结果见表 3。结果表明,在86批样品(包括胶囊、颗粒剂等不同基质类型)中检出74批添加了化学药,阳性率为86.0%,典型的MRM色谱图见图 3。样品中主要检出SH(39批)、呋塞米(20批)、酚酞(23批)、茶碱(1批)、咖啡因(15批),其中检出2种的22批,3种的1批。由于检出的咖啡因在不同品种中检测量差别较大,而且茶叶中含有咖啡因,对一些处方中含有茶叶提取物的品种难以判断,需要规定限量,以防人为添加咖啡因。
表 3(Table 3)

表 3 样品信息及检出成分(n=3)
Table 3 Sample information and detected components (n=3)
| 样品名称 |
规格 |
批准文号 |
标示批号或生产日期 |
标示生产厂家 |
检出药物量 |
| 中药特效胶囊 |
300 mg×30粒 |
无 |
未标示 |
未标示 |
SH 39.4 mg/粒 |
| 瘦身丸(强效型、早) |
无 |
无 |
未标示 |
未标示 |
SH 0.9 mg/粒,酚酞26.3 mg/粒 |
| 瘦身丸(强效型、晚) |
无 |
无 |
未标示 |
未标示 |
未检出 |
| 碧迪牌减肥茶 |
3.0 g/袋 |
国食健字G20140676 |
20150303 |
河南恒生堂药业有限公司 |
咖啡因 |
| 减肥胶囊 |
无 |
无 |
2015/11/23 |
未标示 |
SH 22.2 mg/粒 |
| 舒立轻 |
350 mg |
无 |
未标示 |
Biosearch Highway Company Ltd. |
SH 13.2 mg/粒,酚酞18.0 mg/粒 |
| 瘦身丸(红色软胶囊) |
无 |
无 |
未标示 |
未标示 |
未检出 |
| 瘦身丸(绿色胶色) |
无 |
无 |
未标示 |
未标示 |
SH 7.5 mg/粒 |
| SULILIGUT胶囊 |
300 mg |
无 |
未标示 |
未标示 |
SH 24.1 mg/粒 |
| 威莱斯牌芦荟胶囊 |
0.30 g/粒 |
国食健字G20130622 |
20150409A |
广州万康保健品有限公司 |
未检出 |
| 绿瘦牌奥赛青胶囊 |
0.4 g |
国食健字G20100331 |
20150101 |
西安瑞托药业科技有限公司 |
未检出 |
| 减肥胶囊(天蓝色) |
无 |
无 |
未标示 |
未标示 |
呋塞米53.9 mg/粒 |
| 减肥胶囊(橙色) |
无 |
无 |
未标示 |
未标示 |
呋塞米42.7 mg/粒 |
| 减肥胶囊(深浅绿) |
无 |
无 |
未标示 |
未标示 |
SH 23.3 mg/粒 |
| “COURONNE”减肥胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 17.0 mg/粒 |
| 减肥胶囊(白色) |
无 |
无 |
未标示 |
未标示 |
呋塞米60.7 mg/粒 |
| 减肥胶囊(红色) |
无 |
无 |
未标示 |
未标示 |
呋塞米63.3 mg/粒 |
| 黄金二号减肥胶囊 |
无 |
无 |
未标示 |
未标示 |
呋塞米81.9 mg/粒 |
| 黛维戈 |
无 |
无 |
未标示 |
未标示 |
SH 38.0 mg/粒 |
| 伊可瘦减肥胶囊 |
无 |
无 |
2 015.10.28 |
广东伊可瘦生物科技有限公司 |
SH 25.1 mg/粒 |
| 婷采牌减肥靓颜胶囊 |
0.3 g/粒 |
国食健字G20040364 |
FC373 |
广州市康丽源生物保健品有限公司 |
咖啡因1.6 mg/粒 |
| 十杰牌劲健胶囊 |
白色胶囊 |
无 |
未标示 |
未标示 |
茶碱22.4 mg/粒 |
| 魔鬼瘦身胶囊(黑色壳) |
无 |
无 |
未标示 |
未标示 |
呋塞米78.8 mg/粒 |
| 魔鬼瘦身胶囊(金色壳) |
无 |
无 |
未标示 |
未标示 |
呋塞米75.3 mg/粒,酚酞10.1 mg/粒 |
| 魔鬼瘦身胶囊(天蓝壳) |
无 |
无 |
未标示 |
未标示 |
呋塞米57.2 mg/粒 |
| 魔鬼瘦身胶囊(深蓝壳) |
无 |
无 |
未标示 |
未标示 |
呋塞米141.9 mg/粒,酚酞18.9 mg/粒 |
| 院线溶脂胶囊 |
无 |
国食健字G20110551 |
未标示 |
未标示 |
呋塞米5.5g/粒 |
| 轻松瘦 |
无 |
国食健字G20110551 |
未标示 |
未标示 |
SH 12.9 mg/粒 |
| NV瘦腿胶囊 |
无 |
无 |
未标示 |
未标示 |
咖啡因45.0 mg/粒 |
| 银色胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 9.3 mg/粒 |
| 金色胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 43.7 mg/粒,酚酞30.0 mg/粒 |
| 纯中药瘦身小丸子 |
无 |
无 |
2015/08/15 |
未标示 |
SH 6.8 mg/粒,咖啡因0.7 mg/粒 |
| SULILIGHT(舒立轻) |
350 mg |
无 |
20150405 |
Biosearch Highway Company Ltd. |
SH 14.8 mg/粒 |
| 特效中药 |
无 |
无 |
未标示 |
未标示 |
SH 14.1 mg/粒,酚酞7.0 mg/粒 |
| 溶脂瘦身(红色胶囊) |
无 |
无 |
未标示 |
未标示 |
呋塞米74.4 mg/粒 |
| 溶脂瘦腿(蓝色胶囊) |
无 |
无 |
未标示 |
未标示 |
呋塞米66.5 mg/粒 |
| 溶脂瘦身(橙色胶囊) |
无 |
无 |
未标示 |
未标示 |
呋塞米59.1 mg/粒 |
| 中药瘦身丽人胶囊 |
450 mg |
国食健字G20120007 |
20150809A |
武汉真浩生物工程有限公司 |
SH 13.6 mg/粒,酚酞16.0 mg/粒 |
| 溶脂瘦身胶囊 |
无 |
国食健字G20110551 |
未标示 |
未标示 |
呋塞米45.0 mg/粒 |
| Timi master压缩奶片 |
无 |
无 |
2015/03/18 |
上海语禾生物技术有限公司 |
呋塞米11.5 mg/片 |
| 减肥胶囊 |
0.4 g/粒 |
国食健字G20141178 |
20150409 |
江西复真药业有限公司 |
咖啡因 |
| 减肥胶囊 |
0.4 g/粒 |
国食健字G20141178 |
20150309 |
江西复真药业有限公司 |
咖啡因 |
| 减肥胶囊(黄绿色) |
无 |
无 |
未标示 |
未标示 |
呋塞米50.7 mg/粒 |
| 瘦身丸(红色胶囊) |
无 |
无 |
未标示 |
未标示 |
未检出 |
| 印尼减肥MGSS钻石二号胶囊 |
无 |
无 |
未标示 |
印尼 |
呋塞米20.0 mg/粒 |
| 健康瘦茶多酚荷叶胶囊 |
无 |
国食健字G20050373 |
未标示 |
陕西安恒信健康产业有限公司 |
未检出 |
| 粉色胶囊 |
无 |
无 |
未标示 |
未标示 |
酚酞38.1 mg/粒 |
| 金色胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 7.1 mg/粒,酚酞13.1 mg/粒 |
| 蓝色胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 7.1 mg/粒,酚酞34.8 mg/粒 |
| 珍嗖啦酵素果冻 |
15 g |
无 |
2015/07/20 |
广州市佰利鲜食品有限公司 |
酚酞22.1 mg/粒 |
| 90斤瘦身巧克力豆 |
无 |
无 |
未标示 |
未标示 |
SH 8.3 mg/粒 |
| 溶脂瘦身(黄蓝两色胶囊) |
无 |
无 |
未标示 |
未标示 |
SH 0.2 mg/粒,酚酞2.5 mg/粒 |
| COURONNE 1(胶囊) |
无 |
无 |
未标示 |
未标示 |
SH 77.2 mg/粒 |
| 香草多酚片(压片糖果) |
500 mg |
无 |
2015/11/01 |
未标示 |
酚酞16.4 mg/粒 |
| 苗伊秀减肥颗粒 |
无 |
无 |
未标示 |
南阳市澳福来药业有限责任公司 |
咖啡因 |
| 苗伊秀减肥颗粒(咖啡型) |
4g/袋 |
国食健字G2020130306 |
20150101 |
南阳市澳福来药业有限责任公司 |
咖啡因 |
| TITISO减肥胶囊 |
无 |
无 |
未标示 |
未标示 |
未检出 |
| 赛维欧左旋肉碱强效型 |
400 mg |
国食健字G20120449 |
15/12.26 |
山东威海南波湾生物技术有限公司 |
未检出 |
| 特效中药 |
300 mg |
无 |
未标示 |
未标示 |
SH 2.5 mg/粒 |
| 蛋白瘦身素 |
400 mg |
无 |
无 |
罗斯上海技术开发区分公司 |
SH 8.1 mg/粒,咖啡因0.5 mg/粒 |
| 茶多酚片糖果压片 |
0.7 g |
QS440713011890 |
20160101 |
广东传奇医药科技有限公司 |
咖啡因 |
| 联合邦利牌芦荟软胶囊 |
1 g/粒 |
无 |
9658562-05 |
广州联存医药科技有限公司 |
未检出 |
| 碧生源减肥茶 |
2.5 g/袋 |
(京食药)卫食证字(2006)第110000-JS0031号 |
04150807 |
北京澳特舒尔保健品开发有限公司 |
咖啡因 |
| 威莱斯牌左旋肉碱绿茶减肥颗粒 |
2.0 g/粒 |
国食健字G20100331 |
20150403A |
广州万康保健品有限公司 |
咖啡因3.1 mg/粒 |
| 左旋肉碱 |
0.42 g |
国食健字G20110551 |
14081901 |
委托商:威海紫光生物科技开发有限公司;受委托生产商:威海南波湾生物技术有限公司 |
咖啡因 |
| USA Slimming Capsule(美国减肥胶囊) |
无 |
无 |
未标示 |
未标示 |
SH 17.5 mg/粒 |
| 纯中药瘦身小丸子 |
无 |
无 |
2015/10/08 |
未标示 |
SH 9.5 mg/粒 |
| Devil figure(魔鬼身材减肥胶囊) |
350 mg |
无 |
未标示 |
Biosearch Highway Company Ltd. |
SH 15.6 mg/粒 |
| 阿娇魔鬼组合胶囊(小鬼魔鬼组合) |
400 mg |
无 |
2014/08/10 |
未标示 |
SH 3.1 mg/粒,酚酞29.1 mg/粒 |
| 阿娇魔鬼组合胶囊(大鬼魔鬼组合) |
800 mg |
无 |
2014/08/10 |
未标示 |
SH 21.3 mg/粒 |
| 魔鬼瘦身胶囊(黄色胶囊) |
无 |
无 |
未标示 |
未标示 |
呋塞米80.8 mg/粒,酚酞3.8 mg/粒 |
| 魔鬼瘦身胶囊(蓝色胶囊) |
无 |
无 |
未标示 |
未标示 |
呋塞米48.9 mg/粒、酚酞3.0 mg/粒 |
| USA purchasing(白药瘦身胶囊) |
无 |
无 |
未标示 |
未标示 |
SH 21.4 mg/粒,酚酞23.7 mg/粒 |
| USA purchasing(红药瘦身胶囊) |
无 |
无 |
未标示 |
未标示 |
SH 17.8 mg/粒,酚酞16.7 mg/粒 |
| USA purchasing美国进口减肥胶囊(强效型小白) |
无 |
无 |
未标示 |
未标示 |
SH 26.7 mg/粒 |
| USA purchasing美国进口减肥胶囊(普通型小红) |
无 |
无 |
未标示 |
未标示 |
SH 24.7 mg/粒,酚酞39.0 mg/粒 |
| 老中医百年秘方纯中药瘦身胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 4.5 mg/粒,酚酞66.0 mg/粒 |
| 紫色胶囊(克莱恩减肥胶囊) |
无 |
无 |
未标示 |
未标示 |
SH 30.6 mg/粒,酚酞0.6 mg/粒,咖啡因1.2 mg/粒 |
| 依特美牌纤美丽减肥冲剂 |
20 g/袋 |
卫食健字(1997)第822号 |
20150702 |
委托商:西安天奇天然药物研究开发有限公司;受托商:广东传奇医药科技有限公司 |
未检出 |
| 古方纯中药(强效瘦身型红色软胶囊) |
无 |
国食健字G20110551 |
未标示 |
未标示 |
未检出 |
| 古方纯中药(强效瘦身型绿色胶囊) |
无 |
国食健字G20110551 |
未标示 |
未标示 |
SH 9.9 mg/粒 |
| 红色胶囊(院线溶脂瘦身型) |
无 |
无 |
未标示 |
未标示 |
呋塞米45.0 mg/粒 |
| 华纳兄弟牌茶多酚荷叶胶囊 |
0.4 g |
国食健字G20050373 |
20150901 |
委托生产单位:陕西安恒信健康产业有限公司;受托生产单位:西安大爱健康产业有限公司 |
未检出 |
| OD ORANGE DIAMONDS(OD钻石橙)橙色胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 7.7 mg/粒,酚酞29.3 mg/粒 |
| OD ORANGE DIAMONDS(OD钻石橙)蓝色胶囊 |
无 |
无 |
未标示 |
未标示 |
SH 8.3 mg/粒,酚酞28.7 mg/粒 |
| COURONNE PERDRE DU POIDS(片剂) |
无 |
无 |
未标示 |
未标示 |
SH 0.5 mg/粒,咖啡因8.3 mg/粒 |
|
表 3 样品信息及检出成分(n=3)
Table 3 Sample information and detected components (n=3)
|
进一步分析表 3发现,明确标示生产厂家的25批样品中检出18批添加了化学药,阳性率为72%,其中检出2种的3批。而未明确标示生产厂家的61批样品中检出56批添加了化学药,阳性率为91.8%,其中检出2种的19批,3种的1批。虽然86批抽检样品中非法添加形势严峻,但相较而言,未明确标示生产厂家的产品中非法添加更严重。
3 讨论 本实验利用MRM检测模式建立了一个操作简便、适用范围广、灵敏度高、准确、快速的高通量多成分检测减肥类中成药和保健食品中添加化学药物的平台,分4个时间段对15个减肥类化学药物进行质谱扫描,满足了质谱定量要求,大大提高了定量准确性。不仅可准确检测胶囊剂和颗粒剂样品中添加的化学减肥药,也可用以其他剂型中成药和保健食品的快速筛查。由于中成药成分复杂,仅按质量标准检测不易识别添加的化学药物,且减肥类中成药及保健食品中可添加的化学药越来越多,需要对检测方法不断更新并增加可筛选化学药物的数量,以适应现实检测的需要。本法集快速初筛技术、验证技术和准确定量于一体,既节省了大量的人力物力,又极大地提高了非标检测工作的效率,为药品监管及规范保健食品市场提供技术支撑,具有重要的社会意义。
参考文献
| [1] |
朱健, 裘一婧, 沈国芳. 中药中非法添加问题研究现状与分析[J]. 中草药 , 2014, 45 (3) :437–442.
|
| [2] |
He X, Xi C, Tang B, et al. Simultaneous determination of 30 hormones illegally added to anti-ageing functional foods using UPLC-MS/MS coupled with SPE clean-up[J]. Food Addit Contam Part A Chem Anal Control Expo Risk Assess , 2014, 31 (10) :1625–1638.
DOI:10.1080/19440049.2014.953602 |
| [3] |
Woo H, Kim J W, Han K M, et al. Simultaneous analysis of 17 diuretics in dietary supplements by HPLC and LC-MS/MS[J]. Food Addit Contam Part A Chem Anal Control Expo Risk Assess , 2013, 30 (2) :209–217.
DOI:10.1080/19440049.2012.738939 |
| [4] |
Reepmeyer J C, Woodruff J T. Use of liquid chromatography-mass spectrometry and a hydrolytic technique for the detection and structure elucidation of a novel synthetic vardenafil designer drug added illegally to a "natural" herbal dietary supplement[J]. J Chromatogr A , 2006, 1125 (1) :67–75.
DOI:10.1016/j.chroma.2006.05.018 |
| [5] |
Yamamoto S, Sumioka S, Fujioka M, et al. Study on detection of drugs in slimming health foods using GC-MS/MS[J]. Shokuhin Eiseigaku Zasshi , 2011, 52 (6) :363–369.
DOI:10.3358/shokueishi.52.363 |
| [6] |
Li Y, Zhang H, Hu J, et al. A GC-EI-MS-MS method for simultaneous determination of seven adulterants in slimming functional foods[J]. J Chromatogr Sci , 2012, 50 (10) :928–933.
DOI:10.1093/chromsci/bms092 |
| [7] |
朱健, 裘一婧, 沈国芳. UPLC-MS/MS法快速检测减肥类保健品中13种非法添加化学成分[J]. 中草药 , 2014, 45 (4) :509–515.
|
| [8] |
朱峰, 阮丽萍, 马永建, 等. 超高效液相色谱-串联质谱联用法同时检测降糖类和减肥类保健品中20种非法添加的化学降糖药物[J]. 色谱 , 2014, 32 (1) :13–20.
|
| [9] |
黄越燕, 屠婕红, 徐宏祥, 等. UPLC-MS/MS法快速测定中药及保健食品中非法添加17种抗炎镇痛类化学药的研究[J]. 中草药 , 2016, 47 (2) :246–254.
|
| [10] |
白雪, 张亚锋, 芸艾, 等. HPLC-MS/MS法快速检测中成药及保健食品中6种减肥类非法添加化学成分[J]. 西北药学杂志 , 2016, 31 (1) :48–50.
|
| [11] |
朱健, 裘一婧, 沈国芳. UPLC-MS/MS法快速检测减肥类保健品中13种非法添加化学成分[J]. 中草药 , 2014, 45 (4) :509–515.
|
| [12] |
郝刚, 顾炳仁. UPLC-MS/MS法快速检测减肥类保健食品中5种非法添加化学成分[J]. 中国医药科学 , 2014, 4 (17) :106–117.
|
| [13] |
黎银波, 孟庆玉, 钟庆元, 等. UPLC-MS/MS法快速检测减肥类保健食品中7种违法添加的药物[J]. 中南药学 , 2012, 10 (10) :752–756.
|
| [14] |
夏威标, 水冰洁, 丁兴红. 快速高分离液相色谱-质谱联用法测定减肥药中3种违禁成分的含量[J]. 浙江中医药大学学报 , 2015, 39 (8) :615–620.
|
| [15] |
钮正睿, 张庆生, 曹进, 等. 超高效液相色谱-串联质谱法快速检测保健食品中非法添加的6种减肥类化学成分的研究[J]. 中国实验方剂学杂志 , 2014, 20 (18) :91–94.
|

 2016, Vol. 47
2016, Vol. 47


