2. 江苏省中药资源产业化过程协同创新中心, 江苏 南京 210023
2. Jiangsu Collaborative Innovation Center of Chinese Medicinal Resources Industrialization, Nanjing 210023, China
天麻Gastrodiae Rhizoma为兰科植物天麻Gastrodia elata Bl. 的干燥块茎,列于《神农本草经》上品,为我国传统贵重药材。天麻性甘、平,归肝经,有平肝息风止痉的功效,临床上主要用于头痛眩晕、肢体麻木、小儿惊风、癫痫抽搐、破伤风等的治疗[1]。天麻的主要成分为酚类化合物及其苷、多糖、甾醇等[4, 5, 6, 7, 8]。其中天麻素是主要有效成分,多项药理研究表明天麻素具有镇痛的作用,临床上多用于治疗头痛、眩晕、神经痛、肢体麻木、手足不遂、冠心病、心绞痛等,因此包括《中国药典》2010年版在内的多项标准都是以天麻素作为指标评价天麻饮片的质量。目前,也有较多文献指出天麻中所含香荚兰醇、香荚兰醛、对羟基苯甲醇、对羟基苯甲醛及巴利森苷类成分均具较强的生理活性[9, 10, 11, 12, 13, 14],表明仅采用单一指标测定天麻素量的方法,对天麻内在质量的判断不够全面。
本研究建立了HPLC-MS法同时测定天麻中天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C和巴利森苷A 8个成分的量,以期客观、综合评价天麻饮片的质量,并为其药效物质基础研究提供方法学依据。
1 仪器与试药Shimadzu LC 20A型高效液相色谱仪;AB Sciex Qtrap 5500型三重四级杆线性离子阱质谱仪,配有ESI离子源,Analyst 1.5.1 Software工作站,美国AB公司。Shimadzu Librorael-40SM型电子分析天平,精确到0.01 mg。
天麻素(批号00256-2013)、香荚兰醇(批号01083-2013)、香荚兰醛(批号01147-2013)对照品,购自南京泽朗医药科技有限公司,对羟基苯甲醇(批号2014-0192)、对羟基苯甲醛(批号2014-0193)、巴利森苷A(批号2014-0078)、巴利森苷B(批号2014-0079)、巴利森苷C(批号2014-0080)对照品,购自南京森贝伽生物科技有限公司;上述对照品经HPLC法检测,质量分数均大于98.0%。甲醇为色谱纯,水为纯净水,其余试剂均为分析纯。
收集产地为安徽(编号为S1~S3)、云南(编号为S4~S6)、陕西(编号为S7~S9)、贵州(S10~S11)的11批天麻饮片,均经南京中医药大学吴啟南教授鉴定为兰科天麻属植物天麻Gastrodia elata Bl. 的干燥块茎。
2 方法与结果 2.1 色谱条件[15]Hypersil C18色谱柱(250 mm×4.6 mm,5 μm);流动相为0.5%醋酸水溶液(A)-0.5%醋酸甲醇溶液(B),线性梯度洗脱:0~10 min,98% A;10~60 min,98%~60% A;60~75 min,60% A;体积流量0.8 mL/min;检测波长270 nm;柱温30 ℃;进样量20 μL。
2.2 质谱条件离子源为电喷雾离子化源(ESI);多反应监测模式(MRM)进行定量分析;采用负离子检测模式;源喷射电压(IS)为-4 500 V;离子源温度为550 ℃;雾化气(N2)压力为379.28 kPa(55 psi);辅助气(N2)压力为379.28 kPa(55 psi);气帘气(N2)压力为241.36 kPa(35 psi)。接口加热,全程通入氮气,MRM模式定量。监测的离子对、驻留时间(Dwell)、解簇电压(DP)、碰撞室射出电压(CXP)和碰撞能量(CE)等见表 1。8个被测成分的多重反应监测色谱图见图 1。
| 表 1 8种成分的质谱数据 Table 1HPLC-ESI-MSn data of eight components |
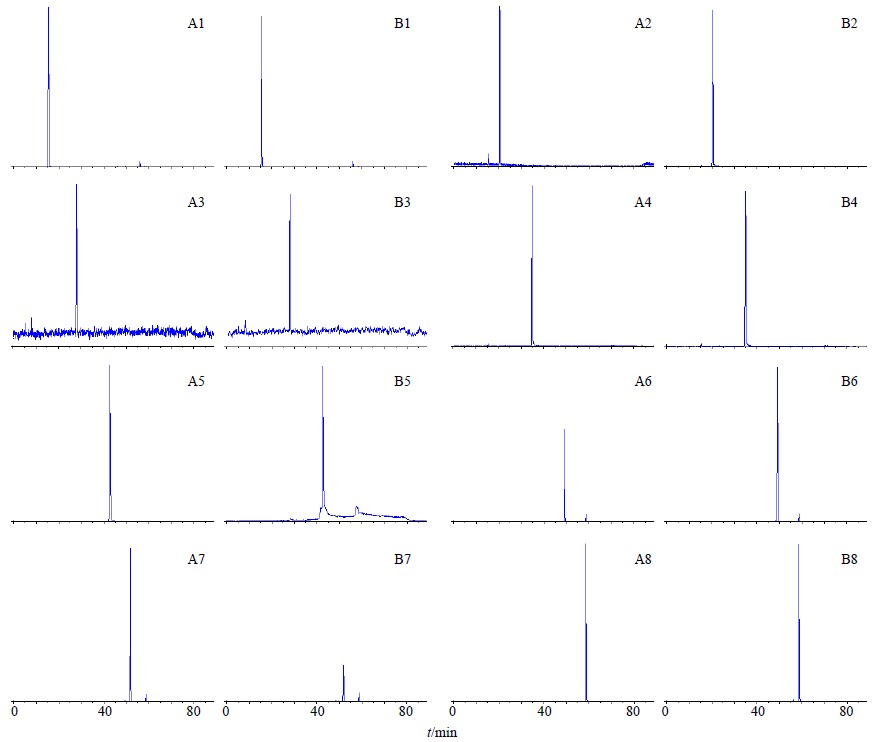 |
1-天麻素 2-对羟基苯甲醇 3-香荚兰醇 4-对羟基苯甲醛 5-香荚兰醛 6-巴利森苷B 7-巴利森苷C 8-巴利森苷A 1-gastrodin 2-p-hydroxybenzyl alcohol 3-vanillyl alcohol 4-vanillin 5-p-hydroxybenzaldehyde 6-parishin B 7-parishin C 8-parishin A 图 1 对照品溶液 (A) 和供试品溶液 (B) 8种成分的MRM色谱图Fig.1 MRM chromatograms of eight components in reference solution (A) and sample solution (B) |
取各对照品适量,加水制成含天麻素120.60 μg/mL、对羟基苯甲醇184.20 μg/mL、香荚兰醇3.06 μg/mL、对羟基苯甲醛10.60μg/mL、香荚兰醛0.69 μg/mL、巴利森苷B 95.536 mg/mL、巴利森苷C 445.73 μg/mL、巴利森苷A 311.66 μg/mL的混合对照品溶液。
2.3.2 供试品溶液的制备[1]取本品粉末(过3号筛)约2 g,精密称定,置具塞锥形瓶中,精密加入稀乙醇50 mL,放置2 h,时时振摇,称定质量,加热回流3 h,放冷,再称定质量,用稀乙醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,浓缩至近干,残渣加甲醇-水(3∶97)混合溶液溶解,转移至25 mL量瓶中。用甲醇-水(3∶97)混合溶液稀释至刻度,摇匀,滤过,取续滤液,即得。
2.4 方法学考察 2.4.1 线性关系、检测限(LOD)与定量限(LOQ)精密量取混合对照品溶液4 mL,置于5 mL量瓶中,加水稀释至刻度。用倍比稀释的方法以甲醇-水(3∶97)混合溶液制成系列对照品溶液,在“2.1”项色谱条件下,分别进样20 μL,每个质量浓度进3针,测定峰面积值。以峰面积平均值与质量浓度进行线性回归。将混合对照品溶液用水不断稀释后分析,得到8种成分的LOD值(S/N≈3)和LOQ值(S/N≈10)。结果见表 2。
| 表 2 8种成分的回归方程及LOD、LOQ值 Table 2Regression equations and values of LOD and LOQ of eight components |
取编号为S7的天麻饮片制备的供试品溶液,进样20 μL,连续进样6次,依法测定,分别记录峰面积,计算RSD。结果天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C、巴利森苷A峰面积的RSD分别为2.47%、3.53%、1.22%、2.84%、2.99%、3.06%、1.60%和0.54%。
2.4.3 稳定性试验取编号为S7的天麻饮片制备的供试品溶液,于0、1、2、4、6、8 h分别进样20 μL,依法测定,分别记录峰面积,计算RSD。结果天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C、巴利森苷A峰面积的RSD分别为2.71%、1.92%、3.48%、1.50%、2.33%、2.61%、3.09%和1.18%,表明供试品溶液中8种成分在8 h内稳定。
2.4.4 重复性试验取编号为S7的天麻饮片6份,每份2 g,按“2.3.2”项下方法制备供试品溶液,依法测定并计算6份样品中8种成分的平均质量分数和RSD。结果,天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C、巴利森苷A的平均质量分数分别为2.573、4.101、0.075 75、0.272、0.018 55、22.265、10.368、7.964 mg/g,RSD分别为2.78%、1.90%、3.33%、3.82%、2.66%、4.05%、2.00%、1.52%。
2.4.5 加样回收率试验取编号为S7的天麻饮片6份,每份1 g,精密称定,精密加入混合对照品溶1 mL(含天麻素2.293 mg/mL、对羟基苯甲醇0.364 mg/mL、香荚兰醇0.082 6 mg/mL、对羟基苯甲醛0.311 mg/mL、香荚兰醛0.199 mg/mL、巴利森苷B 24.261 mg/mL、巴利森苷C 12.836 mg/mL、巴利森苷A 7.281 mg/mL),按“2.3.2”项下方法制备供试品溶液,依法测定并计算6份样品中8种成分的平均加样回收率和RSD。结果,天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C、巴利森苷A的平均加样回收率分别为97.73%、95.56%、97.55%、94.51%、100.12%、102.70%、99.30%、96.81%,RSD分别为2.39%、2.14%、3.03%、1.07%、2.55%、1.91%、1.15%、1.35%。
2.5 样品测定取11批天麻饮片,每批3份,按“2.3.2”项下方法分别制备供试品溶液,各进样20 μL,以各成分峰面积按外标法对其中的天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C、巴利森苷A进行测定,并计算每批3份的平均质量分数,结果见表 3。
| 表 3 11批饮片中8种成分的质量分数 Table 3Determination of eight components in Gastrodiae Rhizoma |
结合文献报道[15],以《中国药典》2010年版天麻定量测定中提取方法为依据,本实验比较了超声提取、加热回流提取等不同提取方式,结果发现加热回流提取优于超声提取,且2次加热回流提取之间间隔较长时间优于2次加热回流提取连续进行。
本实验结果表明,天麻饮片中所含天麻素、对羟基苯甲醇、香荚兰醇、对羟基苯甲醛、香荚兰醛、巴利森苷B、巴利森苷C、巴利森苷A这8种成分的量差异较大,同一个成分的量相差甚至十几至几十倍,分析其原因,主要有(1)产地的影响,我国幅员辽阔,适宜天麻种植的产区较多,不同地区的气候、光照、海拔等环境因素不尽相同,对天麻的生长及其生长过程中各种次生代谢产物的累积也不相同。(2)产地加工的影响,中药材采收后均需在产地进行一定的初加工处理,以便保存其中的主要成分和后续的运输、贮藏,但是不同地区的产地加工方法也不相同,如有的地区对天麻采用蒸的方法,有的地区采用煮的方法,甚至有的地区还用硫磺进行熏蒸。(3)炮制工艺的影响,饮片来源于药材,又不同于药材,还需要经过一定的炮制工艺。不同地区的炮制习惯、不同饮片厂的炮制工艺具体参数和炮制设备也都有所差异,这也会造成各种成分量的差异。此外需要注意的是,受试样品中仍有少数几批的天麻素质量分数低于《中国药典》2010年版的规定(不少于0.20%),说明目前市场上销售的天麻质量问题不容忽视。
从化学结构上观察,巴利森苷A、B、C均为天麻素和柠檬酸结合而成的酯类。本实验结果表明,其量较高,大多数均高于天麻素,有的甚至超出10倍以上。此外,还有一些尚未确定结构的化合物在饮片中亦有较高的量。上述这些成分的存在或其量高低可能会对天麻饮片的质量产生影响。因此,还需对这些质量分数较高的化合物进行结构确证和归属,探索它们对天麻药效的贡献及它们与天麻素之间的内在转化关系,并为进一步完善天麻的质量控制方法提供技术支持和研究基础。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 周 俊, 杨雁宾, 杨崇仁. 天麻的化学研究 [J]. 化学学报, 1979, 37(3): 183-189. |
| [3] | 王 莉, 王艳萍, 肖红斌, 等. 天麻化学成分研究 [J]. 中草药, 2006, 37(11): 1635-1637. |
| [4] | 刘艳华. 天麻素注射液治疗紧张性头痛96例临床疗效观察 [J]. 中国卫生产业, 2013, 22(16): 74-75. |
| [5] | 李惠萍. 天麻素治疗眩晕症疗效观察 [J]. 医学信息, 2011, 24(3): 1329. |
| [6] | 苗 凯, 王 美, 谢 袆. 天麻素治疗冠心病心绞痛临床效果的观察 [J]. 天津药学, 2009, 21(6): 26-27. |
| [7] | 官昌伦, 曹光宇, 熊 波, 等. 天麻素对偏头痛患者疼痛程度的影响及临床疗效的观察 [J]. 内蒙古中医药, 2014, 33(8): 2-3. |
| [8] | 贾 玉. 天麻素治疗血管神经性头痛临床疗效 [J]. 中国现代药物应用, 2015, 9(1): 99-100. |
| [9] | Gao L W, Li W Y, Zhao Y L, et al. The cultivation, bioactive components and pharmacological effects of Armillaria mellea [J]. Afr J Biotechnol, 2009, 8(25): 7383-7390. |
| [10] | 毕 天, 李彦文, 段靖远, 等. 天麻抗老年期痴呆有效成分的研究进展 [J]. 中医药导报, 2013, 19(2): 103-106. |
| [11] | Ha J H, Shin S M, Lee S K, et al. In vitro effects of hydroxybenzaldehydes from Gastrodia elata and their analogues on GABA ergic neurotransmission and a structure-activity correlation [J]. Planta Med, 2001, 67(9): 877-880. |
| [12] | Junko H, Toshikazu S, Shigeyoshi D, et al. Phenolic compounds from Gastrodia Rhizome and relaxant effects of related compounds on isolated smooth muscle preparation [J]. Phytochemistry, 2002, 59(5): 513-519. |
| [13] | 李秀芳, 代 蓉, 李国花, 等. 天麻成分对羟基苯甲醛抗血小板聚集作用及急性毒性研究 [J]. 天然产物研究与开发, 2013, 25(3): 317-320. |
| [14] | 李 艳, 蒋 石, 郭营营, 等. 天麻成分对羟基苯甲醇抗实验性脑血栓形成及抗炎作用研究 [J]. 昆明医科大学学报, 2015, 36(1): 28-31. |
| [15] | 王 莉. 天麻化学物质基础及质量控制方法研究 [D]. 大连: 中国科学院研究生院 (大连化学物理研究所), 2007. |
 2015, Vol. 46
2015, Vol. 46


