2. 桂林三金药业股份有限公司, 广西 桂林 541004;
3. 广西医科大学药学院, 广西 南宁 530021
2. Guilin Sanjin Pharmaceutical Co., Ltd., Guilin 541004, China;
3. School of Pharmacy, Guangxi University of Medicine, Nanning 530021, China
剑叶龙血树系百合科(Liliaceae)植物剑叶龙血树Dracaena cochinchinensis (Lour.) S. C. Chen的含脂木材,收载于《广西壮族自治区壮药质量标准》,壮药名为榧勒垄,具有活血散瘀、定痛止血、敛疮生肌等功效,用于跌打损伤、瘀血作痛、妇女气血凝滞、外伤出血和脓疮久不收口[1]。剑叶龙血树用作提取龙血竭的原料,化学成分研究表明,其主要活性成分为一系列多酚类化合物,主要包括以龙血素A、龙血素B为代表的二氢查耳酮类,以白藜芦醇、紫檀茋为代表的二苯乙烯类和以7,4′-二羟基黄酮为代表的黄酮类成分。目前有关剑叶龙血树的质量评价大多仅限于以龙血素A和/或龙血素B为指标的定量测定研究[2]。
本实验通过对比剑叶龙血树溶液在经1,1-二苯基-2-三硝基苯肼自由基(DPPH)反应前后,溶液中所含白藜芦醇、7,4′-二羟基黄酮、龙血素A、龙血素B、紫檀茋5个代表性成分峰面积衰减情况,计算清除率以反映化合物的抗氧化能力,初步探讨剑叶龙血树抗氧化的谱效关系,为建立谱-效相关的剑叶龙血树质量控制标准提供理论支持。
1 材料 1.1 仪器美国Waters 2690色谱仪,996DAD检测器,Empower2液相色谱工作站;超声波清洗仪(Branson bug 40-60,上海必能信公司),AS404电子天平(Metller Tolite)。
1.2 试药剑叶龙血树药材购自广西中医学院制药厂(批号110303),将桂林三金药业股份有限公司邹节明教授鉴定为剑叶龙血树Dracaena cochinchinensis (Lour.) S. C. Chen 的含脂木材。龙血素A(批号111660-200402)、龙血素B(批号111558-200405)、白藜芦醇(批号111535-200502)对照品均购自中国食品药品检定研究院,紫檀茋和7,4′-二羟基黄酮对照品均为自制,HPLC归一化法检测质量分数均>98%,DPPH购自Sigma公司,甲醇、乙腈(色谱纯);水(超纯水);磷酸(分析纯),其他试剂均为分析纯。
2 方法与结果 2.1 色谱条件色谱柱Phenomenex lura C18(250 mm×4.6 mm,5 μm);流动相为甲醇(A)-乙腈(B)-0.2%磷酸溶液(C),梯度洗脱程序:0~20 min,30% A、10% B、60%C,21~70 min,39% A、13% B、48% C;体积流量为1.0 mL/min;柱温为35 ℃;检测波长为306 nm。理论板数按白藜芦醇计算应不低于4 000[3]。
2.2 对照品溶液的制备精密称取白藜芦醇、7,4-二羟基黄酮、龙血素A、龙血素B和紫檀茋对照品适量,加甲醇制成各对照品质量浓度为0.02 mg/mL的混合对照品溶液。
2.3 供试品溶液的制备取剑叶龙血树粉末约20 mg,精密称定,置25 mL棕色量瓶中,加三氯甲烷20 mL,超声处理20 min,滤过,滤液挥干,加甲醇溶解定容至10 mL棕色量瓶中,从中精密吸取5 mL,置另一10 mL棕色量瓶中,分别加甲醇和0.1 mol/L的DPPH甲醇溶液定容至刻度,分别作为DPPH反应前供试品溶液和DPPH反应后供试品溶液。
2.4 样品测定精密吸取混合对照品溶液和2种供试品溶液各10 μL,注入液相色谱仪,记录60 min的色谱图,见图 1。
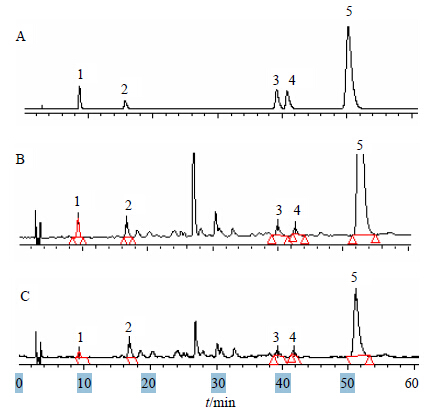 |
1-白藜芦醇 2-7,4′-二羟基黄酮 3-龙血素B 4-龙血素A 5-紫檀茋 1-resveratrol 2-7,4′-dihydroxyflavone 3-loureirin B 4-loureirin A 5-pterstilbene 图 1 混合对照品 (A)、DPPH反应前供试品 (B) 及DPPH反应后供试品(C) 溶液HPLC色谱图Fig.1 HPLC of mixed reference substances (A),samplewithout DPPH (B),and sample with DPPH (C) |
通过测得的DPPH反应前后供试品溶液中各相应对照品峰面积值,计算参与反应的各成分的清除率,评价各成分的抗氧化能力大小,反应前后供试品溶液相应的抗氧化成分的峰面积数据见表 1。
| 表 1 剑叶龙血树主要抗氧化成分峰面积衰减情况及抗氧化作用评价 Table 1Changes of peak area of antioxidants and evaluation of antioxidant capacity in D. cochinchinensis |
清除率=1-A/A0
A0为DPPH反应前供试品溶液相关化合物峰面积,A为DPPH反应后的供试品溶液对应化合物的峰面积 2.6 构效关系分析清除率计算结果显示,虽然同为二苯乙烯类成分,仅取代基不同,但测得抗氧化能力紫檀茋(73.19%)>白藜芦醇(71.10%),几乎相当;虽然同为二氢查耳酮类成分,但测得抗氧化能力龙血素B(39.01%)>龙血素A(12.14%),有显著差异。结合化学结构分析,二苯乙烯类的-OCH3取代较-OH取代活性强,根据分子轨道理论,作为1个共轭体系,白藜芦醇形成自由基与其4′位羟基失去氢质子容易程度有关,而紫檀茋因3,5位羟基被甲基化后,供电子能力增强,通过共轭效应,4′位羟基失去氢质子更容易,故而清除自由基能力略强;虽然同为二氢查耳酮,B环上3个-OCH3取代的龙血素B比2个-OCH3取代的龙血素A的抗氧化能力更强,可能因为共轭链断开,空间构象变为主要的影响因素,因为龙血素B的C-2,4,6位甲氧基取代形成对称结构,使其A环垂直于羰基及B环所在的平面,当与自由基发生清除反应时,更容易发生空间结构改变形成分子内氢键,产生能量供发生自由基清除反应,故而抗氧化能力有显著差异[4];而7,4′-二羟基黄酮虽然在7,4′位有-OH取代,但因其B环上缺乏邻酚羟基,故而未显示相关的抗氧化活性[5]。因此,剑叶龙血树中的二苯乙烯类及二氢查耳酮类成分是其主要的抗氧化活性成分,而7,4′-二羟基黄酮未显示明显的体外抗氧化活性,相关研究可为建立谱-效相关剑叶龙血树质量控制标准提供较好理论支持。
结果表明二苯乙烯类、二氢查耳酮类成分为剑叶龙血树中主要抗氧化活性成分;比较清除率,各主要成分的抗氧化能力强弱依次为紫檀茋>白藜芦醇>龙血素B>龙血素A>7,4′-二羟基黄酮。
3 讨论本研究建立的HPLC-DPPH评价剑叶龙血树中主要抗氧化成分方法,可以直观初步量化各成分的抗氧化能力,为筛选药效指标成分及建立全面谱-效相关质量标准奠定基础。
考察了经DPPH反应后,不同反应时间点下各化合物的峰面积值,结果测得各化合物峰面积值与反应后初次测定值变化很小,表明供试品溶液的稳定性良好,提示DPPH反应可能是在短时间内完成的,说明该方法用于评价复杂中药成分的抗氧化能力具有可行性。
结合抗氧化能力测定及构效关系分析,剑叶龙血树中的二苯乙烯类成分是其主要抗氧化活性成分,故目前药材及成品质量控制标准仅对其中的二氢查耳酮类成分进行测定,尚不能有效评价其质量,亟待建立同步评价多个不同类成分的特征图谱以对其进行更全面的质量控制。
| [1] | 广西壮族自治区壮药质量标准 [S]. 2008. |
| [2] | 闵建国, 周艳林, 邹准, 等. HPLC法测定壮药剑叶龙血树中7-羟基-4'-甲氧基黄烷和紫檀茋 [J]. 中草药, 2013, 44(17): 2471-2473. |
| [3] | 周艳林, 蒋受军, 文建文, 等. 龙血竭特征成分对照指纹图谱研究 [J]. 中华中医药杂志, 2012, 27(12): 3080-3082. |
| [4] | 胡迎庆, 刘岱琳, 周运筹. 天然二氢查耳酮类化合物的生物活性 [J]. 国外医药: 植物药分册, 2002, 17(6): 241-244. |
| [5] | Seyoum A, Asres K, El-Fiky F K. Structure-radical scavenging activity relationships of flavonoids [J]. Phytochemistry, 2006, 67(18): 2058-2070. |
 2015, Vol. 46
2015, Vol. 46


