2. 上海医药工业研究院 创新药物与制药工艺国家重点实验室, 上海 200040
2. State Key Laboratory of New Drug and Pharmaceutical Process, Shanghai Institute of Pharmaceutical Industry, Shanghai 200040, China
南五味子属Kadsura Kaempf. ex Juss.,隶属于木兰科(Magnoliaceae)五味子亚科(Schisandroideae),近年来也有许多植物分类学家倾向于把五味子科单独作为一科进行分类。南五味子属有植物29种,主产于亚洲东部和东南部。我国有10种,产于我国东南部和西南部,包括云南、贵州、四川、广东、广西、福建等省。南五味子属植物的茎在民间通常称为风藤、紫金皮等,主要用于活血止痛、祛风除湿等[1]。南五味子的根茎作为滇鸡血藤被《中国药典》2010年版收载,以其为原料的制剂复方滇鸡血藤膏也被《中国药典》2010年版收载,主治瘀血阻络、肾失所养导致的月经不调[2]。现代药理研究表明,该属植物具有抗白血病、抗氧化、抗乙型肝炎、拮抗血小板活化因子(PAF)等作用。近年来,该属植物抗肿瘤、抗病毒方面的活性尤其受人关注。这些药理活性主要与其含有 的木脂素和三萜类成分有关。值得一提的是,因《中国药典》2010年版收载的南五味子药材其原植物属于五味子科五味子属Schisandra Michx.,为避免混淆,有学者建议取消Kadsura的中文名(南五味子属),更名为冷饭藤属[3]。
20世纪80年代以来国内外学者对南五味子属植物的化学成分和药理作用进行了一系列的研究,取得了一定的进展。本文主要对2003年至今报道的南五味子属植物化学成分和药理作用进行综述。
1 化学成分木脂素和三萜类为南五味子属植物的特征性化学成分。此外该属植物还含有少量倍半萜类成分。
1.1 木脂素类成分木脂素是南五味子属植物中的主要活性成分,根据其骨架类型可分为5大类:(1)联苯环辛烯类(dibenzocyclooctadienes);(2)螺苯骈呋喃型联苯环辛烯类(spirobenzofuranoid dibenzocyclooctadienes);(3)芳基四氢萘类(aryltetralins);(4)二苄基丁烷类(diarylbutanes);(5)四氢呋喃类(tetrahydro- furans)。此外,南五味子属植物还含有少量新木脂素(neolignans)类化合物。
1.1.1 联苯环辛烯类南五味子属植物中分得的木脂素类化合物中主要为联苯环辛烯类木脂素。联苯环辛烯类木脂素其基本母核为联苯环辛烯(I)。因联苯旋转受阻,引起分子的立体异构,联苯环辛烯木脂素分为联苯S和R构型2个系列(II和III),加上分子中可存在其他手性中心,故本类化合物的立体异构较多,其中的八元环构象多为扭曲的船椅式(TBC,IV),部分为扭曲的船式(TB,V)。此外,黑老虎中还发现一些6,9氧桥联苯环辛二烯(VI)。南五味子属植物中联苯环辛烯类木脂素的主要结构骨架及构象见图 1。联苯环上除了C-4和C-11位有2个芳质子之外,其他位置(C-1~3和C-12~14)均为含氧取代,包括甲氧基、亚甲二氧基、羟基和酯基[4]。近年来,从南五味子属植物中分到的联苯环辛烯类木脂素类成分结构见图 2和表 1。
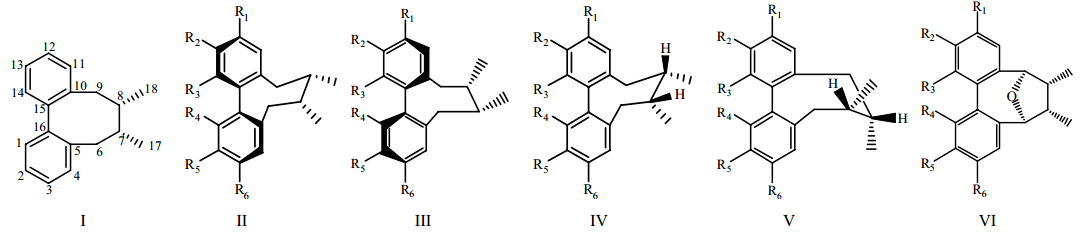 | 图 1 南五味子属植物中联苯环辛烯类木脂素的主要结构骨架及构象Fig. 1 Structural skeleton and conformation of dibenzocyclooctadiene lignans from plants of Kadsura Kaempf. ex Juss. |
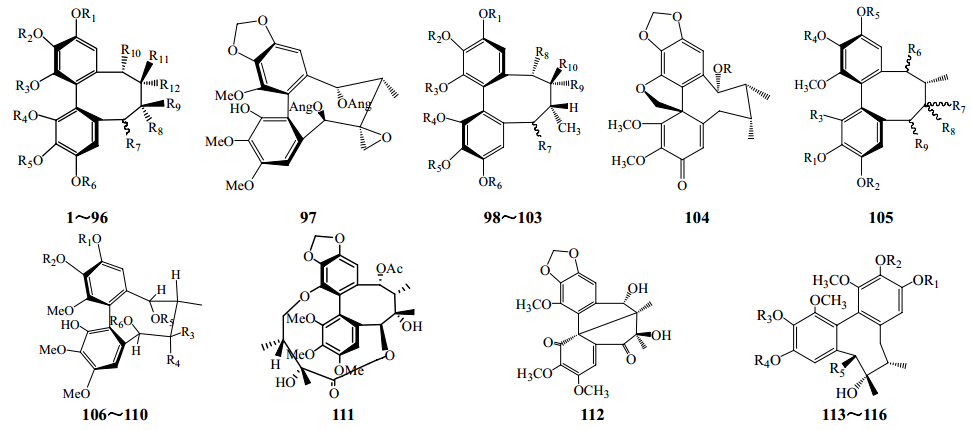 | 图 2 南五味子属植物中常见联苯环辛烯类木脂素类化合物结构Fig. 1 Structures of dibenzocyclooctadiene lignanoids inplants of Kadsura Kaempf. ex Juss. |
| 表 1 从南五味子属植物中分离得到的联苯环辛烯类木脂素类化合物 Table 1 Dibenzocyclooctadiene lignanoids isolated from plants of Kadsura Kaempf. ex Juss. |
1.1.2 螺苯骈呋喃型联苯环辛烯类
螺苯联苯环辛烯木脂素是在联苯环辛烯木脂素的基础上,以C-16为中心,与其他含氧取代基形成1个新的呋喃环,同时含C-16的一个芳环烯酮化。从南五味子属植物中分得的此类化合物中的螺环多数由C-14与C-16的含氧取代基形成,其芳环上的烯酮化有α,β,α′,β′-二烯酮和α,β,γ,δ-二烯酮2种形式(VII和VIII,图 3)[4]。近年来,从南五味子属植物中分到的螺苯骈呋喃型联苯环辛烯类成分见图 4和表 2。
 | 图 3 南五味子属植物中螺苯骈呋喃型木脂素的主要结构骨架Fig. 3 Structural skeleton of spirobenzofuranoid dibenzocy-clooctadiene lignans from plants of Kadsura Kaempf. ex Juss. |
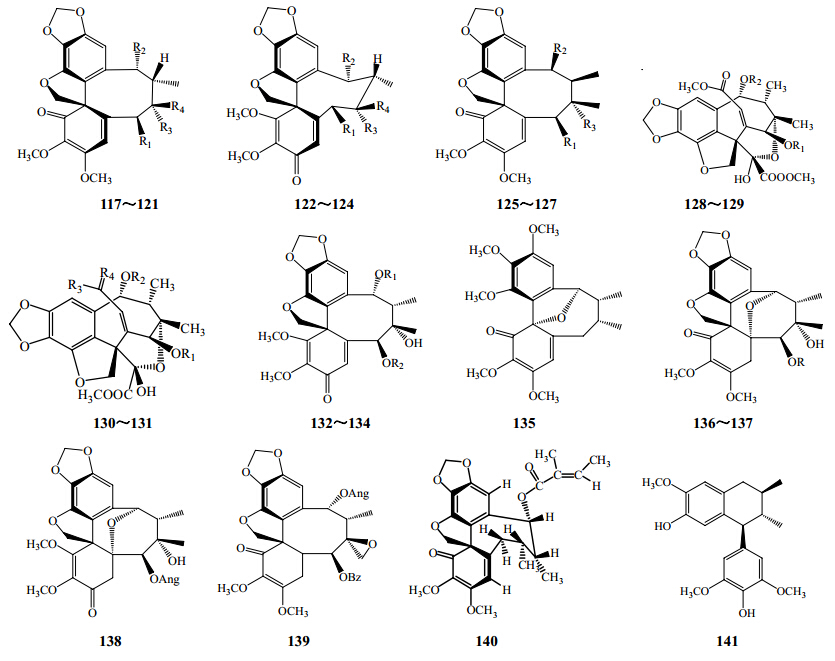 | 图 4 南五味子属植物中螺苯骈呋喃型联苯环辛烯类木脂素结构Fig. 4 Structures of spirobenzofuranoiddibenzocyclooctadiene lignanoids in plants of Kadsura Kaempf. ex Juss. |
| 表 2 南五味子属植物中分离得到的螺苯骈呋喃联苯环辛烯类木脂素类成分 Table 2 Spirobenzofuranoiddibenzocyclooctadiene lignanoids isolated from plants of Kadsura Kaempf. ex Juss. |
1.1.3 芳基四氢萘类
近年来,从南五味子属植物中分离并鉴定的芳基四氢萘类成分有isolariciresinol-9-O-β-D-xylopyranoside(142)[38]和kadsuralignan C(143)[11],结构见图 5。
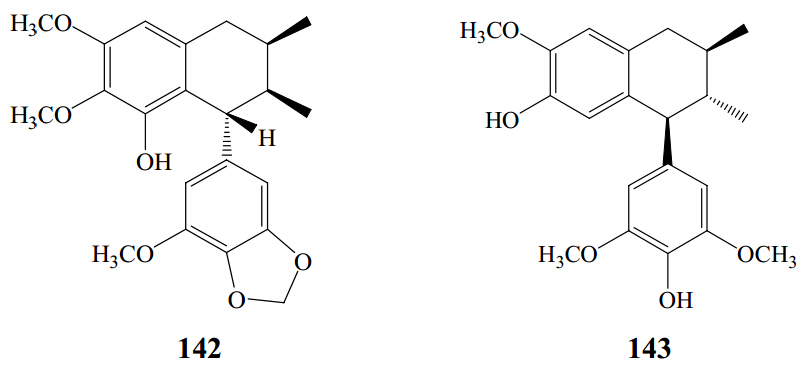 | 图 5 南五味子属植物中芳基四氢萘类木脂素成分结构Fig. 5 Structures of aryltetralin lignanoids in plants of Kadsura Kaempf. ex Juss. |
1.1.4 二苄基丁烷类
近年来,从南五味子属植物中分离并鉴定的二苄基丁烷类成分有meso- dihydroguaiaretic acid[17]、3-methoxy-3′,4′-(methyl- enedioxy)-9,9′-epoxylignan-4,7′-diol[39]、kadsuphilin J[10]、kadsuphilin L[10]、kadsuphilin M[10]、meso- dihydroguaiaretic acid[23]、kadcoccilignan[24]、heteroclitin R[40](144~151),结构见图 6。
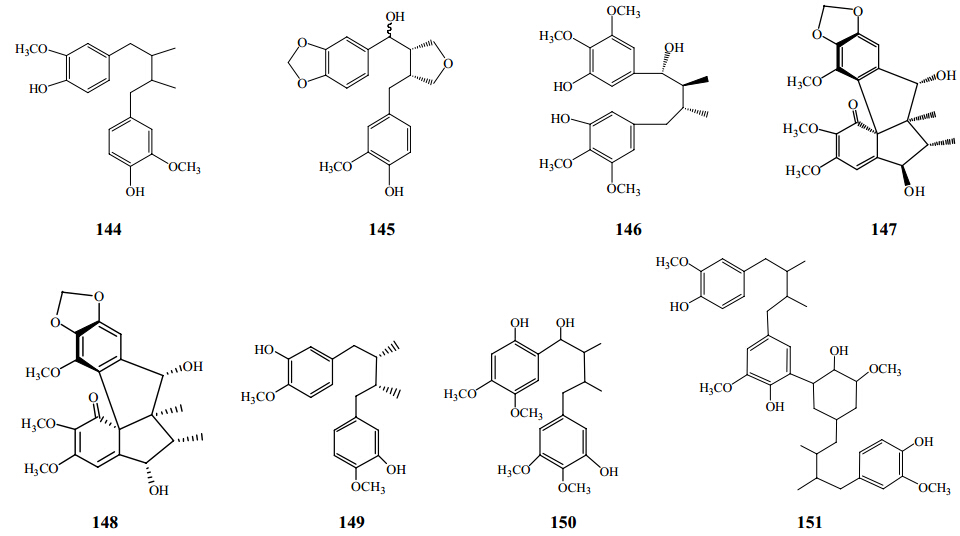 | 图 6 南五味子属植物中二苄基丁烷类木脂素成分结构Fig. 6 Structures of diarylbutane lignanoids in plants of Kadsura Kaempf. ex Juss. |
1.1.5 四氢呋喃类
近年来,从南五味子属植物中分离并鉴定的四氢呋喃类成分有d-epigalbacin[17]、9-(β-D-glucopyranosyloxy)-3′-methoxy-3,4-(methyl- enedioxy)-7,9′-epoxylignan-4′-ol[39]、kadlongirin A[41]、kadlongirin B[41]、grandisin[41]、fragransin B[41](152~157),结构见图 7。
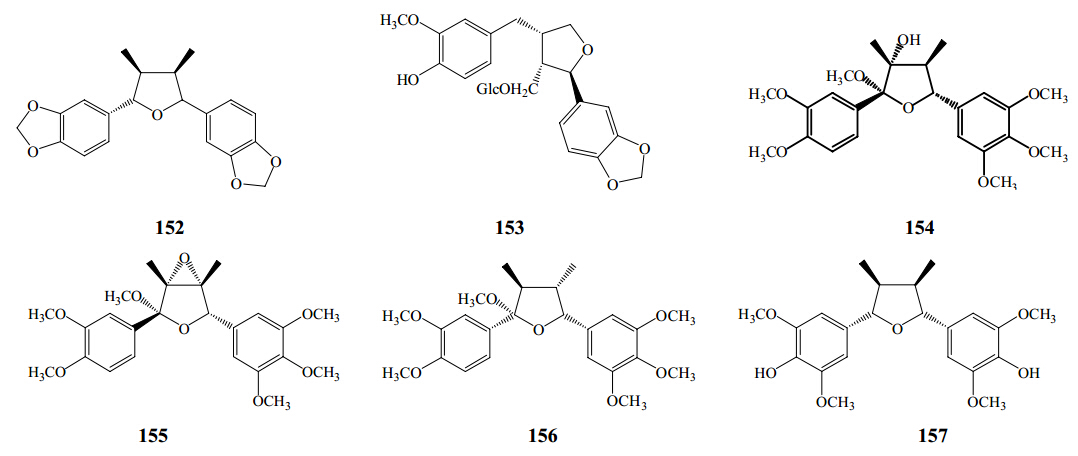 | 图 7 南五味子属植物中四氢呋喃类木脂素成分结构Fig. 7 Structures of tetrahydrofuran lignanoids in plants of Kadsura Kaempf. ex Juss. |
1.1.6 新木脂素类
近年来,从南五味子属植物中分得4个新木脂素类成分 (+)-dihydrodehydrodiconi feryl alcohol-9-O-β-D-glucopyranoside(158)[38]、 taiwankadsurin A、D和E(159~161)[31],结构见图 8和表 3。
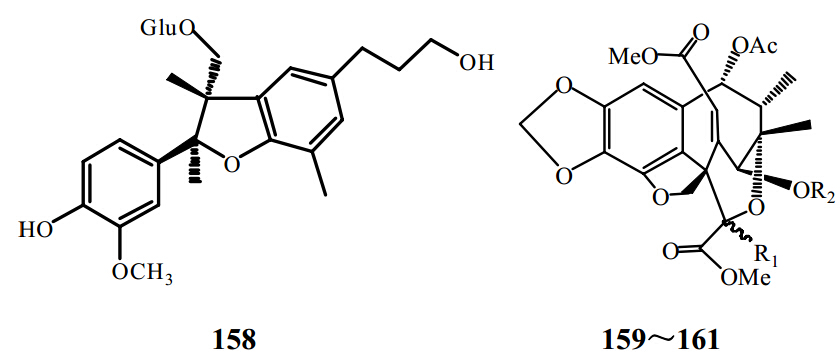 | 图 8 南五味子属植物中新木脂素类成分结构Fig. 8 Structures of neolignan lignanoids in plants of Kadsura Kaempf. ex Juss. |
| 表 3 南五味子属植物中分离得到的新木脂素类化合物 Table 3 Neolignan lignanoids isolated from plants of Kadsura Kaempf. ex Juss. |
三萜是南五味子属植物中主要成分之一,主要包含羊毛脂烷型和环阿屯烷型三萜。近年来,在南五味子属部分植物中分离出多个降三萜类化合物,此外该属植物还含有少量的齐墩果烷型、乌苏烷型和羽扇豆烷型三萜。
1.2.1 羊毛脂烷型此三萜类化合物在南五味子属中最为普遍,目前从南五味属中分得此类化合物见图 9和表 4。
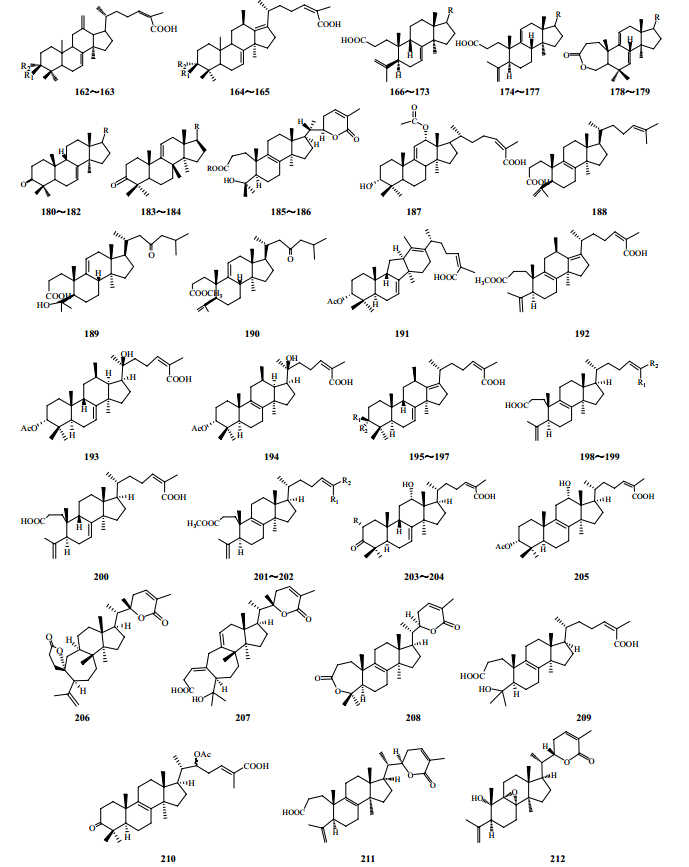 | 图 9 南五味子属植物中羊毛甾脂烷型三萜类成分化合物结构Fig. 9 Structures of lanostane triterpenoids in plants of Kadsura Kaempf. ex Juss. |
| 表 4 南五味子属植物中的羊毛甾脂烷型三萜类化合物 Table 4 Lanostane triterpenoids isolated from plants of Kadsura Kaempf. ex Juss. |
1.2.2 环阿屯烷型
从南五味子属植物中分离得到的环阿屯烷型三萜类化合物见图 10和表 5。
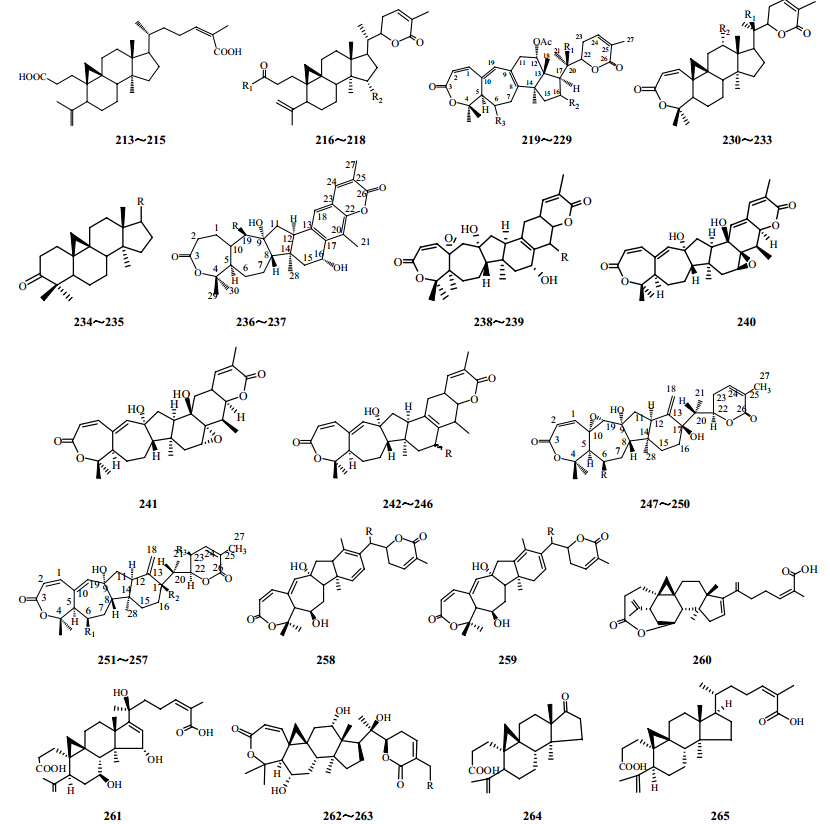 | 图 10 南五味子属植物中环阿屯烷型三萜类化合物结构Fig. 10 Structures of cycloartanes triterpenoids in plants of Kadsura Kaempf. ex Juss. |
| 表 5 南五味子属植物中环阿屯烷型三萜类化合物 Table 5 Cycloartanes triterpenoids isolated from plants of Kadsura Kaempf. ex Juss. |
1.2.3 降三萜
2008年,Gao等[57]从黑老虎中首次分得了10个降三萜化合物。其结构见图 11和表 6。
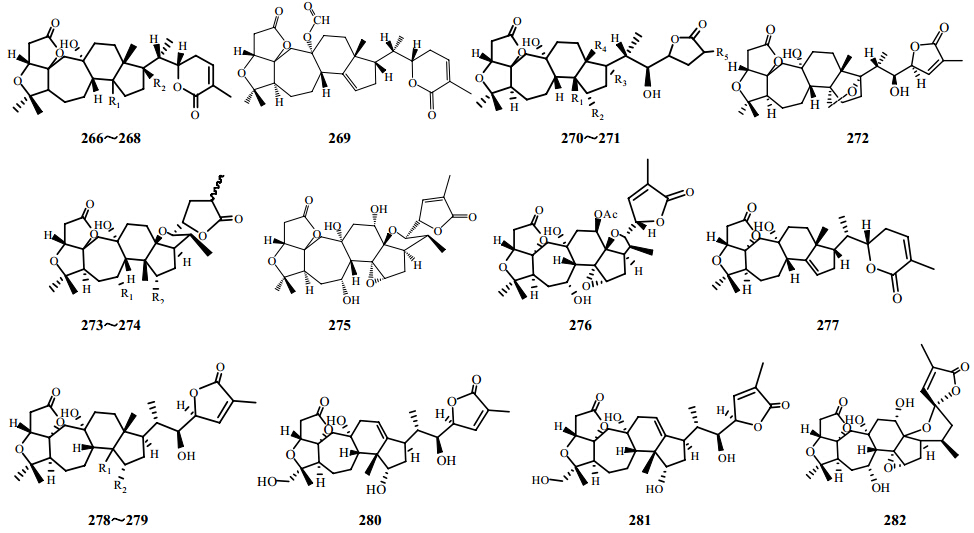 | 图 11 南五味子属植物中降三萜类化合物结构Fig. 11 Structures of nortriterpenod triterpenoids in plants of Kadsura Kaempf. ex Juss. |
| 表 6 南五味子属植物中的降三萜类化合物 Table 6 Nortriterpenod triterpenoids isolated from plants of Kadsura Kaempf. ex Juss. |
1.2.4 其他
周三云等[58]从凤庆鸡血藤K. interior A. C. Smith中分得一些五环三萜类化合物,Song等[59]从黑老虎中分到2个三萜酸,Liang等[60]从黑老虎中分得2个6/6/5/5融合的四环三萜kadcoccitone A、B(291、292)和一个新的与生物起源相关的物质kadcoccitone C(293),其结构见图 12和表 7。
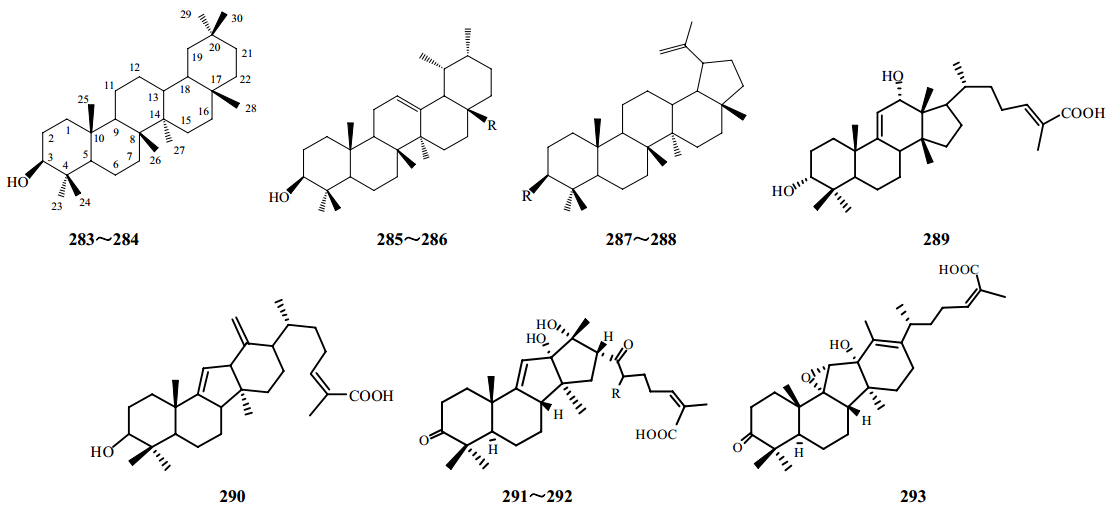 | 图 12 南五味子属植物中其他三萜类化合物结构Fig. 12 Structures of other triterpenoids in plants of Kadsura Kaempf. ex Juss. |
| 表 7 南五味子属植物中其他三萜类化合物 Table 7 Other triterpenoids isolated from plants of Kadsura Kaempf. ex Juss. |
1.3 倍半萜类成分
李贺然等[15]从黑老虎中分得5个倍半萜类成分,分别为cedrelanol、isodonsesquitin A、kadsurae- nol、allospathulenol和naphthalene。Dong等[61]从凤庆鸡血藤分得5个倍半萜类成分,其中2个为新的愈创木内酯型倍半萜,分别为4β,9β-dihydroxy-1α,5α-H-guaia-6,10(14)-dien、4β,9β,10α-trihydroxy- 1α,5α-H-guaia-6-en。
1.4 其他类李顺祥[62]对黑老虎中氨基酸及微量元素进行了分析,分得14种氨基酸,其中人体必需氨基酸占37.87%。王楠等[23]从黑老虎中分得了24ξ-n-丙基-胆甾-3-酮、豆甾-5-烯-7-羰基-3β-醇、豆甾-5-烯-3β,7α-二醇、clovane-2β,9α-diol、美国茶叶花素、正丁基-β-D-吡喃果糖苷、香草酸、香草醛、原儿茶酸、
莽草酸、β-谷甾醇和胡萝卜苷。彭富全等[63]采用GC-MS 联用技术,从黑老虎挥发油中分离出151种化学成分,鉴定出其中的45个,占挥发油总量的64.56%,其中质量分数在1%以上的有18个。
2 药理活性 2.1 抗癌活性Gao等[49]从黑老虎中分得的kadlongilactone A、B对白血病K562细胞、人肝癌Bel-7402细胞以及人肺腺癌A549具有显著的细胞毒性,IC50分别小于0.1、0.1和1.0 μmol/L。Wang等[52]从异形南五味子中分得的heteroclitalactone D对白血病HL-60细胞具有显著的细胞毒性,其IC50为6.76 μmol/L。Shen等[34]从异形南五味子中分离得到的木脂素taiwankadsurin C对人口腔上皮癌细胞KB和人宫颈癌细胞HeLa具有一定的细胞毒性。Mulyaningsih等[64]从南五味子中分离出的挥发油对6种人类癌细胞(HepG2、MIA PAca-2、HeLa、HL-60、MDA- MB-231和SW-480)具有一定的细胞毒性。Pu等[56]从南五味子中分离得到的4个三萜化合物(kadlongilactone A、C、D、E)对3种癌细胞(A549、HT-29、K562)具有显著的细胞毒性,IC50在0.49~3.61 μmol/L。Pu等[65]从南五味子中分离得到的三萜化合物kadlongilactone A、B具有显著抑制K562活性,其IC50分别为1.40、1.71 μg/mL。Wang等[46]从黑老虎中分得seco-coccinic acid A、B、C和E,发现它们均能显著抑制人白血病HL-60细胞增殖,GI50为6.8~42.1 μmol/L。
2.2 抗病毒活性Pu等[35]从异形南五味子中分离出木脂素interiorin和interiorin B,考察其抗HIV活性,发现二者具有一定的抗HIV活性,其EC50分别为1.6、1.4 g/mL。其治疗指数(TI)分别为52.9和65.9。Shen等[55]从菲律宾南五味子中分得的kadsuphilactone B具有抗HBV活性,其IC50为6 μg/mL。Ma等[66]从南五味子中分到的木脂素kadsurindutin A、kadsulignan L和neokadsuranin具有一定的抗HBV活性。Pu等[39]从南五味子中分离得到的木脂素kadlongirin B具有抗HIV-1活性,其EC50为16.0 μg/mL,TI为6.7。Sun等[6]从南五味子中分离的木脂素longipedunins A和schisanlactone A具有抗HIV-1活性,其IC50分别为50、20 μmol/L。Gao等[12]从狭叶南五味子中分得的木脂素binankadsurin A具有一定的抗HIV活性,其EC50为3.86 μmol/L。Kuo等[7]从日本南五味子中分得taiwanschirin A 和taiwanschirin B,二者抗HBV作用显著,在25 μg/mL时具有很强的抗HBsAg和一定的抗HBeAg活性。Wu等[18]从小本红骨蛇中分得gomisin B、gomisin G和 (+)-gomisin K3,活性测试表明其有抗HBV的作用。Xu等[53]从异形南五味子中分到8个化合物,通过荧光和同位素3H试验,对所有化合物抑制HIV-1蛋白酶和逆转录酶进行了测试,发现在质量浓度为10 μg/mL时,化合物kadsuranic acid A和nigranoic acid对HIV-1蛋白酶表现出很强的抑制作用,抑制率分别为(89.2±0.5)%和(85.0±5.5)%;schisandronic acid显示了中等的抑制活性,抑制率为(56.1±8.8)%;其他的化合物对HIV-1蛋白酶则都显示了抑制率低于20%的弱抑制活性。Sun等[32]从狭叶南五味子中分得4个新的环菠萝烷型三萜angustific acid A、B,angusti- fodilactone A、B和6个已知的化合物,通过受感染的C8166细胞测定这些物质的抗HIV活性。结果发现angustific acid A具有很强的抗HIV活性,EC50值是6.1 μg/mL,治疗指数超过32.8。
2.3 保肝作用朱树凡等[67]研究了黑老虎对四氯化碳致大鼠肝损伤模型的保护作用,实验证明黑老虎有较好的降酶、保护肝细胞和抗肝纤维化作用。屈克义等[68]进一步证明黑老虎具有降酶、保护肝细胞和抗肝纤维化作用,并与其抗脂质过氧化作用有关。Ninh等[69]发现从黑老虎中分得的化合物acetylepigomisin R、isovaleroylbinankadsurin A和binankadsurin A具有保护叔丁基过氧化氢致大鼠肝损伤的作用,ED50分别为135.7、26.1和79.3 μmol/L。
2.4 抗氧化作用Sun等[70]从黑老虎果实中提取了花青素和多酚类成分,采用DPPH法考察了它们的抗氧化作用。发现黑老虎果实提取物中的花青素和多酚类成分都具有抗氧化作用,且抗氧化能力顺序为果皮总多酚提取物>花色素提取物>果肉多酚提取物。
2.5 调血脂作用李志春等[71]研究成熟黑老虎果的毒性及其对血脂的调节作用,实验结果表明,黑老虎基本无毒性,而且与对照组比较,果汁组雌雄小鼠的胆固醇水平显著降低(P<0.05),说明黑老虎果具有明显降低胆固醇的作用。三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、血糖水平无显著性差异(P>0.05),均在正常范围。
2.6 体外抑菌作用封毅等[72]研究黑老虎果皮及其提取物的体外抑菌效果,确定黑老虎果皮对伤寒沙门氏菌的最小抑菌浓度、最小杀菌浓度和有效部位。采用滤纸扩散法观察黑老虎果皮及其乙醇提取液和各相萃取液的抑菌作用;用二倍稀释法测定最小抑菌浓度和最小杀菌浓度。实验结果表明,黑老虎果皮及其乙醇提取物对伤寒沙门氏菌有抑制作用,最小抑菌浓度为31.25 mg/mL,最小杀菌浓度为125 mg/mL,抑菌物质主要存在于乙醚萃取相中。
2.7 杀虫作用Li等[73]通过水蒸气蒸馏法提取异型南五味子的挥发油。挥发油显示出强的杀线虫活性,对南方根结线虫的LC50值为122.94 μg/mL。挥发油有触杀作用,对玉米象成虫的触杀LD50值为25.57 μg/成虫,对玉米象也显示了明显的熏蒸剂毒性(LC50值为14.04 mg/L)。
2.8 神经保护作用Dong等[27]从多子南五味子中分得11个新的联苯环辛二烯类木脂素化合物polysperlignan A~K和8个已知的类似物。评估它们对抗由淀粉样蛋白或过氧化氢诱导的PC12细胞神经元毒性的活性,polysperlignan A、B、D、E在体外实验中显示了一定的神经保护作用。Yang等[28]从中泰南五味子中得到14个新的联苯环辛二烯类木脂素化合物:ananolignan
A~N和5个已知的化合物,并且评估了这些木脂素的生物活性,ananolignan F、L在体外实验中表现出较强的神经保护作用。
3 结语南五味子属植物多为地方习用药材,以茎、根入药,如南五味子在云南作为鸡血藤治疗妇科疼痛,异形南五味子在广东、广西作为海风藤治疗风湿痹痛,其他南五味子属植物在民间也广泛用于治疗各种痛证。我国南五味子属资源十分丰富,随着对该属植物成分研究的不断深入,其现代药理研究也取得了较大进展,特别是南五味子属植物中的木脂素、三萜类活性成分在抗肿瘤和抗HIV方面的突出作用尤为引人关注。在对已知活性成分深入研究的基础上,需要进一步明确其在体内的作用机制,以阐明其药效物质基础,并建立稳定、可靠的质量控制标准,为该属植物的进一步开发提供必要的科学依据。
| [1] | 中国科学院中国植物志编辑委员会.中国植物志 (第30卷, 第2分册) [M].北京: 科学出版社, 1979. |
| [2] | 中国药典 [S].一部.2010. |
| [3] | 肖培根, 许利嘉, 肖伟.南五味子属应更名为冷饭藤属的论证 [J].药学学报, 2010, 45(8): 1064-1066. |
| [4] | 陈业高, 秦国伟, 谢毓元.五味子科植物木脂素成分的氢谱特征 [J].波谱学杂志, 2000, 17(5): 427-431. |
| [5] | Chen M, Liao Z, Chen D.Four new dibenzocyclooctene lignans from Kadsura renchangiana [J].Helv Chim Acta, 2004, 87(6): 1368-1376. |
| [6] | Sun Q Z, Chen D F, Ding P L, et al.Three new lignans, longipedunins A—C, from Kadsura longipedunculata and their inhibitory activity against HIV-1 protease [J].Chem Pharm Bull, 2006, 54(1): 129-132. |
| [7] | Kuo Y H, Wu M D, Huang R L, et al.Antihepatitis activity (anti-HBsAg and anti-HBeAg) of C19 homolignans and six novel C18 dibenzocyclooctadiene lignans from Kadsura japonica [J].Planta Med, 2005, 71(7): 646-653. |
| [8] | Shen Y C, Lin Y C, Chen Y B, et al.Dibenzocyclooctadiene lignans from Kadsura philippinensis [J].Phytochemistry, 2009, 70(1): 114-120. |
| [9] | Shen Y C, Liaw C C, Cheng Y B, et al.C18 dibenzocyclooctadiene lignans from Kadsura philippinensis [J].J Nat Prod, 2006, 69(6): 963-966. |
| [10] | Shen Y C, Lin Y C, Cheng Y B, et al.New oxygenated lignans from Kadsura philippinensis [J].Helv Chim Acta, 2008, 91(3): 483-494. |
| [11] | Li H R, Feng Y L, Yang Z G, et al.New lignans from Kadsura coccinea and their nitric oxide inhibitory activities [J].Chem Pharm Bull, 2006, 54(7): 1022-1025. |
| [12] | Gao X M, Pu J X, Huang S X, et al.Lignans from Kadsura angustifolia [J].J Nat Prod, 2008, 71(4): 558-563. |
| [13] | Li H, Wang L, Yang Z, et al.Kadsuralignans H—K from Kadsura coccinea and their nitric oxide production inhibitory effects [J].J Nat Prod, 2007, 70(12): 1999-2002. |
| [14] | Ban N K, Van Thanh B, Van Kiem P, et al.Dibenzocyclooctadiene lignans and lanostane derivatives from the roots of Kadsura coccinea and their protective effects on primary rat hepatocyte injury induced by t-butyl hydroperoxide [J].Planta Med, 2009, 75(11): 1253-1257. |
| [15] | 李贺然, 黑老虎及胡桃枝皮的化学成分成究 [D].北京: 协和医科大学, 2006. |
| [16] | Shen Y C, Lin Y C, Ahmed A F, et al.Four new nonaoxygenated C18 dibenzocylcooctadiene lignans from Kadsura philippinensis [J].Chem Pharm Bull, 2007, 55(2): 280-283. |
| [17] | Wang W, Liu J, Liu R, et al.Four new lignans from the stems of Kadsura heteroclita [J].Planta Med, 2006, 72(3): 284-288. |
| [18] | Wu M D, Huang R L, Kuo L M Y, et al.The anti-HbsAg (human type B hepatitis, surface antigen) and anti-HbeAg (human type B hepatitis, e antigen) C18 dibenzocyclooctadiene lignans from Kadsura matsudai and Schizandra arisanensis [J].Chem Pharm Bull, 2003, 51(11): 1233-1236. |
| [19] | Xu L J, Liu H T, Peng Y, et al.Heteroclitins N—Q, new compounds from stems of Kadsura heteroclita (Roxb.) Craib [J].Helv Chim Acta, 2008, 91(2): 220-226. |
| [20] | Liu H T, Xu L J, Peng Y, et al.Complete assignments of 1H and 13C NMR data for new dibenzocyclooctadiene lignans from Kadsura oblongifolia [J].Magn Reson Chem, 2009, 47(7): 609-612. |
| [21] | Jia Z, Liao Z, Chen D.Two new dibenzocyclooctene lignans from the water extract of Kadsura spp [J].Helv Chim Acta, 2005, 88(8): 2288-2293. |
| [22] | Shen Y C, Cheng Y B, Lan T W, et al.Kadsuphilols A-H, oxygenated lignans from Kadsura philippinensis [J].J Nat Prod, 2007, 70(7): 1139-1145. |
| [23] | 王楠, 李占林, 刘晓秋, 等.黑老虎根化学成分的研究 (II) [J].中国药物化学杂志, 2012, 22(4): 305-309. |
| [24] | Ga X M o, Pu J X, Zhao Y, et al.Lignans from Kadsura angustifolia and Kadsura coccinea [J].J Asian Nat Prod Res, 2012, 14(2): 129-134. |
| [25] | Hu W, Li L, Wang Q, et al.Dibenzocyclooctadiene lignans from Kadsura coccinea [J].J Asian Nat Prod Res, 2012, 14(4): 364-369. |
| [26] | 舒永志, 成亮, 曺濬喆, 等.黑老虎的化学成分研究 [J].中草药, 2012, 43(3): 428-431. |
| [27] | Dong K, Pu J X, Zhan H Y, et al.Dibenzocyclooctadiene lignans from Kadsura polysperma and their antineurodegenerative activities [J].J Nat Prod, 2012, 75: 249-256. |
| [28] | Yang J H, Zhang H Y, Wen J, et al.Dibenzocyclooctadiene lignans with antineurode- generative potential from Kadsura ananosma [J].J Nat Prod, 2011, 74: 1028-1035. |
| [29] | Zhao Q J, Song Y, Chen H S.Cytotoxic dibenzocyclooctadiene lignans from Kadsura coccinea [J].Archiv Pharm Res, 2013, doi: 10.1007/s12272- 013-0186-3. |
| [30] | Cheng Y B, Lin Y C, Khalil A T, et al.Seven new lignan esters from Kadsura philippinensis [J].Helv Chim Acta, 2011, 94: 148-158. |
| [31] | Lin Y C, Cheng Y B, Liaw C C, et al.New lignans from the leaves and stems of Kadsura philippinensis [J].Molecules, 2013, 18: 6573-6583. |
| [32] | Sun R, Song H C, Wang C R, et al.Compounds from Kadsura angustifolia with anti-HIV activity [J].Bioorg Medicinal Chem Lett, 2011, 21: 961-965. |
| [33] | Xu L J, Peng Y, Chen S B, et al.Four new lignans from Kadsura heteroclita [J].Heterocycles, 2007, 71(4): 941-947. |
| [34] | Shen Y C, Lin Y C, Cheng Y B, et al.Taiwankadsurins A, B, and C, three new C19 Homolignans from Kadsura philippinensis [J].Org Lett, 2005, 7(23): 5297-5300. |
| [35] | Pu J X, Yang L M, Xiao, W L, et al.Compounds from Kadsura heteroclita and related anti-HIV activity [J].Phytochemistry, 2008, 69(5): 1266-1272. |
| [36] | Li H, Feng Y, Yang Z, et al.New lignans from Kadsura coccinea and their nitric oxide inihibitoty activities [J].Heterocycles, 2006, 68(6): 1259-1265. |
| [37] | Chen M, Jia Z W, Chen D F.Heteroclitin H, a new lignan from Kadsura heteroclita [J].J Asian Nat Prod Res, 2006, 8(7): 643-648. |
| [38] | 罗艺萍, 王素娟, 赵静峰, 等.异型南五味子的化学成分研究 [J].云南大学学报: 自然科学版, 2009, 31(4): 406-409. |
| [39] | Pu J X, Xiao W L, Li H M, et al.Three new compounds from Kadsura longipedunculata [J].Helv Chim Acta, 2007, 90(4): 723-729. |
| [40] | 许利嘉, 肖伟, 彭勇, 等.异型南五味子藤茎中1个新的木脂素 [J].中国中药杂志, 2010, 35(15): 1970-1972. |
| [41] | Pu J X, Gao X M, Lei C, et al.Three New Compounds from Kadsura longipedunculata [J].Chem Pharm Bull, 2008, 56(8): 1143-1146. |
| [42] | Pu J X, Li R T, Xiao W L, et al.Longipedlactones A—I, nine novel triterpene dilactones possessing a unique skeleton from Kadsura longipedunculata [J].Tetrahedron, 2006, 62(25): 6073-6081. |
| [43] | Li H, Wang L, Miyata S, et al.Kadsuracoccinic acids A—C, ring-A seco-lanostane triterpenes from Kadsura coccinea and their effects on embryonic cell division of Xenopus laevis [J].J Nat Prod, 2008, 71(4): 739-741. |
| [44] | Chen Y G, Hai L N, Liao X R, et al.Ananosic acids B and C, two new 18 (13→12)-abeo-lanostane triterpenoids from Kadsura ananosma [J].J Nat Prod, 2004, 67(5): 875-877. |
| [45] | Dong K, Pu J X, Du X, et al.Kadpolysperins A—N, lanostane triterpene acids possess ing rich structure types from Kadsura polysperma [J].Tetrahedron, 2012, 68: 4820-4829. |
| [46] | Wang N, Li Z, Song D, et al.Lanostane-type triterpenoids from the roots of Kadsura coccinea [J].J Nat Prod, 2008, 71(6): 990-994. |
| [47] | Wang N, Li Z L, Song D D, et al.Five new 3, 4-seco-lanostane-type triterpenoids with antiproliferative activity in human leukemia cells isolated from the roots of Kadsura coccinea [J].Planta Med, 2012, 78: 1661-1666. |
| [48] | Wang N, Li Z L, Li D Y, et al.Five new triterpenoids from the roots of Kadsura coccinea [J].Helv Chim Acta, 2009, 92(7): 1413-1418. |
| [49] | Gao X M, Pu J X, Xiao W L, et al.Kadcoccilactones K—R, triterpenoids from Kadsura coccinea [J].Tetrahedron, 2008, 64(51): 11673-11679. |
| [50] | Yang J H, Wen J, Du X, et al.Triterpenoids from the stems of Kadsura ananosma [J].Tetrahedron, 2010, 66: 8880-8887. |
| [51] | Song Y, Zhao Q J, Jin Y S, et al.A new triterpenoid from Kadsura coccinea [J].Chin Chem Lett, 2010, 21: 1352-1354. |
| [52] | Wang W, Liu J, Han J, et al.New triterpenoids from Kadsura heteroclita and their cytotoxic activity [J].Planta Med, 2006, 72(5): 450-457. |
| [53] | Xu L J, Peng Z G, Chen H S, et al.Bioactive triterpenoids from Kadsura heteroclite [J].Chem Biodiv, 2010, 7: 2289-2295. |
| [54] | Wang W, Xu Z, Yang M, et al.Structural determination of seven new triterpenoids from Kadsura heteroclita by NMR techniques [J].Magn Reson Chem, 2007, 45(6): 522-526. |
| [55] | Shen Y C, Lin Y C, Chiang M Y, et al.Kadsuphilactones A and B, two new triterpene dilactones from Kadsura philippinensis [J].Org Lett, 2005, 7(15): 3307-3310. |
| [56] | Pu J X, Huang S X, Ren J, et al.Isolation and structure elucidation of kadlongilactones C—F from Kadsura longipedunculata by NMR spectroscopy and DFT computational methods [J].J Nat Prod, 2007, 70(11): 1706-1711. |
| [57] | Gao X M, Pu J X, Huang S X, et al.Kadcoccilactones A—J, Triterpenoids from Kadsura coccinea [J].J Nat Prod, 2008, 71(7): 1182-1188. |
| [58] | 周三云, 李蓉涛, 李洪梅.凤庆鸡血藤的化学成分研究 [J].昆明理工大学学报: 理工版, 2008, 33(5): 81-85. |
| [59] | Song Y, Zhao Q J, Jin Y S, et al.Two new triterpenoid acids from Kadsura coccinea [J].Archiv Pharm Res, 2010, 33(12): 1933-1936. |
| [60] | Liang C Q, Shi Y M, Luo R H, et al.Kadcoccitones A and B, two new 6/6/5/5-fused tetracyclic triterpenoids from Kadsura coccinea [J].Org Lett, 2012, 14(24): 6362-6365. |
| [61] | Dong K, Pu J X, Du X, et al.Two new guaianolide-type sesquiterpenoids from Kadsura inrerfor [J].Chin Chem Lett, 2013, 24: 111-113. |
| [62] | 李顺祥.冷饭团的氨基酸及微量元素测定[J].湖南中医杂志, 1996, 12(6): 48. |
| [63] | 彭富全, 邓慧怡.黑老虎挥发油成分的GC-MS分析[J].现代食品与药品杂志, 2006, 16(4): 6-8. |
| [64] | Mulyaningsih S, Youns M, El-Readi M Z, et al.Biological activity of the essential oil of Kadsura longipedunculata (Schisandraceae) and its major components [J].J Pharm Pharmacol, 2010, 62(8): 1037-1044. |
| [65] | Pu J X, Xiao W L, Lu Y, et al.Kadlongilactones A and B, two novel triterpene dilactones from Kadsura longipedunculata possessing a unique skeleton [J].Org Lett, 2005, 7(22): 5079-5082. |
| [66] | Ma W, Ma X, Huang H, et al.Dibenzocyclooctane lignans from the stems of Kadsura induta and their antiviral effect on hepatitis B virus [J].Chem Biodivers, 2007, 4(5): 966-972. |
| [67] | 朱树凡.中药冷饭团对四氯化碳致大鼠实验性肝损伤的保护作用观察 [J].中国现代医生, 2007, 45(10): 7-9. |
| [68] | 屈克义, 黄继海, 李文胜, 等.冷饭团抗肝纤维化的实验研究 [J].中国中西医结合消化杂志, 2001, 9(2): 86-89. |
| [69] | Ninh K B, Bui V T, Phan V K, et al.Dibenzo- cyclooctadiene lignans and lanostane derivatives from the roots of Kadsura coccinea and their protective effects on primary rat hepatocyte injury induced by t-butyl hydroperoxide [J].Planta Med, 2009, 75(11): 1253-1257. |
| [70] | Sun J, Yao J Y, Huang S X, et al.Antioxidant activity of polyphenol and anthocyanin extracts from fruits of Kadsura coccinea (Lem.) A.C.Smith [J].Food Chem, 2009, 117(2): 276-281. |
| [71] | 李志春, 孙健, 封毅, 等.黑老虎果毒理实验及其对血脂的调节作用 [J].食品科学, 2011, 32(1): 203-205. |
| [72] | 封毅, 李志春, 孙健, 等.黑老虎果皮体外抑菌活性的初步研究 [J].时珍国医国药, 2011, 22(4): 822-824. |
| [73] | Li H Q, Bai C Q, Chu S S, et al.Chemical composition and toxicities of the essential oil derived from Kadsura heteroclita stems against Sitophilus zeamais and Meloidogyne incognita [J].J Med Plant Res, 2011, 5(19): 4943-4948. |
 2014, Vol. 45
2014, Vol. 45