2. 沈阳药科大学药学院, 中药质量控制关键技术国家地方联合工程实验室, 辽宁 沈阳 110016
2. State-Local Union Engineering Laboratory of Key Technique of Quality Control of Chinese Medicine, School of Pharmacy, Shenyang Pharmaceutical University, Shenyang 110016, China
五味子是木兰科植物五味子Schisandra chinensis (Turcz.) Baill. 的干燥成熟果实,习称“北五味子”[1]。其味酸、甘,性温;有收敛固涩、益气生津、补肾宁心的功能;用于久咳虚喘、遗精、滑精、遗尿、尿频、久泻不止、自汗、盗汗、津伤口渴、短气脉虚、内热消渴、心悸失眠等症[2]。
五味子主要含有木脂素、多糖、挥发油、有机酸和维生素等多种化学成分,其中木脂素是五味子镇静催眠的主要活性成分[3, 4]。通过HPLC和LC-MS建立五味子的指纹图谱已有大量的文献报道,但单独采用超高效液相色谱(UPLC)法建立五味子的指纹图谱分析方法目前国内还未见报道。UPLC是以1.8 μm的超细色谱柱填料为核心技术的新型色谱分离分析技术,相对于常规HPLC而言,有更好的分离效率及灵敏度[5]。本实验采用UPLC法进行五味子的指纹图谱研究,该方法较HPLC更快速、高效,且较LC-MS更实用,应用更广泛。
1 材料 1.1 仪器ACQUITY UPLC仪,美国Waters公司,包括四元高压梯度泵、真空脱气机、自动进样器、柱温箱、二极管阵列检测器(PDA)、Empower2色谱工作站;BP210S电子天平(德国Sartorius公司);AB135—S十万分之一天平(瑞士Mettler Toledo公司);KQ5200B超声波清洗器(昆山市超声仪器有限公司)。
1.2 试剂对照品五味子醇甲、五味子酯甲、五味子甲素、五味子乙素购自中国食品药品检定研究院(批号:110857-201211,111529-200604,110764-201111,110765-200710),五味子醇乙、当归酰戈米辛H、五味子酯乙、五味子γ-乙素和五味子丙素为实验室自制(经核磁和质谱鉴定,采用峰面积归一化法计算,质量分数均>98.0%)。乙腈为色谱纯(美国Fisher公司),水为娃哈哈纯净水,甲醇为分析纯。19批北五味子来源见表 1,经沈阳药科大学生药教研室贾英教授鉴定,均为正品五味子Schisandra chinensis (Turcz.) Baill. 的果实,密封存放于阴凉干燥处。
|
|
表 1 五味子样品来源 Table 1 Origins of S. chinensis |
ACQUITY UPLC HSS T3(100 mm×2.1 mm,1.8 μm)色谱柱,流动相为水(A)-乙腈(B),梯度洗脱条件:0~6 min,43%~52% B;6~8 min,52%~60% B;8~10 min,60%~62% B;10~11 min,62%~62% B;11~14 min,62%~66% B;14~16 min,66%~70% B;16~18 min,70%~100% B;18~22 min,100% B。体积流量0.5 mL/min,柱温30 ℃;检测波长216 nm;进样量2 μL。
2.2 对照品溶液的制备取五味子醇甲、五味子醇乙、当归戈米辛H、五味子酯甲、五味子酯乙、五味子甲素、五味子γ-乙素、五味子乙素和五味子丙素对照品各适量,精密称定,分别加甲醇溶解制成适当质量浓度的对照品贮备液。精密量取上述对照品贮备液各适量,置同一2 mL的量瓶中,加甲醇稀释至刻度,摇匀,即得五味子醇甲、五味子醇乙、当归酰戈米辛H、五味子酯甲、五味子酯乙、五味子甲素、五味子γ-乙素、五味子乙素和五味子丙素的质量浓度分别为156、25.5、15.3、31.2、10.5、25.9、10.2、40.0、10.5 μg/mL的混合对照品。
2.3 供试品溶液的制备取样品粉末约2 g,精密称定,置100 mL 具塞锥形瓶中,精密加入85%甲醇100 mL,超声处理30 min,放至室温,用甲醇补足减失质量,摇匀,过0.22 μm微孔滤膜滤过,取续滤液作为供试品溶液。
2.4 方法学考察 2.4.1 精密度试验取同一供试品溶液(S2),按“2.1”项下色谱条件连续进样6次,测得各共有峰相对保留时间和相对峰面积RSD均小于2%。
2.4.2 重复性试验分别取同一批(S2)北五味子样品适量,共6份,精密称定,分别按“2.3”项下方法制备供试品溶液,照“2.1”项下色谱条件分别进样分析,测得其各共有峰相对保留时间和相对峰面积的RSD均小于2%,表明重复性良好。
2.4.3 稳定性试验取同一供试品溶液(S2),按“2.1”项下方法操作,分别在0、2、4、8、12、24 h进样,测得其各共有峰相对保留时间和相对峰面积的RSD均小于2%,表明样品在24 h内稳定。
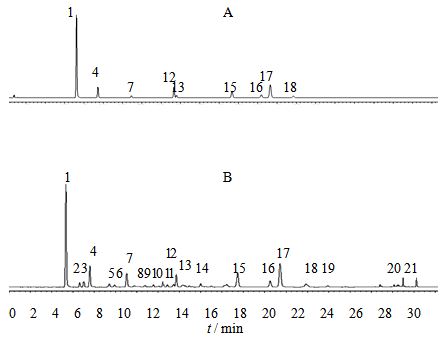
2.5 样品测定取19批北五味子样品,按“2.3”项下制备供试品溶液,在“2.1”项下的色谱条件下依次进样检测,记录色谱图,共获得21个共有峰,指认了其中9个共有峰,分别为1、4、7、12、13、15、16、17和18。混合对照品(A)和典型五味子色谱图(B)见图 1。
|
图 1 混合对照品 (A) 和五味子样品 (B) 的UPLC图谱
Fig. 1 UPLCof mixed reference substances (A) and S. chinensis (B)
1-五味子醇甲 4-五味子醇乙 7-当归酰戈米辛H 12-五味子酯甲 13-五味子酯乙 15-五味子甲素 16-五味子γ-乙素 17-五味子乙素 18-五味子丙素 1-schisandrin 4-schisandrol B 7-angeloylgomisin H 12-schisantherin A 13-schisantherin B 15-deoxyschisandrin 16-γ-schisandrin 17-gomisin N 18-schisandrin C |
在各批次样品图谱中五味子乙素的色谱峰(17号峰)分离良好,峰位居中,峰面积较大且为所有样品共有,所以确定五味子乙素为参比峰。
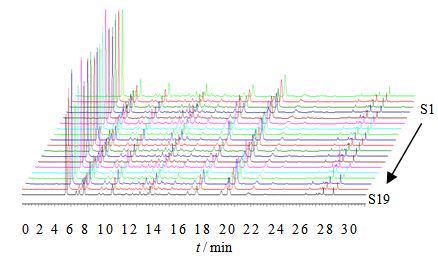
2.6.2 指纹图谱共有模式的建立结合形态学鉴定结果,选择19批五味子建立共有模式。将19批样品色谱图导入《中药色谱指纹图谱相似度评价系统2009版》软件,建立了五味子的指纹图谱共有模式图,结果见图 2。
|
图 2 19批五味子UPLC指纹图谱 Fig. 2 UPLC fingerprints for 19 batches of S. chinensis |
对19批五味子样品的UPLC指纹图谱进行相似度评价,结果见表 2。分析结果显示19批次的五味子相似度均在0.970以上,表明各产地五味子具有较高的相似度。
|
|
表 2 19批五味子的相似度分析 Table 2 Similarity analysis of 19 batches of S. chinensis |
本实验对提取溶剂进行考察,比较了50%、75%、85%、100%甲醇、50%、75%、95%乙醇,结果表明,以85%甲醇提取的样品,色谱峰个数较多,峰面积较大,且无溶剂效应,故提取溶剂选择85%甲醇。对超声与回流2种不同的提取方法考察结果表明,2种提取方法效率相当,考虑到超声操作较简便,故提取选择超声。超声时间30 min,1次即可提取较完全。故最终确定用85%甲醇超声30 min,提取1次。
3.2 色谱条件的选择本实验使用Waters的PDA检测器进行紫外区全波长扫描,结果表明在216 nm波长下,色谱图基线噪音较低,特征峰响应较高,木脂素类成分色谱峰信息较完全,因此选择216 nm作为本实验的检测波长。实验还考察了甲醇-水、乙腈-水、乙腈-甲酸水、乙腈-磷酸水4个流动相系统,结果发现采用乙腈-水流动相系统,各峰的分离度较好,且基线平稳,因此最终采用乙腈-水系统作为流动相系统。
本研究首次建立了22 min内快速鉴别五味子的UPLC指纹图谱方法,相似度评价分析得19批五味子药材的相似度均在0.970以上,表现出很高的相似度。结果表明五味子在东北三省产地的相似度较高,无显著性差异,均为五味子的推荐品。
| [1] | 夏丽文, 彭丽萍, 杨东华, 等. 超高效液相色谱-电喷雾飞行时间质谱分析五味子化学成分[J]. 中医药信息, 2012, 29(4): 27-30. |
| [2] | 中国药典[S]. 一部. 2010. |
| [3] | 周进东, 陆兔林, 毛春芹, 等. HPLC测定五味子不同炮制品中6种木脂素类成分的含量[J]. 中国药学杂志, 2011, 46(17): 1353-1356. |
| [4] | 邓少东, 王莲婧, 林 励, 等. 化橘红黄酮类成分UPLC与HPLC指纹图谱的比较研究[J]. 中草药, 2013, 44(9): 1195-1198. |
| [5] | 史 琳, 王志成, 冯叙桥. 五味子化学成分及药理作用的研究进展[J]. 药物评价研究, 2011, 34(3): 208-212. |
 2014, Vol. 45
2014, Vol. 45


