2. 中药制药过程新技术国家重点实验室, 江苏 连云港 222001
2. State Key Laboratory of New-tech for Chinese Medicine Pharmaceutical Process, Lianyungang 222001, China
芪白平肺颗粒(Qibai Pingfei Granules,QPG)是由人参、黄芪、五味子、川芎、薤白、葶苈子、地龙共7味药组成的中药复方制剂,其中人参、黄芪为君药,川芎、薤白、葶苈子为臣药,五味子、地龙为佐药,诸药合用具有益气、温阳、化痰、散瘀之功效,为治疗慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)的临床经验方[1-5],适用于COPD急性发作期及缓解期。
有关QPG质量控制方面,目前文献主要集中在人参和黄芪皂苷类成分定量测定方面的研究[6-7],尚未见有关QPG的指纹图谱研究。为了更好更全面地控制产品质量,保证临床疗效,完善QPG的质量评价方法,本实验以QPG制剂中五味子醇甲、咖啡酸、阿魏酸、五味子甲素、五味子乙素、五味子酯甲等6个活性成分为主要分析对象,参照相关文献方法[8-17],采用HPLC法同时对QPG进行了指纹图谱研究,以全面反映产品信息,更好地控制产品质量。
1 仪器和材料Ultimate 3000高效液相色谱仪,DAD紫外检测器,美国赛默飞世尔科技公司;Mettler AE240电子分析天平、Mettler XP6型电子分析天平,瑞士梅特勒公司;KQ-250DB型超声波清洗仪,昆山超声仪器有限公司;Centrifuge 5415D高速离心机,德国Eppendorf公司;Milli-Q超纯水机,美国密理博公司。甲醇,色谱纯,美国天地公司;水为超纯水,其余试剂均为分析纯。
对照品五味子醇甲(批号110857-201513,质量分数以99.9%计)、咖啡酸(批号110885-200102,质量分数以100%计)、阿魏酸(批号110773-201313,质量分数以99.6%计)、五味子甲素(批号110764-201513,质量分数以99.5%计)、五味子乙素(批号110765-201512,质量分数以99.0%计)、五味子酯甲(批号111529-201505,质量分数以95.3%计),对照品均购自中国食品药品检定研究院。QPG由江苏康缘药业股份有限公司生产,批号分别为141201、141202、141203、150301、150401、150402、150403、150601、150601、150602。
人参Ginseng Radix et Rhizoma(GRR,批号Y140801)为五加科五加属植物人参Panax ginseng C. A. Mey.的干燥根和根茎、黄芪Astragali Radix(AR,批号Y140203)为豆科黄芪属植物蒙古黄芪Astragalus membranaceus(Fisch.) Bge. var. mongholicus (Bge.) Hsiao的干燥根、五味子Schisandrae Chinensis Fructus(SCF,批号Y140301)为木兰科五味子属植物五味子Schisandra chinensis (Turcz.) Baill.的干燥成熟果实、川芎Chuanxiong Rhizoma(CR,批号Y140502)为伞形科藁本属植物川芎Ligusticum chuanxiong Hort.的干燥根茎、薤白Allii Macrostemonis Bulbus(AMB,批号Y140801)为百合科葱属植物小根蒜Allium macrostemon Bunge的干燥鳞茎、葶苈子Descurainiae Semen Lepidii Semen(DSLS,批号Y140701)为十字花科播娘蒿属播娘蒿Descurainia sophia (L.) Webb. ex Prantl.的干燥成熟种子、地龙Pheretima(批号Y140801)为钜蚓科环毛蚓属动物通俗环毛蚓Pheretima vulgaris Chen的干燥体,由江苏康缘药业股份有限公司药材库提供,由连云港康济大药房连锁有限公司吴舟执业药师完成鉴定。
2 方法与结果 2.1 色谱条件以Phenomenex Luna C18柱(250 mm×4.6 mm,5 μm)为色谱柱;流动相为甲醇-0.2%甲酸水溶液,梯度洗脱:0~20 min,5%~23%甲醇;20~50 min,23%~50%甲醇;50~100 min,50%~95%甲醇;体积流量为1.0 mL/min;检测波长为250 nm;柱温30 ℃;进样量10 μL,理论板数按五味子醇甲峰计算不低于6 000。
2.2 混合对照品溶液的制备精密称定五味子醇甲、咖啡酸、阿魏酸、五味子甲素、五味子乙素、五味子酯甲对照品适量,加50%甲醇制成含五味子醇甲95.61 μg/mL、咖啡酸108.02 μg/mL、阿魏酸115.33 μg/mL、五味子甲素104.17 μg/mL、五味子乙素92.45 μg/mL、五味子酯甲89.77 μg/mL的混合对照品溶液,即得。
2.3 供试品溶液的制备取本品研细,取2 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25 mL,超声提取30 min,放冷,摇匀,离心,取上清液,即得。按处方比例分别称取各单味对照药材,精密称定,同法制备对照药材溶液。
2.4 精密度试验取批号为150301的QPG,按“2.3”项方法制备供试品溶液,连续进样6针,以五味子醇甲为参照峰,计算25个共有峰相对保留时间RSD均小于1.85%。以第1次进样所得指纹图谱作为参照计算后5次进样所得指纹图谱的相似度,结果相似度均大于0.96。
2.5 稳定性试验取批号为150301的QPG,研细,取2 g,精密称定,按“2.3”项方法制备供试品溶液,精密吸取10 μL,分别于0、2、6、10、14、18、24 h注入液相色谱仪。以五味子醇甲为参照峰,计算25个共有峰相对保留时间RSD值均小于1.85%。以第1次进样所得指纹图谱作为参照计算后6次进样所得指纹图谱的相似度,相似度均大于0.96。
2.6 重复性试验取批号为150301的QPG,研细,取2 g,精密称定,按“2.3”项方法平行制备6份供试品溶液,测定,计算。以五味子醇甲为参照峰,计算各个共有峰相对保留时间RSD值均小于1.96%。以第1份样品所得指纹图谱作为参照计算另5份样品所得指纹图谱的相似度,结果相似度均大于0.96。
2.7 指纹图谱的研究 2.7.1 参照物的选择选择保留时间适中,分离度较好的五味子醇甲作为参照物。
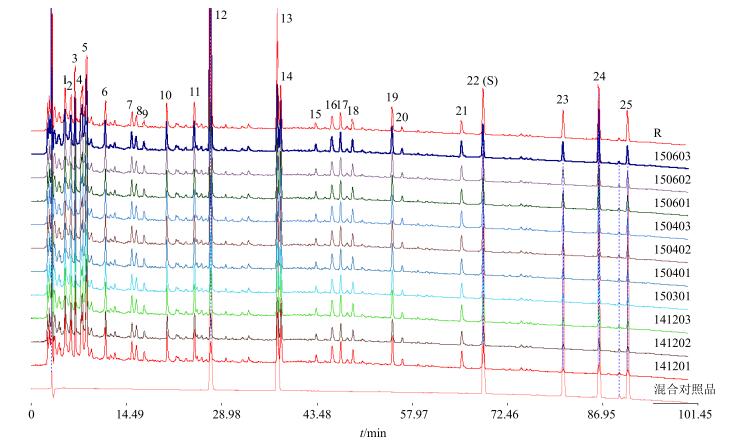
2.7.2 指纹图谱的建立与技术参数根据10批QPG检测所得图谱,确定25个共有峰,采用国家药典委员会颁布的《中药色谱指纹图谱相似度评价系统A版》(2012年版)进行分析,经数据匹配,以中位数法建立对照指纹图谱,见图 1。10批所测供试品色谱图与对照指纹图谱相似度分别为0.974、0.982、0.969、0.965、0.980、0.986、0.971、0.978、0.963和0.996。
|
12-咖啡酸13-阿魏酸22-五味子醇甲23-五味子酯甲24-五味子甲素25-五味子乙素 12-caffeic acid 13-ferulic acid 22-schizandrol A 23-schisantherin A 24-deoxyschizandrin 25-schisandrin 图 1 10批QPG指纹图谱、对照指纹图谱 (R) 及混合对照品HPLC图 Fig.1 HPLC fingerprint for 10 batches of QPG and mixed reference substances |
2.7.3 指纹图谱中共有峰的归属与指认
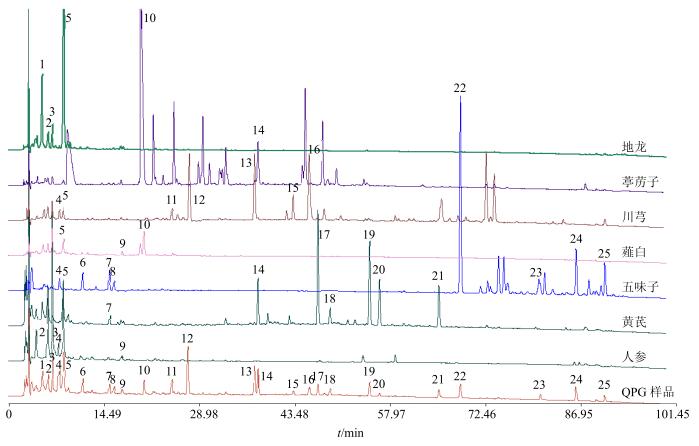
取人参、黄芪、五味子、川芎、薤白、葶苈子、地龙7味药材粉末(过3号筛)各约1 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25 mL,超声提取45 min,放冷,摇匀,离心,取上清液,即得。按“2.1”项下色谱条件进行分析,结果显示1号峰来源于地龙,2、3号峰来源于地龙和人参,4号峰来源于人参、五味子和川芎,5号峰来源于人参、薤白、川芎和地龙,6、8、22、23、24、25号峰来源于五味子,7号峰来源于黄芪和五味子,9号峰来源于人参和薤白,10号峰来源于薤白和葶苈子,11、12、13、15、16号峰来源于川芎,14号峰来源于黄芪和葶苈子,17、18、19、20、21号峰来源于黄芪。见图 2。通过与混合对照品图谱对比,其中12号峰为咖啡酸,13号峰为阿魏酸,22号峰为五味子醇甲,23号峰为五味子酯甲,24号峰为五味子甲素,25号峰为五味子乙素。
|
图 2 QPG指纹图谱中各共有峰归属色谱图 Fig.2 Fingerprint of characteristic peaks in QPG |
2.8 已指认共有成分的定量测定 2.8.1 色谱条件
同“2.1”项下色谱条件。
2.8.2 混合对照品溶液的制备同“2.2”项内容。
2.8.3 供试品溶液的制备同“2.3”项下供试品溶液的制备方法。
2.8.4 线性关系考察取混合对照品溶液,等比稀释,注入液相色谱仪,测定。以对照品质量浓度为横坐标(X),以对照品的峰面积为纵坐标(Y),绘制标准曲线,得线性回归方程,分别为五味子醇甲Y=1.046 2 X+1.250 1,r=0.999 9;咖啡酸Y=1.108 1 X-0.144,r=0.999 9;阿魏酸Y=1.303 5 X-0.232 9,r=0.999 9;五味子甲素Y=1.051 1 X-0.111,r=0.999 9;五味子乙素Y=1.034 X-0.716 6,r=0.999 9;五味子酯甲Y=1.017 4 X-1.009 1,r=0.999 9。五味子醇甲在2.99~95.61 μg/mL、咖啡酸在3.38~108.02 μg/mL、阿魏酸在3.60~115.33 μg/mL、五味子甲素在3.26~104.17 μg/mL、五味子乙素在2.89~92.45 μg/mL、五味子酯甲在2.81~89.77 μg/mL,呈良好的线性关系。
2.8.5 精密度试验取批号为150301的QPG,制备供试品溶液,连续进样6针,以峰面积计算各指标成分RSD值,五味子醇甲为0.11%、咖啡酸为0.06%、阿魏酸为0.10%、五味子甲素为0.15%、五味子乙素为0.23%、五味子酯甲为0.12%。
2.8.6 稳定性试验取批号为150301的QPG,研细,取2 g,精密称定,按“2.3”项方法制备供试品溶液,精密吸取10 μL,分别于0、2、6、10、14、18、24 h注入液相色谱仪,以峰面积为指标计算各成分的RSD值,五味子醇甲为0.34%、咖啡酸为0.11%、阿魏酸为0.11%、五味子甲素为0.17%、五味子乙素为0.30%、五味子酯甲为0.25%。结果表明供试品溶液24 h内具有良好的稳定性。
2.8.7 重复性试验取批号为150301的QPG,研细,取2 g,精密称定,按“2.3”项方法平行制备6份供试品溶液,按“2.8.1”项条件测定,计算各指标成分的质量分数。五味子醇甲、咖啡酸、阿魏酸、五味子甲素、五味子乙素、五味子酯甲的质量分数分别为0.195、0.417、0.302、0.209、0.131、0.152 mg/g,RSD值分别为0.32%、0.18%、0.27%、0.39%、0.48%、0.68%,结果表明本方法重复性良好。
2.8.8 加样回收率试验取批号为150301的QPG,研细,取1 g,取9份,精密称定,置具塞锥形瓶中,3份1组,分别精密加入五味子醇甲195.58 μg/mL、咖啡酸417.35 μg/mL、阿魏酸302.11 μg/mL、五味子甲素209.64 μg/mL、五味子乙素131.50 μg/mL、五味子酯甲152.08 μg/mL的混合对照品溶液0.8、1.0、1.2 mL,精密加入50%甲醇25 mL,超声提取30 min,放冷,摇匀,离心,取上清液,即得。测定,计算回收率。结果五味子醇甲、咖啡酸、阿魏酸、五味子甲素、五味子乙素、五味子酯甲的平均回收率分别为99.62%、99.86%、99.47%、99.48%、98.49%、98.43%,RSD分别为0.59%、0.32%、0.60%、0.62%、0.76%、0.78%。
2.8.9 样品测定结果取10批QPG,按照“2.3”项下方法制备供试品溶液,按照“2.1”项下色谱条件进样分析,分别计算6种成分的质量分数,结果见表 1。
|
|
表 1 QPG样品测定结果 (n=2) Table 1 Determination of QPG samples (n=2) |
可见10批QPG样品中咖啡酸在0.412~0.429 mg/g,阿魏酸在0.302~0.317 mg/g,五味子醇甲在0.182~0.195 mg/g,五味子酯甲在0.179~0.195 mg/g,五味子甲素在0.203~0.215 mg/g,五味子乙素在0.131~0.144 mg/g,不同批次间各指标成分的量变化较小,样品质量较稳定。
3 讨论通过DAD检测器在190~400 nm范围进行全波长扫描,结果发现在250 nm波长时,色谱峰多,可代表的信息较全面,色谱峰基线平稳且各色谱峰分离较好,因此选择250 nm作为指纹图谱的采集波长同时作为五味子醇甲、咖啡酸、阿魏酸、五味子甲素、五味子乙素、五味子酯甲6个成分定量测定的波长。
通过对供试品的提取方法、提取时间和提取溶剂用量的考察,确定了本实验中的供试品溶液制备方法,适用于指纹图谱分析;比较了甲醇-0.02%三氟乙酸、甲醇-水、甲醇-0.2%甲酸、乙腈-水系统对指纹图谱的影响,结果甲醇-0.2%甲酸流动相系统所得指纹图谱中各色谱峰的分离情况和峰形较好;比较了使用Waters symmetry C18(250 mm×4.6 mm,5 μm)、Phenomenex Luna C18(250 mm×4.6 mm,5 μm)和Kromasil C18(250 mm×4.6 mm,5 μm)3种色谱柱对指纹图谱的影响,结果3种色谱柱无明显差异。比较了柱温为25、30、35 ℃所得图谱,结果柱温为30 ℃时所得指纹图谱中各色谱峰分离较好;比较了体积流量为0.8、1.0、1.2 mL/min所得图谱,结果体积流量为1.0 mL/min时所得指纹图谱中各色谱峰分离较好。方法学验证结果表明实验中所采用的检测方法专属性强,耐用性较好。
10批QPG定量测定结果和指纹图谱显示,该制剂中指标成分质量较稳定,不同批次间样品中指标成分量差异不大。10批不同批次的QPG指纹图谱具有较好的相似度、相对保留时间和相对峰面积的比值范围。标示出的25个共有峰主要来自于川芎、黄芪和五味子。本实验根据QPG处方中各药材特性,建立了指纹图谱并建立了五味子醇甲、咖啡酸、阿魏酸、五味子甲素、五味子乙素、五味子酯甲6个成分的定量测定方法,该检测方法简便准确,可以更好地控制QPG的质量。
| [1] | 童佳兵, 王传博, 彭波, 等. 芪白平肺胶囊治疗慢性阻塞性肺疾病痰瘀阻肺证疗效分析[J]. 中华中医药学刊, 2012, 30(1):44–45. |
| [2] | 陆梅. 423例COPD中医证候分布特点及芪白平肺胶囊对COPD痰瘀阻肺证模型大鼠能量代谢影响的研究[D].合肥:安徽中医药大学, 2016. |
| [3] | 尹婷婷, 李泽庚, 王婕琼, 等. 芪白平肺胶囊对慢性阻塞性肺疾病肺血管收缩大鼠肺功能及内皮素水平-1、缺氧诱导因子-1α的影响[J]. 长春中医药大学学报, 2014, 30(5):793–795. |
| [4] | 童祥丽. 367例COPD临床疗效回顾性分析及芪白平肺胶囊含药血清对低氧大鼠肺动脉平滑肌细胞凋亡的影响[D].合肥:安徽中医药大学, 2016. |
| [5] | 方莉, 王传博, 王婕琼, 等. 芪白平肺胶囊对慢性阻塞性肺疾病痰瘀阻肺证大鼠血清Rock-1、Rock-2表达的影响[J]. 成都中医药大学学报, 2015, 38(3):13–16. |
| [6] | 付娟, 张海弢, 杨素德, 等. HPLC法同时测定芪白平肺颗粒中4种皂苷类成分的含量[J]. 中国药房, 2015, 26(33):4698–4700. |
| [7] | 靳瑞婷, 杨素德, 付娟, 等. 一测多评法测定芪白平肺颗粒中8种皂苷类成分[J]. 中草药, 2015, 46(24):3682–3686. |
| [8] | 冯雪松, 刘雅茹, 孟繁浩, 等. 五味子药材HPLC指纹图谱的研究[J]. 化学与生物工程, 2006, 5(23):60–62. |
| [9] | 付绍平, 杨博, 陈彤, 等. 北五味子的液相色谱指纹图谱的建立[J]. 色谱, 2008, 1(26):64–67. |
| [10] | 王英婷, 韩勇. 川芎药材HPLC法指纹图谱的研究[J]. 中国药事, 2011, 25(10):1017–1019. |
| [11] | 秦建平, 吴建雄, 毕宇安, 等. HPLC同时测定益心舒片中五味子醇甲、五味子酯甲、五味子甲素、五味子乙素和丹参酮A的含量[J]. 中国实验方剂学杂志, 2012, 18(2):77–79. |
| [12] | 刘芷, 贾英, 赵旭, 等. 五味子的UPLC指纹图谱研究[J]. 中草药, 2014, 45(11):1631–1633. |
| [13] | 胡芳弟, 赵健雄, 封士兰, 等. 黄芪的高效液相色谱指纹图谱及主成分含量测定[J]. 中药材, 2004, 27(11):831–834. |
| [14] | 杨孝容, 向清祥, 熊俊如, 等. HPLC测定柏子养心丸中五味子酯甲、五味子甲素和五味子乙素的含量[J]. 药物分析杂志, 2006, 26(11):1558–1561. |
| [15] | 张婷, 郑夺, 王文彤, 等. 指纹图谱结合一测多评模式在参芎养心颗粒质量评价中的应用研究[J]. 中草药, 2015, 46(13):1920–1925. |
| [16] | 刘洋, 石任兵, 刘斌, 等. 川芎药材化学成分HPLC指纹图谱研究[J]. 北京中医药大学学报, 2006, 29(5):335–337. |
| [17] | 林夏, 崔培超, 徐桂红, 等. 基于UPLC的注射用活血通络指纹图谱研究及多成分定量测定[J]. 中草药, 2016, 47(2):262–266. |
 2017, Vol. 48
2017, Vol. 48


