2. 中国科学院上海药物研究所 新药研究国家重点实验室, 上海 201203
2. State Key Laboratory of Drug Research, Shanghai Institute of Materia Medica, Chinese Academy of Sciences, Shanghai 201203, China
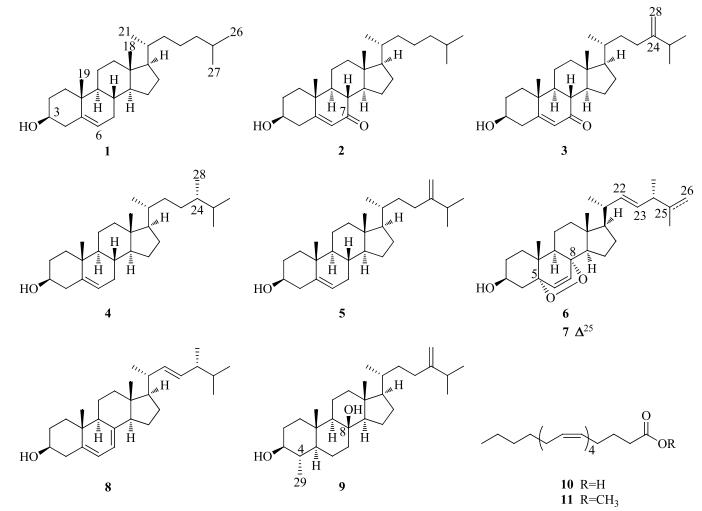
软珊瑚是海洋低等无脊椎动物,生物分类学上属于腔肠动物门(Coelenterata)珊瑚虫纲(Anthozoa)八放珊瑚亚纲(Octocorallia)软珊瑚目(或称海鸡冠目,Alcyonacea)。该类生物富含结构新颖、活性多样的次级代谢产物,是获取海洋活性先导化合物的重要资源宝库[1-2]。我国南海生态环境保存完整,物种多样性丰富,具有独特的软珊瑚资源,其中的短指软珊瑚到处可见[3]。多年来,短指软珊瑚一直是海洋天然产物研究的热点,其次级代谢产物涉及脂类、甾醇、萜类等不同新颖结构类型的化合物。而且体外活性筛选实验表明,这些化合物具有抗炎、抗菌、抗氧化、抗肿瘤等多方面的生物活性[2, 4]。为了开发利用我国的海洋生物资源,从中寻找更多具有生物活性及药用前景的海洋天然产物[5-9],本课题组对采自我国南海的短指软珊瑚的化学成分开展了前期研究,从中发现了多羟基甾醇、倍半萜、二萜等多种新颖结构类型的次级代谢产物,而且其中一些化合物具有抑制人蛋白酪氨酸酶、抗菌、神经保护等多种显著的生物活性[10-13]。本实验对短指软珊瑚Sinularia sp.开展进一步的化学成分研究,发现了11个化合物(图 1),分别鉴定为胆固醇(1)、3β-羟基胆甾-5-烯-7-酮(2)、3β-羟基麦角甾-5, 24 (28)-二烯-7-酮(3)、菜油甾醇(4)、24-亚甲基胆固醇(5)、过氧化麦角甾醇(6)、axinysterol(7)、麦角甾醇(8)、(3β, 4α, 5α, 8β)-4-甲基麦角甾-24(28)-烯-3, 8-二醇(9)、花生四烯酸(10)、花生四烯酸甲酯(11)。其中化合物1~9属于3种不同类型的甾醇,化合物10、11属于不饱和脂类。化合物7和11为首次从短指软珊瑚属中分离得到。
|
图 1 化合物1~11的结构 Fig.1 Structures of compounds 1-11 |
1 仪器与材料
Bruker DRX-400核磁共振仪(德国Bruker公司);Finnigan-MAT-95型质谱仪(美国Finnigan公司);Q-TOF Micro LC-MS质谱仪(美国Waters公司);Shimadzu LC-6AD制备液相色谱仪(日本岛津制作所);Shimadzu SPD-20A紫外检测器(日本岛津制作所);Sephadex LH-20(瑞典Amersham Biosciences公司);柱色谱硅胶(200~300、300~400目,青岛海洋化工有限公司);GF254薄层色谱硅胶板(烟台江友硅胶开发有限公司);色谱级甲醇、乙腈为DiKMA有限公司产品;其他有机试剂均为分析纯,购自国药集团化学试剂有限公司。
实验材料于2011年9月采自我国海南陵水海域水下15 m处,采集后立即冷冻备用。由中国科学院南海海洋研究所的黄晖教授鉴定为南海短指软珊瑚Sinularia sp.。样品标本(LS-179)保存在中国科学院上海药物研究所国家新药研究重点实验室。
2 提取与分离冷冻的软珊瑚样品LS-179(干质量75 g)切碎后于室温下用丙酮超声提取5次,每次15 min,提取液减压浓缩除去有机溶剂,得到棕色总浸膏。将总浸膏加水混悬,用等体积的乙醚及正丁醇各萃取3次,收集有机相萃取液,减压浓缩分别得乙醚粗浸膏1.1 g和正丁醇粗浸膏500 mg。乙醚粗浸膏经硅胶(200~300目)柱色谱,石油醚-乙醚(乙醚0→100%)梯度洗脱,分为A~E共5个部位。采取与前期研究相同的分离手段[10],组分C先后经过凝胶Sephadex LH-20柱色谱(石油醚-氯仿-甲醇2:1:1)和硅胶(300~400目)柱色谱(石油醚-乙醚25:1、10:1),得到化合物1(8.9 mg)、9(31.1 mg)、10(211.9 mg)、11(68.5 mg)和亚组分C1。C1经高效液相分离(甲醇-水95:5,2.0 mL/min)得到化合物2(45.0 mg)和3(3.6 mg)。组分D先后经过凝胶Sephadex LH-20柱色谱(石油醚-氯仿-甲醇2:1:1)和硅胶(300~400目)柱色谱(石油醚-乙醚10:1、6:1),得到化合物4(11.6 mg)、5(3.9 mg)、6(2.7 mg)、7(1.3 mg)和8(4.5 mg)。
3 结构鉴定化合物1:白色针晶(石油醚-乙醚25:1),分子式为C27H46O。EI-MS m/z: 386 [M]+。1H-NMR (400 MHz, CDCl3) δ: 5.33 (1H, d, J=2.5 Hz, H-6), 3.52 (1H, m, H-3), 1.01 (3H, s, H-19), 0.91 (3H, d, J=6.6 Hz, H-21), 0.86 (6H, J=6.6 Hz, H-26, 27), 0.68 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 37.3 (C-1), 31.7 (C-2), 71.8 (C-3), 42.3 (C-4), 140.8 (C-5), 121.7 (C-6), 31.9 (C-7), 31.8 (C-8), 50.2 (C-9), 36.5 (C-10), 21.1 (C-11), 39.8 (C-12), 42.3 (C-13), 56.8 (C-14), 24.3 (C-15), 28.3 (C-16), 56.2 (C-17), 11.9 (C-18), 19.4 (C-19), 35.8 (C-20), 18.7 (C-21), 36.2 (C-22), 23.8 (C-23), 39.6 (C-24), 28.3 (C-25), 22.6 (C-26), 22.8 (C-27)。以上数据与文献报道一致[14-15],故鉴定化合物1为胆固醇。
化合物2:白色固体,分子式为C27H44O2。ESI-MS m/z: 423.3 [M+Na]+。1H-NMR (400 MHz, CDCl3) δ: 5.69 (1H, s, H-6), 3.68 (1H, m, H-3), 1.20 (3H, s, H-19), 0.92 (3H, d, J=6.8 Hz, H-21), 0.87 (3H, d, J=6.9 Hz, H-26), 0.86 (3H, d, J=6.8 Hz, H-27), 0.68 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 36.3 (C-1), 31.3 (C-2), 70.5 (C-3), 41.9 (C-4), 165.1 (C-5), 126.1 (C-6), 202.3 (C-7), 45.5 (C-8), 50.0 (C-9), 38.4 (C-10), 21.3 (C-11), 38.8 (C-12), 41.8 (C-13), 50.0 (C-14), 28.6 (C-15), 26.4 (C-16), 54.8 (C-17), 12.0 (C-18), 17.3 (C-19), 35.8 (C-20), 18.9 (C-21), 36.4 (C-22), 23.9 (C-23), 39.6 (C-24), 28.1 (C-25), 22.9 (C-26), 22.6 (C-27)。以上数据与文献报道一致[16-17],故鉴定化合物2为3β-羟基胆甾-5-烯-7-酮。
化合物3:白色固体,分子式为C27H44O2。ESI-MS m/z: 435.3 [M+Na]+。1H-NMR (400 MHz, CDCl3) δ: 5.69 (1H, s, H-6), 4.72 (1H, brs, H-28a), 4.66 (1H, brs, H-28b), 3.68 (1H, m, H-3), 1.20 (3H, s, H-19), 1.03 (6H, d, J=6.9 Hz, H-26, 27), 0.96 (3H, d, J=6.9 Hz, H-21), 0.69 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 36.3 (C-1), 31.2 (C-2), 70.5 (C-3), 41.9 (C-4), 165.1 (C-5), 126.1 (C-6), 202.3 (C-7), 45.5 (C-8), 50.0 (C-9), 38.4 (C-10), 21.3 (C-11), 38.8 (C-12), 43.2 (C-13), 50.0 (C-14), 26.4 (C-15), 28.6 (C-16), 54.8 (C-17), 12.0 (C-18), 17.3 (C-19), 35.8 (C-20), 18.9 (C-21), 34.6 (C-22), 31.0 (C-23), 156.8 (C-24), 33.8 (C-25), 21.9 (C-26), 22.0 (C-27), 106.0 (C-28)。以上数据与文献报道一致[18-19],故鉴定化合物3为3β-羟基麦角甾-5, 24(28)-二烯-7-酮。
化合物4:白色针晶(石油醚-乙醚10:1),分子式为C28H48O。EI-MS m/z: 400 [M]+。1H-NMR (400 MHz, CDCl3) δ: 5.35 (1H, d, J=2.5 Hz, H-6), 3.52 (1H, m, H-3), 1.01 (3H, s, H-19), 0.91 (3H, d, J=6.6 Hz, H-21), 0.86 (6H, d, J=6.8 Hz, H-26, 27), 0.78 (3H, d, J=6.5 Hz, H-28), 0.67 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 37.2 (C-1), 31.7 (C-2), 71.7 (C-3), 42.2 (C-4), 140.7 (C-5), 121.6 (C-6), 31.8 (C-7), 31.6 (C-8), 50.2 (C-9), 36.5 (C-10), 21.0 (C-11), 39.7 (C-12), 46.0 (C-13), 56.8 (C-14), 24.3 (C-15), 28.2 (C-16), 56.7 (C-17), 11.8 (C-18), 19.5 (C-19), 36.3 (C-20), 18.8 (C-21), 33.6 (C-22), 31.6 (C-23), 39.0 (C-24), 33.8 (C-25), 19.0 (C-26), 18.9 (C-27), 15.5 (C-28)。以上数据与文献报道一致[20-21],故鉴定化合物4为菜油甾醇。
化合物5:白色针晶(石油醚-乙醚10:1),分子式为C28H46O。EI-MS m/z: 398 [M]+。1H-NMR (400 MHz, CDCl3) δ: 5.34 (1H, d, J=2.5 Hz, H-6), 4.70 (1H, brs, H-28a), 4.65 (1H, brs, H-28b), 3.50 (1H, m, H-3), 1.02 (6H, d, J=6.8 Hz, H-26, 27), 1.01 (3H, s, H-19), 0.94 (3H, d, J=6.6 Hz, H-21), 0.68 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 37.2 (C-1), 31.9 (C-2), 71.9 (C-3), 42.2 (C-4), 140.7 (C-5), 121.6 (C-6), 31.8 (C-7), 35.7 (C-8), 50.2 (C-9), 36.5 (C-10), 21.0 (C-11), 39.7 (C-12), 42.3 (C-13), 56.8 (C-14), 24.3 (C-15), 28.2 (C-16), 56.0 (C-17), 11.8 (C-18), 19.4 (C-19), 35.0 (C-20), 18.8 (C-21), 33.8 (C-22), 31.8 (C-23), 156.9 (C-24), 33.8 (C-25), 21.8 (C-26), 22.0 (C-27), 106.0 (C-28)。以上数据与文献报道一致[22],故鉴定化合物5为24-亚甲基胆固醇。
化合物6:白色粉末,分子式为C28H44O3。EI-MS m/z: 428 [M]+。1H-NMR (400 MHz, CDCl3) δ: 6.50 (1H, d, J=8.4 Hz, H-6), 6.22 (1H, d, J=8.4 Hz, H-7), 5.20 (1H, dd, J=15.2, 7.6 Hz, H-22), 5.15 (1H, dd, J=15.2, 7.6 Hz, H-23), 3.95 (1H, m, H-3), 0.99 (3H, d, J=6.6 Hz, H-21), 0.90 (3H, d, J=6.8 Hz, H-28), 0.87 (3H, s, H-19), 0.82 (3H, d, J=6.8 Hz, H-27), 0.80 (3H, d, J=6.8 Hz, H-26), 0.79 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 34.6 (C-1), 30.1 (C-2), 66.5 (C-3), 36.9 (C-4), 82.1 (C-5), 135.4 (C-6), 130.7 (C-7), 79.4 (C-8), 51.0 (C-9), 36.9 (C-10), 20.6 (C-11), 39.3 (C-12), 44.5 (C-13), 51.6 (C-14), 23.4 (C-15), 28.6 (C-16), 56.1 (C-17), 12.8 (C-18), 18.1 (C-19), 39.7 (C-20), 20.8 (C-21), 135.2 (C-22), 132.3 (C-23), 42.7 (C-24), 33.0 (C-25), 19.6 (C-26), 19.9 (C-27), 17.5 (C-28)。以上数据与文献报道一致[23],故鉴定化合物6为过氧化麦角甾醇。
化合物7:白色粉末,分子式为C28H42O3。EI-MS m/z: 426 [M]+。1H-NMR (400 MHz, CDCl3) δ: 6.50 (1H, d, J=8.4 Hz, H-6), 6.23 (1H, d, J=8.4 Hz, H-7), 5.25 (1H, dd, J=15.0, 7.5 Hz, H-22), 5.23 (1H, dd, J=15.0, 7.5 Hz, H-23), 4.69 (2H, brs, H-26), 3.96 (1H, m, H-3), 2.69 (1H, m, H-24), 1.66 (3H, brs, H-27), 1.07 (3H, d, J=6.6 Hz, H-28), 0.99 (3H, d, J=6.6 Hz, H-21), 0.88 (3H, s, H-19), 0.81 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 34.7 (C-1), 30.1 (C-2), 66.4 (C-3), 37.0 (C-4), 82.1 (C-5), 135.4 (C-6), 130.7 (C-7), 79.4 (C-8), 51.0 (C-9), 36.9 (C-10), 20.6 (C-11), 39.3 (C-12), 44.6 (C-13), 51.6 (C-14), 23.4 (C-15), 28.6 (C-16), 56.1 (C-17), 12.9 (C-18), 18.2 (C-19), 39.6 (C-20), 20.6 (C-21), 135.3 (C-22), 131.9 (C-23), 43.6 (C-24), 149.7 (C-25), 108.9 (C-26), 20.6 (C-27), 18.8 (C-28)。以上数据与文献报道一致[24-25],故鉴定化合物7为axinysterol。
化合物8:白色固体,分子式为C28H44O。EI-MS m/z: 396 [M]+。1H-NMR (400 MHz, CDCl3) δ: 5.56 (1H, m, H-6), 5.38 (1H, m, H-7), 5.22 (1H, dd, J=15.0, 7.3 Hz, H-22), 5.17 (1H, dd, J=15.0, 7.3 Hz, H-23), 3.64 (1H, m, H-3), 1.03 (3H, d, J=6.6 Hz, H-21), 0.94 (3H, s, H-19), 0.92 (3H, d, J=6.8 Hz, H-28), 0.84 (3H, d, J=6.8 Hz, H-26), 0.82 (3H, d, J=6.6 Hz, H-27), 0.63 (3H, s, H-18);13C-NMR (100 MHz, CDCl3) δ: 38.4 (C-1), 32.0 (C-2), 70.4 (C-3), 40.8 (C-4), 139.8 (C-5), 19.6 (C-6), 116.3 (C-7), 141.3 (C-8), 46.2 (C-9), 37.0 (C-10), 21.3 (C-11), 39.1 (C-12), 42.8 (C-13), 54.6 (C-14), 23.0 (C-15), 28.3 (C-16), 55.7 (C-17), 12.1 (C-18), 16.3 (C-19), 40.4 (C-20), 21.1 (C-21), 135.5 (C-22), 132.0 (C-23), 42.8 (C-24), 33.1 (C-25), 19.9 (C-26), 19.6 (C-27), 17.6 (C-28)。以上数据与文献报道一致[26-27],故鉴定化合物8为麦角甾醇。
化合物9:白色固体,分子式为C29H50O2。EI-MS m/z: 430 [M]+。1H-NMR (400 MHz, CDCl3) δ: 4.70 (1H, brs, H-28a), 4.64 (1H, brs, H-28b), 3.07 (1H, dt, J=9.2, 4.7 Hz, H-3), 1.02 (6H, d, J=6.6 Hz, H-26, 27), 1.00 (3H, s, H-19), 0.96 (3H, d, J=6.2 Hz, H-21), 0.95 (3H, s, H-18), 0.92 (3H, d, J=6.6 Hz, H-29);13C-NMR (100 MHz, CDCl3) δ: 37.5 (C-1), 30.5 (C-2), 76.7 (C-3), 38.5 (C-4), 51.5 (C-5), 20.0 (C-6), 39.8 (C-7), 73.6 (C-8), 56.3 (C-9), 36.3 (C-10), 19.0 (C-11), 41.0 (C-12), 43.0 (C-13), 59.4 (C-14), 18.3 (C-15), 27.7 (C-16), 56.7 (C-17), 13.6 (C-18), 13.5 (C-19), 35.1 (C-20), 18.3 (C-21), 34.3 (C-22), 30.9 (C-23), 156.9 (C-24), 33.8 (C-25), 21.8 (C-26), 22.0 (C-27), 106.0 (C-28), 15.1 (C-29)。以上数据与文献报道一致[10],故鉴定化合物9为 (3β, 4α, 5α, 8β)-4-甲基麦角甾-24 (28)-烯-3, 8-二醇。
化合物10:无色油状物,分子式为C20H32O2。EI-MS m/z: 304 [M]+。1H-NMR (400 MHz, CDCl3) δ: 5.45~5.30 (8H, m, H-5, 6, 8, 9, 11, 12, 14, 15), 2.90~2.73 (6H, br, H-7, 10, 13), 2.35 (2H, t, J=7.6 Hz, H-2), 2.14~2.08 (2H, m, H-4), 2.07~2.01 (2H, m, H-16), 1.71 (2H, q, J=7.6 Hz, H-3), 1.40~1.20 (6H, br, H-17~19), 0.86 (3H, t, J=7.6 Hz, H-20);13C-NMR (100 MHz, CDCl3) δ: 176.9 (C-1), 33.2 (C-2), 24.6 (C-3), 26.5 (C-4), 128.9 (C-5), 128.2 (C-6), 25.6 (C-7), 128.8 (C-8), 127.9 (C-9), 25.6 (C-10), 128.1 (C-11), 128.6 (C-12), 25.6 (C-13), 127.5 (C-14), 130.5 (C-15), 27.2 (C-16), 29.3 (C-17), 31.5 (C-18), 22.6 (C-19), 14.0 (C-20)。以上数据与文献报道一致[28-29],故鉴定化合物10为花生四烯酸。
化合物11:无色油状物,分子式为C21H34O2。EI-MS m/z: 318 [M]+。1H-NMR (400 MHz, CDCl3) δ: 5.48~5.29 (8H, m, H-5, 6, 8, 9, 11, 12, 14, 15), 3.66 (3H, s, H-1′), 2.90~2.73 (6H, br, H-7, 10, 13), 2.33 (2H, t, J=7.6 Hz, H-2), 2.14~2.08 (2H, m, H-4), 2.07~2.01 (2H, m, H-16), 1.71 (2H, quinet, J=7.6 Hz, H-3), 1.40~1.20 (6H, brd, H-17, 18, 19), 0.86 (3H, t, J=7.6 Hz, H-20);13C-NMR (100 MHz, CDCl3) δ: 174.0 (C-1), 33.4 (C-2), 24.8 (C-3), 26.5 (C-4), 128.9 (C-5), 128.2 (C-6), 25.6 (C-7), 128.8 (C-8), 127.9 (C-9), 25.6 (C-10), 128.1 (C-11), 128.6 (C-12), 25.6 (C-13), 127.5 (C-14), 130.5 (C-15), 27.2 (C-16), 29.3 (C-17), 31.5 (C-18), 22.6 (C-19), 14.0 (C-20), 51.3 (C-1′)。以上数据与文献报道一致[29-30],故鉴定化合物11为花生四烯酸甲酯。
4 讨论通过对中国南海短指软珊瑚Sinularia sp.的化学成分研究,从中分离得到11个化合物,包含9个甾醇和2个不饱和脂类。其中,化合物7和11为首次从该属软珊瑚中分离得到。
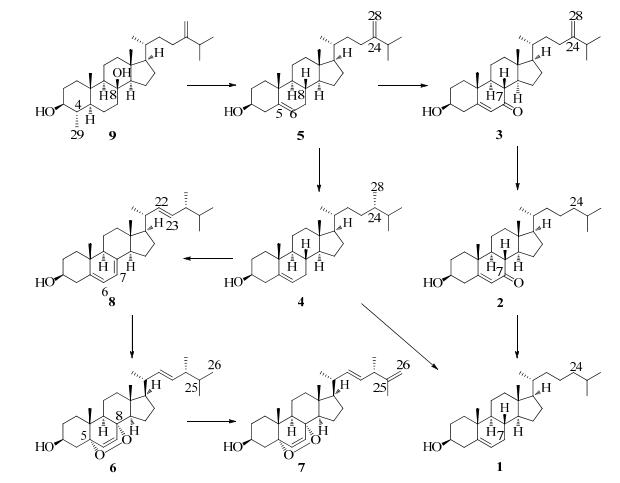
甾醇类化合物在海洋生物中普遍存在,其生物学意义现在还未研究清楚,但不可否认的是其对海洋生物的生长、繁殖、防御等生命活动具有重要影响[31]。本实验得到的一系列甾醇类化合物可分为3种类型:胆甾烷型(化合物1、2)、麦角甾烷型(化合物3~8)、4-甲基甾烷型(化合物9)。参考本课题组对南海软珊瑚Scleronephthya sp.化学成分生源关系的探讨[32],对短指软珊瑚Sinularia sp.的化学成分中甾醇类化合物1~9可能产生的生源途径进行初步推测,可能的生源关系如图 2所示。
|
图 2 化合物1~9的生源关系推测 Fig.2 Possible biosynthesis of compounds 1-9 |
在体内生物酶的作用下,4-甲基甾烷型化合物9经过脱甲基、脱羟基、脱氢等一系列生物转化,得到麦角甾烷型化合物5。麦角甾烷型化合物3由5经C-7位生物氧化得到,其C-24位还原、脱甲基后生成2,2再经还原生成1。甾醇1也可由5的C-24位还原产物4经脱甲基得到。麦角甾醇8是4的C-7/8、C-22/23脱氢衍生物,其与活性氧分子的Diels-Alder加成反应得到6,该产物经C-25/26脱氢衍生出7。
上述研究结果进一步丰富了短指软珊瑚的化学成分多样性,为软珊瑚的药效物质的探索提供参考。
| [1] | Liang L F, Guo Y W. Terpenes from the soft corals of the genus Sarcophyton:chemistry and biological activities[J]. Chem Biodivers, 2013, 10(12): 2161–2196. DOI:10.1002/cbdv.v10.12 |
| [2] | 梁林富, 李玉芬, 刘海利, 等. 短指软珊瑚属次级代谢产物化学成分及其生物活性研究进展[J]. 国际药学研究杂志, 2013, 40(6):643–649. |
| [3] | 郭跃伟. 海洋天然产物和海洋药物研究的历史、现状和未来[J]. 自然杂志, 2009, 31(1):27–32. |
| [4] | Chen W T, Li Y, Guo Y W. Terpenoids of Sinularia soft corals:chemistry and bioactivity[J]. Acta Pharm Sin B, 2012, 2(3): 227–237. DOI:10.1016/j.apsb.2012.04.004 |
| [5] | Jiang C S, Müller W E G, Schröder H C, et al. Disulfide-and multisulfide-containing metabolites from marine organisms[J]. Chem Rev, 2012, 112(4): 2179–2207. DOI:10.1021/cr200173z |
| [6] | Liang L F, Kurtán T, Mándi A, et al. Unprecedented diterpenoids as a PTP1B inhibitor from the Hainan soft coral Sarcophyton trocheliophorum Marenzeller[J]. Org Lett, 2013, 15(2): 274–277. DOI:10.1021/ol303110d |
| [7] | Liang L F, Wang T, Cai Y S, et al. Brominated polyunsaturated lipids from the Chinese sponge Xestospongia testudinaria as a new class of pancreatic lipase inhibitors[J]. Eur J Med Chem, 2014, 79: 290–297. DOI:10.1016/j.ejmech.2014.04.003 |
| [8] | Zhou Z F, Menna M, Cai Y S, et al. Polyacetylenes of marine origin:chemistry and bioactivity[J]. Chem Rev, 2015, 115(3): 1543–1596. DOI:10.1021/cr4006507 |
| [9] | Huang R Y, Chen W T, Kurtán T, et al. Bioactive isoquinolinequinone alkaloids from the South China Sea nudibranch Jorunna funebris and its sponge-prey Xestospongia sp.[J]. Future Med Chem, 2016, 8(1): 17–27. DOI:10.4155/fmc.15.169 |
| [10] | Liang L F, Wang X J, Zhang H Y, et al. Bioactive polyhydroxylated steroids from the Hainan soft coral Sinularia depressa Tixier-Durivault[J]. Bioorg Med Chem Lett, 2013, 23(5): 1334–1337. DOI:10.1016/j.bmcl.2012.12.087 |
| [11] | Chen W T, Liu H L, Yao L G, et al. 9, 11-Secosteroids and polyhydroxylated steroids from two South China Sea soft corals Sarcophyton trocheliophorum and Sinularia flexibilis[J]. Steroids, 2014, 92: 56–61. DOI:10.1016/j.steroids.2014.08.027 |
| [12] | Jiang C S, Li Y, Han G Y, et al. Further casbane-type diterpenes from the soft coral Sinularia depressa[J]. Chin J Nat Med, 2014, 12(11): 853–856. |
| [13] | Chen W T, Li J, Wang J R, et al. Structural diversity of terpenoids in the soft coral Sinularia flexibilis, evidenced by a collection from the South China Sea[J]. RSC Adv, 2015, 5(30): 23973–23980. DOI:10.1039/C5RA01151E |
| [14] | 曹馨, 唐旭利, 李平林, 等. 中国南海短指软珊瑚化学成分研究[J]. 中国海洋药物, 2012, 31(2):38–42. |
| [15] | 刘艳萍, 黄立刚, 李科凯, 等. 玫瑰树中非生物碱类化学成分研究[J]. 中草药, 2015, 46(6):798–802. |
| [16] | Notaro G, Piccialli V, Sica D. New steroidal hydroxyketones and closely related diols from the marine sponge Cliona copiosa[J]. J Nat Prod, 1992, 55(11): 1588–1594. DOI:10.1021/np50089a005 |
| [17] | 雷辉, 周雪峰, 杨亚玲, 等. 南海多室草苔虫甾醇类化学成分研究[J]. 中药材, 2011, 34(2):180–183. |
| [18] | Guerriero A, D'Ambrosio M, Pietra F, et al. Pteridines, sterols, and indole derivatives from the lithistid sponge Corallistes undulatus of the Coral Sea[J]. J Nat Prod, 1993, 56(11): 1962–1970. DOI:10.1021/np50101a015 |
| [19] | 李婷, 廖小建, 徐石海. 丛柳珊瑚的化学成分研究[J]. 中国药学杂志, 2010, 45(6):420–422. |
| [20] | 姚宗仁, 钟惠民. 豆荚软珊瑚 (Lobophytum sp.) 化学成分的研究[J]. 青岛科技大学学报:自然科学版, 2009, 30(2):135–137. |
| [21] | Abou-Hussein D R, Badr J M, Youssef D T A. Dragmacidoside:a new nucleoside from the Red Sea sponge Dragmacidon coccinea[J]. Nat Prod Res, 2014, 28(15): 1134–1141. DOI:10.1080/14786419.2014.915828 |
| [22] | Lu W, Zhang C, Zeng L, et al. Synthesis of polyhydroxysterols (V):efficient and stereospecific synthesis of 24-methylene-cholest-5-ene-3β, 7α-diol and its C-7 epimer[J]. Steroids, 2004, 69(13/14): 803–808. |
| [23] | 邵志宇, 郭跃伟, 于嘉陵, 等. 南海海绵Dysidea sp.的化学成分研究[J]. 天然产物研究与开发, 2004, 16(1):19–22. |
| [24] | 李震宇, 郭跃伟. 南海海绵Axinyssa sp.的化学成分[J]. 中国天然药物, 2008, 6(3):183–185. |
| [25] | Iguchi K, Shimura H, Yang Z, et al. A new 5α, 8α-epidioxy sterol from the Okinawan marine sponge of the Axinyssa genus[J]. Steroids, 1993, 58(9): 410–413. DOI:10.1016/0039-128X(93)90080-7 |
| [26] | 贾睿, 郭跃伟, 黄才国. 两种中国南海海绵的化学成分和生物活性研究[J]. 天然产物研究与开发, 2013, 25(6):767–771. |
| [27] | 张庆华, 田峰, 李谦, 等. 红海榄内生真菌BGD22抑菌活性成分的初步研究[J]. 中国新药杂志, 2010, 19(24):2331–2335. |
| [28] | Jyothirmayi N, Ramadoss C S, Divakar S. Nuclear magnetic resonance studies of cyclodextrin complexes of linoleic acid and arachidonic acid[J]. J Agric Food Chem, 1991, 39(12): 2123–2127. DOI:10.1021/jf00012a004 |
| [29] | Januar H I, Chasanah E, Motti C A, et al. Cytotoxic cembranes from Indonesian specimens of the soft coral Nephthea sp.[J]. Mar Drugs, 2010, 8(7): 2142–2152. DOI:10.3390/md8072142 |
| [30] | Rui F, Boland W. Algal pheromone biosynthesis:stereochemical analysis and mechanistic implications in gametes of Ectocarpus siliculosus[J]. J Org Chem, 2010, 75(12): 3958–3964. DOI:10.1021/jo1004372 |
| [31] | Sarma N S, Krishna M S, Pasha S G, et al. Marine metabolites:the sterols of soft coral[J]. Chem Rev, 2009, 109(6): 2803–2828. DOI:10.1021/cr800503e |
| [32] | 严小红, 郭跃伟, 朱兴族, 等. 中国南海软珊瑚Scleronephthya sp.化学成分的研究[J]. 有机化学, 2004, 24(10):1233–1238. |
 2017, Vol. 48
2017, Vol. 48


