2. 中国医学科学院 北京协和医学院药物研究所, 北京 100050 ;
3. 中国医学科学院 北京协和医学院药用植物研究所, 北京 100193
2. Institute of Materia Medica, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100050, China ;
3. Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100193, China
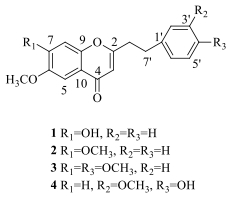
沉香为瑞香科(Thymelaeaceae)沉香属AquilariaLam.植物含有黑色树脂的木材,主要分布于东南亚地区。沉香是中国、日本、印度、东南亚以及中东国家传统名贵的药材和天然香料[1]。国产沉香的来源植物为白木香Aquilaria sinensis (Lour.) Spreng.,主要分布于我国海南、广东、广西、福建等省区。沉香作为我国传统中药,具有降气温中、暖肾纳气的功能,主要用于治疗喘息、呕吐呃逆、脘腹胀痛、腰膝虚冷、大肠虚秘、小便气淋、男子精冷等症[2]。国内外学者[3-6]先后对沉香的化学成分进行了研究,从中分离得到了多个倍半萜和色酮类化合物。本课题组在前期研究中,从国产沉香中分离得到多个具有良好生物活性的化合物[7-10]。为进一步研究其化学成分,合理开发利用沉香资源,本实验继续对国产沉香的石油醚提取物进行分离纯化,从中得到4个2-(2-苯乙基)色酮衍生物,分别鉴定为6-甲氧基-7-羟基-2-(2-苯乙基)色酮[6-methoxy-7-hydroxy-2-(2-phenylethyl) chromone,1]、6, 7-二甲氧基-2-(苯乙基)色酮[6, 7-dimethoxy-2-(2-phenylethyl) chromone,2]、6, 7-二甲氧基-2-[2-(4′-甲氧基苯)乙基]色酮(6, 7-dimethoxy-2-[2-(4′-methoxyphenyl) ethyl] chromone,3)、6-甲氧基-2-[2-(3′-甲氧基-4′-羟基苯)乙基]色酮(6-methoxy-2-[2-(3′-methoxy-4′-hydroxyphenyl) ethyl] chromone,4)。化合物1为新化合物,命名为沉香酮J。化合物4为首次从国产沉香中分离得到,结构见图 1。
|
图 1 化合物1~4的结构 Fig.1 Chemical structures of compounds 1-4 |
1 仪器与材料
Nicolet 5700 FT-IR红外光谱仪(美国Thermo公司);Varian MP-400或VNS-600型核磁共振波谱仪(美国Varian公司);Q-trap ESI高分辨质谱仪(美国Agilent公司);半制备型高效液相色谱仪:岛津LC-6AD,岛津RID-10A示差检测器,威马龙数据工作站;Grace Adsorbosphere XL C18反相半制备色谱柱(250 mm×10 mm,5 μm,美国Alltech公司),体积流量为3 mL/min。柱色谱用硅胶和GF254硅胶板为青岛海洋化工厂生产;葡聚糖凝胶Sephadex LH-20(美国Amersham Biosciences公司);实验所用试剂均为北京化工厂生产,分析纯。
药材国产沉香于2009年购自海南省寿南山参业有限公司,由中国医学科学院药用植物研究所郭顺星研究员鉴定为白木香Aquilaria sinensis(Lour.) Spreng.含树脂的木材。
2 提取与分离国产沉香A级7.5 kg,粉碎后用石油醚回流提取3次,每次6~8 h。减压回收溶剂得石油醚提取物258 g。
取石油醚提取物212 g,经硅胶柱色谱,石油醚-醋酸乙酯(100:0→0:100)梯度洗脱得8个流分Fr. 1~8。Fr. 7(12.65 g)用石油醚-丙酮(99:1→9:1)梯度洗脱得到11个亚流分Fr. 7a~7k。Fr. 7c(0.95 g)经凝胶Sephadex LH-20色谱(甲醇)初步分离,然后通过反相半制备HPLC(甲醇-水7:3)纯化得到化合物2(72 mg,tR=16.4 min)。Fr. 7d(1.46 g)经硅胶柱色谱,二氯甲烷-甲醇(99:1→97:3)梯度洗脱后经反相半制备HPLC(甲醇-水7:3)得到化合物3(15 mg,tR=15.3 min)。Fr. 7f(1.48 g)经硅胶柱色谱,二氯甲烷-甲醇(99:1→9:1)梯度洗脱得到11个亚流分Fr. 7f-1~7f-11,Fr. 7f-1(128 mg)经反相半制备HPLC(甲醇-水67:33)得到化合物4(2.9 mg,tR=12.7 min)、1(1.7 mg,tR=14.8 min)。
3 结构鉴定化合物1:白色无定形粉末。HR-ESI-MS m/z: 297.111 8 [M+H]+ (C18H17O4,计算值为297.112 1);UVλmaxMeOH(nm): 211 (4.48), 230 (4.32), 283 (3.81), 319 (3.89);IRνmaxKBr(cm−1): 3 402 (OH), 2 931, 2 573, 1 634, 1 591, 1 547, 1 522, 1 452, 1 388, 1 265, 1 221, 1 183, 1 160, 1 087, 964, 854, 749。高分辨质谱确定化合物1分子式为C18H16O4,不饱和度为11。紫外光谱(211, 230, 283, 319 nm)显示色原酮类衍生物的特征吸收[7]。红外光谱显示羟基(3 402 cm−1)、色原酮类化合物不饱和羰基(1 634 cm−1)、醚(1 160 cm−1)和苯环(1 452, 1 265, 854 cm−1)的吸收峰。化合物1的1H-NMR (400 MHz, Pyridine-d5)谱中(表 1)显示1个甲氧基信号δH 3.75 (3H, s),1个共轭双键的质子信号δH 6.33 (1H, s, H-3),1组单取代芳香苯环的质子信号δH 7.26~7.32 (5H, m, H-2′~6′),2个单峰的芳香质子信号δH 7.86 (1H, s, H-5), 7.26 (1H, s, H-8),提示两者可能位于4取代苯环的对位;2组亚甲基质子信号δH 2.85 (t, J=6.8 Hz, H-8′), 2.97 (t, J=6.8 Hz, H-7′)中的3重峰及偶合常数表明2个亚甲基直接相连。13C-NMR (150 MHz, C5D5N)(表 1)中显示有18个碳,包括1个羰基碳共振信号(δC 177.1),3取代双键碳的共振信号[δC 109.7 (CH)和167.5 (qC)],3个连氧的芳香碳共振信号[δC 147.6 (qC)、153.4 (qC)和154.5 (qC)],1个甲氧基碳的共振信号(δC 55.9),2个亚甲基碳的共振信号(δC 33.1和35.8),以及9个芳香碳的共振信号。以上数据显示化合物1为具有1个甲氧基和1个羟基的2-(2-苯乙基)色原酮衍生物,且取代位点分别为C-6和C-7。上述数据与文献报道的化合物6-羟基-7-甲氧基-2-(2-苯乙基)色原酮[11]的数据非常接近,不同之处在于2个化合物的C-6和C-7的化学位移有少许差异,提示2个化合物的2个取代基团的取代位点可能相反,化合物1的甲氧基可能连接在C-6上。通过1D-NOE差谱分析验证了以上推测。照射甲氧基的质子(δH 3.75)时,引起H-5相对应地明显增益,显示这个甲氧基取代位置位于C-6。因此化合物1的结构被确定为6-甲氧基-7-羟基-2-(2-苯乙基)色原酮,为新化合物,命名为沉香酮J。
|
|
表 1 化合物1的1H-NMR和13C-NMR数据 Table 1 1H-NMR and 13C-NMR data of compound 1 |
化合物2:白色无定形粉末。ESI-MS m/z: 311 [M+H]+,分子式为C19H18O4。1H-NMR (600 MHz, CDCl3) δ: 6.16 (1H, s, H-3), 7.54 (1H, s, H-5), 6.88 (1H, s, H-8), 7.32 (2H, brd, J=7.2 Hz, H-2′, 6′), 7.23 (2H, brd, J=7.2 Hz, H-3′, 5′), 7.25 (1H, brd, J=7.2 Hz, H-4′), 3.08 (2H, t, J=7.8 Hz, H-7′), 2.94 (2H, t, J=7.8 Hz, H-8′), 4.01 (3H, s, -OCH3), 3.99 (3H, s, -OCH3);13C-NMR (150 MHz, CDCl3) δ: 167.6 (C-2), 109.6 (C-3), 177.5 (C-4), 104.4 (C-5), 147.5 (C-6), 154.3 (C-7), 99.6 (C-8), 152.5 (C-9), 117.0 (C-10), 139.8 (C-1′), 128.7 (C-2′), 128.3 (C-3′), 126.6 (C-4′), 128.3 (C-5′), 128.7 (C-6′), 33.1 (C-7′), 36.0 (C-8′), 56.4 (7-OCH3), 56.3 (6-OCH3)。以上数据与文献报道一致[12],故鉴定化合物2为6, 7-二甲氧基-2-(2-苯乙基)色酮。
化合物3:白色无定形粉末。ESI-MS m/z: 341 [M+H]+,分子式为C20H20O5。1H-NMR (400 MHz, CDCl3) δ: 6.45 (1H, s, H-3), 7.49 (1H, s, H-5), 6.88 (1H, s, H-8), 7.07 (2H, brd, J=8.4 Hz, H-2′, 6′), 6.79 (2H, brd, J=8.4 Hz, H-3′, 5′), 2.96 (2H, t, J=7.8 Hz, H-7′), 2.90 (2H, t, J=7.8 Hz, H-8′), 3.97 (3H, s, -OCH3), 3.94 (3H, s, -OCH3), 3.74 (3H, s, -OCH3);13C-NMR (150 MHz, CDCl3) δ: 167.0 (C-2), 109.3 (C-3), 177.6 (C-4), 104.4 (C-5), 148.1 (C-6), 155.2 (C-7), 99.7 (C-8), 153.2 (C-9), 116.9 (C-10), 131.8 (C-1′), 129.4 (C-2′), 114.3 (C-3′), 158.5 (C-4′), 114.3 (C-5′), 129.4 (C-6′), 32.5(C-7′), 36.7 (C-8′), 56.8 (7-OCH3), 56.6 (6-OCH3), 55.5 (4′-OCH3)。以上数据与文献报道一致[13],故鉴定化合物3为6, 7-二甲氧基-2-[2-(4′-甲氧基苯)乙基]色酮。
化合物4:白色无定形粉末。ESI-MS m/z: 327 [M+H]+,分子式为C19H18O5。1H-NMR (400 MHz, CDCl3) δ: 6.14 (1H, s, H-3), 7.55 (1H, d, J=3.2 Hz, H-5), 7.24 (1H, dd, J=9.2, 3.2 Hz, H-7), 7.37 (1H, d, J=9.2 Hz, H-8), 6.67 (1H, d, J=3.2 Hz, H-2′), 6.83 (1H, d, J=8.0 Hz, H-5′), 6.70 (1H, dd, J=8.0, 3.2 Hz, H-6′), 2.99 (2H, t, J=7.6 Hz, H-7′), 2.89 (2H, t, J=7.6 Hz, H-8′), 3.89 (3H, s, -OCH3), 3.82 (3H, s, -OCH3);13C-NMR (100 MHz, CDCl3) δ: 168.3 (C-2), 109.5 (C-3), 178.2 (C-4), 104.8 (C-5), 156.8 (C-6), 123.5 (C-7), 119.2 (C-8), 151.3(C-9), 124.3 (C-10), 131.6 (C-1′), 114.5 (C-2′), 144.2 (C-3′), 146.5 (C-4′), 110.8 (C-5′), 120.9 (C-6′), 32.8(C-7′), 36.4 (C-8′), 55.9 (6-OCH3), 55.8 (3′-OCH3)。以上数据与文献报道一致[11],故鉴定化合物4为6-甲氧基-2-[2-(3′-甲氧基-4′-羟基苯)乙基]色酮。
利用谷氨酸诱导的PC12细胞神经损伤和皮质酮诱导的人类U251细胞神经损伤模型对4个化合物进行神经保护体外活性评价[7],结果表明4个化合物在10 μmol/L浓度下均未显示明显的神经保护作用。
| [1] | Barden A, Awang A N, Mulliken T, et al. Heart of the matter:Agarwood use and trade and CITES implementation for Aquilaria malaccensis[A]//Securing the future of medicinal plant resources[C]. Cambridge:TRAFFIC International, 2000. |
| [2] | 肖培根. 新编中药志(第二卷)[M]. 北京: 化学工业出版社, 2002 . |
| [3] | 杨峻山. 沉香化学成分的研究概况[J]. 天然产物研究与开发 , 1997, 10 (1) :99–103. |
| [4] | Yagura T, Shibayama N, Ito M, et al. Three novel diepoxy tetrahydrochromones from agarwood artificially produced by intentional wounding[J]. Tetrahedron Lett , 2005, 46 (25) :4395–4398. DOI:10.1016/j.tetlet.2005.04.072 |
| [5] | Yang D L, Wang H, Guo Z K, et al. A new 2-(2-phenylethyl) chromone derivative in Chinese agarwood 'Qi Nan' from Aquilaria sinensis[J]. J Asian Nat Prod Res , 2014, 16 (7) :770–776. DOI:10.1080/10286020.2014.896342 |
| [6] | Chen D, Xu Z R, Chai X Y, et al. Nine 2-(2-phenylethyl) chromone derivatives from the resinous wood of Aquilaria sinensis and their inhibition of LPS-induced NO production in RAW 264.7 cell[J]. Eur J Org Chem , 2012, 27 (27) :5389–5397. |
| [7] | Yang L, Qiao L R, Xie D, et al. 2-(2-Phenylethyl) chromones from Chinese eaglewood[J]. Phytochemistry , 2012, 76 (1) :92–97. |
| [8] | Yang L, Qiao L R, Zhang J J, et al. Two new sesquiterpene derivatives from Chinese eaglewood[J]. J Asian Nat Prod Res , 2012, 14 (11) :1054–1058. DOI:10.1080/10286020.2012.704910 |
| [9] | Yang L, Qiao L R, Ji C X, et al. Antidepressant abietane diterpenoids from Chinese eaglewood[J]. J Nat Prod , 2013, 76 (2) :216–222. DOI:10.1021/np3006925 |
| [10] | 郭珮怡, 杨林, 戴均贵, 等. 国产沉香二萜类化学成分研究(Ⅲ)[J]. 中草药 , 2015, 46 (4) :486–489. |
| [11] | Konishi T, Konoshima T, Shimada Y, et al. Six new 2-(2-phenylethyl) chromones from agarwood[J]. Chem Pharm Bull , 2002, 50 (3) :419–422. DOI:10.1248/cpb.50.419 |
| [12] | Shimada Y, Tominaga T, Konishi T, et al. Studies on the agarwood. I. Structures of 2-(2-phenylethyl) chromone derivatives[J]. Chem Pharm Bull , 1982, 30 (10) :3791–3795. DOI:10.1248/cpb.30.3791 |
| [13] | 杨峻山, 王玉兰, 苏亚伦. 国产沉香化学成分的研究V:三个2-(2-苯乙基)色酮衍生物的分离和鉴定[J]. 药学学报 , 1990, 25 (3) :186–190. |
 2016, Vol. 47
2016, Vol. 47


