青皮Citri Reticulatae Pericarpium Viride为芸香科(Rutaceae)柑橘属Citrus L. 植物橘Citrus reticulata Blanco及其栽培变种的干燥幼果或未成熟果实的果皮。其味苦、辛,性温,归肝、胆、胃经;具有疏肝破气、消积化滞的功效,主治胸胁胀痛、疝气疼痛、乳癖、食积气滞、脘腹胀痛等[1]。橙皮苷是青皮的主要化学成分,约占总质量的5%以上,具有多种药理活性,如维持血管正常渗透压、降低血管脆性、降低人体中胆固醇量、抗炎、抗菌、抗过敏、降血压,抑制口腔癌、食道癌、大肠癌等的癌变和抗病毒作用[2-4]。因此,《中国药典》2015年版将橙皮苷作为青皮质量控制的指标[1]。
在《中国药典》2015年版中[1],青皮定量测定的样品是全部通过5号筛,且含能通过6号筛不少于95%的药材细粉,而没有过筛的药粉或纤维所含的橙皮苷量与药材细粉中测得的量可能并不完全一样。有研究表明[5],栀子和木蝴蝶原药材过筛粉末与未过筛粉末指标成分量相差较大,苦参过筛与否指标成分量基本无差异。基于此,本课题组在药材“真实量”以及提取转移率的基础上提出了“中药成分临床利用量”的概念。“中药成分临床利用量”是指药材在临床应用时,药材中的化学成分可被临床使用时利用的量[6]。另外,据相关文献报道[7-9],陈皮中的有效成分橙皮苷提取转移率低,最高者不超过25%,低者仅有3%左右,而目前对于青皮中橙皮苷的提取转移研究甚少。
本实验在单因素试验基础上,采用星点设计-效应面法[10-11]优选青皮的提取工艺,并在“真实量”以及提取转移率的基础上对各地市场上流通的11批青皮药材采用橙皮苷临床利用量的方法对其品质进行了考察,对研究其有效成分在临床上被实际利用的情况具有重要参考价值,同时以青皮为例,对其他药材的品质评价提供了一种新的方法。
1 仪器与材料P230 II型高效液相色谱仪,大连依利特分析仪器有限公司;SQP Satorious型电子天平,赛多利斯科学仪器(北京)有限公司,d=0.01 mg;BS-6KH型电子天平,上海友声衡器有限公司,d=0.2 g;FA2004型电子分析天平,上海良平仪器仪表有限公司生产,d=0.1 mg;DZF-6050A型真空干燥箱,北京中兴伟业仪器有限公司。
青皮药材购自各地大型药材市场及药房,经成都大学刘涛研究员鉴定,除购自新疆温宿县福仁大药房(产地安徽)的为芸香科柑橘属植物橘Citrus reticulata Blanco的干燥幼果,其余的均为芸香科柑橘属植物橘Citrus reticulata Blanco的未成熟果实的果皮,见表 1。橙皮苷对照品,批号140721,HPLC测定质量分数>98%,四川省维克奇生物科技有限公司;甲醇为色谱纯,水为娃哈哈纯净水,其余试剂均为分析纯。
|
|
表 1 青皮药材来源 Table 1 Origins of CRPV |
2 方法与结果 2.1 橙皮苷的测定[1] 2.1.1 色谱条件
色谱柱为Hypersil ODS 2柱(250 mm×4.6 mm,5 μm);流动相为甲醇-水(43∶57);检测波长为284 nm;进样量10 μL;理论板数按橙皮苷峰计算不低于1 000。
2.1.2 对照品溶液的制备取橙皮苷对照品适量,精密称定,加甲醇制成含橙皮苷0.28 mg/mL的对照品溶液,即得。
2.1.3 供试品溶液的制备精密量取青皮水提液(后文各提取操作所得水提液)1 mL至5 mL量瓶中,加流动相稀释至刻度,摇匀,即得。
2.1.4 线性关系考察分别精密量取橙皮苷对照品溶液1.0、2.0、3.0、4.0、5.0、6.0 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,分别制成含橙皮苷0.028、0.056、0.084、0.112、0.140、0.168 mg/mL的对照品溶液,按照“2.1.1”项下色谱条件,分别进样10 μL,测定峰面积。以峰面积为纵坐标(Y),橙皮苷质量浓度为横坐标(X),绘制标准曲线,得回归方程为Y=16 355 X-10.8,r=0.999 0,表明橙皮苷在0.028~0.168 mg/mL线性关系良好。
2.2 浸膏得率的测定精密量取青皮水提取液100 mL,置于已干燥至恒定质量的蒸发皿中蒸干,于105 ℃干燥3 h,置干燥器中冷却30 min,迅速精密称定,重复干燥、冷却及称定操作,直至2次称定质量相差小于5 mg,计算浸膏得率[11-12]。
浸膏得率=浸膏质量/药材总质量
2.3 青皮药材中橙皮苷的测定取药材40 g,精密称定,粉碎,过筛,收集过筛后的全部药材细粉与未过筛的全部粉末,分别精密称定其质量,并按照《中国药典》2015年版一部青皮定量测定项下方法测定,结果见表 2(其中,方法1为按照《中国药典》2015年版规定,取过筛后药材细粉测定,计算药材中橙皮苷量;方法2为用过筛的粉末质量与未过筛的粉末质量根据其所占的比例计算的橙皮苷量,即为药材中橙皮苷的真实量)。
|
|
表 2 青皮药材粉碎后各部位质量及定量测定结果 (n = 3) Table 2 Content and quantitative determination of each part from CRPV after crushing (n = 3) |
结果表明,采用过筛与未过筛粉末所占的比例计算的橙皮苷量,比按照《中国药典》2015年版中仅取过筛后药材细粉测定的橙皮苷量低1%左右,编号为9号的样品甚至低3%左右。同时,编号为10的样品按照《中国药典》2015年版的方法测定则橙皮苷量符合要求,但采用过筛与未过筛粉末所占的百分比计算后得到的药材中橙皮苷量则不符合《中国药典》2015年版规定的要求(《中国药典》2015年版中规定,青皮原药材中橙皮苷量不得低于5%,饮片中橙皮苷量不得低于4%,编号为1、2、3、6、9、10号的青皮为饮片),这将会对提取转移率的计算产生一定的影响。故本实验在后续研究中,采用青皮药材的真实量进行提取转移率的计算,即方法2所得的橙皮苷量。
2.4 单因素试验 2.4.1 溶媒用量考察青皮中含有大量黄酮类化合物,橙皮苷属于其中的1种,常见的提取方法有水提和醇提[13],本课题组在前期研究中已经采用乙醇提取对其进行了研究,橙皮苷的提取转移率较低。另外,由于水是临床上使用最广泛的溶媒,为研究青皮的临床利用量,本实验采用水进行提取。
称取药材(11号)50 g,平行9份,分别加入6、8、10、12、16、20、24、30、36倍量水,提取3次,每次1 h,合并提取液,滤过,测定其橙皮苷提取转移率以及浸膏得率,结果见表 3。随着溶媒用量的增加,橙皮苷提取转移率以及浸膏得率也在不断增加,当溶媒用量达到20倍时,橙皮苷提取转移率和浸膏得率基本趋于稳定,不再增加,因此选择20倍的溶媒量。
|
|
表 3 溶媒用量对橙皮苷提取转移率及浸膏得率的影响 Table 3 Effect of solvent volume on extraction transfer rate of hesperidin and extract yield |
2.4.2 提取时间考察
称取药材(11号)50 g,平行6份,分别加入20倍量水,提取3次,每次提取时间分别为0.5、1.0、1.5、2.0、2.5、3.0 h,合并提取液,滤过,测定其橙皮苷提取转移率以及浸膏得率,结果见表 4。随着提取时间的延长,橙皮苷提取转移率以及浸膏得率也随之增加,当提取时间为2.5 h时,橙皮苷提取转移率较大,之后反而有下降的趋势,而浸膏得率在2.5 h时趋于稳定,因此选择提取时间为2.5 h。
|
|
表 4 提取时间对橙皮苷提取转移率及浸膏得率的影响 Table 4 Effect of extraction time on extraction transfer rate of hesperidin and extract yield |
2.4.3 提取次数考察
称取药材(11号)50 g,平行5份,分别加入20倍量水,分别提取1、2、3、4、5次,每次提取时间为2.5 h,合并提取液,滤过,测定其橙皮苷提取转移率以及浸膏得率,结果见表 5。随着提取次数的增加,橙皮苷提取转移率以及浸膏得率也随之增加,当提取次数为3次时,浸膏得率增加的趋势有所减缓。结合工业生产的实际,以及在实际操作中,提取次数过多会导致青皮药材煮烂,同时由于提取次数为非连续变量,回归处理难以实现,因此将提取次数定为3次。
|
|
表 5 提取次数对橙皮苷提取转移率及浸膏得率的影响 Table 5 Effect of extraction times on extraction transfer rate of hesperidin and extract yield |
2.5 星点设计-效应面优化提取工艺 2.5.1 星点试验设计与结果
根据单因素试验结果,选取加水量(X1)10~30倍、提取时间(X2)1.5~3.5 h,提取次数为3次。根据星点设计的原理,每因素设5水平,用代码值−α、−1、0、1、α来表示(2因素设计的α=$\sqrt{2}$)。代码值所表示的实际操作物理量见表 6(所用样品为11号)。将考察指标橙皮苷提取转移率(Y1)、浸膏得率(Y2)数值标准化为0~1的归一值(d),并 将d求算几何平均数,得总评归一值(OD),OD=(d1×d2×…×dk)1/k(k为指标数),对取值越小越好的效应和取值越大越好的效应,采用Hassan方法分别进行数学转换求其d(dmin和dmax),dmin=(Ymax-Yi)/(Ymax-Ymin),dmax=(Yi-Ymin)/(Ymax-Ymin)[14-16]。而本实验要求Y1及Y2越高越好,结果见表 6。
|
|
表 6 星点试验设计与结果 Table 6 Central composite design and results |
2.5.2 模型拟合
采用Design-Expert V8.0.6.(1) 软件,以各OD对自变量进行多元线性回归和2项式拟合。得多元线性方程为Y=−0.452 55+0.039 55 X1+0.117 85 X2,r=0.859 5,P<0.000 1;2项式方程为Y=−0.741 85+0.101 01 X1-0.093 633 X2+0.008 466 64 X1X2-0.002 065 62 X12+0.008 430 87 X22,r=0.965 0,P<0.000 1。根据统计软件对各项系数进行的t检验结果,删除P>0.05的项后,再进行2项式方程拟合,达到简化模型目的。所得方程为Y=−1.219 36+0.122 62 X1+0.117 85 X2-0.002 076 71 X12,r=0.955 7,P<0.000 1。从拟合方程的r可见,多元线性回归方程的r较低,而多元2项式拟合方程r较高,拟合效果较好。
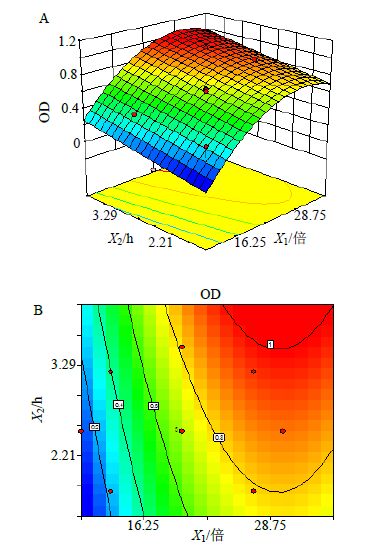
2.5.3 效应面优化及预测性评价根据优化后的2项式方程,运用Design-Expert V8.0.6.(1) 软件绘制评价指标随因素变化的三维效应面图和等高线图,见图 1。从效应面和等高线图可知,最优区域OD值>0.8,当X1的取值范围在18.75~35倍,X2的取值范围在1.75~3.5 h时,OD值落在最高效应值区间。进一步通过Design-Expert V8.0.6.(1) 软件预测分析,获得1组OD值最大的优化条件:X1为28倍,X2为3.5 h;但在实际操作过程中,青皮每次提取时间超过2.5 h极易煮烂,同时结合生产实际综合考虑,选择最佳提取工艺为加水倍量24倍,提取3次,每次2.5 h。
|
图 1 溶媒用量 (X1) 和提取时间 (X2) 对OD效应面 (A) 和等高线 (B) 图 Fig.1 Effectof solvent volume (X1) and extraction time (X2) on response surface chart (A) and contour surface chart (B) of OD |
2.6 验证试验
称取药材200 g,平行3组,按优选的提取工艺进行验证试验,并将方程预测值与验证试验实测值进行偏差计算,结果见表 7。可知,预测值与实测值间的偏差[偏差=(预测值-实测值)/预测值]为1.61%,表明采用星点设计-效应面法选择的青皮提取工艺重复性好,建立的数学模型具有较好的预测性,拟合结果合理、可靠。
|
|
表 7 验证试验结果 (n = 3) Table 7 Results of verification test (n = 3) |
2.7 市售11批青皮药材中橙皮苷临床利用量测定
按照优选的提取工艺,对市售的11批青皮药材进行提取,测定其橙皮苷量,并计算提取转移率,并根据表 2中方法2所得的橙皮苷量计算橙皮苷的临床利用量,结果见表 8。结果表明,编号为10的药材真实橙皮苷量最低,提取转移率却最高,而真实橙皮苷量最高的11号药材的提取转移率偏低,从而临床利用量也并非最高。表明药材中橙皮苷量的高低与橙皮苷的临床利用量大小并非呈正相关。
|
|
表 8 11批青皮药材临床利用量测定结果 Table 8 Results of clinically utilized quantity of 11 batches of CRPV |
橙皮苷临床利用量=青皮药材中真实橙皮苷量×橙皮苷提取转移率
3 讨论青皮和陈皮中均含有橙皮苷,目前已有研究表明[4, 7-9],不管采用醇提取还是水提取,陈皮中的有效成分橙皮苷提取转移率低,最高者不超过30%,低者仅有3%左右,而目前对于青皮中橙皮苷的提取转移研究甚少。本课题组在前期研究中已经采用60%乙醇对其进行了提取研究,橙皮苷的提取转移率仅在35%左右。在临床上,青皮既可以单独使用也可以配伍使用,如青皮甘草散(《金鉴》卷四十九)中与甘草配伍,本课题组已对青皮和甘草配伍后橙皮苷的提取转移率进行了研究,其提取转移率也仅为35%左右。再如乳增消痛巴布膏剂,青皮与三棱、莪术等配伍,转移率也较低[17],可见,青皮无论单独使用或配伍使用,其提取转移率均不高。本实验在单因素试验基础上,采用星点设计-效应面法优选青皮的水提取工艺,并对各地市场上流通的11批青皮药材的提取转移率进行了测定,结果均低于50%,这可能和橙皮苷的性质有关。
《中国药典》2015年版一部中,中药药材和饮片的定量检查项,基本均采用过规定号数的药筛,取过筛后的粉末进行定量测定,并确定为整体药材的指标成分量,从而判断药材或饮片是否合格。然而在实际粉碎过程中,过筛部分与未过筛部分往往是药材的不同部位,且未过筛部分还占有较大的比重。如栀子过筛部位基本为果皮,而未过筛部位基本为种子;葛根中的纤维部分基本不能过筛。由于部位不同,故过筛部分与未过筛部分的指标成分量也极可能存在较大的差异。据文献报道[5],采用《中国药典》中的方法计算木蝴蝶中指标成分量为2%左右,而采用过筛的指标成分量与未过筛的指标成分量根据其所占的比例计算的指标成分量为1.4%左右,2种方法测定的指标成分量相差较大;同样的方法,栀子也有较大的差异,而苦参基本无差异。本实验同样采用这2种方法对11批青皮药材中橙皮苷量进行了研究,结果药材中真实橙皮苷量要比采用《中国药典》2015年版中的方法低1%左右,其中编号为10的药材按照《中国药典》2015年版中的方法其量为4.67%,大于4%,应为合格饮片,而其真实橙皮苷量为3.72%,小于4%,不合格。因此,《中国药典》中,仅采用过筛后的药粉测定其指标成分量的方法还有待商榷。建议在研究过程中计算成分提取转移率时,对于过筛部分与未过筛部分指标成分量差异较大的药材,采用过筛部分的指标成分量与未过筛部分的指标成分量根据其所占的比例计算所得到指标成分量来规定其指标成分量的限度。
目前,测定指标成分或有效成分量的高低是中药材品质评价的主要方式,往往认为其量高,药材的品质好,其量低则品质劣[18]。然而,在实际提取过程中,指标成分量高的药材提取转移率不一定高。本实验结果表明,青皮中橙皮苷的提取转移率的高低与其量的高低并非呈正相关,因此,在实际生产中,使用橙皮苷量高的青皮药材进行投料,所制得的成品中橙皮苷量可能较低,或在临床运用中,患者购买橙皮苷量高的青皮药材,进行煎煮提取后,能被利用的反而较少。所以采用指标成分或有效成分量的高低评价中药材品质的方法尚存在一定的缺陷。因此,在“真实量”以及提取转移率基础上提出的“中药成分临床利用量”评价中药品质的方法就具有一定的优势。
“中药成分临床利用量”是指药材成分在临床应用时,药材中的化学成分可被临床使用时利用的量,其计算公式:P=W1×T1×N1+W2×T2×N2+W3×T3×N3+…+Wn×Tn×Nn,其中P为药材中化学成分的临床利用量,W为100 g药材中化学成分的“真实量”,T为药材中相应化学成分的提取转移率,N为该成分的权重系数(对某一药效的贡献度)[6]。在本研究中,只采用橙皮苷作为评价指标,未涉及对青皮药效评价,故将N值取为1。本实验旨在以青皮为例,为其他中药材品质的评价提供一种新的方法。
| [1] | 中国药典[S]. 一部. 2015. |
| [2] | 张锐, 施旻, 刘建群, 等. 亚临界水提取陈皮中橙皮苷的工艺研究[J]. 中成药 , 2013, 35 (11) :2531–2533. |
| [3] | 钱俊臻, 王伯初. 橙皮苷的药理作用研究进展[J]. 天然产物研究与开发 , 2010, 22 (1) :176–180. |
| [4] | 赵祎姗. 源于同一植物的陈皮与青皮的品质评价研究[D]. 成都:成都中医药大学, 2011. |
| [5] | 刘涛, 郭晓恒, 吴春梅, 等. 肺毒清颗粒中有效成分的含量测定及转移率考察[J]. 中国实验方剂学杂志 , 2013, 19 (10) :54–56. |
| [6] | 刘涛, 苟小军, 万德光, 等. 基于"中药成分临床利用率"的中药材药用品质评价模式的商建[J]. 中草药 , 2015, 46 (13) :1863–1866. |
| [7] | 蔡庆顺, 钟小群, 余华. 陈皮不同提取工艺橙皮苷提取率分析[J]. 中成药 , 2010, 32 (6) :1067–1070. |
| [8] | 鲁劲松, 王红芬, 李云霞. 藿香正气水中陈皮渗漉工艺的优化[J]. 中草药 , 2014, 45 (8) :1096–1101. |
| [9] | 郑艳春, 杨冬丽, 崔雅慧, 等. 藿香正气水中橙皮苷转移率优化[J]. 中国实验方剂学杂志 , 2011, 17 (24) :27–28. |
| [10] | 李颖, 曾茂贵, 郑笈, 等. 星点设计-效应面法优化鱼腥草挥发油-β-环糊精包合物的制备工艺[J]. 中草药 , 2014, 45 (13) :1855–1862. |
| [11] | 杨涛, 盛欢欢, 李岩, 等. 星点设计-效应面法优化穿心莲提取工艺[J]. 中国药学杂志 , 2011, 46 (3) :208–213. |
| [12] | 林小玲, 田成旺, 张铁军. 星点设计-效应面法优选参芪消岩颗粒渗漉提取工艺[J]. 中草药 , 2013, 44 (4) :430–433. |
| [13] | 郑一敏, 胥秀英, 傅善权, 等. 青皮总黄酮的提取工艺与测定[J]. 华西药学杂志 , 2007, 22 (5) :580–581. |
| [14] | 符少莲, 冯翠娟, 李沙. 星点设计-效应面法优化脂溶性丹参提取物速释滴丸处方工艺[J]. 中成药 , 2013, 35 (4) :690–695. |
| [15] | 黄元红, 卫天喜, 张发生, 等. 星点设计-效应面法优选丹参提取工艺[J]. 中国实验方剂学杂志 , 2010, 16 (17) :28–31. |
| [16] | 吕维, 吴恋, 罗红丽, 等. 星点设计-效应面法优化川芎提取工艺[J]. 药物评价研究 , 2014, 37 (1) :53–57. |
| [17] | 庄桂霞. 乳增消痛巴布膏药学研究[D]. 北京:北京中医药大学, 2005. |
| [18] | 赖燕华. 液相色谱和光谱法结合化学计量学用于中药指纹图谱研究——不同基源、产地或炮制的中药质量评价与质量控制[D]. 南昌:南昌大学, 2010. |
 2016, Vol. 47
2016, Vol. 47


