九味羌活口服液(Jiuwei Qianghuo Oral Liquid, JQOL)收载于《中国药典》2015年版,具有疏风解表、散寒除湿的作用。用于外感风寒挟湿所致的感冒,症见恶寒、发热、无汗、头重而痛、肢体疼痛[1]。该中成药由羌活、防风、苍术、细辛、川芎、白芷、黄芩、甘草、地黄9味药材组成,目前,《中国药典》2015年版以黄芩苷作为定量测定的指标成分,质控指标单一,专属性不强。文献报道中对于九味羌活制剂的定量都以2~3个成分为指标进行测定[2-9]或者测定其挥发性成分[10]。九味羌活制剂中,羌活辛苦性温,散表寒、祛风湿、利关节、止痹痛,为治太阳风寒湿邪在表之要药,故为君药;防风辛甘性温,为风药中之润剂,祛风除湿、散寒止痛;苍术辛苦而温,功可发汗祛湿,为祛太阴寒湿的主要药物;两药相合,协助羌活祛风散寒、除湿止痛、是为臣药;细辛、白芷、川芎祛风散寒、宣痹止痛,其中细辛善治少阴头痛、白芷擅解阳明头痛、川芎长于止少阳厥阴头痛,此3味药与羌活、苍术合用,为本方“分经论治”的基本结构;生地、黄芩清泄里热,并防诸辛温燥烈之品伤津,以上5药俱为佐药;甘草调和诸药为使药。按照中药质量标志物(Q-Marker)的概念[11-12],其中的欧前胡素、异欧前胡素药理研究发现这2种成分具有抗炎、抗菌和镇痛等活性[8],可以作为该中成药的中药质量标志物之一。根据《中国药典》对于单味中药的质量标准,羌活的指标成分为羌活醇与异欧前胡素,防风的指标成分为升麻素苷与5-O-甲基维斯阿米醇苷,川芎的指标成分为阿魏酸,甘草的指标成分为甘草苷与甘草酸铵,苍术的指标成分为苍术素,黄芩的指标成分为黄芩苷,细辛的指标成分为细辛脂素,白芷的指标成分为欧前胡素,地黄的指标成分为梓醇与毛蕊花糖苷,确定了采用13种成分控制该中成药的质量。因此,本实验从多种有效成分同时监控的角度出发,建立一种RP-HPLC法同时测定JQOL中13种成分,能较为全面地反映该中成药的质量。
1 仪器与试药Agilent 1260高效液相色谱仪,包括DAD检测器,四元泵,自动进样器、化学工作站等,美国Agilent公司;BP211D型电子天平,德国Satrorius公司。
对照品梓醇(批号110808-201210,质量分数98.1%)、甘草苷(批号111610-201106,质量分数93.7%)、甘草酸铵(批号110731-201418,质量分数93.1%)、细辛脂素(批号111889-201504,质量分数100.0%)、毛蕊花糖苷(批号111530-201512,质量分数96.7%)、苍术素(批号111924-201404,质量分数99.7%)、阿魏酸(批号110773-201313,质量分数99.6%)、欧前胡素(批号110826-201415,质量分数99.7%)、羌活醇(批号111820-201504,质量分数99.9%)、异欧前胡素(批号110827-201410,质量分数99.7%)、黄芩苷(批号110715-201318,质量分数93.3%)、升麻素苷(批号111522-201511,质量分数94.8%)、5-O-甲基维斯阿米醇苷(批号111523-201509,质量分数95.8%),中国食品药品检定研究院提供;乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。9批JQOL由重庆东方药业股份有限公司提供,批号150912、150913、150914、151102、151103、151104、151222、151223、151224。
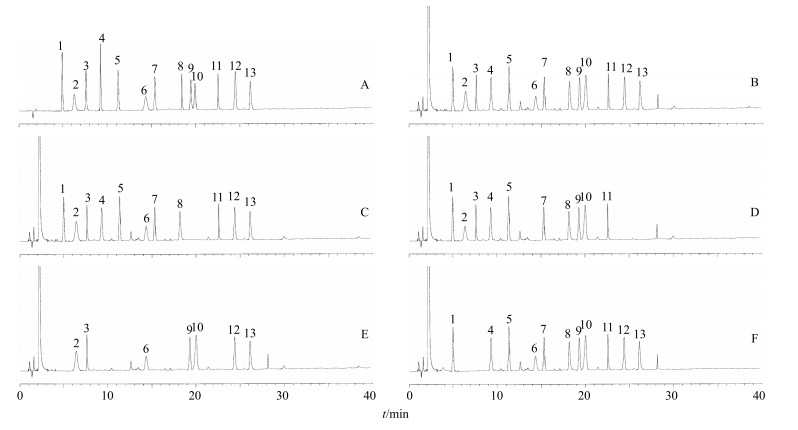
2 方法与结果 2.1 色谱条件及系统适应性试验色谱柱Zorbax Eclipse XDB-C18柱(250 mm×4.6 mm,5 μm);柱温40 ℃;流动相为乙腈-5.0 mmol/L KH2PO4溶液(稀磷酸调节pH值至3.0)(15:85),梯度洗脱:0~5 min,15%乙腈;5~30 min,15%~80%乙腈;30~32 min,80%~15%乙腈;32~40 min,15%乙腈;体积流量为1.0 mL/min;分段变波长测定:0~5.0 min为210 nm,5.0~9.0 min为237 nm,9.0~10.0 min为287 nm,10.0~17.0 min为330 nm,17.0~21.0 min为310 nm,21.0~23.0 min为280 nm,23.0~30.0 min为254 nm;进样量为10 μL。色谱图见图 1。
|
1-梓醇 2-甘草苷 3-甘草酸铵 4-细辛脂素 5-毛蕊花糖苷 6-苍术素 7-阿魏酸 8-欧前胡素 9-羌活醇 10-异欧前胡素 11-黄芩苷 12-升麻素苷 13-5-O-甲基维斯阿米醇苷 1-catalpol 2-liquiritin 3-ammonium glycyrrhizinate 4-asarinin 5-verbascoside 6-atractylodin 7-ferulic acid 8-imperatorin 9-notopterol 10-isoimperatorin 11-baicalin 12-prim-O-glucosylcimifugin 13-5-O-methylvisammioside 图 1 混合对照品(A)、JQOL供试品(B)、缺少羌活的阴性对照(C)、缺少防风和苍术药材的阴性对照(D)、缺少细辛、川芎、白芷、黄芩、地黄药材的阴性对照(E)、缺少甘草药材的阴性对照(F)的HPLC-DAD色谱图 Fig.1 HPLC-DAD chromatograms of mixed reference substances (A), JQOL sample (B), negative control without Notopterygii Rhizoma et Radix (C), negative control without Saposhnikoviae Radix and Atractylodis Rhizoma (D), negative control without Asari Herba, Chuanxiong Rhizoma, Angelicae Dahuricae Radix, Scutellariae Radix, or Rehmanniae Radix (E), negative control without Glycyrrhizae Radix (F) |
2.2 对照品溶液制备
精密称取梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷适量,分别置10 mL量瓶中,加甲醇溶解并稀释至刻度,得各对照品储备液,备用。再精密吸取各对照品储备液适量置25 mL量瓶中,甲醇稀释至刻度,得含梓醇10 μg/mL、甘草苷20 μg/mL、甘草酸铵50 μg/mL、细辛脂素25 μg/mL、毛蕊花糖苷10 μg/mL、苍术素20 μg/mL、阿魏酸15 μg/mL、欧前胡素10 μg/mL、羌活醇60 μg/mL、异欧前胡素30 μg/mL、黄芩苷60 μg/mL、升麻素苷30 μg/mL和5-O-甲基维斯阿米醇苷40 μg/mL的混合对照品溶液,备用。
2.3 供试品溶液制备精密量取本品1 mL,置25 mL量瓶中,加甲酵至刻度,摇匀,滤过,取续滤液,即得。
2.4 阴性对照溶液制备按JQOL处方比例和工艺,分别制备缺少羌活药材的阴性对照样品;缺少防风和苍术药材的阴性对照样品;缺少细辛、川芎、白芷、黄芩、地黄药材的阴性对照样品;缺少甘草药材的阴性对照样品;并按“2.3”项下方法制备各阴性对照溶液。
2.5 线性关系考察精密量取对照品储备液1.0、2.5、5.0、10、15 mL于25 mL量瓶中,加流动相稀释至刻度,摇匀,得系列混合对照品溶液。按“2.1”项下色谱条件进样,记录色谱峰峰面积,以峰面积积分值为纵坐标(Y),对照品质量浓度为横坐标(X)进行线性回归,得到13个成分的标准曲线方程、相关系数(r)和线性范围,结果分别为梓醇Y=34.23 X+33.745,r=0.999 5,2.08~31.22 μg/mL;甘草苷Y=564.22 X+93.62,r=0.999 2,4.01~60.15 μg/mL;甘草酸铵Y=66.21 X+8.539,r=0.999 2,10.09~151.31 μg/mL;细辛脂素Y=7.358 X+0.839 5,r=0.999 4,4.98~74.63 μg/mL;毛蕊花糖苷Y=7 438.1 X+84.38,r=0.999 6,2.05~30.74 μg/mL;苍术素Y=9.637 X+47.48,r=0.999 6,4.10~61.46 μg/mL;阿魏酸Y=44.62 X+843.5,r=0.999 3,2.93~43.98 μg/mL;欧前胡素Y=5.374 X+83.41,r=0.999 5,2.04~30.66 μg/mL;羌活醇Y=5.397 X+0.482,r=0.999 7,12.54~181.55 μg/mL;异欧前胡素Y=49.35 X+73.22,r=0.999 5,53.95~89.23 μg/mL;黄芩苷Y=834.5 X+2.364,r=0.999 5,12.05~180.68 μg/mL;升麻素苷Y=75.25 X+6.324,r=0.999 4,5.97~89.51 μg/mL;5-O-甲基维斯阿米醇苷Y=4.385 X+0.738 4,r=0.999 6,7.99~119.82 μg/mL。
2.6 精密度试验精密吸取同一对照品溶液10 μL,重复进样6次,记录峰面积。结果显示,梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷的峰面积RSD值分别为1.3%、1.1%、1.0%、0.7%、1.2%、1.4%、1.4%、1.7%、1.2%、0.8%、1.6%、1.8%、1.9%,表明仪器精密度良好。
2.7 重复性试验取同一批JQOL(批号150912)6份,按“2.3”项下方法平行制备6份供试品溶液,按“2.1”项下色谱条件测定,结果显示,梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷的平均质量浓度分别为0.251、1.245、0.874、0.368、0.163、0.955、0.538、0.287、1.053、0.064、3.649、0.183、0.083 mg/mL,RSD分别为1.5%、0.8%、0.6%、0.7%、1.4%、1.9%、1.9%、1.6%、1.7%、0.7%、0.8%、0.9%、1.8%,表明方法的重复性良好。
2.8 稳定性试验精密吸取同一JQOL供试品溶液(批号150912)各10 μL,按“2.1”项下色谱条件分别于0、2、4、8、12、24 h进样测定,结果显示梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷的质量浓度RSD分别为1.8%、0.6%、0.4%、0.9%、1.3%、1.5%、1.5%、1.1%、1.4%、0.3%、0.5%、0.4%、1.9%,表明供试品溶液在24 h内稳定。
2.9 加样回收率试验取同一批号JQOL样品(批号为150912),每份约0.5 mL,精密称定,分成3组,分别按已知质量分数的50%、100%、150% 3个水平加入混合对照品溶液,按“2.3”项下方法制备,依法测定,计算各个指标成分的回收率。结果发现梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷的平均加样回收率分别为98.8%、98.6%、101.2%、99.4%、100.1%、99.7%、98.9%、99.4%、100.5%、98.7%、101.2%、98.3%、99.1%,RSD分别为1.9%、1.8%、1.5%、0.8%、0.6%、0.9%、1.2%、2.0%、1.6%、0.8%、1.4%、1.5%、1.7%。
2.10 样品测定取9批JQOL样品,按“2.3”项下方法制备供试品溶液,依法测定,用外标法计算样品中梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷的质量浓度,结果见表 1。9批次JQOL供试品中梓醇、甘草苷、甘草酸铵、细辛脂素、毛蕊花糖苷、苍术素、阿魏酸、欧前胡素、羌活醇、异欧前胡素、黄芩苷、升麻素苷和5-O-甲基维斯阿米醇苷质量浓度分别为0.229~0.259 mg/L、1.231~1.260 mg/L、0.849~0.877 mg/L、0.357~0.371 mg/L、0.149~0.169 mg/L、0.941~0.967 mg/L、0.529~0.547 mg/L、0.269~0.294 mg/L、1.039~1.067 mg/L、0.043~0.064 mg/L、3.631~3.649 mg/L、0.157~0.183 mg/L、0.068~0.084 mg/L。结果表明本品各批次之间13种成分的量基本稳定。
|
|
表 1 样品测定结果 Table 1 Determination of samples |
3 讨论
本实验首次建立HPLC同时测定JQOL中13种成分的方法,方法简单、结果准确,可作为JQOL多指标定量测定方法,可用于JQOL的质量控制。
考察对比了不同的流动相系统,包括甲醇-水、乙腈-水、乙腈-甲酸水溶液、乙腈-乙酸水溶液、乙腈-磷酸二氢钾水溶液、乙腈-磷酸氢二钾水溶液、乙腈-磷酸二氢钠水溶液、最终选择乙腈-磷酸二氢钾水溶液体系;同时考察了不同浓度磷酸二氢钾水溶液(2.0、5.0、10.0 mmol/L)对分离的影响,确定了5.0 mmol/L磷酸二氢钾水溶液;进一步考察了不同pH值的影响(pH 2.5、3.0、3.5、4.0、4.5),确定了pH 3.0为最佳的pH值;最后考察了不同的梯度洗脱方法。
本实验采用分段变波长检测法对13种成分进行测定,在210 nm波长下检测梓醇,在237 nm波长下检测甘草苷与甘草酸铵,在287 nm波长下检测细辛脂素,在330 nm波长下检测苍术素、阿魏酸与毛蕊花糖苷,在310 nm波长下检测羌活醇、异欧前胡素与欧前胡素,在280 nm波长下检测黄芩苷,在254 nm波长下检测升麻素苷与5-O-甲基维斯阿米醇苷。
测定结果表明,与文献报道中丸剂、颗粒剂相比[2],本实验测定的JQOL中甘草酸、黄芩苷、阿魏酸、升麻素苷、欧前胡素与异欧前胡素的量还是有差异,目前只有1个厂家生产该品种,分析原因可能是所用药材产地和质量不同造成的。
| [1] | 中国药典[S].一部. 2015. |
| [2] | 宋九华, 李琼, 万东海. HPLC测定九味羌活丸中甘草酸的含量[J]. 乐山师范学院学报 , 2010, 25 (5) :43–44. |
| [3] | 宋九华, 王刚, 刘素君. HPLC测定九味羌活丸中黄芩苷、甘草酸和异甘草素含量[J]. 中成药 , 2010, 32 (11) :1914–1916. |
| [4] | 张锋忠, 骆天功. HPLC法测定九味羌活丸中5-羟甲基糠醛的含量[J]. 药物分析杂志 , 2014, 25 (44) :4206–4208. |
| [5] | 宋九华. HPLC测定九味羌活丸中甘草酸和异甘草素的含量[J]. 乐山师范学院学报 , 2011, 26 (5) :13–14. |
| [6] | 李巧玲, 王冬梅, 苗秋艳, 等. RP-HPLC法同时测定九味羌活丸中升麻素苷等5种有效成分的含量[J]. 沈阳药科大学学报 , 2016, 33 (2) :114–119. |
| [7] | 赵渤年, 刘青, 丁晓彦. HPLC测定九味羌活颗粒中欧前胡素的含量[J]. 中国药房 , 2007, 27 (12) :1967–1968. |
| [8] | 曲永胜. 不同工艺对九味羌活颗粒中欧前胡素及异欧前胡素含量的影响[J]. 齐鲁药事 , 2009, 28 (11) :692–694. |
| [9] | 何丹, 杨林, 张景勍. 超高效液相色谱法测定九味羌活颗粒中欧前胡素和异欧前胡素的含量[J]. 中国医院药学杂志 , 2014, 33 (24) :2053–2055. |
| [10] | 张幸福, 张炜. 九味羌活制剂中挥发性成分的气相色谱-质谱分析[J]. 中国药业 , 2014, 23 (15) :4–6. |
| [11] | 刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker):中药产品质量控制的新概念[J]. 中草药 , 2016, 47 (9) :1443–1457. |
| [12] | 张铁军, 许浚, 韩彦琪, 等. 中药质量标志物(Q-marker)研究:延胡索质量评价及质量标准研究[J]. 中草药 , 2016, 47 (9) :1458–1467. |
 2016, Vol. 47
2016, Vol. 47


