2. 浙江中医药大学第二附属医院 药剂科, 浙江 杭州 310005
2. The Second Affiliated Hospital of Zhejiang Chinese Medical University, Hangzhou 310005, China
复方健肾方是(Compound Jianshen Granules, CJG)名中医临床经验方,具有降低血糖,保护肾脏的功能。由熟地、黄芪、黄精、蝉花4味药组成。方中熟地为君药,其性味甘、微温,具有补血滋阴、益精填髓的作用;黄芪性味甘、微温,具有补气升阳、利水消肿、生津养血的作用,用于气虚水肿、内热消渴;黄精味甘性平,具有补气养阴、益肾的作用,用于精血不足、内热消渴;蝉花是一种菌虫复合体,其中的活性组分与冬虫夏草相当,属于优质虫草,具有提高免疫力、改善肾功能等作用[1-3]。
本研究根据相关文献报道[4-5],确定醇提和水提的最佳提取工艺。在此基础上进行颗粒剂的制备工艺考察,以颗粒成型率、吸湿率、休止角为考察指标,对药辅比、赋形剂、润湿剂的种类和用量进行考察[6-7],以确定最佳制备工艺,旨在研究出质量稳定可控、服用方便的复方健肾颗粒(CJG)。
1 仪器与材料微电脑控温电热板,深圳市艾力电子科技有限公司;UV759S紫外-可见分光光度计、水分测定仪,上海仪电分析仪器有限公司;JA203H电子分析天平、HH-4数显恒温水浴锅,常州市幸运电子设备有限公司;OFY-400摇摆式高速万能粉碎机,温岭市林大机械有限公司;FT-104B休止角测定仪,宁波海曙瑞柯仪器有限公司。
药材均经浙江中医药大学中药资源与鉴定教研室陈孔荣教授鉴定,熟地为玄参科地黄属植物地黄Rehmannia glutinosa Libosch.干燥块根的炮制加工品。黄芪为豆科黄芪属植物蒙古黄芪Astragalus membranaceus (Fisch.) Bge. var. mongholicus (Bge.) Hsiao的干燥根。黄精为百合科黄精属植物黄精Polygonatum sibiricumRed.干燥根茎炮制品。蝉花为麦角菌科虫草菌属真菌大蝉草Cordyceps cicadae Shing的分生孢子阶段即蝉棒束孢菌及其寄主山蝉Cicada flammata Dist.幼虫的烦躁体。
黄芪甲苷对照品,成都曼斯特生物科技有限公司,批号11092002,质量分数≥98%;葡萄糖对照品,中国食品药品检定研究院,批号110833-201205,质量分数99.5%;药用规格的淀粉、糊精、微晶纤维素、α-乳糖、甘露醇;实验中所用的其他试剂均为分析纯。
2 方法与结果 2.1 复方健肾方提取工艺将黄芪先进行醇提,提取总皂苷有效成分之后,其药渣与其余3味药材按照复方比例进行水煎,醇沉得到总多糖有效成分。
2.2 总皂苷定量测定 2.2.1 对照品溶液的配制精密称取干燥至恒定质量的黄芪甲苷对照品5.27 mg,置于干燥的10 mL量瓶中,加无水乙醇超声溶解并定容至刻度,摇匀,即得黄芪甲苷对照品溶液,备用。
2.2.2 供试品溶液的制备称取黄芪药材粗粉4 g,加甲醇40 mL,加热回流提取4 h,抽滤,浓缩近干,残渣加水10 mL,微热使溶解,用水饱和正丁醇振摇萃取4次,每次40 mL,合并正丁醇液,蒸干,用无水乙醇溶解并转移入25 mL量瓶中,定容,摇匀,滤过,取续滤液,即得黄芪总皂苷供试品溶液。
2.2.3 最大吸收波长的确定精密吸取黄芪甲苷对照品溶液0.4 mL至干燥具塞试管中,加无水乙醇至0.5 mL,加入8%香草醛试剂0.5 mL,缓缓加入5.0 mL体积分数为72%的硫酸,混匀,置于62 ℃水浴中,保温20 min,取出,置冰浴中冷却10 min,以空白试剂作参比,于紫外-可见分光光度计上从400~700 nm进行全波长扫描,测得最大吸收波长为544 nm。
2.2.4 标准曲线的绘制分别精密移取黄芪甲苷对照品溶液0.15、0.20、0.25、0.30、0.35、0.40、0.45 mL加入到干燥具塞刻度试管中,用无水乙醇补齐至0.5 mL,加入8%香草醛溶液0.5 mL,摇匀,缓缓加入5.0 mL体积分数为72%的硫酸,摇匀,置于62 ℃水浴中,保温20 min,取出,置冰浴中冷却10 min,另精密吸取无水乙醇0.5 mL同法操作,以此溶液作为空白对照,于波长544 nm处测定吸光度(A)值,以A值对黄芪甲苷质量浓度进行线性回归,绘制标准曲线,标准曲线方程为Y=0.018 4 X-0.065 9,r2=0.996 7,表明其在13.175~39.525 μg/mL线性关系良好。
2.2.5 精密度试验分别精密移取同一对照品溶液,按照“2.2.4”项下方法,自“用无水乙醇补齐至0.5 mL”起,依法测定其A值,平行测定6次,RSD为0.16%,表明方法精密度良好。
2.2.6 重复性试验称取6份黄芪粗粉2 g,按照总皂苷供试品溶液的制备方法制备总皂苷供试液,精密移取适量,按照“2.2.4”项下方法,自“用无水乙醇补齐至0.5 mL”起,依法测定其A值,RSD为2.22%,表明本方法重复性良好。
2.2.7 稳定性试验精密吸取供试品溶液,按照“2.2.4”项下方法,自“用无水乙醇补齐至0.5 mL”起,同法操作,分别于冰浴终止反应后0、10、20、30、40、50、60 min,依法测定其A值,RSD为2.74%。表明样品在60 min内测定稳定性良好。
2.2.8 加样回收率试验精密吸取已测定的黄芪总皂苷样品溶液0.1 mL,共9份,分别精密加入“2.2.1”项下黄芪甲苷对照品溶液0.10、0.12、0.14 mL各3份,按照“2.2.4”项下方法,自“用无水乙醇补齐至0.5 mL”起,依法测定其A值,计算加样回收率。结果平均回收率为98.78%,RSD为1.78%。
2.3 醇提工艺研究 2.3.1 单因素考察分别对浸泡时间、乙醇体积分数、乙醇倍量、提取时间、提取次数进行了考察,结果表明浸泡时间对总皂苷提取效率几乎无影响,故选择不浸泡直接进行提取;乙醇体积分数为85%、乙醇倍量为10倍、提取时间为1.5 h时,总皂苷提取率最大;而随着提取次数的增加,总皂苷提取率增加。
2.3.2 正交设计优化醇提工艺为了综合考察多因素对黄芪总皂苷提取效率的影响,本研究采用4因素3水平正交设计试验来确定最佳提取工艺条件。根据单因素试验结果以总皂苷提取率为指标,以乙醇体积分数(A)、溶剂倍量(B)、提取时间(C)、提取次数(D)为考察因素,选用L9(34)正交表进行正交设计,因素水平表见表 1,正交设计结果见表 1,方差分析见表 2。
|
|
表 1 正交试验设计与结果 Table 1 Design and results of orthogonal test |
|
|
表 2 方差分析 Table 2 Analysis of variance |
根据直观分析及方差分析结果可得,4个因素对总皂苷提取效率的影响大小分别为D>B>C>A,即提取次数>乙醇倍量>提取时间>乙醇体积分数。各因素不同水平间均无显著性差异,因此确定最佳提取工艺为A2B2C3D3,即85%乙醇,10倍量,提取2次,每次2 h。
2.3.3 验证试验根据正交试验结果,按最佳工艺提取,测定3份提取物中总皂苷的提取率,结果表明3份提取物中总皂苷平均提取率为3.08%,RSD为0.93%,该工艺条件稳定、合理、可行。
2.3.4 浸膏得率考察据验证试验结果,按最佳工艺提取,平行3份,计算浸膏平均得率为36.62%,RSD为1.58%。
2.4 总多糖定量测定 2.4.1 对照品溶液的制备精密称取置于五氧化二磷干燥器中干燥24 h的D-无水葡萄糖对照品3.56 mg,置25 mL量瓶中,加蒸馏水溶解并稀释至刻度,摇匀,即得D-无水葡萄糖对照品溶液。
2.4.2 供试品溶液的制备将黄芪醇提后的药渣挥干乙醇,与熟地、黄精、蝉花一起,加入10倍量水,煎煮1 h,离心取上清液,在旋转蒸发仪上浓缩至药材-药液比为1:1,加入95%乙醇使含醇量为80%,放于冰箱中静置24 h,倾去上清液,加水复溶,转移入50 mL量瓶中,加水定容,摇匀。从中精密移取1 mL至25 mL量瓶中,加水定容,摇匀,即得供试品溶液。
2.4.3 最大吸收波长的确定精密吸取D-无水葡萄糖对照品溶液和供试品溶液0.4 mL,分别置于干燥具塞试管中,用蒸馏水补至2 mL,依次加入5%苯酚溶液1 mL,摇匀,浓硫酸5 mL,摇匀,室温静置反应20 min。另精密移取蒸馏水2 mL同法操作,以此溶液作为空白对照,在波长400~600 nm进行扫描。结果对照品和供试品溶液均在488 nm有最大吸收。
2.4.4 标准曲线绘制精密移取对照品溶液0.1、0.2、0.3、0.4、0.5、0.6 mL,置于干燥具塞试管中,用蒸馏水补至2 mL,依次加入5%苯酚溶液1 mL,摇匀,浓硫酸5 mL,摇匀,室温静置反应20 min。另精密移取蒸馏水2 mL同法操作作为空白对照测定A值,以A值对质量浓度进行线性回归,得回归方程为Y=56.075 X-0.003 5,r2=0.999 4,表明其在5.34~14.24 mg/mL线性关系良好。
2.4.5 精密度试验分别精密移取同一供试品溶液,按照“2.4.4”项下的方法,自“用蒸馏水补至2 mL”起,依法测定其A值,平行测定6次,RSD值为0.59%,表明该法精密度良好。
2.4.6 重复性试验按照复方各药材比例精密称取6份药材8 g,按照总多糖供试品溶液的制备方法制备多糖供试品溶液按照“2.4.4”项下方法,自“用蒸馏水补至2 mL”起,依法测定其A值,RSD为1.51%,表明本处理方法制备的总多糖重复性良好。
2.4.7 稳定性试验精密吸取供试品溶液,按照“2.4.4”项下方法,自“用蒸馏水补至2 mL”起,同法操作,分别于显色后0、10、20、30、40、50 min,依法测定其A值,RSD值为0.69%。表明样品在50 min内测定稳定性良好。
2.4.8 加样回收率试验精密移取已测定多糖量的供试品溶液9份,分别按照样品含糖量的80%、100%、120%加入D-无水葡萄糖对照品溶液,按照“2.4.4”项下方法,自“加入5%苯酚溶液1 mL”起,同法操作,测定A值,计算加样回收率。结果平均回收率为99.71%,RSD为2.98%。
2.5 水提工艺研究 2.5.1 单因素考察分别对浸泡时间、溶剂倍量、提取时间、提取次数进行了考察,结果表明由于浸泡时间对总多糖提取效率几乎无影响,故选择不浸泡直接进行提取;溶剂倍量为12倍、提取时间为1 h时,提取率达到最大;而随着提取次数的增加,总多糖提取率增加。
2.5.2 正交设计优化工艺为了综合考察多因素对总多糖提取率的影响,本研究采用3因素3水平试验对提取过程进行研究。以总多糖提取率为指标,确定加水倍量(A)、提取时间(B)、提取次数(C)为考察因素,选用L9(34)正交表进行试验,因素水平表见表 3,正交设计结果见表 3,方差分析见表 4。
|
|
表 3 正交试验设计与结果 Table 3 Design and results of orthogonal test |
|
|
表 4 方差分析 Table 4 Analysis of variance |
由直观分析可知,A、B、C 3因素对提取工艺影响的大小顺序为C>A>B,即煎煮次数>加水倍量>煎煮时间。方差分析结果表明,各因素不同水平间均无显著性差异。从节约时间的角度考虑,综合分析,确定总多糖的最佳提取工艺为A3B1C3,即加14倍量的水,提取3次,每次30 min。
2.5.3 验证试验按处方比例称取黄芪药渣和其余3味药材,按上述优选出的最佳提取工艺条件加入14倍量的水,提取3次,每次30 min,平行3份,提取后测定总多糖的提取率。结果3份提取物平均总多糖提取率为16.06%,RSD为0.16%,水提工艺条件稳定、合理、可行。
2.5.4 浸膏得率测定根据验证试验结果,按最佳提取工艺操作,醇沉后,放于冰箱中静置过夜,倾去上清液,将稠浸膏蒸干,恒定质量,计算浸膏得率为24.15%。
2.6 复方健肾颗粒制备工艺研究 2.6.1 剂型选择本品处方为名中医临床经验方,原方采用药材直接煎煮给药,用于临床多年,疗效确切,但存在服用剂量大、口感差,久置易发霉变质,携带不方便,不适应现代化生活的需要等缺点,由于本方主要用于治疗气阴两虚型2型糖尿病肾病,病程比较长,故首先考虑选择制成固体制剂。鉴于本方1日服用生药量为48 g,1日服用3次(相当于每次服用生药16 g),根据醇提及水提的最佳提取工艺,计算出每日需服用浸膏量15.87 g,故考虑将其制备成颗粒剂。
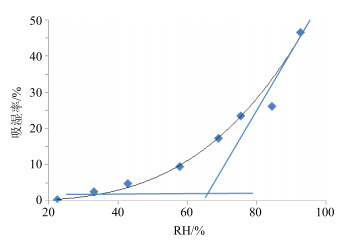
2.6.2 浸膏粉的临界相对湿度测定[8-9]取适量浸膏粉干燥至恒定质量后,精确称取1 g,置于已标记并恒定质量的称量瓶中,将称量瓶分别置于盛有7种不同过饱和盐溶液的干燥器内(称量瓶盖打开),置于25 ℃恒温培养箱中,定时称量,至恒定质量,每个干燥器中平行测定3份。计算吸湿率。以吸湿率数据为纵坐标,相对湿度(RH)为横坐标作图,作曲线两端的切线,两切线交点对应的横坐标即为临界相对湿度。结果见图 1。由结果计算出干浸膏粉的临界相对湿度为63.3%。因此浸膏粉的制备以及储存应在相对湿度小于63.3%的环境下进行。
|
图 1 不同相对湿度下浸膏粉的吸湿率 Fig.1 Hygroscopic rates in different RH |
2.6.3 评价指标
以制备过程中软材情况、制粒情况、颗粒情况、成型率、溶化性等对制备工艺进行评价。
颗粒成型率=能通过1号筛但不能通过5号筛的颗粒质量/(药粉质量+辅料质量)
2.6.4 辅料考察[10-11]取5份浸膏粉末,每份10 g,按辅料与浸膏粉按一定比例混合,用85%乙醇为润湿剂制备软材,挤压过10目筛制粒,60 ℃干燥2 h,用1号筛和5号筛整粒,收集1号筛和5号筛之间的颗粒。在制粒过程中,观察并记录软材、制粒、颗粒情况,计算颗粒成型率。
(1)单一辅料考察:将浸膏粉与辅料按1:1比例混合,以85%乙醇为润湿剂,10目筛挤压制粒,结果见表 5。
|
|
表 5 单一辅料考察结果 Table 5 Investigation of one excipient |
(2)混合辅料比例考察:将不同配比的糊精和乳糖组成混合辅料,与浸膏粉按1:1的比例混合,按“2.5.4”法制粒,结果见表 6。
|
|
表 6 混合辅料比例考察结果 Table 6 Investigation of ratio in mixed excipients |
(3)辅料用量考察:将糊精和乳糖的混合辅料与浸膏粉按2:1、1:1、1:2的比例混合制粒,结果见表 7。
|
|
表 7 辅料用量考察结果 Table 7 Investigation of dosage in mixed excipients |
(4)润湿剂浓度考察:分别采用不同体积分数的乙醇作为润湿剂制粒,结果见表 8。
|
|
表 8 润湿剂浓度考察结果 Table 8 Investigation of concentration in wetting agents |
(5)润湿剂用量考察:将混合辅料与药粉按1:1的比例混合,分别加入辅料与浸膏粉总量5%、10%、20%、30%的85%乙醇制粒,结果见表 9。由以上结果确定复方健肾颗粒的最佳制备工艺为糊精-乳糖(4:1),浸膏粉-辅料(1:1),85%乙醇,用量15%。
|
|
表 9 润湿剂用量考察结果 Table 9 Investigation of dosage in wetting agents |
(6)成型工艺验证:按最佳成型工艺平行制备3批复方健肾颗粒,采用FT-104B休止角测定仪进行测定,计算出休止角(tgα=h/r),结果见表 10。从验证性试验结果可知,按照此成型工艺进行制备,所得软材适中,易制粒,颗粒均匀,硬度适中,颗粒成型率较高,溶化性合格,休止角小于40°,流动相较好,工艺切实可行。
|
|
表 10 成型工艺验证结果 Table 10 Verification of moulding technology |
(7)干燥时间考察:复方健肾颗粒在制备时使用高体积分数的乙醇为润湿剂,易于干燥。分别考察干燥0.5、1.0、1.5、2.0 h后颗粒的水分,确定干燥时间。结果颗粒含水量分别为7.30%、5.91%、4.21%、2.82%。干颗粒含水量控制在3%以内,由结果确定健肾颗粒剂的干燥时间为2.0 h。
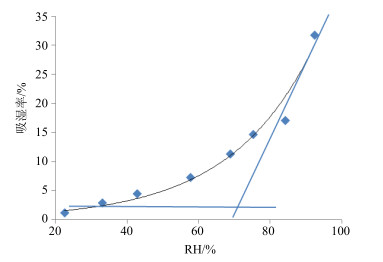
2.7 颗粒剂临界相对湿度测定取制备好的颗粒干燥至恒定质量后,精确称取1 g,置于已标记并恒定质量的称量瓶中,按“2.5.2”项相同的方法测定颗粒剂的临界相对湿度。结果见图 2。颗粒剂的临界相对湿度为70.0%,为颗粒的分剂量、包装和储存条件提供参考依据。
|
图 2 不同相对湿度下颗粒的吸湿率 Fig.2 Hygroscopic rates of granules in different RH |
3 讨论
黄芪总皂苷的显色方法有香草醛硫酸法和香草醛高氯酸法,由于香草醛高氯酸法需要将样品溶液全部挥干,耗时长,故从节约时间,操作方便的角度考虑选择香草醛硫酸法进行显色[4, 11]。
黄芪醇提液中可能会有黄酮类和少量糖类成分提出,会对其定量测定产生干扰,因此在进行定量测定前用正丁醇进行萃取3~4次,使总皂苷富集。采用水煎煮法进行总多糖成分的提取时,会有大量单糖、低相对分子质量糖提出,对多糖的测定产生干扰,并且使多糖浸膏量增加,因此,需要对其醇沉处理使总多糖富集[5, 12]。
根据单因素以及正交设计试验确定醇提的最佳提取工艺为10倍量85%乙醇,提取3次,每次2 h。水提最佳提取工艺为14倍量的水,提取3次,每次30 min。
本处方为名中医临床经验方,疗效确切,将其制备成固体制剂,服用、携带、储存方便,由于总皂苷、总多糖浸膏量较多,故考虑将其制备成颗粒剂。进行浸膏粉以及颗粒剂的临界相对湿度测定是为颗粒剂的制备以及储存条件提供依据。在制备颗粒剂时需考虑当天的湿度情况,以避免发生吸潮团聚现象。
单独的浸膏很难制备成质量合格的颗粒,为了使颗粒具有相对较小的吸湿性以及相对较好的流动性,对制粒辅料进行了筛选。颗粒剂中常使用2种及以上辅料,因此本研究对辅料的种类、比例以及用量进行考察。中药浸膏粉常具有较强的吸湿性,因此考虑乙醇为润湿剂,并对其体积分数以及用量进行考察[13]。
由实验结果确定干浸膏粉的临界相对湿度为63.3%,颗粒剂的临界相对湿度为70.0%,因此颗粒剂的制备应在小于60%湿度下进行,制备好的颗粒剂应储存于小于70%湿度下。复方健肾颗粒的最佳制备工艺为糊精-乳糖(4:1),浸膏粉-辅料(1:1),85%乙醇,用量15%。颗粒剂成型率大于90%,流动性较好,休止角小于40°,溶化性较好,能在5 min内全部溶解,颗粒干燥时间为2 h。此方法制备的复方健肾颗粒剂质量可控、服用方便。
| [1] | 鲁吉珂, 古国峰, 汪瑞, 等. 蝉花多糖提取工艺优化研究[J]. 食品工业科技 , 2013, 34 (22) :196–199. |
| [2] | 刘伟敬, 唐阳敏, 谢淑华, 等. 蝉花菌丝对糖尿病肾病大鼠的肾脏保护作用机制研究[J]. 中国中西医结合肾病杂志 , 2014, 15 (8) :665–668. |
| [3] | 金周慧, 陈以平. 蝉花汤延缓慢性肾功能衰竭进展的临床观察[J]. 中医药学刊 , 2006, 24 (8) :1457–1459. |
| [4] | 吴雪钗, 蒋燕, 谭永红. 黄芪提取工艺优选[J]. 西南国防医药 , 2012, 55 (7) :716–719. |
| [5] | 赵强强, 韩丽, 潘媛, 等. 黄芪中黄芪多糖含量的测定[J]. 中国现代中药 , 2011, 13 (7) :29–30. |
| [6] | 席小兰.养血愈风颗粒制备工艺与质量标准研究[D].成都:成都中医药大学, 2013. http://cdmd.cnki.com.cn/article/cdmd-10633-1014172246.htm |
| [7] | 丁冬梅, 严红梅, 袁嘉瑞, 等. 可溶性大豆多糖作为淫羊藿颗粒成型辅料的研究[J]. 中草药 , 2014, 45 (1) :46–49. |
| [8] | 那溪元, 刘毅, 殷明阳, 等. 麻杏止咳平喘颗粒剂成型工艺研究[J]. 中草药 , 2016, 45 (5) :767–769. |
| [9] | 罗云, 熊志伟, 张婧, 等. 三七总皂苷微丸的成型性与原料物性的相关性研究[J]. 中草药 , 2015, 46 (17) :2540–2548. |
| [10] | 朱裕林, 张兰, 彭祥雪, 等. 骨疏灵颗粒防潮辅料优选[J]. 中草药 , 2014, 45 (14) :2005–2008. |
| [11] | 张小鸿, 吴杨峥, 徐先祥. 不同显色剂对牛膝总皂苷含量测定的影响[J]. 中国实验方剂学杂志 , 2013, 19 (21) :113–116. |
| [12] | 石航, 白洁, 冯欣, 等. 多指标优选芪归银方的水提醇沉工艺[J]. 中华中医药学刊 , 2015, 33 (4) :813–816. |
| [13] | 肖琼, 沈平姨, 朱莲华. 中药固体制剂防潮技术与辅料应用的研究[J]. 中成药 , 2007, 29 (2) :208–209. |
 2016, Vol. 47
2016, Vol. 47


