2. 解放军第二军医大学药学院, 上海 200433
2. School of Pharmacy, Second Military Medical University, Shanghai 200433, China
畲药“土木香”又名红木香、南五味子根等,为福建畲族民间常用草药之一,收载于《闽东畲族文化全书(医药卷)》[1]、《福建药物志》[2]、《福建中草药》[3]等地方民族特色的草药书中,据调查报道,其来源植物不仅包括木兰科南五味子属多种植物[4],甚至还包括五味子属的华中五味子Schisandra sphenanthera Rehd.et Wils的根及藤茎等。尽管有较多华中五味子的根及茎藤在民间药用价值的文献,近年来有关华中五味子果实及种子的化学成分及药理的研究报道很多[5-9],但关于其根及藤茎的研究报道较少[10],未见有关化学成分方面的研究。本实验为了进一步研究分析华中五味子有效成分,以及新药的开发利用提供依据,对华中五味子藤茎进行了化学成分研究,分离鉴定了13个化合物,包括6个木脂素、6个为三萜、1个甾体类化合物,分别为华中五内酯素(sphendilactone,1)、南五内酯(kadsulactone,2)、五内酯E(schisanlactone E,3)、12β-羟基黑老虎酸(12-β-hydroxycoccinic acid,4)、五味子酸(schizandronic acid,5)、schisanbilactone A(6)、β-谷甾醇(β-sitosterol,7)、内消旋二氢愈创木脂酸(meso-dihydroguaiaretic acid,8)、去氧五味子素(deoxychizandrin,9)、五味子酯甲(schizantherin A,10)、五味子酚乙(schisanhenol B,11)、五味子乙素(γ-schizandrin,12)和当归酰基戈米辛M1 [R-(+)-angeloygomisin M1,13]。其中化合物1为新化合物,命名为华中五内酯素。其中五味子酚乙、去氧五味子素、当归酰基戈米辛M1、南五味子内酯、五内酯E、12β-羟基黑老虎酸和schisanbilactone A等7个化合物为华中五味子中首次分离得到。
1 仪器与材料HP5989A型质谱仪(美国安捷伦公司);HR-ESI-MS Bruker APEXIII 7.0 TESLA FTMS型质谱仪、Bruker DRX 400/DRX600核磁共振光谱仪(德国Bruker公司)。95%乙醇(化学纯),乙醚、丙酮、石油醚、无水硫酸钠均为分析纯,柱色谱硅胶(试剂级),硅胶板(青岛谱科分离材料有限公司)。
供试材料于2010年10月采自福建省福安市康厝畲族乡,经第二军医大学生药学教研室秦路平教授鉴定为五味子科植物华中五味子Schisandra sphenanthera Rehd.et Wils的藤茎,凭证标本(FJ201010-1)存于福建中医药大学中药鉴定室。
2 提取与分离华中五味子茎藤粉碎得药材粗粉750 g,室温下以95%乙醇反复冷浸及超声提取数次后,减压回收溶剂,得到浸膏,浸膏悬浮于蒸馏水中,水蒸气蒸馏法提取挥发油,提取挥发油后的水溶液以乙醚萃取4次,回收乙醚,得到萃取物30 g。取乙醚萃取物进行硅胶柱色谱,依次以石油醚、石油醚-醋酸乙酯(15:1→1:2)、醋酸乙酯进行梯度洗脱,得到2个流分。其中流分1(石油醚-醋酸乙酯10:1洗脱部分)再进行硅胶柱色谱,经石油醚-醋酸乙酯(15:1→3:1)反复洗脱后,从8:1洗脱流分中得到化合物7(25 mg);从6:1洗脱流分中得到化合物1(12 mg)、2(40 mg)和6(21 mg);从4:1洗脱流分中得到化合物3(8 mg)和5(6 mg)。流分2(石油醚-醋酸乙酯5:1洗脱部分)再进行硅胶柱色谱,经石油醚-醋酸乙酯(10:1→2:1)反复硅胶柱色谱后,从10:1洗脱流分中得到化合物4(3 mg)、8(60 mg)、9(170 mg)、12(3 mg)和13(4 mg);从4:1洗脱流分中得到化合物10(30 mg)和11(50 mg)。
3 结构鉴定化合物1:无色方晶(石油醚-丙酮)。[α]D25+46.7°(c 0.3, 甲醇),EI-MS谱给出分子离子峰为m/z 468,通过高分辨质谱HR-EI-MS(m/z 467.324 0 [M-H]−;计算值467.323 9)可确定分子式为C30H44O4,不饱和度为9。1H-和13C-NMR谱数据(表 1)表明该化合物是三萜类化合物,且波谱数据与南五内酯kadsulactone类化合物较为相似[11]。1H-NMR(表 1)中δH 6.60(1H, d, J=6.2 Hz), 4.46(1H, dt, J=13.2, 3.7 Hz)和13C-NMR谱(表 1)中δC 166.5, 139.3, 128.3等信号都表明侧链为不饱和内酯。同时另一个酯羰基δC 175.2的存在,提示该化合物骨架类型与kadsudilactone一致(化合物1参照此碳原子编号及相对立体构型),即3,4位开环后,又形成七元环内酯的结构。具有7个甲基信号δH 0.69, 0.74, 1.23, 1.46, 1.47, 1.91(各3H, s)及δH 0.98(3H, d, J=6.6 Hz, ),同时高场区没有环丙烷的特征信号,提示19位不与9位构成环丙烷,而是以甲基的形式存在。那么9位很可能形成双键。13C-NMR谱中的1对双键碳信号δC 146.5, 117.1表明有双键的存在,一般该类化合物的双键多为8(9)位双键或9(11)位双键,1H-NMR谱中1个烯质子信号δH 5.35,提示双键出现在9(11)位。
|
|
表 1 化合物1的1H-NMR和13C-NMR数据(600/100 MHz, CDCl3) Table 1 1H-NMR and 13C-NMR data of compound 1 (600/100 MHz, CDCl3) |
从对HMQC和HMBC谱(图 1)相关信号的分析可知,δH 1.23(3H, s, H-19)与δC52.8(C-5)、146.5(C-9)相关;δH 5.35(1H, d, J=6.1 Hz, H-11)与δC42.0(C-8), 44.5(C-13)相关,再加上1H-1H COSY谱(图 1)中δH 5.40(1H, d, J=6.1 Hz, H-11)与δH 2.10~2.14(2H, m, H-12)的关系,证明双键位于9(11)位。结合HMQC和HMBC谱和1H-1H COSY谱,其他位置的信号也得到一一归属。
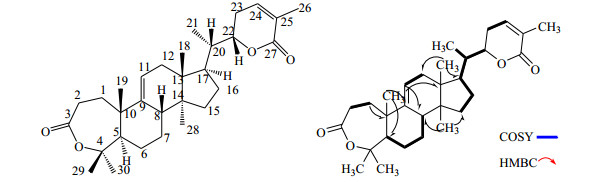
|
图 1 化合物1的结构及主要HMBC、1H-1H COSY相关 Fig.1 Key HMBC and 1H-1H COSY correlations in compound 1 |
参照kadsudilactone的相对立体构型,化合物1的相对立体化学可通过对NOESY谱(图 2)相关信号的分析得以证实。Me-29/Me-19、Me-29/H-8、H-8/Me-18、Me-18/H-22、H-22/H-20的NOESY相关表明上述氢质子取向相同,为β-构型;而Me-30/H-5、Me-21/H-17、Me-21/Me-28的相关表明为上述氢质子取向相同,均为α-构型。相对立体构型与kadsudilactone完全一样。

|
图 2 化合物1的关键NOESY关系 Fig.2 Key NOESY correlation for compound 1 |
综上所述,化合物1的母核为五味子类药物中代表性的羊毛甾烯型四环三萜内酯,在A环的3(4)位置开环,再闭环为七元环内酯,和已知化合物kadsudilactone结构基本相同,不同之处在于化合物kadsudilactone的9(19)位形成环丙烷,而化合物1中9(11)位形成双键,19位为甲基。化合物1的结构最终确定为3, 4-开环-羊毛甾-9, 24-双烯-3, 26-双内酯,并命名为华中五内酯素。
化合物2:白色结晶(石油醚-醋酸乙酯),1H-NMR(400 MHz, CDCl3) δ: 0.59, 0.80(各1H, d, J=4.3 Hz, 19-CH2), 0.89(3H, s, 28-CH3), 1.03(3H, s, 29-CH3), 1.04(3H, s, 30-CH3), 1.09(3H, s, 18-CH3), 1.91(3H, s, 27-CH3), 0.97(3H, d, J=6.6 Hz, 21-CH3), 4.44(1H, dt, J=12.9, 3.1 Hz, H-22), 6.60(1H, d, J=6.7 Hz, H-24);13C-NMR(100 MHz, CDCl3)δ: 216.5(C-3), 166.6(C-26), 139.4(C-4), 128.2(C-24), 80.5(C-22), 50.1(C-4), 48.7, 48.3(C-5, 8), 48.1, 45.7(C-13, 14), 47.7(C-17), 39.0(C-20), 37.4(C-16), 35.5, 33.3, 32.5, 29.4, 26.9, 26.5, 25.9, 22.1(C-12, 1, 2, 6, 11, 15, 7), 25.8(C-19), 23.4(C-23), 21.4(C-10), 20.9, 20.7(C-30, C-29), 17.0(C-28, 18), 19.3(C-29), 17.8(C-27), 13.0(C-21)。以上数据与文献报道一致[11],故鉴定化合物2为南五内酯。
化合物3:白色颗粒状结晶(石油醚-醋酸乙酯),1H-NMR(400 MHz, CDCl3)δ: 6.61(1H, d, J=6.3 Hz, H-24), 4.80, 4.72(各1H, s, H2-30), 4.46(1H, dt, J=12.9, 3.5 Hz, H-22), 1.91(3H, s, 27-CH3), 1.66(3H, s, 29-CH3), 0.98(3H, s, 18-CH3), 0.96(3H, d, J=6.7 Hz, 21-CH3), 0.91(3H, s, 28-CH3), 0.73, 0.41(各1H, d, J=4.50 Hz, 19-CH2);13C-NMR(100 MHz, CDCl3) δ: 180.0(C-3), 166.6(C-26), 149.2(C-25), 139.5(C-4), 128.2(C-24), 111.6(C-28), 80.5(C-22), 48.5, 48.0(C-5, 8), 47.5, 45.5(C-13, 14), 45.8(C-17), 39.1(C-20), 35.5(C-16), 32.8, 31.5, 31.4, 29.8, 28.7, 26.7, 26.9(C-12, 1, 2, 6, 11, 15, 7), 27.5(C-9), 24.9(C-19), 23.4(C-23), 21.1(C-10), 19.4, 17.0(C-30, 18), 19.6(C-29), 17.8(C-27), 13.0(C-21)。以上数据与文献报道一致[12],故鉴定化合物3为五内酯E。
化合物4:无色针晶(石油醚-丙酮),1H-NMR(400 MHz, CDCl3)δ: 6.09(1H, t, J=7.1 Hz, H-24), 5.29(1H, d, J=4.1 Hz, H-11), 3.89(1H, m, H-12), 1.92(3H, s, 27-CH3), 1.23(3H, s, 19-CH3), 1.07(3H, s, 18-CH3), 1.04(3H, s, 28-CH3), 0.96(3H, d, J=14.5 Hz, 21-CH3), 0.75(3H, s, 29-CH3), 0.68(3H, s, 30-CH3)。以上数据与文献报道基本一致[13],故鉴定化合物4为12β-羟基黑老虎酸。
化合物5:无色针晶(醋酸乙酯),1H-NMR(400 MHz, CDCl3)δ: 6.60(1H, d, J=6.8 Hz, H-24), 5.35(1H, d, J=5.9 Hz, H-3), 4.47(1H, dt, J=13.2, 3.5 Hz, H-22), 1.92(3H, s, 27-CH3), 1.00(3H, d, J=6.9 Hz, 21-CH3), 0.93(3H, s, 18-CH3), 0.83(3H, s, 28-CH3), 0.75(3H, s, 29-CH3), 0.70(3H, s, 30-CH3), 0.51, 0.34(各1H, d, J=4.2 Hz, 19-CH2)。以上数据与文献报道一致[14],故鉴定化合物5为五味子酸。
化合物6:无色针晶(醋酸乙酯),1H-NMR(600 MHz, CDCl3)δ: 6.60(1H, d, J=6.4 Hz, H-24), 6.04(1H, d, J=12.8 Hz, H-1), 5.92(1H, d, J=12.7 Hz, H-2), 5.30(1H, s, H-6), 4.46(1H, dt, J=13.4, 3.6 Hz, H-22), 2.03(3H, s, J=3.8 Hz, OAc), 1.91(3H, s, 27-CH3), 1.48(3H, s, 29-CH3), 1.41(3H, s, 30-CH3), 1.23, 1.74(各2H, d, J=4.6 Hz, H-19), 1.02(3H, s, 18-CH3), 0.97(3H, t, J=7.5 Hz, 21-CH3), 0.93(3H, s, 28-CH3);13C-NMR(150 MHz, CDCl3)δ: 171.0(C-1′), 168.1(C-3), 167.8(C-26), 151.9(C-1), 140.7(C-24), 129.8(C-25), 121.3(C-2), 85.0(C-4), 81.8(C-22), 71.9(C-6), 49.6(C-17), 49.6(C-5), 49.2(C-13), 47.0(C-14), 42.2(C-7), 40.5(C-8), 37.9(C-20), 37.2(C-19), 33.9(C-15), 33.4(C-12), 30.2(C-10), 29.9(C-11), 29.4(C-9), 29.3(C-16), 28.4(C-7), 25.3(C-23), 24.9(C-30), 22.6(C-2′), 20.9(C-28), 19.4(C-18), 18.8(C-27), 14.7(C-21)。以上数据与文献报道一致[15],故鉴定化合物6为schisanbilactone A。
化合物7:白色针晶(甲醇),1H-NMR(400 MHz, CDCl3)δ: 5.38(1H, d, J=5.1 Hz, H-6), 3.49(1H, s, H-3), 1.25(3H, s, 18-CH3), 1.01(3H, s, 19-CH3), 0.92(3H, d, J=6.6 Hz, 21-CH3), 0.83(3H, m, 29-CH3), 0.85(3H, m, 30-CH3), 0.68(3H, m, 27-CH3)。以上数据与文献报道一致[16],故鉴定化合物7为β-谷甾醇。
化合物8:无色针晶(石油醚-醋酸乙酯),1H-NMR(400 MHz, CDCl3) δ: 6.83(2H, d, J=8.4 Hz, H-5, 5′), 6.65(2H, dd, J=8.4, 1.6 Hz, H-6, 6′), 6.61(2H, d, J=1.6 Hz, H-2, 2′), 5.46(2H, brs, 2×OH), 3.86(6H, s, 2×OCH3), 2.73, 2.28(各2H, dd, J=13.8, 5.4 Hz, H-7, 7′), 1.75(2H, q, J=6.0 Hz, H-8, 8′), 0.84(6H, d, J=6.3 Hz, H-9, 9′);13C-NMR(100 MHz, CDCl3)δ: 146.4(C-3, 3′), 143.7(C-4, 4′), 133.8(C-1, 1′), 121.8(C-6, 6′), 114.0(C-5, 5′), 111.0(C-2, 2′), 55.9(OCH3), 39.2(C-7, 7′), 39.0(C-8, 8′), 16.3(C-9, 9′)。以上数据与文献报道一致[17],故鉴定化合物8为内消旋二氢愈创木脂酸。
化合物9:白色方晶(石油醚-丙酮),1H-NMR(400 MHz, CDCl3)δ: 6.54(2H, s, H-6, 6′), 3.62, 3.90, 3.91(各6H, s, 6×OCH3), 2.38, 2.20(各2H, m, H2-7, 7′), 1.61(2H, m, H-8, 8′), 1.02(6H, d, J=7.2 Hz, 2×CH3);13C-NMR(100 MHz, CDCl3)δ: 152.8(C-5, 5′), 151.0(C-3, 3′), 139.8(C-4, 4′), 138.0(C-2, 2′), 122.6(C-1, 1′), 107.5(C-6, 6′), 60.9, 60.5, 55.8(3×OCH3), 42.7(C-7, 7′), 40.7(C-8, 8′), 23.6(C-9, 9′)。以上数据与文献报道一致[18],故鉴定化合物9为去氧五味子素。
化合物10:无色晶体(石油醚-丙酮),1H-NMR(400 MHz, CDCl3) δ: 7.58~7.29(5H, m, H-3′~7′), 6.82, 6.56(各1H, s, H-4, 11), 5.82, 5.78(各1H, s, H-19), 5.66(1H, t, J=4.8 Hz, H-6), 3.95, 3.84, 3.56, 3.30(各3H, s, 4×OCH3), 2.35(1H, dt, J=19.8, 9.9 Hz, H-8), 2.19, 2.13(各1H, m, H-9), 1.37(3H, s, 17-CH3), 1.18(3H, d, J=7.1 Hz, 18-CH3);13C-NMR(100 MHz, CDCl3)δ: 152.2(C-3), 152.0(C-12), 148.8(C-1), 141.9(C-14), 140.2(C-13), 135.2(C-5), 134.2(C-10), 130.4(C-2), 122.3(C-15), 121.1(C-16), 110.0(C-11), 102.4(C-4), 100.4(C-19), 84.9(C-6), 72.3(C-7), 60.8, 60.7, 58.7, 55.9(4×OCH3), 42.7(C-8), 36.5(C-9), 28.2(C-18), 18.9(C-17), 164.8(C-1′), 129.4(C-3′, 7′), 129.5(C-2′), 127.9(C-4′, 6′), 132.9(C-5′)。以上数据与文献报道一致[19],故鉴定化合物10为五味子酯A。
化合物11:无色晶体(石油醚-丙酮),1H-NMR(400 MHz, CDCl3)δ: 6.50(1H, s, H-4), 6.37(1H, s, H-11), 5.93(2H, s, H-19), 2.52~2.56(2H, m, H-6), 2.02~2.30(2H, m, H-9), 1.78(1H, m, H-7), 1.88(1H, m, H-8), 0.74(3H, d, J=7.1 Hz, 17-CH3), 0.96(各3H, d, J=7.1 Hz, 18-CH3), 3.85, 3.87, 3.91(各3H, s, 3×OCH3);13C-NMR(100 MHz, CDCl3)δ: 150.4(C-3), 148.9(C-12), 146.9(C-1), 141.0(C-14), 138.4(C-13), 134.7(C-5), 134.5(C-10)133.6(C-2), 120.2(C-15), 116.7(C-16), 107.2(C-11), 103.4(C-4), 100.8(C-19), 61.0, 59.7, 55.7(3×OCH3), 40.8(C-7), 39.2(C-9), 35.7(C-6), 33.5(C-8), 21.5(C-18), 12.9(C-17)。以上数据与文献报道一致[20],故鉴定化合物11为五味子酚乙。
化合物12:无色晶体(石油醚-丙酮),1H-NMR(400 MHz, CDCl3)δ: 6.69(1H, s, H-4), 6.41(1H, s, H-11), 5.94(2H, s, H-19), 3.54, 3.82, 3.88, 3.89(各3H, s, 4×OCH3), 2.53~2.57(2H, m, H-6), 2.0~2.3(2H, m, H-9), 1.88(1H, m, H-7), 1.78(1H, m, H-8), 0.96(3H, d, J=7.2 Hz, 17-CH3), 0.73(3H, d, J=7.2 Hz, 18-CH3)。以上数据与文献报道一致[21],故鉴定化合物12为γ-schizandrin。
化合物13:白色粉末,1H-NMR(400 MHz, CDCl3) δ: 6.55(1H, s, H-4), 6.47(1H, s, H-11), 5.90(1H, m, H-3′), 5.88(2H, s, H-19), 3.81, 3.83, 3.90(各3H, s, 3×OCH3), 2.57~2.60(2H, m, H-6), 2.10~2.33(2H, m, H-9), 1.78(1H, m, H-7), 1.90(1H, m, H-8), 1.79(3H, s, 5′-CH3), 1.25(3H, d, J=7.0 Hz, 4′-CH3), 0.95(3H, d, J=7.0 Hz, 17-CH3), 0.75(3H, d, J=7.0 Hz, 18-CH3)。以上数据与文献报道一致[22],故鉴定化合物13为当归酰基戈米辛M1。
| [1] | 钟雷兴. 闽东畲族文化全书(医药卷)[M]. 北京: 民族出版社, 2009 . |
| [2] | 福建中医药研究院. 福建药物志(修订本第一卷)[M]. 福州: 福建科技出版社, 1994 . |
| [3] | 福建省医药研究所. 福建中草药[M]. 福州: 福建科技出版社, 1970 . |
| [4] | 范世明, 黄泽豪. 闽产红木香的原植物鉴别[J]. 福建中医学院学报 , 2008, 18 (3) :32–34. |
| [5] | Wang C R, Sun R, Yang C R, et al. Two new lignans from the fruits of Schisandra sphenanthera[J]. Nat Prod Commun , 2009, 4 (11) :1571–1574. |
| [6] | 孙, 彭修娟, 徐虹, 等. 南五味子化学成分及药理学研究进展[J]. 陕西中医学院学报 , 2007, 30 (4) :74–75. |
| [7] | Huang F, Xu L J, Du G H, et al. In vitro antioxidative and cytotoxic activities of Schisandra sphenanthera Rehd.Et Wils[J]. Nat Prod Res Dev , 2006, 18 (1) :85–87. |
| [8] | 樊秦, 赵文君, 李应东, 等. 华中五味子含药血清对成骨细胞增殖分化的影响[J]. 中国实验方剂学杂志 , 2009, 15 (2) :33–35. |
| [9] | 史琳, 王志成, 冯叙桥. 五味子化学成分及药理作用的研究进展[J]. 药物评价研究 , 2011, 34 (3) :208–212. |
| [10] | 张洁, 薛金龙. 华中五味子藤茎的生药鉴定[J]. 中药材 , 1999, 22 (4) :177–179. |
| [11] | Tan R, Xue H, Li L N. Kadsulactone and kadsudilactone, two new triterpenoid lactones from Kadsura species[J]. Planta Med , 1991, 57 (1) :87–88. DOI:10.1055/s-2006-960031 |
| [12] | 刘嘉森, 黄梅芬. 五内酯E和长南酸的分离与结构[J]. 化学学报 , 1991, 49 (5) :502–506. |
| [13] | Li L, Xue H. Treiterpenoids from roots and stems of K.coccimea[J]. Planta Med , 1986, 52 (6) :492–493. DOI:10.1055/s-2007-969264 |
| [14] | Takahashi K, Takani M. Constituents of medicinal plants.XIV.Constituents of Schisandra nigra[J]. Chem Pharm Bull , 1975, 23 (3) :538–542. DOI:10.1248/cpb.23.538 |
| [15] | Ma W H, He J, Li L, et al. Two new triterpenoids from the stems of Schisandra bicolor[J]. Helv Chim Acta , 2009, 92 (10) :2086–2091. DOI:10.1002/hlca.v92:10 |
| [16] | 刘海涛, 李兴博, 张进, 等. 华中五味子果实石油醚部位化学成分的研究[J]. 中国中药杂志 , 2012, 37 (11) :1597–1601. |
| [17] | Liu J S, Huang M F, Gao Y G, et al. The structure of chicanine, a new lignan from Schisandra sp[J]. Can J Chem , 1981, 59 (11) :1680–1684. DOI:10.1139/v81-250 |
| [18] | 王洪洁, 陈延镛. 红花五味子中木脂素成分的化学研究[J]. 药学学报 , 1985, 20 (11) :832–841. |
| [19] | Ikeya Y, Taguchi H, Yosioka I, et al. The constituents of Schisandra chinensis Baill.I.Isolation and structure determination of five new lignans, gomisin A, B, C, E and F, and the absolute structure of schizandrin[J]. Chem Pharm Bull , 1979, 27 (6) :1383–1394. DOI:10.1248/cpb.27.1383 |
| [20] | Ikeya Y, Taguchi H, Yosioka I, et al. The constituents of Schisandra chinensis Baill.Ⅷ.The structures of two new lignans, tigloylgomisin P and angeloylgomisin P[J]. Chem Pharm Bull , 1980, 28 (11) :3357–3361. DOI:10.1248/cpb.28.3357 |
| [21] | Chen Y Y, Shu Z B, Li L N. Studies on Fructus Schisandra.Isolation and determination of the active compounds (in lowering high SGPT levels) of Schisandra chinensis Baill[J]. Sci China Math , 1976, 19 (2) :276–290. |
| [22] | Tan R, Li L N, Fang Q C. Studies on the chemical constituents of Kadsura longipedunculata:Isolation and structure elucidation of five new lignans[J]. Planta Med , 1984, 50 (5) :414–417. DOI:10.1055/s-2007-969751 |
 2016, Vol. 47
2016, Vol. 47

