2. 安徽济人药业有限公司, 安徽 亳州 236800 ;
3. 安徽中医药大学药学院, 安徽 合肥 230012
2. Anhui Jiren Pharmaceutical Co., Ltd., Bozhou 236800, China ;
3. College of Pharmacy, Anhui University of Traditional Chinese Medicine, Hefei 230012, China
白芷Angelicae Dahuricae Radix为伞形科(Umbelliferae)植物白芷Angelica dahurica (Fisch. ex Hoffm.) Benth. et Hook. f.或杭白芷Angelica dahurica (Fisch. ex Hoffm.) Benth. et Hook. f. var. formosana (Boiss.) Shan et Yuan的干燥根[1]。安徽亳州是白芷的主要种植基地,2004年以来,亳州年产白芷药材达4 000 t以上,其种植历史悠久,质量优、产量大。白芷配方颗粒是以白芷药材为原料,经加工炮制、提取、浓缩、干燥、制粒而成[2]。本研究建立了白芷药材-饮片-提取物及配方颗粒的HPLC特征图谱,对其相关性进行评价,为白芷配方颗粒质量控制提供借鉴。
1 仪器与材料YP1002N型电子天平、FA2104SN型电子天平,上海精密科学仪器有限公司;Agilent 1200型高效液相色谱仪,美国安捷伦公司;HH型数显恒温水浴锅,江苏省金坛市金城国胜实验仪器厂;岛津UV1700紫外分光光度计,日本岛津仪器科技有限公司;HU10260B型超声波清洗器,天津恒奥科技发展有限公司。
10批白芷药材分别于2013年8-12月收集于亳州谯城区不同乡镇的白芷种植基地,经安徽中医药大学金传山教授鉴定为伞形科当归属植物白芷Angelica dahurica (Fisch. ex Hoffm.) Benth. et Hook. f.的干燥根,由济人药业配方颗粒工艺研究室制成同批号白芷饮片、提取物干膏粉、配方颗粒,编号及药材具体来源见表 1。
|
|
表 1 样品信息 Table 1 Information of sample sources |
对照品欧前胡素(批号110826-201415,质量分数99.7%)、异欧前胡素(批号110827-201109,质量分数99.6%),中国食品药品检定研究院;乙醇、甲醇,分析纯,郑州派尼化学试剂厂;甲醇,色谱纯,郑州派尼化学试剂厂;其他试剂均为分析纯。
2 方法与结果 2.1 色谱条件与系统适应性[1]色谱柱为Agilent HC-C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-水(60:40);检测波长300 nm;体积流量1.0 mL/min;柱温30 ℃;进样量20 μL;理论板数按欧前胡素峰计算不低于3 000。
2.2 对照品溶液制备精密称取欧前胡素对照品5.0 mg置于50 mL量瓶中,加甲醇溶解定容至刻度,摇匀,精密量取1 mL置10 mL量瓶中,用甲醇稀释至刻度,摇匀,即得10 μg/mL的欧前胡素对照品溶液。
2.3 供试品溶液制备称取白芷药材、饮片、提取物及配方颗粒粉末各0.4 g,精密称定,置50 mL量瓶中,加甲醇45 mL,超声处理(功率300 W,频率50 kHz)1 h,放冷,加甲醇至刻度,摇匀,滤过,取续滤液,即得。
2.4 样品定量测定分别取对照品溶液、供试品溶液20 μL,按“2.1”项下的色谱条件测定,药材A1~A10中欧前胡素分别为0.189%、0.184%、0.226%、0.225%、0.258%、0.331%、0.157%、0.255%、0.170%、0.185%(n=2),均值为0.218%;饮片B1~B10中欧前胡素分别为0.181%、0.176%、0.127%、0.201%、0.180%、0.219%、0.087%、0.223%、0.140%、0.145%(n=2),均值为0.168%;提取物C1~C10中欧前胡素分别为0.423%、0.345%、0.584%、0.524%、0.608%、0.568%、0.303%、0.531%、0.352%、0.359%(n=2),均值为0.417%;配方颗粒D1~D10中欧前胡素分别为0.369%、0.320%、0.540%、0.469%、0.691%、0.559%、0.342%、0.532%、0.460%、0.348%(n=2),均值为0.426%。结果显示10批白芷药材中欧前胡素质量分数在0.157%~0.331%,均大于0.080%,符合《中国药典》2015年版的要求;10批白芷饮片中欧前胡素质量分数在0.087%~0.223%,表明由药材加工成饮片会有少量的香豆素类成分的丢失;饮片经溶剂提取浓缩干燥,得提取物膏粉,10批提取物中欧前胡素质量分数平均值为0.417%,10批配方颗粒欧前胡素质量分数平均值为0.426%,表明在现代制粒条件下,提取物到配方颗粒的制备过程对欧前胡素质量分数无明显影响;但从饮片加工成提取物时,存在欧前胡素转移率不高的现象,原因有待进一步研究。
2.5 白芷药材-饮片-提取物及配方颗粒特征图谱的建立 2.5.1 色谱条件色谱柱为Agilent HC-C18柱(250 mm×4.6 mm,5 μm),流动相为乙腈-水,梯度洗脱:0~50 min,5%~65%乙腈;50~70 min,65%~95%乙腈;体积流量1.0 mL/min;柱温25 ℃;检测波长320 nm;进样量10 μL;分析时间100 min。
2.5.2 对照品溶液的制备分别取欧前胡素、异欧前胡素对照品2 mg,分别置于5 mL量瓶中,用甲醇溶解并定容至刻度。
2.5.3 供试品溶液的制备取白芷药材、饮片、提取物及配方颗粒粉末各0.5 g,精密称定,置锥形瓶中,分别精密加入甲醇溶剂25 mL,回流提取0.5 h,滤过,蒸干,加甲醇溶解并定容到10 mL,分别用微孔滤膜(孔径0.45 μm)滤过,滤液作为供试品溶液。
2.5.4 定量测定分别取对照品溶液、供试品溶液10 μL,按“2.5.1”项下的色谱条件测定,记录100 min色谱图,见图 1~5。
|
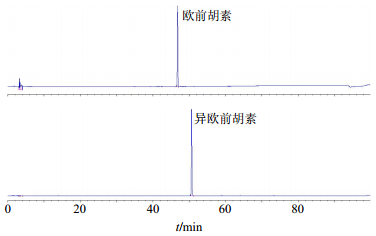
图 1 对照品欧前胡素和异欧前胡素的HPLC图 Fig.1 HPLC of reference imperatorin and isoimperatorin |
|
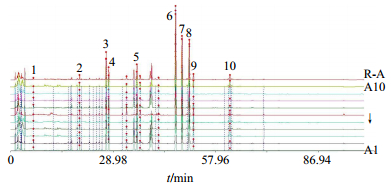
6-欧前胡素8-异欧前胡素,下图同 6-imperatorin 8-isoimperatorin, same as below 图 2 10批白芷药材HPLC指纹图谱及其对照指纹图谱(R-A) Fig.2 HPLC characteristic spectrum of 10 batches of medicinal material of ADR and its reference characteristic spectra (R-A) |
|
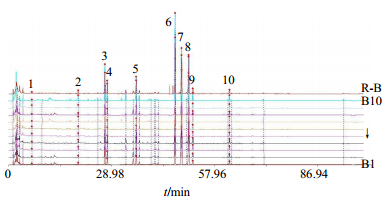
图 3 10批白芷饮片HPLC指纹图谱及其对照指纹图谱(R-B) Fig.3 HPLC characteristic spectrum of 10 batches of decoction pieces of ADR and its reference characteristic spectra (R-B) |
|
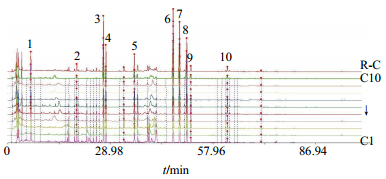
图 4 10批白芷提取物HPLC指纹图谱及其对照指纹图谱(R-C) Fig.4 HPLC characteristic spectrum of 10 batches of extract of ADR and its reference characteristic spectra (R-C) |
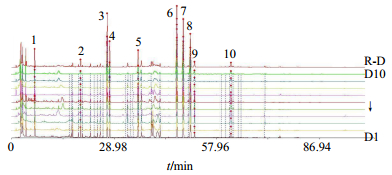
|
图 5 10批白芷配方颗粒HPLC指纹图谱及其对照指纹图谱(R-D) Fig.5 HPLC characteristic spectrum of 10 batches of ADR dispensing granules and its reference characteristic spectra (R-D) |
2.6 方法学考察 2.6.1 精密度试验
取“2.5.3”项下同一供试品(编号A1)溶液,连续进样6次,考察进样精密度,结果各共有峰保留时间的RSD<2.1%,各共有峰峰面积的RSD<3.0%,表明仪器精密度良好。
2.6.2 重复性试验取同批次药材(编号A1),按“2.5.3”项方法分别制备6份供试品溶液,平行测定,结果各共有峰保留时间的RSD<2.4%,各共有峰峰面积的RSD<3.0%,表明方法重复性良好。
2.6.3 稳定性试验取“2.5.3”项下相同供试品溶液,分别在0、3、6、9、24、48 h进样测定。结果各共有峰保留时间的RSD<2.3%,各共有峰峰面积的RSD<3.0%,表明供试品溶液在48 h内稳定性良好。
2.7 共有峰的标定将各批配方颗粒的HPLC特征图谱数据导入“中药色谱指纹图谱相似度评价系统软件”(2004A版),选择时间窗宽度为0.10,平均数法生成对照图谱,对色谱图进行多点校正后,自动匹配,生成图谱,经比较分析后确定10个共有峰。同法采集白芷药材、饮片和提取物的特征图谱,发现提取物、药材、饮片均有10个共有峰。与欧前胡素、异欧前胡素对照品色谱图进行比对,确认配方颗粒样品图中6号峰为欧前胡素,8号峰为异欧前胡素。对照品色谱图见图 1,白芷药材、饮片、提取物和配方颗粒对照特征图谱见图 6。由图 6可见,1~10号峰是药材、饮片、提取物和配方颗粒的共有峰。各图谱的相似度见表 2。结果显示,10批药材特征图谱与对照特征图谱的相似度在0.911~0.968;饮片在0.894~0.968;提取物在0.941~0.994;配方颗粒在0.953~0.993。结果提示,药材、饮片、提取物和配方颗粒整体具有相似性。
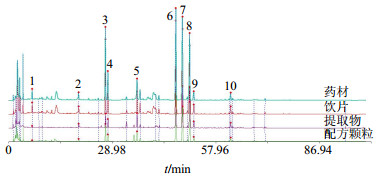
|
6-欧前胡素8-异欧前胡素 6-imperatorin 8-isoimperatorin 图 6 白芷药材、饮片、提取物和配方颗粒HPLC对照特征图的比较 Fig.6 Comparison on HPLC reference characteristic spectra of raw herbs, decoction pieces, and extract with ADR dispensing granules |
|
|
表 2 各图谱的相似度计算结果 Table 2 Similarity of characteristic chromatograms |
2.8 相关性分析
从整体上看,白芷药材、饮片、提取物及配方颗粒HPLC特征图谱的1~10号峰是药材、饮片、提取物和配方颗粒的共有峰,见图 6。结果显示,S1~S10批次白芷药材、饮片、提取物、配方颗粒特征图谱相似度分别在0.916~0.963、0.930~0.967、0.911~0.988、0.968~0.991、0.894~0.990、0.964~0.984、0.956~0.990、0.962~0.983、0.926~0.953、0.966~0.994,其化学成分相关性较好。将白芷药材、饮片、提取物、配方颗粒的特征图谱进行重叠比较,白芷药材中主要色谱峰在饮片、提取物及配方颗粒的色谱图中均有体现,而饮片、提取物及配方颗粒的主要色谱峰也能在药材的图谱中找到追溯。将特征图谱用于中药配方颗粒全过程监控,可以反映生产过程各环节的量质传递变化规律[3]。
3 讨论欧前胡素、异欧前胡素是白芷药材中已知的主要有效成分,也是评价药材质量的主要指标成分[4],但这2种香豆素类成分在水中溶解度小,水提取有效成分转移率低。本实验采用了醇提加水提的白芷配方颗粒生产工艺:加10倍量60%乙醇,回流提取2.5 h,药渣再加9倍量水,提取1.5 h。按此法制得配方颗粒,较单一用水提取较大限度地提高欧前胡素和异欧前胡素的提取率,使白芷配方颗粒保留了原料中的主要活性成分群。
对不同提取溶剂及热回流、超声不同提取方法进行考察,从提取的全面性、稳定性、操作便捷性等方面考察,选择甲醇为白芷的提取溶剂,回流提取为白芷的提取方法。选择料液比、提取时间优化白芷配方颗粒特征图谱的提取工艺,优化所得的白芷加热回流最佳工艺为料液比25 mL/g,加热回流提取0.5 h。
本实验对色谱条件中的流动相体系进行考察,考察了甲醇-水二元梯度洗脱[5],乙腈-0.5%磷酸水溶液二元梯度洗脱[6],并对上述洗脱条件进行调整,结果表明以乙腈-水为流动相、梯度洗脱,所得色谱峰有10个明显的主峰,峰形较好,峰分离理想。
| [1] | 中国药典[S].一部. 2015. |
| [2] | 陈培胜, 朱月信. 中药配方颗粒行业标准研究思路[J]. 中医杂志 , 2012, 53 (6) :469–472. |
| [3] | 孙源源, 施萍. 借助中药配方颗粒推进中药国际化的对策研究[J]. 中草药 , 2013, 44 (8) :929–934. |
| [4] | 常新全, 丁丽霞. 中药活性成分分析手册[M]. 北京: 学苑出版社, 2002 . |
| [5] | 袁亚洲, 倪永年. 不同产地白芷药材高效液相色谱指纹图谱研究[J]. 分析科学学报 , 2009, 25 (2) :26–28. |
| [6] | 张翠英, 李振国, 王青晓. 白芷饮片HPLC指纹图谱研究[J]. 中药材 , 2007, 30 (11) :1374–1376. |
 2016, Vol. 47
2016, Vol. 47


