2. 天津药物研究院, 天津 300193 ;
3. 沈阳药科大学 基于靶点的药物设计与研究教育部重点实验室, 辽宁 沈阳 110016
2. Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China ;
3. Key Laboratory of Structure-Based Drug Design and Discovery, Shenyang Pharmaceutical University, Ministry of Education, Shenyang 110016, China
积雪草Centella asiatica (L.) Urban为伞形科(Umbelliferae)积雪草属Centella L.植物,其性寒,味苦、辛,具有清热利湿、解毒消肿之功效[1-2]。研究表明,积雪草中的主要活性成分是乌苏烷型和齐墩果烷型三萜化合物[3-4],对多种肿瘤细胞株具有不同程度的抑制活性[3-7]。植物提取物的酸水解反应可以获得更多活性天然产物衍生物(尤其是新皂苷元)。本实验对积雪草皂苷进行酸水解反应,对水解产物的化学成分进行了分离和结构鉴定。采用硅胶柱色谱、凝胶柱色谱等方法进行分离、纯化,分离并鉴定了4个苷元化合物,分别为2α, 3β, 23-三羟基乌苏-6, 12-二烯-28-酸(2α, 3β, 23-trihydroxyurs-6, 12-dien-28-oic acid,1)、积雪草酸(asiatic acid,2)、6β-羟基积雪草酸(6β-hydroxy asiatic acid,3)、terminolic acid(4)。其中,化合物1鉴定为新的乌苏烷苷元化合物,命名为积雪草-6-烯。此外,本实验还对新化合物的体外抗肿瘤活性进行了测试,结果显示化合物1对所测试的肿瘤细胞无抑制活性。
1 仪器与材料Shimadzu UV-2201(日本岛津仪器有限公司);Bruker ARX-600型超导核磁共振仪(德国布鲁克公司);TOF-Q质谱仪(美国布鲁克海文仪器公司);X-4数字显示显微熔点测定仪(温度计未校正,北京华乐达科技有限公司);MIR-253超低温冰箱(日本SANYO公司);YXQG01高压蒸汽灭菌锅(山东新华医疗器械厂);450型酶标定量测试仪(美国Bio-Rad公司);BS-124S精密电子天平(德国赛多利斯公司)。柱色谱用硅胶(300~400目)和薄层色谱用硅胶(10~40 μm)均为青岛海洋化工有限公司生产;Sephadex LH-20为Pharmacia公司出品;胎牛血清(浙江天杭生物科技有限公司);MTT(美国Sigma公司)。所用试剂均为分析纯。
积雪草总皂苷(批号20120913),购于陕西惠科植物开发有限公司,含总皂苷大于50%,含积雪草苷大于10%。
2 化合物的分离应用文献报道的方法[8],对积雪草总皂苷200 g进行水解反应。用醋酸乙酯萃取,得萃取物83 g。硅胶柱色谱(300~400目)分离;石油醚-丙酮(40:1、20:1、10:1、6:1、4:1、2:1、1:1、0:1)梯度洗脱,合并流分后得到A~J部分[A(1.2 g),B(2.3 g),C(4.6 g),D(5.5 g,fractions 21~35),E(3.0 g),F(7.5 g),G(6.7 g),H(8.5 g),I(9.2 g),J(8.2 g)],再经硅胶柱色谱分离、反复重结晶,得到4个化合物。其中从H部分得到化合物1(14 mg)和2(80 mg);G部分得到化合物3(130 mg)和4(230 mg)。
3 体外抗肿瘤活性测试应用MTT法,对分离得到的化合物1进行了人白血病细胞株HL-60、人肺癌细胞株A549、人脑胶质瘤细胞株U87增殖抑制活性的研究[9]。实验以依托泊苷为阳性对照,采用SPSS(16.0)统计软件进行检验分析,用IC50值来评估样品抗肿瘤活性[10]。
4 结构鉴定化合物1:无色鳞片状结晶(甲醇),[α]D25+24.4。(c 0.34, 甲醇)。HR-ESI-TOF-MS显示准分子离子峰m/z 509.323 4 [M+Na]+(理论值509.323 7)。结合NMR数据推测分子式为C30H46O5。UV 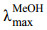
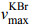
1H-NMR (600 MHz, C5D5N)谱中,可以看到6个甲基质子信号,其中δ 0.90 (3H, d, J=6.6 Hz)和0.97 (3H, d, J=6.8 Hz)为乌苏烷典型的29,30位甲基氢信号,此外还有4个甲基单峰δ 1.06 (3H, s), 1.11 (3H, s), 1.16 (3H, s), 1.26 (3H, s)。氢谱中还显示4组连氧碳上的氢信号δ 3.80 (1H, d, J=10.2 Hz);4.18 (1H, d, J=10.2 Hz);4.24 (1H, brd, J=12.6 Hz);4.34 (1H, m);3个连在双键上的氢信号δ 5.63 (1H, brs);5.61(1H, dd, J=10.5, 2.4 Hz);6.00 (1H, d, J=10.5 Hz),其中后2个氢呈相互偶合关系。该化合物13C-NMR (150 MHz, C5D5N)谱显示了30个碳原子信号。羰基碳信号δ 179.5以及2个烯碳信号δ 126.4,139.7,提示该化合物可能为乌苏酸型苷元衍生物。3个连氧碳信号δ 65.8,68.6,77.92为积雪草中常见的2α, 3β, 23-三羟基乌苏酸的特征碳信号。通过与化合物3(6β-羟基积雪草酸)的核磁共振碳谱数据对比[11],发现除了C-5, 6, 7, 8的化学位移值有很大变化外,其余的碳谱数据十分接近。在核磁共振碳谱中,除了12和13位双键碳外,尚余1组化学位移为δ 133.8,126.7的sp2杂化碳信号,结合HSQC和氢谱,可知它们为“-CH=CH-”片段,因此,这个双键可能位于B环的C-6与C-7间。HMBC谱(图 1,表 1)
|
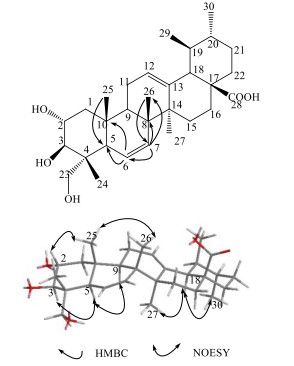
图 1 化合物1的主要的HMBC及NOESY相关 Fig.1 Key HMBC and NOESY correlations of compound 1 |
|
|
表 1 化合物1的1H-NMR和13C-NMR数据 Table 1 1H-NMR and 13C-NMR spectral data of compound 1 |
显示下列远程相关,证实了C-6、C-7之间双键的存在:H-5 (δ 2.70)与C-6 (δ 133.8)、C-7 (δ 126.7)、C-10 (δ 36.9);H-6(δ 5.61)与C-5 (δ 47.0)、C-7 (δ 126.7)、C-10(δ 36.9);H-7 (δ 6.00)与C-6 (δ 133.8)、C-8(δ 44.0)、C-9 (δ 47.5)、C-26 (δ 17.7);H-9(δ 2.18)与C-7 (δ 126.7)。NOESY(图 1)显示H-5与H-3、H-9均相关,说明H-5和H-9均在α位;H3-25与H-2、H3-26均相关,说明H-2在β位。根据以上数据综合解析,化合物1的结构鉴定为2α, 3β, 23-三羟基乌苏-6, 12-二烯-28-酸,为新化合物,命名为积雪草-6-烯。其NMR数据归属见表 1。
另外,通过化合物2~4的13C-NMR数据(表 2)与文献报道对照[12-14],鉴定化合物2为积雪草酸,化合物3为6β-羟基积雪草酸,化合物4为terminolic acid。
|
|
表 2 化合物2~4的13C-NMR (150 MHz, C5D5N)数据 Table 2 13C-NMR (150 MHz, C5D5N) spectral data of compounds 2—4 |
5 生物活性研究
采用MTT法,对化合物1进行了HL-60、A549、U873细胞株的增殖抑制活性测试,以依托泊苷为阳性对照。结果表明化合物1对3种肿瘤细胞株的IC50均大于100 μmol/L,显示无细胞毒活性。
| [1] | 中国药典[S].一部. 2015. |
| [2] | 代百东, 张翠, 王佳, 等. 积雪草的研究现状[J]. 上海医药 , 2008, 29 (2) :88–91. |
| [3] | 齐红梅, 王冬梅. 积雪草化学成分及药理研究进展[J]. 中国药业 , 2010, 19 (16) :89–90. |
| [4] | 戴卫波, 梅全喜, 孔祥廉. 积雪草的化学成分与药理作用研究进展[J]. 时珍国医国药 , 2009, 20 (6) :1566–1568. |
| [5] | 陈军, 华维一, 孙宏斌. 积雪草酸及其衍生物的生物活性研究概况[J]. 中草药 , 2006, 37 (3) :458–460. |
| [6] | 黄云红, 张胜华, 甄瑞贤, 等. 积雪草甙诱导肿瘤细胞凋亡及增强长春新碱的抗肿瘤作用[J]. 癌症 , 2004, 23 (12) :1599–1604. |
| [7] | 孟艳秋, 王楠, 张良锋. 积雪草酸生物活性的研究进展[J]. 化学通报 , 2013, 76 (8) :721–724. |
| [8] | 陈业高, 吕瑜平, 桂世鸿. 三七叶甙制备原人参二醇及其差向异构体[J]. 精细化工 , 2003, 20 (7) :425–426. |
| [9] | Lammer C, Wagerer S, Saffrich R, et al. The cdc25B phosphatase is essential for the G2/M phase transition in human cells[J]. J Cell Sci , 1998, 11 (16) :2445–2453. |
| [10] | 赵斌, 葛金芳, 朱娟娟. 小议在MTT法测细胞增殖抑制率中IC50的计算方法[J]. 安徽医药 , 2007, 11 (9) :834–835. |
| [11] | Sahu N P, Roy S K, Mahato S B. Spectroscopic determination of structures of triterpenoid trisaccharides from Centella asiatica[J]. Phytochemistry , 1989, 28 (10) :2852–2854. DOI:10.1016/S0031-9422(00)98106-8 |
| [12] | 王锦亮, 李兴从, 熊江, 等. 云南揭布罗香树脂的化学成分[J]. 云南植物研究 , 1991, 13 (3) :335–340. |
| [13] | Cheung H T, Wong C S. Structures of triterpenes from Dryobalanops aromatica[J]. Phytochemistry , 1972, 11 (5) :1771–1780. DOI:10.1016/0031-9422(72)85035-0 |
| [14] | 李亚楠, 李志辉, 霍丽妮, 等. 积雪草化学成分的研究[J]. 广西中医药 , 2015, 38 (2) :78–80. |
 2016, Vol. 47
2016, Vol. 47


