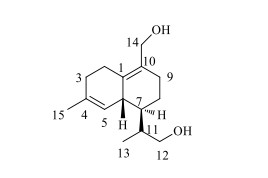
金钗石斛Dendrobium nobile Lindl.又名吊兰花、扁金钗、小黄草,为兰科(Orchidaceae)石斛属Dendrobium Sw.植物,是贵州省道地药材,也是我国传统名贵中药。其主要生长于海拔800~1 700 m的山坡、林中、树上或路边岩石上,分布于我国西南及台湾、湖北、广东、海南、广西等省。金钗石斛以茎入药,味甘,性微寒,益胃生津、滋阴清热,用于阴伤津亏、口干烦渴、食少干呕、病后虚热、目暗不明[1]。研究表明,石斛属植物具有抗肿瘤、增强机体免疫能力、抗氧化、抗血小板凝集及降血糖等作用[2-3]。金钗石斛含有的化学成分复杂多样,主要有生物碱类、芳香类和倍半萜类化合物[4-6]。为了阐明黔产金钗石斛的化学成分,为贵州道地药材的利用奠定坚实的物质基础,本实验进一步对采自遵义赤水的金钗石斛进行了研究,从其乙醇提取物非生物碱部位中分离得到1个新倍半萜类化合物,鉴定为δ-杜松萜烯-12, 14-二醇(图 1)。
|
图 1 化合物1的结构 Fig.1 Structure of compound 1 |
1 仪器与材料
Finnigan LCQDECA型质谱仪(美国Thermo公司);Agilent DD2400-MR型核磁共振仪,TMS为内标(美国Agilent公司);Bruker BiOTOF Q型质谱仪(德国Bruker公司);UV3600紫外可见近红外分光光度计(日本岛津公司);Varian1000红外光谱仪,KBr压片(美国Varian公司);Sepacore中压制备系统(瑞士B CHI公司);LC3000型高效液相色谱仪(中国北京创新通恒公司);C18半制备HPLC柱(250 mm×10 mm,5 μm,日本YMC公司);20~45 μm ODS填料(日本Fuji Silysia公司);薄层色谱硅胶GF254和柱色谱硅胶(100~200,300~400目,青岛海洋化工公司);MCI树脂(日本Mitsubishi公司)。
金钗石斛茎于2014年9月采自遵义赤水,由遵义医学院生药学教研室杨建文教授鉴定为金钗石斛Dendrobium nobile Lindl.,样品标本(20141011)保存在遵义医学院天然药物实验室。
2 提取与分离金钗石斛干燥品50 kg粉碎后用乙醇回流提取3次,减压浓缩提取液得乙醇提物4.8 kg,将其分散于2.0%盐酸水溶液中,减压滤过得酸水不溶物。该酸水不溶物用乙醇溶解后拌入100~200目硅胶,挥干溶剂后先用石油醚(3 L)提取,脱脂后以石油醚-醋酸乙酯(1:1,3 L)和醋酸乙酯(3 L)分别提取3次,减压浓缩得石油醚-醋酸乙酯(1:1)部位浸膏350 g。该浸膏经中压硅胶柱色谱(70 mm×460 mm,石油醚-醋酸乙酯梯度洗脱)分为10个部分Fr. 1~10。Fr. 3经MCI柱(90%甲醇-水洗脱)除去色素后经ODS柱色谱(甲醇-水梯度洗脱)分为7个部分Fr. 3.1~3.7;Fr. 3.2经半制备HPLC分离(乙腈-水,55:45,体积流量4 mL/min)得到化合物1(tR=16.5 min,15 mg)。
3 结构鉴定化合物1为浅黄色胶状物,[α]D20+12 (c 0.18, MeOH)。HR-ESI-MS给出其准分子离子峰[M+Na]+峰m/z: 259.166 0(C15H24O2Na+,计算值259.166 9),确定其分子式为C15H24O2,不饱和度为4。紫外光谱显示在245 nm处有最大吸收。红外光谱显示3 422 cm−1处有羟基伸缩振动。1H-NMR (400 MHz, CDCl3)谱(表 1)显示有1个烯氢δH 5.41 (1H, brs),4个连氧的仲氢[δH 3.56 (2H, m);δH 4.03, 4.24 (各1H, d, J=11.4 Hz)],2个甲基氢信号[δH 1.66 (3H, s);δH 0.83 (3H, dd, J=6.9, 1.3 Hz)]。13C-NMR (100 MHz, CDCl3)谱中显示有15个碳信号分别为4个sp2杂化碳δC 135.5, 134.6, 123.5, 128.3;2个连氧的仲碳δC 67.0, 62.4;3个叔碳δC 39.8, 39.1, 35.2;4个仲碳δC 32.6, 28.1, 26.2, 21.7;2个甲基碳δC 23.4, 10.6。分析波谱数据推测其可能为萘环型倍半萜骨架[7]。进一步通过HMBC谱推测其可能为杜松烷型倍半萜骨架,分析化合物1的NMR数据发现其和化合物agripilol C及tyromol B相似[8-9],相比而言多了一个双键。HMBC谱中(表 1)H-14 (δH4.03, 4.24)和C-1 (δC128.3), C-10 (δC 135.5), C-9 (δC 28.1)相关,可以得出1个双键处于C-1和C-10上,1个羟基处于C-14上;H-15 (δH1.66)和C-3 (δC32.6), C-4 (δC 134.6), C-5 (δC 123.5)相关,H-5 (δH5.41)和C-3 (δC32.6), C-4 (δC 134.6), C-6 (δC 39.1), C-15(δC 23.4)相关,可以推断另外1个双键处于C-4和C-5上;H-12 (δH3.56)和C-7 (δC35.2), C-11 (δC 39.8), C-13 (δC10.6)相关,可以判定另外1个羟基处于C-12上。最后,通过H-6的邻位偶合常数J=8.4 Hz推测H-6和H-7处于反式α键上,进一步通过和(+)-δ-杜松萜烯对比旋光度得出化合物构型。综上,化合物1的结构得到确定,命名为(+)-δ-杜松萜烯-12, 14-二醇。
|
|
表 1 化合物1的1H-NMR、13C-NMR和HMBC数据 Table 1 1H-NMR, 13C-NMR, and HMBC data of compound 1 |
4 讨论
倍半萜类是天然产物中一类重要的化合物,其骨架在萜类化合物中最为多变,活性也很广泛。杜松烷型倍半萜属于萘环倍半萜类,在药用植物中分布并不普遍,其活性也有待深入研究。本实验从贵州道地药材金钗石斛茎中分离得到1个新的杜松烷型倍半萜类化合物,为金钗石斛用药提供了科学依据,也进一步丰富了其物质基础研究。
| [1] | 张惠源, 张志英. 中国中药资源志要[M]. 北京: 科学出版社, 1994 . |
| [2] | Xu J, Han Q B, Li S L, et al. Chemistry, bioactivity and quality control of Dendrobium, a commonly used tonic herb in traditional Chinese medicine[J]. Phytochem Rev , 2013, 12 (2) :341–367. DOI:10.1007/s11101-013-9310-8 |
| [3] | 宋广青, 刘新民, 王琼, 等. 石斛药理作用研究进展[J]. 中草药 , 2014, 45 (17) :2576–2580. |
| [4] | Yang H, Sung S H, Kim Y C. Antifibrotic phenanthrenes of Dendrobium nobile stems[J]. J Nat Prod , 2007, 70 (12) :1925–1929. DOI:10.1021/np070423f |
| [5] | Zhang X, Xu J K, Wang J, et al. Bioactive bibenzyl derivatives and fluorenones from Dendrobium nobile[J]. J Nat Prod , 2007, 70 (1) :24–28. DOI:10.1021/np060449r |
| [6] | Zhang X, Liu H W, Gao H, et al. Nine new sesquiterpenes from Dendrobium nobile[J]. Helv Chim Acta , 2007, 90 (90) :2386–2394. |
| [7] | 龚运淮, 丁立生. 天然产物核磁共振碳谱分析[M]. 昆明: 云南科技出版社, 2006 . |
| [8] | 郭华, 冯涛, 李正辉, 等. 担子菌薄皮干酪菌中两个新的倍半萜(英文)[J]. 药学学报 , 2014, 49 (11) :1578–1581. |
| [9] | Shan W G, Chen X X, Ying Y M, et al. Sesquiterpenoids from Fusarium sp., an Endophytic fungus in Agriminia pilosa[J]. ., an Endophytic fungus in Agriminia pilosa , 2011, 94 (7) :1254–1259. |
 2016, Vol. 47
2016, Vol. 47

