银杏Ginkgo biloba L. 是冰川时期存活在地球上的孑遗植物,素有“活化石”之称。中国是银杏的发源地,其资源占世界总量的70%左右。宋健在1997年召开的 ' 97银杏国际研讨会上对银杏资源开发利用前景做了精辟的论述:“银杏是神奇大自然赐予人类的宝贵财富,这一珍贵的物种在经历一亿五千万年的沧桑轮回之后,在现代科学技术的作用下,正焕发出蓄积已久的光彩,服务于人类的健康和文明”。本文从银杏叶的活性成分、药理作用、毒性与临床应用、各国药典质量标准的比较、药用发展史和我国银杏叶研究开发的现状进行详尽地阐述、分析与讨论。
1 银杏叶的主要活性成分目前从银杏叶中已发现有160多种化合物[1-4],研究证实其主要有效成分为银杏黄酮类和银杏萜内酯类,以及银杏酸类化合物。
1.1 黄酮类(flavonoides)从银杏叶中共分离得到58个黄酮类化合物,分为黄酮及黄酮醇类(flavones and flavonols)43个,其中包括桂皮酰黄酮醇苷(cinnamoyl flavonol glycosides)8个,二氢黄酮(flavanones)2个,双黄酮(double flavonoids)9个及黄烷醇(flavanols)4个。
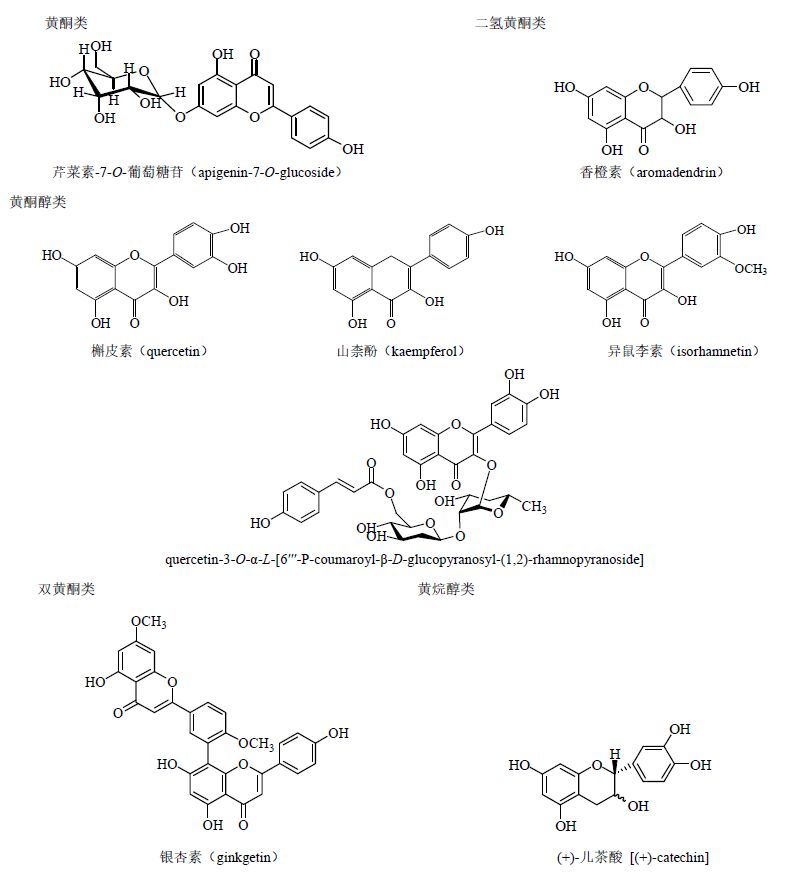
黄酮及黄酮醇类主要是槲皮素(quercetin)、山柰酚(kaempferol)、异鼠李素(isorhamnetin)、杨梅素(myricetin)、丁香亭(syringetin)、木犀草素(luteolin)及以这些黄酮为苷元的单、双、三糖苷。其中大多数是槲皮素、山柰酚及其苷类化合物[5-9]。各类代表化合物见图 1。
|
图 1 银杏叶中主要的黄酮类化合物结构 Fig.1 Structures of main flavonoides in GBL |
1.2 萜类(terpenoids)
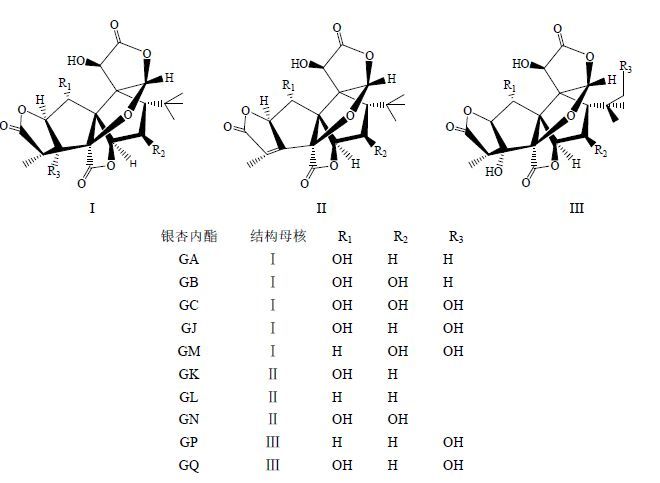
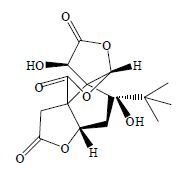
银杏叶中的萜类主要是萜内酯化合物(terpene lactones),有独特结构的二萜内酯(diterpene lactones)及倍半萜内酯衍生物(sesquiterpene lactones),为其特征性成分。萜内酯是少见的含有1个叔丁基和3个γ-内酯环的一类化合物;6个五元环和螺 [4, 4] 壬烷碳骨架化合物银杏内酯(ginkgolide,G)A、B、C、J、M、K、L、N、P、Q(图 2)及倍半萜衍生物白果内酯(bilobalide,BB,图 3)具有神经保护作用,近年来受到科学家高度重视[10-17]。银杏萜内酯化合物是一类罕见的天然化合物,迄今尚未在其他植物中发现。
|
图 2 银杏叶中二萜内酯化合物结构 Fig.2 Structures of diterpenoid lactones in GBL |
|
图 3 白果内酯的结构 Fig.3 Structure of bilobalide |
2001年,采用LC-DAD-ESI/MS联用技术,从银杏叶中鉴定了2个新化合物的结构,分别为1,10-二羟基-3,14-二去氢银杏内酯和10-羟基-3,14-二去氢银杏内酯,并命名为GK和GL[18](图 2)。2009年,从银杏叶分离得到1个新的银杏内酯化合物1,7,10-三羟基-3,14-去氢银杏内酯,命名为银杏内酯N(GN,图 2)[19];2011年,又分离得到2个新化合物银杏内酯P和Q(GP和GQ,图 2)[20]。GK、GL、G N、GP和GQ均是中国的科学家近年来发现的。
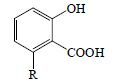
1.3 银杏酸类(ginkgolic acids)银杏酸系水杨酸衍生物,其中C-6位侧链R为直链饱和或不饱和单烯的C15或C17或C13化合物,以C15化合物为主,银杏酸为主要化合物,占总银杏酸近50%,均属于烷基酚酸类化合物(alkyl phenolic acid compounds)[21-24],结构见表 1。
|
|
表 1 银杏中银杏酸类成分 Table 1 Ginkgo acids in GBL |
由于抗菌、抗癌等活性和对皮肤的刺激性、强过敏性及引起接触性皮炎等,使得这些化合物引起国内外学者关注。
1.4 有机酸类(organic acids)银杏叶中含有3-甲氧基-4-羟基苯甲酸(3-methoxy- 4-hydroxybenzoic acid)、4-羟基苯甲酸(4-hydroxy benzoic acid)、3,4-二羟基苯甲酸(3,4-dihydroxy benzoic acid)、抗坏血酸(ascorbic acid)、硬脂酸(stearic acid)、亚油酸(linoleic acid)、棕榈酸(palmitic acid)、莽草酸(shikimic acid)、犬尿喹啉酸(kynurenic acid)和6-羟基犬尿喹啉酸(6-hydroxy kynurenic acid,6-HKA)10种有机酸。由于6-HKA 能作为广谱中枢神经氨基酸拮抗剂,因而颇受关注。6-HKA直接作用于N-甲基-D-天冬氨酸(NM-DA),能改善脑缺氧。
1.5 酚酸类(phenolic acids)银杏叶中酚酸有7种,原儿茶酸(protocatechuic acid)、p-羟基苯酸(p-hydroxybenzoic acid)、香草酸(vanillic acid)、咖啡酸(caffeic acid)、p-香豆酸(p-coumaric acid)、阿魏酸(ferulic acid)和绿原酸(chlorogenic acid)。不同的酚酸药理作用也不同。
1.6 聚戊烯醇类(polypentene alcohols)聚戊烯醇是存在于银杏叶中的一种类脂化合物,量较高,属多烯醇类,具有很强的生物活性,是重要的新药资源。其80%属于桦木聚戊烯醇型,异戊烯基单元数为15~21,因而银杏叶中所含有的聚戊烯醇类成分作为哺乳动物多萜醇的结构类似物而引起注目。
2 药理作用、毒性研究与临床应用 2.1 药理作用[25-27]药理研究表明,银杏叶具有抗氧化、清除体内自由基、抗血小板激活因子(platelet activating factor,PAF)、降低血液黏度、改善微循环、改善记忆力、增加脑血流量、保护脑微血管平滑肌细胞、减轻脑损伤、对胃黏膜的保护作用、提高神经可塑性、改善神经退行性疾病、抗辐射作用等多种药理作用。
银杏叶提取物(EGb761)对整个血管树(动脉、毛细血管、静脉)具有调节作用。可刺激内皮衍生血管舒张因子(vascular endothelium-derived relaxing factor,EDRF)的分泌,EGb761可消除动脉痉挛,对小动脉血管有扩张作用;相反,对静脉血管有收缩作用。它能调节因体位改变而引起的静脉容量变化,降低毛细血管的高渗透性并增强毛细血管的耐受力。EGb761在脑水平和外周均有强力抗水肿作用,保护血-脑和血-视网膜屏障。而且对许多由病理现象所引起的血清蛋白水解作用的升高具有较强的抑制作用。EGb761可改善血小板和红细胞高凝状态的流变学以及微循环凝血过程的流变学。其特性基于对膜的稳定作用,干扰前列腺素代谢,抑制某些活性物质(组织胺、缓激肽等)以及对血小板激活因子的抑制作用。EGb761对细胞代谢,特别是脑神经和神经感觉细胞代谢具有保护作用。在动物实验中,这种保护作用可体现在提高细胞存活率,增加皮层细胞的ATP水平,以及改善葡萄糖和氧的摄取。EGb761参与神经递质的释放、再摄取和分解代谢(去甲肾上腺素、多巴胺、乙酰胆碱等)或干扰这些物质与膜受体的结合能力。EGb761对细胞膜自由基和脂质过氧化物的产生具有较强的拮抗作用,这与其某些药理作用是相关的。
2.2 金纳多(银杏叶提取物注射液)毒性研究 2.2.1 急性毒性小鼠ig给药的LD50为7.725 g/kg,ip给药的LD50为1.900 g/kg,iv给药的LD50为1.100 g/kg;大鼠ig给药的LD50>10.000 g/kg,ip给药的LD50为2.100 g/kg,iv给药的LD50为1.100 g/kg。
2.2.2 亚急性和慢性毒性在亚急性毒性研究中,每天给予大鼠剂量为15~100 mg/kg,ig给药12周;每天iv给予犬剂量为7.5~30 mg/kg或im剂量5 mg/kg,给药8周。在慢性毒性实验中,每天给予大鼠和犬20~100 mg/kg,逐渐增加剂量,给予大鼠300、400和500 mg/kg,给予犬300和400 mg/kg,ig给药6个月。组织学、生化和血液学研究结果都显示金纳多毒性很低。
2.2.3 生殖毒性每天ig给予大鼠剂量100、400和1 600 mg/kg,ig给予兔剂量100、300和900 mg/kg,研究结果证明金纳多无生殖毒性。
2.2.4 致突变致癌研究结果显示金纳多无致突变或致癌作用。
2.3 临床应用[28-30]近年来,银杏叶的中药制剂对冠心病、心绞痛、大脑退行性病变及心血管疾病引起的脑功能障碍、老年痴呆症等疗效确切,引起医药界的广泛关注。银杏叶提取物可提升大脑血流量并对神经系统有较好的滋补作用。临床研究证实,银杏叶提取物对包括大脑血流不足和老年患者的智力衰退在内的诸多问题有功效。银杏对许多与衰老有关症状都有很好的效果,如焦虑和忧郁、记忆损伤、难以集中注意力、机敏度下降、智力下降、眩晕、头痛耳鸣(耳中鸣响)、视网膜黄斑部退化(成人失明的最普遍原因)、内耳骚动(会导致部分失聪)、末端循环不良、阴茎血流不良导致的阳痿。
银杏叶提取物可以同时减轻血胆固醇、三酰甘油、极低密度脂蛋白对人体的不利影响,减少血脂,改善微循环,抑制凝血,这些对高血压的治疗效果显著。
目前医学上已经有使用银杏叶提取物代替胰岛素供糖尿病人使用的药物,说明银杏叶具备胰岛素的调节血糖的功能,很多的葡萄糖耐量试验均证明银杏叶提取物对调节血糖、改善胰岛素抵抗、增强胰岛素的敏感性效果明显。
银杏叶提取物还可明显地减轻月经前不快的症状,特别是乳房疼痛和情绪不稳定。
2.3.1 国外主要银杏叶制剂适应症(1)德国Schwabe公司的金纳多注射液:注射液每支含有银杏叶提取物17.5 mg,其中银杏黄酮苷4.2 mg;片剂每片含有银杏叶提取物40 mg,其中银杏黄酮苷9.6 mg,萜类内酯2.4 mg。其适应症主要用于脑部、周围血流循环障碍:①急慢性脑功能不全及其后遗症:脑卒中、注意力不集中、记忆力衰退、痴呆;②耳部血流及神经障碍:耳鸣、眩晕、听力减退、耳迷路综合征;③眼部血流及神经障碍:糖尿病引起的视网膜病变及神经障碍、老年黄斑变性、视力模糊、慢性青光眼;④周围循环障碍:各种周围动脉闭塞症、间歇性跛行症、手脚麻痹冰冷、四肢酸痛。
(2)法国Beaufour-Ipsen公司的达纳康:口服,每日3次,每次l片(40 mg)。适应症:①老年人慢性神经感觉和认知的病理性缺陷的症状治疗(不包括阿尔茨海默病和其他痴呆)。②下肢慢性阻塞性动脉病的间歇性跛行(2期)的症状治疗,该适应症基于双盲、安慰剂对照试验的临床研究。研究结果表明,50%~60%接受治疗的患者行走距离至少增加50%,而在只遵循保健和饮食疗法的患者中,20%~40%行走距离增加50%以上。③改善雷诺氏现象。血管性原因所致视力下降和视野损害的辅助性治疗和血管性原因所致听力下降和眩晕综合征和/ 或耳鸣的辅助性治疗。
2.3.2 国产银杏叶制剂适应症(1)银杏叶片:每片含银杏叶提取物80 mg(含总黄酮醇苷19.2 mg,萜类内酯4.8 mg)。适应症:脑卒中、稳定性心绞痛、脑梗死、胸痹心痛、冠心病、心绞痛、中风、胸痹。功能主治:活血化瘀通络,用于瘀血阻络引起的胸痹、心痛、中风、半身不遂、舌强语蹇;冠心病稳定型心绞痛、脑梗死见上述证候者。
(2)舒血宁注射液:每支2 mL,折合银杏叶提取物为7.0 mg(含总黄酮醇苷1.68 mg,银杏叶内酯0.28 mg)。适应症:扩张血管、改善微循环,用于缺血性心脑血管疾病、冠心病、心绞痛、脑栓塞、脑血管痉挛等。功能主治同上述国产银杏叶片。
3 质量标准《中国药典》与欧美药典对银杏叶提取物主要检测指标的比较见表 2。
|
|
表 2 银杏叶提取物各药典质量标准主要检测指标的比较 (HPLC法) Table 2 Comparison on main indexes of quality standard of GBL extract in each Pharmacopoeia (HPLCmethod) |
总黄酮醇苷量=(槲皮素量+山柰素量+异鼠李素量)×2.51,此值于1993年首先由Sticher[35]提出以槲皮素、山柰素、异鼠李素的转化因子来计算总黄酮醇苷的量,上述转化因子是根据银杏叶黄酮苷中认为活性最强的桂皮酰黄酮苷的平均相对分子质量(760)与苷元的相对分子质量换算而来;随后《欧洲药典》《美国药典》和《中国药典》已普遍采用以转化因子(槲皮素2.504、山柰素2.588、异鼠李素2.437)或平均转化因子(2.51)来计算总黄酮醇苷的量,这些转化因子是以黄酮醇苷的平均相对分子质量(756.7)换算而来。
自2015年5月以来,因企业擅自改变银杏叶提取物生产工艺而引发行业“银杏叶事件”[31],国家食品药品监管总局(CFDA)开展银杏叶及其制剂的专项治理行动,为了应对现行银杏叶提取物标准不能检测出由稀醇提取改为3%盐酸提取的“工艺过程改变”和目前市场上出现银杏叶提取物靠添加部分芦丁(槲皮素-3-O-芸香糖,银杏叶黄酮主成分)、槲皮素等黄酮化合物提取物,甚至完全以芦丁勾兑,以达到24%总黄酮醇苷标准的行为。添加物质主要来源于豆科植物槐Sophora japonica L. 的干燥花蕾及成熟果实,前者称槐米,后者称槐角的提取物,或者从槐米提取分离纯化的芦丁、槲皮素。为此CFDA对银杏叶提取物及其制品于2015年6月4日与8月10日分别发布了2个补充检查方法第66号公告(增加了游离槲皮素、山柰素、异鼠李素检查)和第142号公告(增加了槐角苷检查)来监管行业中广泛存在的工艺改变和非法添加违规问题。
通过比较银杏叶提取物在各国药典现行质量标准的主要指标,说明《中国药典》与欧美药典存在明显差距,一是表现在两类活性成分定量测定方面,总黄酮醇苷欧美药典由±10%上下限来控制质量,我国药典只设下限;萜类内酯欧美药典由上下限来控制质量,规定了BB单一成分的量占总萜类内酯不少于48%,GA+GB+GC为2.8%~3.4%,而我国药典仅规定总萜类内酯的量,且只设下限。二是表现在总银杏酸《中国药典》高于欧美药典的限量1倍,银杏酸具有潜在的致敏和致突变作用和强烈的细胞毒性,可引起严重的过敏反应、基因突变、神经损伤,导致恶心和胃灼热、过敏性休克、过敏性紫癜、剥脱性皮炎、消化道黏膜过敏、痉挛和神经麻痹等不良反应,被广泛认为是银杏叶提取物及其制剂中的毒性物质,WHO及多国药典要求银杏提取物中总银杏酸的量不得大于5 mg/kg,现行《中国药典》要求银杏叶提取物中银杏酸限度小于10 mg/kg,显然已经落后于国际标准。三是表现在《美国药典》采用 芦丁≤4%与槲皮素≤0.5%限量测定来检测工艺改变和非法添加物,而我国药典未作检查规定。欧美药典质量标准检测的主要指标制定严谨、缜密、控制严格,所以在干燥银杏叶提取物原料制法上只要能达到质量标准要求,可采用适合溶剂提取和分离方法,不作严格具体规定,而《中国药典》从提取溶剂、分离和干燥方法都要给予某些规定。
4 银杏叶的药用发展史 4.1 医药价值始于中国宋代从《神农本草经》开始就有银杏的记载,但是银杏(白果)、银杏叶的医药价值始于宋代(960—1279年),后元代《日用本草》、明代《本草品汇精要》《本草纲目》及清代《本草逢源》等多种本草药籍均有记述。
4.2 黄酮类化合物的分离和抗核辐射的神秘力量1929年,日本人首先从银杏叶中分离到一些黄酮类化合物。
1945年,世界科学界因广岛、长崎原子弹爆炸事件,银杏树是遭受原子弹袭击后当时仅存活的植物,自此发现了银杏树具有神秘力量(是目前所知唯一可以抵抗核辐射的植物)。
4.3 银杏内酯的发现1967年,日本人Nakanishi[10]首先从银杏根皮中分离到银杏内酯;Okabe等[16]从银杏叶中分离得到银杏内酯A、B、C、M。20世纪60年代后,相关实验已证明银杏叶具有重要的药用价值中西香尔(Koji Nakanishi)教授(图 4)被誉为银杏内酯结构发现的第一人。他于日本名古屋大学(Nagoya University)化学系博士毕业,曾在美国哈佛大学(Harvard University)做博士后研究,现为美国哥伦比亚大学(Columbia University)化学系终身教授。中西香尔教授带领研究小组研究了银杏的起源、生物活性及银杏内酯的作用机制[17]。

|
图 4 中西香尔教授 Fig.4 Professor Koji Nakanishi |
4.4 EGb761开启了现代银杏叶制剂的先河
银杏叶的现代应用研究与开发始于德国,银杏叶制剂“梯波宁(Tebonin)”是由德国最大的植物药企业威玛舒培博士药厂(Dr. Willmar Schwabe Gmbh & CO. KG)于1965年研发出来,首次注册了银杏叶的一种简单提取物,并于1972年申请了专利(W Schwabe DE176708和DE2117429),定名为EGb761,其成分包括黄酮(24%)、萜内酯(6%),被认为是黄金配比,质量标准一直被沿用,还含有7%原花青素类和2%儿茶素类。将其用于治疗和预防阿尔茨海默病(老年性痴呆)、末端血管阻塞等疾病。其提取工艺在欧洲获得永久专利,生产标准已成为国际银杏叶产品的标准。德国威玛舒培博士制药业公司出口的银杏叶制剂专用名称为金纳多,有针剂、口服液、静脉注射用针剂、糖衣片及长效缓释片5种制剂,在60多个国家上市销售,颇受患者欢迎。5种制剂在德国年销售额达600万美元,全球年销售创下10亿美元的记录[36]。据统计,威玛舒培博士药厂银杏提取物制剂2009年全球的年销售额达到20亿美元左 右。
4.5 开发利用得到足够重视1968年,韩国成立银杏研究院对银杏叶的药用成分进行了深入的研究,特别是近几年,韩国注意对银杏叶的综合加工利用和研究。
20世纪70年代以来,银杏叶的开发利用在国外已引起人们的极大兴趣,国内外对银杏叶的开发利用已十分重视。1975年法国Beaufour-Ipsen公司的开发Tanakan(达纳康),年销售金额高达1亿欧元[36]。
4.6 银杏内酯B高专属性PAF受体阻断作用的发现1985年,Pierre发现其中银杏内酯B具有高专属性的PAF(platelet activating factor)受体阻断作用后,这类化合物因此受到当今世界药学家的关注,导致其半合成与合成、类似物合成及这类化合物细胞组织培养的研究非常活跃,世界上许多国家对银杏叶药物药理、化学成分及临床应用进行了广泛地研究。
4.7 科雷教授获诺贝尔奖美国哈佛大学有机化学教授科雷(Elias J Corey,图 5)因合成激素赤霉酸及中国传统中药银杏内酯的成功等,获1990年诺贝尔化学奖[37]。

|
图 5 1990年诺贝尔化学奖获得者科雷教授 Fig.5 Professor Elias J. Corey,1990 Nobel Chemistry Prize winner |
4.8 全球银杏叶提取物市场
2001年,世界卫生组织宣称EGb761是治疗、预防心脑血管等疾病的首选药品。
在美国,这些产品的年销售额可达20亿美元。目前,德法2个制药集团银杏叶制剂销售额已达28亿法郎。除德、法外,瑞士、瑞典、荷兰、比利时、西班牙、韩国等国家也先后大力进行银杏叶加工利用,年销售额已超过20亿美元。
全球各种银杏制剂加上银杏保健食品与含银杏叶提取物的化妆品等充满市场,在心血管疾病发病率较高的美国、西欧及北欧等全世界至少有130多个国家在销售银杏叶提取物制剂。2013年,银杏叶制剂全球销售额高达70亿美元。
目前,德国、法国、美国已成为银杏叶提取物3大销售市场,而在亚洲,以日本、中国和韩国的银杏叶提取物销售情况较好(日本银杏制剂销售额在亚洲居第1位,中国和韩国分居第2、3位),但在金额上仍无法与欧美相比。日本国内已形成银杏树种植、采叶、提取加工到制剂销售的完整产业链,其代表企业为常磐植物产品株式会社。据悉,该公司已形成年销售额达10亿美元的生产规模。
4.9 我国银杏叶提取物市场在我国医院处方药和零售药市场中,银杏叶制剂在心血管疾病和神经内科多种疾病的联合用药中占据重要地位,是载入《2009年国家医保目录》《国家基本药物目录》(2012年版)(银杏叶胶囊、片、滴丸)和《低价药目录》(银杏叶片、胶囊)的药物。
我国银杏叶提取物制剂年销售额从2000年的6亿发展到2007年的22亿,2011年超过50亿,成为心脑血管领域中药领先品种之一。据媒体报道,有行业数据显示,2013年,国内医院脑血管及抗痴呆药物市场已达到225亿元,其中银杏叶制剂市场占据了20%,约45亿元。此外,银杏叶提取物销售市场已达到10亿元市场规模。
CFDA南方医药经济研究所分析,银杏叶提取物制剂样本医院的需求是71亿,据测算,从样本推广到总体市场销售,大概在150个亿左右。150个亿中有70%是针剂,30%是口服制剂。银杏叶提取物及其制剂已成为中药“重磅炸弹”型超级品种。
5 我国银杏叶研究开发现状1969年11月,北京市科委科研立项,进行舒血宁注射液和舒血宁片研究,开启了我国银杏叶产品的研究与开发,银杏叶制剂市场在1997—2000年曾经快速增长,各地大量种植银杏树,开辟种植园,创新药物研究与新剂型开发20世纪末到21世纪初如火如荼,银杏叶制剂的各种剂型均受市场欢迎,片剂、注射剂成为制剂市场的主导剂型。
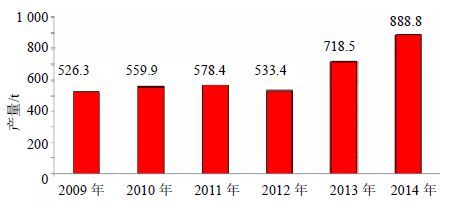
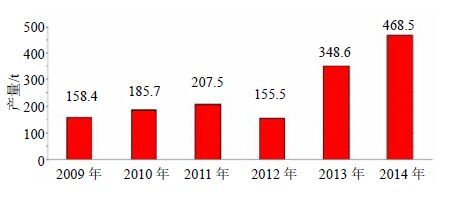
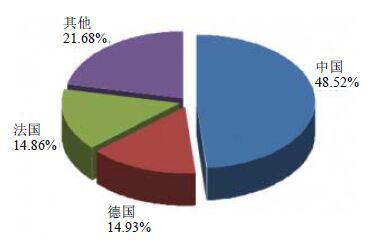
5.1 银杏叶提取物市场发展情况根据智研数据中心的数据显示,近年全球银杏叶提取物产量趋势见图 6,我国银杏叶提取物产量 趋势见图 7、8。
|
图 6 2009—2014年全球银杏叶提取物产量走势 Fig.6 Chart of global GBL extract yield in 2009—2014 |
|
图 7 2009—2014年中国银杏叶提取物产量统计 Fig.7 Chart of China GBL extract yield in 2009—2014 |
|
图 8 2014年全球银杏叶提取物产量统计 Fig.8 Chart of global GBL extract yield in 2014 |
中国是全球第一大银杏叶提取物生产国,行业产能占全球总产能的50%以上,2013年中国银杏叶提取物产量达到348.6 t,占全球同期总产量的48.5%。
5.2 银杏叶口服制剂根据CFDA官网数据显示,银杏叶口服制剂国产药品剂型包括片剂、分散片、软胶囊、胶囊、颗粒剂、口服液、丸剂、滴剂、酊剂、露,其中片剂批准文号最多80件。片剂、分散片、软胶囊、胶囊、颗粒、丸剂的规格是含总黄酮醇苷19.2 mg、萜类内酯4.8 mg或含总黄酮醇苷9.6 mg,萜类内酯2.4 mg。银杏叶口服制剂国产药品信息见表 3~5。国家共批准11个银杏叶口服制剂,浙江康恩贝制药股份有限公司通过与中国科学院上海药物研究所5年的合作开发,1993年天保宁牌银杏叶片成为国内第1个上市银杏叶制剂。
|
|
表 3 银杏叶口服制剂国产药品信息 Table 3 Domestic information on GBL oral preparation |
|
|
表 4 银杏酮酯国产药品信息 Table 4 Domestic information on Yinxing Tongzhi |
|
|
表 5 复方银杏叶口服制剂国产药品信息 Table 5 Domestic information on compound GBL oral preparations |
银杏酮酯(原料药)系国家二类新药,优质规范的提取物成为银杏叶提取物的引领者。其主要用于血瘀型胸痹(冠心病心绞痛)及血瘀型轻度脑动脉硬化引起的眩晕。近几年,银杏酮酯发展速度很快,据不完全统计,按照药品零售价格计算,银杏酮酯的市场份额大概15亿左右。表 4中的7家企业成立了一个“中国银杏酮酯产业战略合作组织”,分享银杏酮酯在药效、药理、临床等科研成果,一起推动这个领域的发展,把银杏叶制剂带入酮酯时代,更多地是为中国银杏叶药品领域创造一个示范,为中国消费者提供一个更加优质的健康的银杏叶制剂。
5.3 银杏叶注射剂银杏叶注射剂国产药品信息见表 6。舒血宁注射液最早源于1969年11月北京市科委项目双鹤高科研制的“6911”注射液,于1970年经北京市卫生局批准在国内上市;1998年经过二次开发,提出了国家部颁标准,成为当时卫生部批准的首家上市厂家。据中国医疗保险研究会发布的《2009—2011年全国城镇基本医疗保险参保住院患者中药利用情况分析》显示,舒血宁注射液在内科用药排位第1位,使用费用24.93亿元。
|
|
表 6 银杏叶注射剂国产药品信息 Table 6 Domestic information on GBL injections |
CFDA批准上市的银杏叶提取物注射液是德国威玛舒培博士药厂金纳多注射液的仿制药,说明书也几乎与金纳多相同,缺乏创新性。
成都百裕科技制药有限公司研发的银杏内酯注射液和江苏康缘药业有限公司研发的银杏二萜内酯葡胺注射液,分别于2011年和2012年CFDA批准上市,是银杏叶创新中药新药高水平的体现,也是现代中药注射剂典范。通过康缘药业银杏二萜内酯和舒血宁的对照试验,无论从脑梗、腔梗有效率,副反应和其他指标来看,都胜于舒血宁,因此银杏内酯注射液的市场规模应该远比金纳多和舒血宁要大,将会成为中药注射剂大品种。
5.4 银杏叶原料药银杏叶原料药国产药品信息见表 7。银杏酮酯原料药与银杏叶提取物质量标准相比,含总黄酮醇苷不得少于24%,萜类内酯不得少于6%,两者相同,而总银杏酸限量降低了1倍,为百万分之五,此外,前者增加采用分光光度法测定总黄酮量,以芦丁计不得少于44.0%。因此在质量标准上有了明显提高。
|
|
表 7 银杏叶原料药国产药品信息 Table 7 Domestic information on raw materials for GBL |
5.5 银杏叶创新药物和缓释制剂研究
银杏叶注射剂和原料药新药注册信息及银杏叶缓释剂和银杏叶提取物注册信息见表 8、9。注射剂的申报主要集中在2002年及以后,考虑到银杏叶中活性成分黄酮醇香豆酸酯和乙酰化的花色素类等黄酮易氧化和水解,所以研发以冻干制剂为主。银杏内酯B及其注射液一类新药开发有望获批。该类新药注册体现了银杏叶产品开发的高水准与创新水平。银杏内酯及银杏内酯B注射剂作为第3代银杏产品取代第2代产品舒血宁将是大趋势。
|
|
表 8 银杏叶注射剂和原料药新药注册信息 Table 8 New drug registration information of GBL Injection and raw materials |
|
|
表 9 银杏叶缓释制剂和银杏叶提取物注册信息 Table 9 Registration information on GBL sustained-release preparation and GBL extract |
银杏叶提取物制剂作为治疗心脑血管疾病的药物,需要长期服用,目前开发的口服制剂,给药间隔时间短,有效血药浓度波动大,而缓释制剂可延长服药时间,减少服药次数,降低药物的不良反应,增加患者顺应性,使人体获得平衡的有效治疗血药浓度,得到稳定的治疗效果。银杏叶缓释制剂的研发是银杏叶提取物剂型的创新。
在CFDA的官网上未查询到国产药品银杏叶提取物信息,这就意味着银杏叶提取物制剂生产企业,只要按《中国药典》颁布的银杏叶提取物质量标准生产即可。
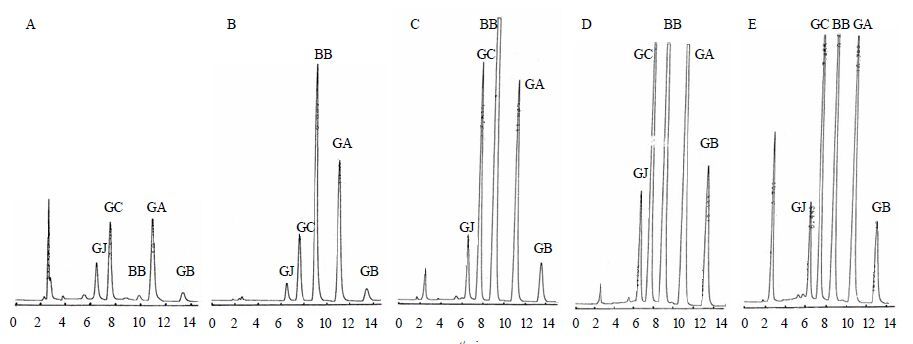
5.6 几种银杏叶提取物制剂银杏萜类内酯的HPLC色谱比较HPLC色谱比较见图 9。由图 9可知,扬子江药业生产的银杏叶片与法国、瑞士品牌产品萜类内酯成分及其各成分相对量一致。但德国生产的金纳多注射液与注射用银杏叶(冻干)产品萜类内酯成分及其各成分相对量不一致,金纳多注射液中具有神经保护作用的BB成分几乎检测不到,所以金纳多注射液萜类内酯不作质量标准控制,我国研制的注射银杏叶(冻干)产品工艺技术已获授权专利保护,均进行银杏内酯A、B、C、J及BB定量测定,并规定BB占总萜内酯35%以上。
|
图 9 金纳多注射液 (A)、注射用银杏叶 (冻干,B)、达纳康片 (法国,C)、扬子江药业银杏叶片 (D)、Gincosan胶囊 (瑞士,E) 的HPLC比较 Fig.9 HPLC of Ginaton Injection (A),GBL Injection (lyophilized,B),Tanakan Tablet (France,C),Yangtze River Pharm GBL Tablet (D),and Gincosan Capsules (Switzerland,E) |
通过上述我国银杏叶研究开发现状的介绍,足以说明我国银杏叶创新药物的研究已取得了长足进展,获得了重大成果,不落后于德国和法国并超越了他们的创新成果,但我国的产业集中度较低。
6 结语 6.1 银杏叶成为创新药物研发的典范银杏叶药用发展史充分体现了其是神奇大自然赐予人类的宝贵财富,锐意创新成为中药/植物药研究开发的典范。银杏叶的医药价值始于我国宋代,在多种本草药籍均有记述。日本、德国的科学家在研究开发方面作出了开创性重要贡献,美欧银杏叶提取物市场占有率最高。我国从20世纪末以来,对银杏叶及其制剂进行大量的创新研究,取得了瞩目成绩,形成了产业优势,已成为中药/植物药“重磅炸弹”型超级品种。
6.2 我国银杏叶相关制剂质量标准与欧美差距显著我国银杏叶提取物及其制剂的质量标准与欧美存在明显差距,《美国药典》2015 USP 38版收载的银杏叶提取物及其胶囊与片剂质量标准较高,是制定游戏规则的,可以通过提高门槛、提高标准来限制其他企业的准入,削弱对手的优势。我国银杏叶提取物及其制剂处于全球产业链的低端,抑制了我国企业议价能力的提升,靠卖资源、卖产品,在残酷的价格竞争中生存,务必彻底改变这种现状。
6.3 我国银杏叶创新药物研发已超越德国和法国我国银杏叶创新药物的研发已超越德国和法国,相信在提高质量标准方面也能有所作为,引领行业,制定出更高、更严的质量标准,塑造和建立我国银杏叶提取物及其制剂的品牌,把产业做强、做大,进入国际主流市场。
2025年中国要成为制造强国。在这个宏伟目标中,中国的医药产业特别是中药产业应该有所作为,银杏叶提取物及其制剂产业更应该成为这个宏伟目标中的杰出代表。
| [1] | 汪素娟, 康安, 狄留庆, 等. 银杏叶提取物主要活性成分药动学研究进展[J]. 中草药 , 2013, 44 (5) :626–631. |
| [2] | 杨义芳, 吴国友. 银杏叶化学成份研究概况[J]. 江西药学 , 1996 (4) :7–14. |
| [3] | 魏学立, 曲摇玮, 梁敬钰. 银杏的研究进展[J]. 海峡药学 , 2013, 25 (3) :1–8. |
| [4] | Nicolaou K C, Montagnon T. Molecules that Changed the World[M]. Weinheim: Wiley-VCH, 2008 . |
| [5] | Hasler A, Sticher O. Identification and dertermination of the flavonoids from Ginkgo biloba by high-performance liquid chromatography[J]. J Chromatogr , 1992, 605 (1) :41–48. |
| [6] | 唐于平, 楼凤昌, 王景华, 等. 银杏叶中黄酮类成分的研究[J]. 中国药学杂志 , 2001, 36 (4) :231–233. |
| [7] | Chamel N, Micheline H B, Annelise L G, et al. Kaempferol coumaroyl glucorhamnoside from Ginkgo biloba[J]. Phytochemistry , 1986, 25 (3) :770–771. |
| [8] | Krauze-Baranowska M, Sowinski P. 2, 3-dihydrobiflavone from Ginkgo biloba[J]. Planta Med , 1999, 65 (5) :482–484. |
| [9] | Sook K H, Sam S K, Kun H S, et al. Biflavone glucosides from Ginkgo biloba yellow leaves[J]. Chem Pharm Bull , 2005, 53 (9) :1200–1201. |
| [10] | Nakanishi K. The ginkgolides[J]. Pure Appl Chem , 1967, 14 (1) :89–113. |
| [11] | Maruyama M, Terahara A, Itagaki Y, et al. The ginkgolides Ⅰ isolation and characterization of the various groups[J]. Tetrahedron Lett , 1967, 8 (4) :299–302. |
| [12] | Maruyama M, Terahara A, Itagaki Y, et al. The ginkgolides Ⅱ. Denivation of partial structures[J]. Ibid , 1967, 8 (4) :303–308. |
| [13] | Maruyama M, Terahara A, Nakadaira Y, et al. The ginkgolides Ⅲ. The structure of ginkgolides[J]. Ibid , 1967, 8 (4) :309–313. |
| [14] | Maruyama M, Terahara A, Itagaki Y, et al. The Ginkgolides IV. Stereochemistry of the ginkgolides[J]. Ibid , 1967, 8 (4) :315–319. |
| [15] | Woods M C, Miura I, Nakadaira Y, et al. The ginkgolides V. Some apects of the their NMR spectra[J]. Ibid , 1967, 8 (4) :321–326. |
| [16] | Okabe K, Yamada K, Yamamura S, et al. Ginkgolides[J]. J Chem Soc C Org , 1967, 7 (7) :2201–2206. |
| [17] | Nakanishi K. Terpene trilactones from Gingko biloba:From ancient times to the 21st century[J]. Bioorg Med Chem , 2005, 13 (17) :4987–5000. |
| [18] | 王颖, 盛龙生, 楼风昌. 银杏内酯提取物中微量成分的LC/DAD/ESI/MS分析及结构鉴定[J]. 药学学报 , 2001, 38 (8) :606–608. |
| [19] | Zhang X T, Li Y, Zhang L H, et al. A new ginkgolide from Ginkgo biloba[J]. J China Pharm Univ , 2009, 40 (4) :306–309. |
| [20] | Liao H J, Zheng Y F, Li H Y, et al. Two new ginkgolides from the leaves of Ginkgo biloba[J]. Planta Med , 2011, 77 (16) :1818–1821. |
| [21] | Verotta L, Peterlongo F. Selective extraction of phenolic components from Ginkgo biloba extracts using supercritical carbon dioxide and off-line capillary gas chromatography/mass spectrometry[J]. Phytochem Anal , 1993, 4 (4) :178–182. |
| [22] | Itokawa H, Totsuka N, Nakahara K, et al. Antitumor principle from Ginkgo biloba L[J]. Chem Pharm Bull , 1987, 35 (7) :3016–3020. |
| [23] | Van Beek T A, Taylor L T. Sample proparation of standardized extracts of Ginkgo biloba by supercritical fluid extraction[J]. Phytochem Anal , 1996, 7 (4) :185–191. |
| [24] | 刘平平, 潘苏华. 银杏叶制剂中银杏酚酸研究进展[J]. 中国中药杂志 , 2012, 37 (3) :274–277. |
| [25] | 杨义芳. 银杏叶药理研究概况(I)[J]. 现代应用药学 , 1995, 12 (5) :12–15. |
| [26] | 杨义芳. 银杏叶药理研究概况(II)[J]. 现代应用药学 , 1995, 12 (6) :5–9. |
| [27] | 王雁, 杨义芳. 银杏叶的药理作用及其机制的研究进展[J]. 中国现代应用药学 , 2001, 18 (1) :1–4. |
| [28] | 王捷, 龙禹, 汪小祝, 等. 银杏叶药理作用、临床应用及制剂研究综述[J]. 中外医疗 , 2011 (5) :116–117. |
| [29] | 王琛, 李昌煜. 银杏叶提取物药理作用研究新进展[J]. 中国现代中药 , 2009, 11 (3) :10–12. |
| [30] | 齐惠珍, 周霞瑾, 王明霞. 银杏叶提取物的药理作用及其临床应用研究进展[J]. 河北中医 , 2013 (12) :1899–1901. |
| [31] | 杨扬, 周斌, 赵文杰. "银杏叶事件"的分析与思考[J]. 中草药 , 2016, 47 (14) :2397–2407. |
| [32] | 中国药典[S]. 一部. 2015. |
| [33] | USP31/38[S]. 2015. |
| [34] | European Pharmacopoeia 8.0[S]. 2014. |
| [35] | Sticher O. Quality of Ginkgo preparation[J]. Planta Med , 1993, 59 (1) :2–11. |
| [36] | 天拓咨询. 浅谈银杏叶制剂市场现状[EB/OL].[2016-07-15]. http://www.askci.com/2013/11/13. |
| [37] | 卓宗一. 科雷改革有机合成方法获1990年诺贝尔化学奖[J]. 化学世界 , 1991 (3) :141–142. |
 2016, Vol. 47
2016, Vol. 47