2. 天津国际生物医药联合研究院中药新药研发中心, 天津 300457 ;
3. 天津中医药大学中药学院, 天津 300193
2. Research and Development Center of Traditional Chinese Medicine, Tianjin International Joint Academy of Biotechnology and Medicine, Tianjin 300457, China ;
3. Department of Traditional Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
稳定性是制剂安全性和有效性的前提和保证。制剂的稳定性受多种因素综合作用的影响。现有化学药物制剂稳定性研究主要遵循人用药品注册技术要求国际协调会(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use,ICH)和FDA稳定性指导原则,包括影响因素试验、加速试验、长期试验及药物制剂临用时配制和使用过程中的稳定性,以及包装材料稳定性与选择及药物制剂处方或生产工艺、包装材料改变后的稳定性研究[1]。现有的中药制剂稳定性研究以制剂中单一质量控制指标成分量的变化规律预测其有效期[2],缺乏对其中多种成分量的监测,也没有降解产物及有关物质的考察,难以全面反映稳定性变化对中药制剂产生的影响[2]。
二至丸水蜜丸制剂是由酒制女贞子wine- processed Ligustri Lucidi Fructus和墨旱莲Eclipta prostrata L. 等份配比而成的中药复方制剂,收载于《中国药典》2015年版。二至丸始载于明•吴旻辑的《扶寿精方》[3],为阴补肾之方药[4],传统用于肝肾阴虚所致的眩晕耳鸣、咽干鼻燥、腰膝酸软、月经量多等症。现代研究表明其具有保肝降酶[5]、增强免疫、抑制肿瘤等药理活性[6-7]。现在二至丸临床上多应用于女性更年期综合征[8]及骨质疏松[9-11]等疾病的治疗,其用药特点决定患者可能需要长期使用药物,在此过程中药品质量极有可能受到环境影响而发生变化。然而,目前尚无对二至丸制剂进行稳定性研究的报道。二至丸中所含成分主要为环烯醚萜苷类及苯乙醇苷类,其化学结构易受攻击发生降解。课题组前期研究发现二至丸中药效活性成分特女贞苷、红景天苷等易在酸性、碱性、高温和强光照射条件下发生降解[12]。明确二至丸制剂中所含化学成分结构,且在此基础上对制剂中绝大多数成分稳定性变化进行系统评价是本研究亟待解决的问题。
本研究采用UPLC-Q-TOF/MS技术,首先对二至丸制剂进行了多成分定性、定量研究。在此基础上,根据ICH制剂稳定性指导原则Q1A(Stability testing of new drug substances and products Q1A)和Q1B(Stability testing:Photostability testing of new drug substances and products Q1B)中关于植物药原料药和制剂稳定性研究指导原则的要求,对二至丸制剂稳定性进行了较为系统的研究。此外,针对传统中药制剂较缺乏关注的影响因素——包装材料和密封条件,本研究也进行了考察,从而对实际使用条件下的二至丸制剂可能发生的稳定性变化趋势进行描绘、寻找潜在降解产物并对影响因素对制剂稳定产生的干扰进行准确的评价;从而以稳定性的角度较为全面、系统地对传统的水蜜丸中药制剂二至丸进行质量控制,为提高中药制剂质量控制水平及保障临床用药安全提供技术支持。
1 仪器与材料Acquity H-class超高效液相色谱配置DAD检测器,美国Waters公司;超高效液相色谱-飞行时间质谱仪配置Acquity Synapttm G2质谱仪,美国Waters公司;Climacell 222L系列标准恒温恒湿箱,德国MMM Group公司;Mill-QⅡ型超纯水器,美国Millipore公司;3K15高速离心机,美国Sigma公司;KQ-250E超声波清洗器,昆山市超声仪器有限公司;BP121S万分之一天平,德国Sartorius公司。乙腈和甲酸,色谱纯,美国Sigma公司;无水乙醇,天津市大茂化学试剂厂;超纯水,美国Millipore公司。
特女贞苷(批号111926-201102)、红景天苷(批号110818-201005)、女贞苷(批号111918-201407)、槲皮素(批号111827-201106)、木犀草素(批号111520-200504)和橄榄苦苷(批号110635- 20120420),质量分数均大于98.0%,均购自天津中新药业集团股份有限公司。二至丸(生产批号JB34001095、JB34001067、JB34001026、JB34001027、JB34001056、JB34001045、JB34001037、JB340010239、JB34001068、JB34001096),均购自上海雷允上药业有限公司。
2 方法与结果 2.1 液相色谱条件Waters Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm)色谱柱与Waters VanGuard BEH C18(5 mm×2.1 mm,1.7 μm)保护柱串联。流动相为0.1%甲酸水溶液-乙腈,梯度洗脱:0~20 min,2%~45%乙腈;体积流量0.2 mL/min;柱温35 ℃;检测波长224 nm。
2.2 质谱条件电喷雾电离源(ESI);正、负离子模式扫描;扫描范围:m/z 100~1 700;离子源温度100 ℃;脱溶剂温度400 ℃;气帘气体积流量50 L/h;脱溶剂气体积流量600 L/h;毛细管电压3.0 kV;锥孔电压40 V;喷雾器电压241.36 kPa(35 psi);碰撞气能量35 eV;碰撞室电压175 V。
2.3 对照品溶液的制备分别精密称取特女贞苷、红景天苷、女贞苷、橄榄苦苷适量于10 mL棕色量瓶中,以50%乙醇溶解分别配制成质量浓度为656.02、665.16、463.04、493.14 μg/mL的对照品溶液。精密吸取适量各对照品溶液配制成质量浓度分别为328.01、332.58、231.52、246.57 μg/mL的混合对照品储备溶液。
2.4 供试品溶液的制备精密称取1.001 0 g二至丸粉末于200 mL具塞锥形瓶中,精密加入50%无水乙醇50 mL,采用补足失重法配制成质量浓度约为50 μg/mL。14 000 r/min离心10 min,取上清液用0.22 μm微孔滤膜滤过,取续滤液,即得二至丸供试品溶液。
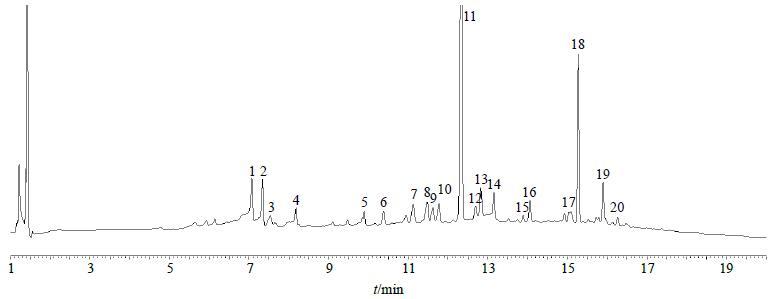
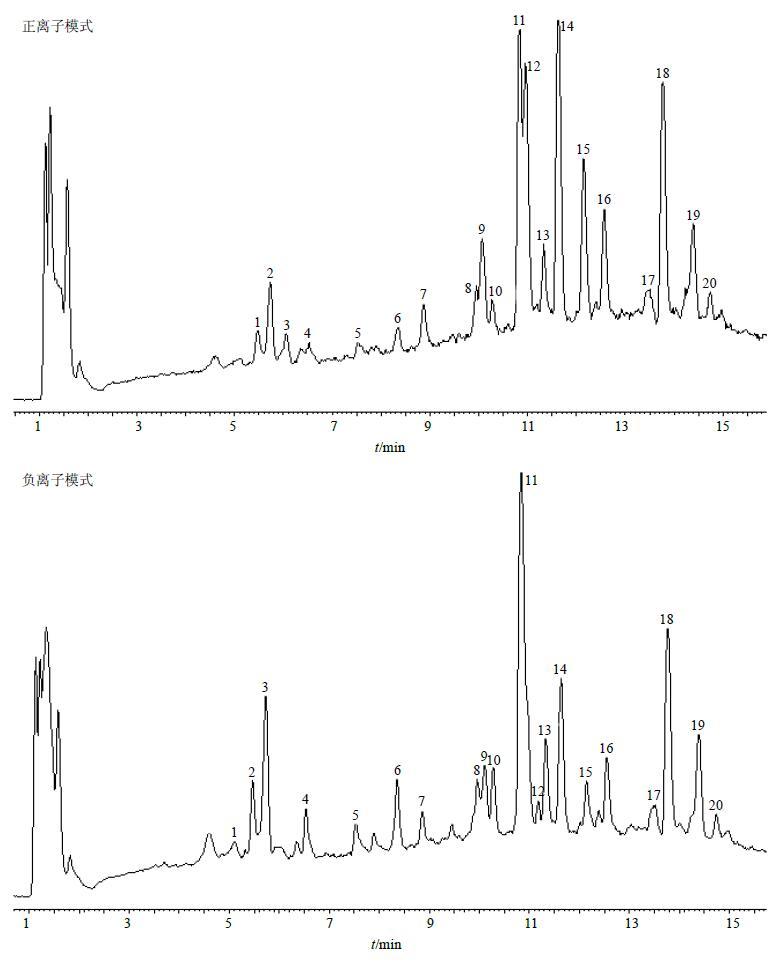
2.5 二至丸水蜜丸制剂UPLC-Q-TOF/MS多成分定性研究通过UPLC-Q-TOF/MS对二至丸水蜜丸制剂中多种化学成分进行分析,在优化色谱条件和电离强度的基础上,同时采用正、负离子模式下对样品进行扫描。结合其紫外响应光谱图(图 1)和质谱响应图(图 2),共鉴定出二至丸制剂中20个化学成分(表 1)。
|
图 1 二至丸样品UPLC-Q-TOF/MS多成分定性鉴别紫外光谱图 Fig.1 UV chromatogram of multiple componentsqualitative research of Er-Zhi-Wan by UPLC-Q-TOF/MS |
|
图 2 二至丸样品UPLC-Q-TOF/MS多成分定性鉴别质谱响应谱图 (一级质谱图) Fig.2 MS of multiple components qualitative research of Er-Zhi-Wan by UPLC-Q-TOF/MS,chromatogram of positive mode of Er-Zhi-Wan (primary MS positive) |
|
|
表 1 二至丸水蜜丸制剂中化学成分的质谱解析 Table 1 MS analysis of chemical components in Er-Zhi-Wan (water honey pills) |
2.6 二至丸水蜜丸制剂定量研究
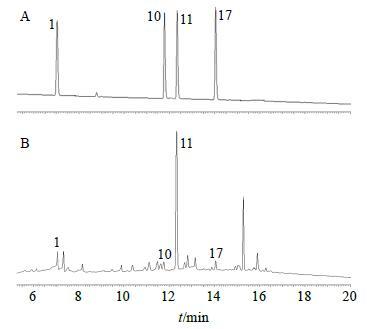
《中国药典》2015年版收载的二至丸定量测定是采用HPLC法检测其中特女贞苷的量。药理研究证明除特女贞苷外,红景天苷、女贞苷和橄榄苦苷等成分具有提高机体免疫力、抗氧化、抗肿瘤、降血糖、抗菌消炎等与临床作用紧密有关的活性[13-15],故本研究增选了红景天苷、女贞苷和橄榄苦苷共同作为定量测定指标成分,采用UPLC色谱仪建立并优化了二至丸多成分同时定量测定方法,并进行方法学研究,分别对该测定方法的线性范围、精密度、重复性、准确度和稳定性进行了考察,对10批次二至丸样品中特女贞苷、红景天苷、女贞苷和橄榄苦苷进行了定量测定(图 3)。
|
图 3 混合对照品 (A) 和二至丸水蜜丸样品 (B) 溶液的UPLC图 Fig.3 UPLC of mixed reference solution (A) and Er-Zhi-Wan (water honey pills) sample (B) |
2.6.1 线性关系考察
精密量取“2.3”项下混合对照品溶液用50%乙醇按倍数逐级稀释,摇匀,制得系列对照品溶液。按“2.1”项下的色谱条件进样测定,以对照品质量浓度(X)对峰面积(Y)进行线性回归,得到4个成分的回归方程、相关系数(r)和线性范围分别为特女贞苷Y=16 920 X+27 649,r=0.999 9,线性范围6.3~328.0 μg/mL;红景天苷Y=19 154 X+120 000,r=0.999 4,线性范围6.4~332.5 μg/mL;女贞苷Y=23 805 X-6 429.2,r=0.999 9,线性范围4.4~231.5 μg/mL;橄榄苦苷Y=17 602 X-26 321,r=0.999 6,线性范围4.3~1-红景天苷 10-女贞苷 11-特女贞苷 17-橄榄苦苷 1-salidroside 10-nuezhenide 11-specnuezhenide 17-oleuropeinin 246.5 μg/mL。
2.6.2 精密度试验取“2.3”项下同一混合对照品溶液,连续进样6次,分析计算特女贞苷、红景天苷、女贞苷、橄榄苦苷平均峰面积的RSD,结果分别为0.1%、0.1%、1.1%、0.1%。
2.6.3 重复性试验取3批二至丸水蜜丸样品(JB34001095、JB34001067、JB34001026),按“2.4”项下方法制备供试品溶液6份,按“2.1”项色谱条件进样测定,分析计算4个成分平均质量分数的RSD,结果分别为1.8%、2.2%、3.4%、3.1%。
2.6.4 稳定性试验取同一份供试品(JB34001067)溶液,室温下放置,分别于0、2、4、8、12、18、24 h进样测定,记录色谱峰面积。计算特女贞苷、红景天苷、女贞苷、橄榄苦苷的峰面积对应的RSD,结果分别为1.2%、0.8%、3.1%、3.2%。
2.6.5 回收率试验精密称取已测定的二至丸样品(JB34001067),平行操作6份,加入特女贞苷、红景天苷、女贞苷、橄榄苦苷的对照品溶液,按“2.4”项下的方法制备供试品溶液,进样测定,计算4个成分的平均回收率分别为102.7%、99.6%、93.5%、94.8%,RSD分别为1.4%、2.6%、1.9%、2.1%。
2.6.6 供试品中多成分的定量测定取3批二至丸水蜜丸制剂样品,每批取2份,依照“2.4”项下方法制备供试品溶液,精密量取供试品溶液和对照品溶液各5 μL,分别注入超高效液相色谱仪,记录色谱图,读取峰面积值,以标准曲线法计算特女贞苷、红景天苷、女贞苷、橄榄苦苷的平均质量分数,结果分别为10.583、0.802、0.538、0.429 mg/g。
二至丸中特女贞苷等成分均符合定量测定要求。经质谱信息对照,鉴定出的二至丸中其余的16个成分,采用半定量方法,利用面积归一化法,将其量与外标法定量所得的特女贞苷进行半定量计算,各成分相对质量分数见表 2[16-17]。
|
|
表 2 二至丸制剂中16个成分的半定量测定结果 Table 2 Quantitative determination of content of 16 chemical components in Er-Zhi-Wan by semi-quantitative research |
2.7 二至丸水蜜丸制剂稳定性研究 2.7.1 二至丸制剂长期稳定性试验
在二至丸定性定量研究的基础上,以ICH制剂稳定性指导原则Q1A和Q1B中关于原料药和制剂稳定性研究的要求为准则,对二至丸水蜜丸中各成分受长期稳定性研究条件影响改变产生的变化进行全面跟踪定量研究。取有效期内的二至丸供试品3批(JB34001095、JB34001067、JB34001026),恒温恒湿箱[(25±2)℃,相对湿度(RH)(60±5)%]中放置18个月,分别于各个月月末取样1次。通过多成分定性定量分析,分析各成分随稳定性研究时间延长而改变的情况。
表 3中将W0计作0个月样品中每个化合物的初始量,18个月期间样品中每个化合物的量计作Wi。各抽样月份样品中各化合物的量较0个月份样品的降低百分比(DP)作为二至丸稳定性改变的定量变化跟踪依据。
|
|
表 3 二至丸长期稳定性样品和加速稳定性样品定量比较 Table 3 Quantitative comparison on chemical components content in Er-Zhi-Wan inlong-term and accelerated stability testing |
DP=(W0-Wi)/W0
由表 3可见在长期稳定性研究中,18个月后20种成分的量无明显变化,RSD均小于3%。此外,样品高分辨质谱图正、负离子响应中均未见降解产物生成。可见常温条件下市售包装中的二至丸成分基本保持稳定。
2.7.2 二至丸制剂加速稳定性试验在长期稳定性研究的基础上,取有效期内的二至丸3批(JB34001027、JB34001056、JB34001045),以市售包装置于恒温恒湿箱中[(40±2)℃,RH(75±5)%]进行加速稳定性试验。在试验期间第0、1、2、3、6、12个月末分别取样,对各批次样品进行多成分定性定量分析。由表 3可见20个成分中有11个成分的量随时间的延长而降低,其中以松果菊苷和橄榄苦苷酸的量降低最为明显,DP超过60%,然而样品UPLC-Q/TOF-MS图中仍未见加速稳定性研究中出现新的降解产物。
2.7.3 包装材料对二至丸制剂稳定性影响观察二至丸稳定性研究结果发现高湿、高温对其质量有关键性的影响。现有二至丸市售包装为药用聚酯包材,气密性较差。试验中采用钠钙玻璃包装制备与原包装瓶尺寸和开口大小一致的瓶装包装,提高包装气密性,并用合成树脂为主要成分的热塑性封口膜和锡纸密封,制成保持与市售包装规格一致的制剂。将2种包装的制剂各3个批次(JB34001041、JB340010243、JB34001069)分别置于恒温恒湿箱中[(40±2)℃,RH(75±5)%],进行加速试验研究。分别于各个月月末分别取样,对各批次样品进行多成分定性、定量分析,由表 4结果可见,在相同密封条件下自制钠钙玻璃包装中9个成分的量降低程度明显小于原包装。
|
|
表 4 2种包装材质二至丸样品稳定性比较 Table 4 Comparison on two kinds of packaging materials for stability of Er-Zhi-Wan |
2.7.4 密封条件对二至丸制剂稳定性影响
试验中设计将3个批次(JB34001037、JB340010239、JB34001068)的有效期内市售包装(固体药用聚酯)及自制钠钙玻璃包材包装的二至丸样品敞口置于恒温恒湿箱中[(40±2)℃,RH(75±5)%],分别于各个月月末分别取样,经定量和半定量分析后与正常密封条件下样品中各成分的量对比,确证敞口条件下样品中各成分的量明显低于封口条件的。由表 5结果显示,无论在原包装样品还是玻璃包装样品,在敞口条件下,均有9个成分的量下降程度远远大于其在密封条件下的。除女贞苷外其他8个成分在敞口条件玻璃包装中其量降低程度均高于封口条件的2倍以上。
|
|
表 5 密封条件对二至丸样品稳定性影响 Table 5 Effect of sealing situation on stability of Er-Zhi-Wan |
3 讨论
本实验采用UPLC-Q-TOF/MS联用的方法对二至丸水蜜丸制剂进行多成分定性定量研究,为二至丸的质量控制提供了一定的参考。在此基础上,按照ICH制剂稳定性指导原则,对传统中药制剂二至丸进行了稳定性研究。采用UPLC-Q-TOF/MS以及参考文献的方法共鉴定了20种化学成分,在长期试验中无明显变化而在加速试验[(40±2)℃,RH(75±5)%]中,共有11个成分的峰面积随时间降低,说明二至丸水蜜丸制剂受高温、高湿环境的影响较大。且实验中发现钠钙玻璃包装材料制剂的稳定性比市售聚酯包装材料制剂的稳定性好;采用相同包材时,封口的二至丸稳定性明显优于敞口条件下的稳定性。推测可能塑料包装(聚酯类)本身存在的通透性、沥漏性、对其他成分的吸附性以及化学稳定性差等都会对药物的质量产生影响。本研究提供了中药二至丸质量控制的依据也为保障临床用药安全提供了技术支持,此方法也适合其他中药水蜜丸制剂的稳定性研究。
| [1] | 崔福德. 药剂学[M]. 北京: 人民卫生出版社, 2004 . |
| [2] | 梁锦杰, 吴燕红, 张燕梅, 等. 中药制剂稳定性研究中含量测定的问题分析[J]. 中国实验方剂学杂志 , 2014, 20 (12) :253–258. |
| [3] | 吴旻. 扶寿精方[M]. 北京: 中医古籍出版社, 1986 . |
| [4] | 中国药典 [S]. 一部. 2015. |
| [5] | Cheng M, Wang Q, Fan Y, et al. A traditional Chinese herbal preparation, Er-Zhi-Wan, prevent ovariectomy- induced osteoporosis in rats[J]. J Ethnopharmacol , 2011, 138 (2) :279–285. |
| [6] | Pamela R, Norazlina M, Shuid A N. Beneficial effects of traditional Chinese medicine on the treatment of osteoporosis on ovariectomised rat models[J]. Curr Drug Targets , 2013, 14 (14) :1689–1693. |
| [7] | Xu H, Su Z R, Huang W, et al. Er Zhi Wan, an ancient herbal decoction for woman menopausal syndrome, activates the estrogenic response in cultured MCF-7 cells: an evaluation of compatibility in defining the optimized preparation method[J]. J Ethnopharmacol , 2012, 143 (1) :109–115. |
| [8] | Zhang H, Xing W W, Li Y S, et al. Effects of a traditional Chinese herbal preparation on osteoblasts and osteoclasts[J]. Maturitas , 2008, 61 (4) :334–339. |
| [9] | Yao W F, Gu H W, Zhu J J, et al. Integrated plasma and urine metabolomics coupled with HPLC/QTOF-MS and chemometric analysis on potential biomarkers in liver injury and hepatoprotective effects of Er-Zhi-Wan[J]. Anal Bioanal Chem , 2014, 406 (28) :7367–7378. |
| [10] | 李磷, 丁安伟, 孟丽. 二至丸免疫调节作用活性部位的研究[J]. 中医药研究 , 2002 (5) :42–43. |
| [11] | 张玉仁, 郑里翔, 朱卫丰, 等. 二至丸对阴虚荷瘤小鼠抑瘤作用的研究[J]. 江西中医药大学学报 , 2007, 19 (6) :58–59. |
| [12] | Wang F F, Jin X L, Huang H H, et al. Stability-indicating method of specnuezhenide in bulk drug and its kinetics and mechanisms of degradation in aqueous solutions[J]. Med Plant , 2014, 5 (Z1) :13–18. |
| [13] | 黄雯, 苏子仁, 毕文川, 等. HPLC法测定女贞子药材中女贞苷的含量[J]. 药物分析杂志 , 2009, 29 (5) :824–826. |
| [14] | 李昱柳, 苏巧娟. 红景天苷药理活性研究进展[J]. 武警后勤学院学报: 医学版 , 2007, 16 (1) :98–100. |
| [15] | 郝婷, 崔建玲, 赵桂琴, 等. 橄榄苦苷提取分离和药理活性的研究进展[J]. 承德医学院学报 , 2010, 27 (1) :69–72. |
| [16] | 贺凤成, 李守信, 赵志全, 等. 一测多评法测定五味子中4种木脂素类成分的含量[J]. 药学学报 , 2012, 47 (7) :930–933. |
| [17] | 何兵, 杨世艳, 张燕. 一测多评中待测成分校正和定位的新方法研究[J]. 药学学报 , 2012, 47 (12) :1653–1659. |
 2016, Vol. 47
2016, Vol. 47


