2. 天津中医药大学, 天津 300193 ;
3. 安徽济人药业有限公司, 安徽 亳州 236800 ;
4. 中药现代制剂与质量控制技术国家地方联合工程实验室(天津), 天津 300193
2. Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China ;
3. Anhui Jiren Pharmaceutical Co., Ltd., Bozhou 236800, China ;
4. National & Local United Engineering Laboratory of Modern Preparation and Quality Control Technology of Traditional Chinese Medicine (Tianjin), Tianjin 300193, China
败酱草为一种传统中药,古籍考证出自《神农本草经》,《中国药典》1977年版收载败酱草为败酱科植物黄花败酱Patrinia scabiosaefolia Fisch.或白花败酱Patrinia viliosa Juss.的干燥全草[1],其性微寒,味苦、辛,归肺、大肠、肝经,具有清热解毒、排脓破瘀之功效。近年来国内外学者对黄花败酱的化学成分进行了大量研究,据文献报道[2-4]黄花败酱主要成分为三萜皂苷类化合物,其次为环烯醚萜类、香豆素类和黄酮类化合物,此外也含有少量挥发油和有机酸等,其中以三萜皂苷和黄酮类为其主要活性成分。现代研究证明败酱草具有镇静、抗菌、抗病毒、抗肿瘤等多方面的药理作用,临床上用于治疗流行性腮腺炎、鼻窦炎、慢性盆腔炎及阑尾脓肿和结肠炎等。
疏风解毒胶囊是由虎杖、连翘、败酱草等药味组成,临床上用于治疗小儿急性上呼吸道感染[5],处方中败酱草的基原植物为败酱科植物黄花败酱的干燥全草,其药材的质量对于产品的质量及稳定性至关重要。现行的败酱草标准,仅规定了药材的性状、显微鉴别、理化鉴别、水分、总灰分检查等项目,较为简单。毛红梅等[6]和刘海涛等[7]采用HPLC同时测定败酱草中常春藤皂苷元、齐墩果酸和熊果酸的量以及同时测定败酱草中原儿茶酸、绿原酸及咖啡酸的量,也有以败酱草理化鉴别、薄层色谱鉴别和总皂苷的测定建立败酱草的质量标准,但所测定成分非败酱草的独有成分,理化鉴别的颜色反应专属性差,紫外方法测定总皂苷量代表性不强。
本实验利用HPLC法建立了败酱草药材的指纹图谱,分别对不同批次的败酱草的指纹图谱进行了测定,并通过聚类分析,为败酱草的全面评价提供依据。
1 仪器及材料Agilent1100高效液相色谱仪,电热恒温水浴锅(江苏省医疗器械厂),Mettler Toledo PB303-N电子天平,Mettler Toledo AB204-N电子天平(瑞士Mettler Toledo公司)。甲醇和乙腈(色谱纯,天津市康科德科技有限公司),磷酸(分析纯,天津市化学试剂三厂),娃哈哈纯净水。
败酱草药材由安徽济人药业有限公司提供,具体信息见表 1,经天津药物研究院张铁军研究员鉴定为黄花败酱Patrinia scabiossefolia Fisch.的干燥全草。
|
|
表 1 败酱草药材来源 Table 1 Sources of Patriniae Herba |
2 方法 2.1 HPLC色谱条件
色谱柱:Orca C18柱(250 mm×4.6 mm,5μm);检测波长230 nm;柱温35℃。体积流量1 mL/min;流动相为乙腈(A)-0.05%磷酸水溶液(B);梯度洗脱,0~7 min,0~7% A,7~17 min,7%~14% A,17~60 min,14%~35% A,60~70 min,35%~45% A,70~75 min,45%~80% A;进样量为10μL。
2.2 供试品溶液的制备取败酱草药材粉碎过40目筛,取粉末约1 g,精密称定,加入70%甲醇25 mL,置锥形瓶中,密塞,称定质量,回流提取45 min,冷却至室温,再称定质量,用70%甲醇补足减失的质量,摇匀滤过,取续滤液,即得。
2.3 方法学考察 2.3.1 精密度试验按“2.2”项下的方法制备供试品溶液,在“2.1”项色谱条件下测定,连续进样6次,测定HPLC色谱图,以3号峰的保留时间和色谱峰面积为参照,计算出各色谱峰的相对保留时间和相对峰面积,其RSD值均小于5%,符合指纹图谱的要求和规定。
2.3.2 稳定性试验按“2.2”项下的方法制备供试品溶液,密闭,放置于室温,分别在0、3、6、9、12、24 h测定指纹图谱,以3号峰的保留时间和色谱峰面积为参照,计算出各色谱峰的相对保留时间和相对峰面积,其RSD值均小于5%,符合指纹图谱的要求。本供试品溶液在24 h内稳定。
2.3.3 重复性试验取败酱草药材粉末约1 g,按“2.2”项下的方法制备供试品溶液,制备6份,按法测定,记录色谱图,以3号峰的保留时间和色谱峰面积为参照,计算出各色谱峰的相对保留时间和相对峰面积,其RSD值均小于5%,符合指纹图谱的要求。
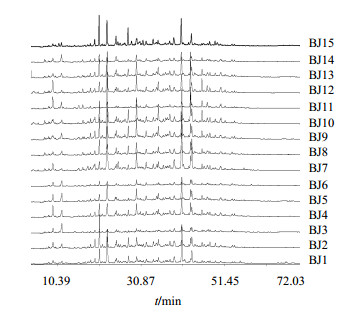
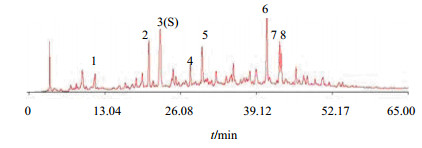
2.4 结果与分析 2.4.1 对照药材指纹图谱的生成取15批败酱草药材进行指纹图谱测定,将15批药材的指纹图谱数据导入《中药色谱指纹图谱相似度评价系统》中,以表 2中色谱峰较多,峰面积大小适中的BJ1号败酱草药材的指纹图谱为参照图谱,采用多样本平均数矢量综合作为共有模式矢量,时间宽度设定为0.10,多点校正后,确定了8个主要的色谱特征峰为共有峰。选取峰面积较大、出峰时间适中且稳定的3号峰作为参照峰(S),计算各色谱峰相对峰面积。数据见表 2,15批药材的指纹图谱见图 1。根据对15批败酱草药材的聚类分析结果,从中选取归属于I类的12批药材的色谱图生成对照指纹图谱,见图 2。
|
|
表 2 15批败酱草药材指纹图谱测定结果 Table 2 Fingerprint results of 15 batches of P atriniae Herba |
|
图 1 15批败酱草药材HPLC指纹图谱 Fig.1 HPLC fingerprints of 15 batches of Patrinia Herba |
|
图 2 败酱草药材HPLC对照指纹图谱 Fig.2 Control fingerprint of Patriniae Herba |
2.4.2 聚类分析
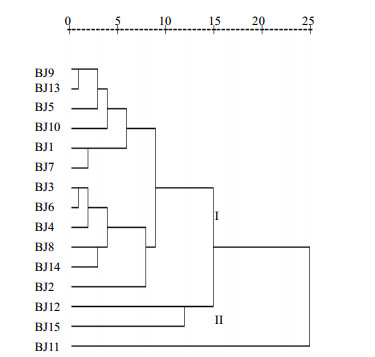
将各色谱峰占总色谱峰的峰面积量化,得到15×8阶原始数据矩阵,运用SPSS软件对其进行聚类分析。聚类分析将15个败酱草样品分为2大类,可判定败酱草内在质量具有差异性。聚类分析图见图 3。其中,样品号为BJ1、BJ2、BJ3、BJ4、BJ5、BJ6、BJ7、BJ8、BJ9、BJ10、BJ13、BJ14的样品属于I类,样品号为BJ11、BJ12、BJ15的样品属于II类。
|
图 3 败酱草药材聚类分析图 Fig.3 Cluster analysis of 15 batches of Patriniae Herba |
2.4.3 相似度分析
利用《中药色谱指纹图谱相似度评价系统》对上述15批样品与对照指纹图谱进行匹配,进行相似度评价,结果见表 3。结果表明I类药材BJ1、BJ2、BJ3、BJ4、BJ5、BJ6、BJ7、BJ8、BJ9、BJ10、BJ13、BJ14各批败酱草药材与对照指纹图谱间的相似度为0.987~0.907,表明各批次药材之间具有较好的一致性;II类药材BJ11、BJ12、BJ15批败酱草药材与对照指纹图谱的差异较大。
|
|
表 3 败酱草药材相似度评价 Table 3 Fingerprint similarity of Patriniae Herba |
本研究中相似度评价结果表明药材败酱草的HPLC色谱图很相似,通过聚类分析可以看到不同批次的败酱草在主要成分量上有一定差别,并根据这种差别可以将其分为2大类。
3 讨论采用二极管阵列检测器分析比较各波长下的色谱图中特征峰,确定在230 nm下,色谱峰较多,各峰分离良好,且峰型较好;考察提取条件和方式,确定了样品的处理方法。通过研究,建立了败酱草药材标准指纹图谱,标记了其中8个主要色谱峰。测定了15批次的败酱草样品,由败酱草相似度评价结果可以看出,各批败酱草与对照指纹图谱间的相似度值存在较大的差异,可能受品种、生长环境、生长时间、采收时间等因素的影响。本实验对败酱草药材HPLC指纹图谱的构建进行了研究,可用于疏风解毒胶囊的原材料败酱草药材的质量控制。本研究建立的败酱草指纹图谱方法,具有准确可靠、重复性好、特征性强、方法简便等特点,对败酱草药材的质量评价具有重要的意义。
| [1] | 中国药典[S]. 1977. |
| [2] | 李延芳, 楼凤昌, 唐于平, 等. 败酱属植物的研究概况[J]. 天然产物研究与开发, 2001,13 (3) :71–75. |
| [3] | 姜泓, 初正云, 王虹霞, 等. 黄花败酱化学成分[J]. 中草药, 2003,34 (11) :978–980. |
| [4] | 李延芳, 李明慧, 楼凤昌, 等. 黄花败酱的化学成分研究[J]. 中国药科大学学报, 2002,33 (2) :101–103. |
| [5] | 湖南省中药材标准[S]. 1993. |
| [6] | 毛红梅, 平欲晖, 宗星星, 等. HPLC同时测定败酱草中常春藤皂苷元、齐墩果酸和熊果酸的含量[J]. 中国实验方剂学杂志, 2012,18 (15) :89–92. |
| [7] | 刘海涛, 雷鹏, 刘英慧, 等. 双波长HPLC法同时测定败酱草中原儿茶酸、绿原酸及咖啡酸的含量[J]. 药物分析杂志, 2013,33 (4) :611–615. |
 2016, Vol. 47
2016, Vol. 47


