腊肠树Cassia fistula L. 为豆科(Leguminosae)苏木亚科决明属木本植物,学名阿勃勒,又名波斯皂荚,在傣族民间被称为锅拢良。该种原产印度、缅甸和斯里兰卡,在中国南部和西南部各省区均有栽培,是南方常见的庭园观赏树木。除用于观赏外,该植物在多方面都有着突出的贡献:其树皮可做红色染料及制皮革[1];木材可作支柱、桥梁、车辆及农具[1]等的材料;而其在民间被用于治疗呕血、瘙痒、白斑、糖尿病、丹毒、皮肤病和骨折等疾病更是突显出了其巨大的药用价值[2]。
目前国内外学者对腊肠树进行过一些研究,主要报道的化学成分有色酮、黄酮、萜、甾体、生物碱等类化合物[3-5]。为了从腊肠树中发现更多的活性成分,本实验对产自云南西双版纳的腊肠树进行化学成分研究,从中分离到1个新的三环生物碱类化合物,命名为决明碱L(cassiarin L,1)。初步生物活性测试显示该化合物具有明显的细胞毒活性。
1 仪器与材料UV-2401A紫外光谱仪(日本岛津公司);Bio-Rad FTS-185傅里叶变换红外光谱仪(美国伯乐BIO-RAD 公司);DRX-500型核磁共振仪(瑞士布鲁克公司);半制备HPLC分析仪器为岛津LC-8A型高效液相色谱仪,色谱柱为安捷伦公司Zorbax PrepHT GF(250 mm×21.2 mm,7 μm)和安捷伦Zorbax C18(250 mm×9.4 mm,5 μm)。
柱色谱硅胶(80~100、200~300目)、GF254(100 mm×100 mm)硅胶板,均为青岛海洋化工厂生产;凝胶为Sephadex LH-20;薄层色谱法显色,显色剂为5%H2SO4乙醇溶液,喷洒后适当加热即可;工业用三氯甲烷、甲醇、醋酸乙酯、石油醚;色谱纯乙腈、四氢呋喃;超纯水。
腊肠树于2012年8月购自云南西双版纳傣医院,产地为云南西双版纳州磨憨县,经西双版纳傣医院林艳芳医师鉴定为豆科苏木亚科决明属植物腊肠树Cassia fistula L. 的枝条。
2 提取与分离取腊肠树的枝条2.5 kg晒干,粉碎后过30目筛,然后用95%乙醇水溶液提取4次,每次用量为3.5 L,室温浸泡、超声4次(每次30 min),滤过,合并提取液,用10 L 3%酒石酸溶液稀释后用醋酸乙酯萃取。水相用氢氧化钠调节pH值为9.0~10.0后用醋酸乙酯萃取,将醋酸乙酯相减压浓缩得浸膏22.8 g。浸膏用25 g粗硅胶(80~100目)拌样,烘干,用150 g硅胶(150~200目)柱色谱,三氯甲烷-丙酮(20∶1、9∶1、8∶2、7∶3、6∶4、5∶5)梯度洗脱,分成6个部分。将三氯甲烷-丙酮7∶3洗脱部分用甲醇溶解,以甲醇为流动相,用葡聚糖凝胶柱Sephadex LH-20净化后经HPLC进一步分离:采用Agilent公司的Zorbax PrepHT GF(250 mm×21.2 mm,7 μm)反相柱,以45%甲醇水溶液为流动相,体积流量为15 mL/min,收集33.6 min的色谱峰,得化合物粗品。粗品再用甲醇溶解,以70%乙腈水溶液为流动相,体积流量为3 mL/min,收集15.2 min的色谱峰,得化合物1(12.8 mg)。
3 结构鉴定化合物1:红色粉末,(nm): 215 (4.12),242 (3.47),290 (3.80),328 (3.95);(cm−1): 3 418,1 695,1 605,1 542,1 484,862,758;ESI-MS m/z: 252 [M+Na]+;HR-ESI-MS m/z: 252.063 2 [M+Na]+(计算值252.063 7,C13H11NNaO3)。HR-ESI-MS m/z: 显示其准分子离子峰为252.063 2 [M+Na]+,结合1H-和13C-NMR谱确定分子式为C13H11NO3。其红外光谱显示化合物中有羟基 (3 418 cm−1) 和芳环 (1 605,1 542,1 484 cm−1) 信号,紫外光谱在215、242、290、328 nm有最大吸收,也证实化合物中存在芳环结构。化合物的1H-NMR和13C-NMR谱数据(表 1)显示其含有13个碳和11个氢,包括7个sp2季碳、4个sp2次甲基、1个芳环上的甲基、1个羟甲基和1个酚羟基。5个季碳 (δC 163.5,151.5,143.5,140.6,
|
|
表 1 化合物1的1H-NMR和13C-NMR数据(500/125 MHz,C5D5N) Table 1 1H-NMR and 13C-NMR data of compound 1 (500/125 MHz,C 5D 5N) |
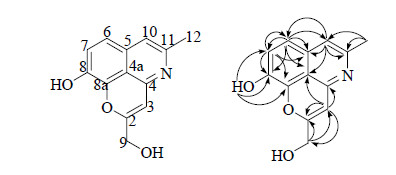
148.4) 的化学位移值显示它们和氧或氮原子相连。同时,通过这些数据也可推测该化合物为1个和cassiarin A类似的三环生物碱[6]。而该化合物中H-3与C-4、C-4a,H-6与C-4a、C-5、C-8、C-10,H-10与C-4a、C-5、C-6的HMBC相关(图 1)可进一步证实该化合物为三环生物碱。化合物的基本骨架确定后,剩余的取代基(1个甲基,1个羟甲基和1个酚羟基)的位置也可通过HMBC相关确定。根据甲基氢 (H3-12) 和C-10、C-11的HMBC相关,可证实甲基取代在C-11位;羟甲基氢 (H2-9) 和C-2、C-3的HMBC相关可证实羟甲基取代在C-2位;酚羟基氢和C-7、C-8、C-8a的HMBC相关,可证实酚羟基取代在C-8位。至此,该化合物的结构得到确定,命名为决明碱L。
|
图 1 化合物1的结构和主要HMBC (  |
4 化合物的细胞毒活性
由于多数文献报道生物碱类化合物具有明显的细胞毒活性,因此对化合物1进行了细胞毒活性筛选。细胞毒活性检测参照文献方法[7]采用改良的MTT测定法,以紫杉醇为阳性对照药,采用5种人源癌细胞株(NB4、A549、SHSY5Y、PC3和MCF7),紫杉醇的IC50值分别为0.03、0.02、0.05、0.05、0.03 μmol/L,化合物1的IC50值分别为1.8、2.6、3.5、4.2、2.3 μmol/L,结果表明化合物1对所测试的人源肿瘤细胞增殖具有明显的细胞毒活性。
| [1] | 马洁, 张丽霞, 管艳红. 决明属5种傣药植物介绍[J]. 中国民族民间医药杂志, 2004 (68) :178–180. |
| [2] | Bhakta T, Banerjee S, Mandal S C, et al. Hepatoprotective activity of Cassia fistula leaf extract[J]. Phytomedicine, 2001, 8 (3) :220–224 . |
| [3] | Lee C K, Lee P H, Kuo Y H. The chemical constituents from the aril of Cassia fistula L[J]. J Chin Chem Soc, 2001, 48 (6A) :1053–1058 . |
| [4] | Luximon-Ramma A, Bahorun T, Soobrattee M A, et al. Antioxidant activities of phenolic, proanthocyanidin, and flavonoid components in extracts of Cassia fistula[J]. J Agric Food Chem, 2002, 50 (18) :5042–5047 . |
| [5] | Misra T N, Singh R S, Pandey H S, et al. A new diterpene from Cassia fistula pods[J]. Fitoterapia, 1997, 68 (4) :375–376 . |
| [6] | Morita H, Oshimi S, Hirasawa Y, et al. Cassiarins A and B, novel antiplasmodial alkaloids from Cassia siamea[J]. Org Lett, 2007, 9 (18) :3691–3693 . |
| [7] | Hu Q F, Zhou B, Ye Y Q, et al. Cytotoxic deoxybenzoins and diphenylethylenes from Arundina graminifolia[J]. J Nat Prod, 2013, 76 (10) :1854–1859 . |
 2016, Vol. 47
2016, Vol. 47


