2. 江苏康缘药业股份有限公司, 江苏 连云港 222001;
3. 中药制药过程新技术国家重点实验室, 江苏 连云港 222001
2. Jiangsu Kanion Pharmaceutical Co., Ltd., Lianyungang 222001, China;
3. State Key Laboratory of New-tech for Chinese Medicine Pharmaceutical Process, Lianyungang 222001, China
岛津高效液相色谱仪,日本岛津公司;XP6电子天平、BP211D型电子分析天平,Mettler Toledo。
对照品没食子酸(批号110831-200803,质量分数90.1%)、5-羟甲基糠醛(5-HMF,批号110626-201308,质量分数>98%)、马钱苷(批号110640-201005,质量分数99.2%)、芍药苷(批号110736-201136,质量分数94.9%)、丹皮酚(批号110708-200506,质量分数>98%)、熊果酸(批号110742-201220,质量分数为99.3%)对照品均购自中国食品药品检定研究院。莫诺苷系由军事医学科学院从山茱萸药材中分离所得,经1H-NMR、13C-NMR结构鉴定,HPLC峰面积归一化法分析测得质量分数为95.7%。乙腈,色谱纯;水为自制纯化水;其余试剂均为分析纯。本实验所采用的熟地黄Rehmanniae Radix Praeparata(玄参科地黄属植物地黄Rehmannia glutinosa Libosch. 的干燥块根的炮制加工品)、山茱萸Corni Fructus(山茱萸科山茱萸属植物山茱萸Cornus officinalis Sieb. et Zucc. 的干燥成熟果肉)、牡丹皮Moutan Cortex(毛莨科芍药属植物牡丹Paeonia suffruticosa Andr. 的干燥根皮)、茯苓[多孔菌科茯苓属植物真菌茯苓Poria cocos (Schw) Wolf的干燥菌核]、泽泻[泽泻科泽泻属植物泽泻Alisma orientalis (Sam) Juzep. 的块茎]和山药(薯蓣科薯蓣属植物薯蓣Dioscorea opposite Thunb. 的干燥根茎)6味药材购自连云港康济大药房,经江苏康缘药业股份有限公司吴舟执业药师鉴定均为正品。
| 表 1 六味地黄浓缩丸的编号、生产厂家及批号 Table 1 Code number,manufacturers,and batch numbers of Liuwei Dihuang Concentrated Pills |
色谱柱为Agilent TC-C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.02%三氟乙酸水溶液,梯度洗脱:0~5 min,4%乙腈;5~30 min,4%~16%乙腈;30~40 min,16%乙腈;40~55 min,16%~92%乙腈;55~70 min,92%~95%乙腈;体积流量为1.0 mL/min;柱温为30 ℃;检测波长:0~60 min,238 nm;60~70 min,210 nm。色谱图见图 1。
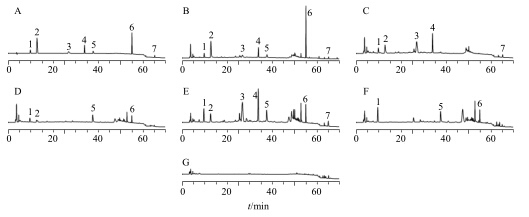 | 1-gallic acid 2-5-HMF 3-morroniside 4-loganin 5-paeoniflorin 6-paeonol 7-ursolic acid > 图 1 混合对照品 (A),六味地黄浓缩丸样品 (B) 及缺牡丹皮 (C)、缺山茱萸 (D)、缺熟地黄 (E)、缺熟地黄+山茱萸 (F) 和缺熟地黄+山茱萸+牡丹皮 (G) 阴性样品的HPLC图Fig.1 HPLC of mixed reference substances (A),Liuwei Dihuang Concentrated Pills sample (B),negative sample without Moutan Cortex (C),without Corni Fructus (D),without Rehmanniae Radix Praeparata (E),without Rehmanniae Radix Praeparata + Corni Fructus (F),and Rehmanniae Radix Praeparata + Corni Fructus + Moutan Cortex (G) |
分别精密称取没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸对照品适量,精密称定,置棕色量瓶中,加甲醇分别制成含没食子酸37.8 μg/mL、5-HMF 188.5 μg/mL、莫诺苷21.2 μg/mL、马钱苷34.6 μg/mL、芍药苷22.9 μg/mL、丹皮酚39.9 μg/mL、熊果酸24.5 μg/mL的混合对照品溶液。
2.3 供试品溶液的制备取质量差异下的六味地黄浓缩丸样品,研细,精密称取0.5 g,置具塞锥形瓶中,精密加入甲醇25 mL,密塞,称定质量,水浴回流(70 ℃)30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,过0.45 μm微孔滤膜,即得。
2.4 阴性对照溶液按处方比例分别称取除熟地黄,除山茱萸(制),除牡丹皮,除熟地黄和山茱萸(制),除牡丹皮、山茱萸(制)、熟地黄以外的其余药味,按六味地黄浓缩丸制备工艺分别制备缺熟地黄,缺山茱萸(制),缺牡丹皮,缺熟地黄及山茱萸,缺熟地黄、山茱萸(制)、牡丹皮阴性样品,按“2.3”项下方法制备阴性对照溶液。
2.5 精密度试验精密吸取对照品溶液10 μL,按“2.1”色谱条件,进样,测定,连续6次。以没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸的峰面积计算,其RSD分别为0.40%、0.33%、0.33%、0.33%、0.86%、0.34%、0.34%,结果表明,仪器精密度良好。
2.6 线性关系考察取没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸对照品适量,精密称定,加甲醇制成所需浓度的对照品溶液,即得。分别吸取上述溶液10 μL,注入高效液相色谱仪,测定,以峰面积平均值为纵坐标(Y),对照品质量浓度为横坐标(X),绘制标准曲线,得回归方程、相关系数(r)和线性范围,分别为没食子酸:Y=10 160 895 X-5 687.5,r=0.999 8,线性范围3.8~75.6 μg/mL;5-HMF:Y=12 986 231 X-26 220,r=0.999 7,线性范围18.845~376.9 μg/mL;莫诺苷:Y=19 711 638 X-6 364.9,r=0.999 8,线性范围2.12~42.4 μg/mL;马钱苷:Y=18 918 031 X-9 313.8,r=0.999 8,线性范围3.46~69.2 μg/mL;芍药苷:Y=16 380 034 X-8 502,r=0.999 7,线性范围2.29~45.8 μg/mL;丹皮酚:Y=25 552 672 X-7 906.1,r=0.999 7,线性范围3.99~79.8 μg/mL;熊果酸:Y=54 664 962 X-1 788.3,r=0.999 8,线性范围2.45~49.0 μg/mL。结果表明,没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸在各自的质量浓度范围内与峰面积呈良好的线性关系。
2.7 稳定性试验精密吸取“2.3”项供试品溶液,分别于制备后0、2、6、8、10、12、24 h分别进样,按“2.1”项色谱条件测定,以没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸峰面积计算,结果RSD值分别为0.85%、1.42%、1.63%、1.31%、1.47%、0.63%、1.06%,结果表明供试品溶液放置24 h稳定。
2.8 重复性试验按“2.3”项下的方法,制备6份供试品溶液,按“2.1”项色谱条件测定,结果没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸平均质量分数分别为1.92、6.82、0.82、1.72、0.89、1.99、0.12 mg/g,RSD值分别为1.05%、1.49%、1.47%、0.85%、1.57%、1.48%、0.81%,RSD值均小于2%,表明该方法重复性良好。
2.9 回收率试验精密称取已测定的样品(样品1,研细)粉末0.25 g,共6份,精密加入没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸对照品适量,按“2.3”项下方法制备供试品溶液,测定7个指标性成分的量,计算回收率。结果没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸的平均回收率分别为97.68%(RSD 1.74%)、100.82%(RSD 1.69%)、98.74%(RSD 1.03%)、100.70%(RSD 1.53%)、98.61%(RSD 1.94%)、100.33%(RSD 1.19%)、100.66%(RSD 2.15)。结果显示,准确性较好。
2.10 样品的测定
取不同厂家六味地黄丸,按“2.3”项下的方法制备供试品溶液,每次进样量10 μL。取“2.2”项下的对照品溶液,进样10 μL。按“2.1”项下色谱条件测定,记录峰面积,计算7种成分的量,结果见表 2。
| 表 2 六味地黄浓缩丸中7种成分测定结果 Table 2 Determination of seven major components in Liuwei Dihuang Concentrated Pills |
应用SPSS 18.0软件,采用组间均联法(between-groups Linkage),选用夹角余弦(cosine)作为刻度,将上述20个测试样品进行聚类分析,结果见图 2。通过聚类分析,根据各样品之间的距离差异将该20个不同厂家的样品分为2类,其中,编号4、6、8、9、11、14和16的厂家样品被归为一类,质量差异相对较小;其余厂家产品被归为一类,产品之间7种成分的量差异不大。该树状图能够直观地反映不同厂家生产的六味地黄浓缩丸中检测成 分之间所存在的差异。
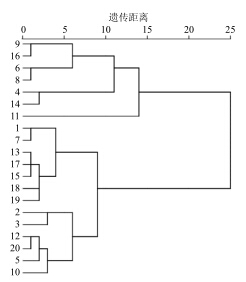 | 图 2 20个厂家的六味地黄浓缩丸聚类分析树状图Fig.2 Dendrogram of cluster analysis on of Liuwei Dihuang Concentrated Pills from 20 manufacturers |
本实验比较了乙腈-0.1%甲酸[8]、乙腈-0.015%磷酸水溶液[9]和乙腈-0.02%三氟乙酸水溶液3种流动相系统,结果采用乙腈-0.02%三氟乙酸水溶液待测成分分离效果最佳,且梯度洗脱才能检出所测成分。应用二极管阵列检测器在210~400 nm扫描,结果选取238 nm作为检测波长,能检测除熊果酸以外其他成分,鉴于熊果酸为末端吸收(210 nm),本实验采用切换波长法同时测定样品中7种成分的量。结果表明此方法切实可行,可以用于同时测定样品中的指定成分的量。
本实验建立了一种简便、快捷测定六味地黄浓缩丸中没食子酸、5-HMF、莫诺苷、马钱苷、芍药苷、丹皮酚、熊果酸7种成分的定量分析方法。并通过聚类分析法,以7种成分的量为指标,对20个厂家的样品进行分类,图谱结果佐证了不同厂家产品各成分量之间存在差异,其中芍药苷差别最大,这可能与投料药材或者工艺过程有关。中药通常以复方形式存在,呈现出多成分、多靶点、多通路调控机体的特点,由此达到治疗疾病的目的[10],因此,中药质量控制需要同时控制多个成分的量,从而使中药疗效更稳定。
综上所述,不同厂家生产的同一品种仅依靠2个指标来评价,不足以反映中药多组分、多靶点的特性,应尽可能多地对其药效成分进行研究[4, 11, 12, 13],
但是分别检测多个成分费时、费力,同时测定多种成分量的方法可以实现中药材及其制剂的有效质量控制,亦可以减少资源的浪费。通过对比定量测定结果,可以发现各厂家马钱苷和丹皮酚的量均符合《中国药典》2010年版规定[6],且其量差别较小;但其他成分(芍药苷、5-HMF、没食子酸和莫诺苷)差别较大,因此建议完善企业内部质量控制标准,同时对原料来源和工艺过程严格把关,以保证该产品的疗效。本研究从多成分测定的角度出发,通过切换波长法,建立了一种可以同时测定浓缩丸中7种成分量的方法,为六味地黄浓缩丸质量评价的提升提供一定的参考依据。
| [1] | 张尊如, 陈建国. 六味地黄丸滋阴功效的思考 [J]. 中成药, 2006, 28(8): 1244-1245. |
| [2] | 何福财. 六味地黄丸加针灸治疗老年2型糖尿病肾阴亏虚证的临床研究 [D]. 南京: 南京中医药大学, 2007. |
| [3] | 曹占花. 阿卡波糖联合六味地黄丸治疗早期糖尿病肾病的临床疗效观察 [J]. 现代药物与临床, 2013, 28(5): 760-762. |
| [4] | 唐 庆, 胡 慧, 王全胜, 等. 六味地黄加味胶囊对糖尿病肾病大鼠肾脏蛋白激酶C活性及结缔组织生长因子的影响 [J]. 中草药, 2010, 41(1): 77-81. |
| [5] | 王喜军, 张 宁, 孙 晖, 等. 六味地黄丸的血清药物化学研究 [J]. 中国天然药物, 2004, 2(4): 29-32. |
| [6] | 中国药典 [S]. 一部. 2010. |
| [7] | 郝延军, 赵晓笠, 桑育黎, 等. 六味地黄丸对照提取液的实验研究 [J]. 中草药, 2013, 44(2): 180-182. |
| [8] | 封 亮, 贾晓斌, 李长春, 等. HPLC同时测定六味地黄浓缩丸中4种主要成分的含量 [J]. 中国药科大学学报, 2009, 40(1): 59-61. |
| [9] | 罗 云, 郝伟伟, 王 洁, 等. 高效液相色谱法测定六味地黄浓缩丸特征图谱及4种主要成分的含量 [J]. 中国医院药学杂志, 2012, 32(10): 748-751. |
| [10] | 刘 娟, 周 瑶, 张广献, 等. 六味地黄丸入血成分增效自杀基因杀伤肝癌细胞的缝隙连接机制 [J]. 广州中医药大学学报, 2014, 31(1): 103-108. |
| [11] | Liang X, Li H, Li S. A novel network pharmacology approach to analyse traditional herbal formulae: the Liu-Wei-Di-Huang pill as a case study [J]. Mol BioSyst, 2014, 10(5): 1014-1022. |
| [12] | 戴 冰. 六味地黄方含药血清及其入血成分对大鼠前脂肪细胞增殖、分化的影响 [D]. 长沙: 湖南中医药大学, 2006. |
| [13] | 王喜军, 孙文军, 张 宁, 等. 六味地黄丸血中移行成分的分离及结构鉴定 [J]. 中国天然药物, 2007, 5(4): 277-280. |
 2015, Vol. 46
2015, Vol. 46


