2. 宁夏回药现代化工程技术研究中心, 宁夏 银川 750004;
3. 回医药现代化省部共建教育部重点实验室, 宁夏 银川 750004;
4. 成都中医药大学民族医药学院, 四川 成都 610075
2. Ningxia Research Center of Modern Hui Medicine Engineering and Technology, Yinchuan 750004, China;
3. Key Laboratory for Modernization of Hui Medicine, Co-construction by Province and Ministry of Education, Yinchuan 750004, China;
4. School of Ethnomedicine in Chengdu University of Traditional Chinese Medicine, Chengdu 610075, China
麻黄Ephedra Herba为常用中药,临床应用广泛。《中国药典》2010年版一部收载麻黄为麻黄科(Ephedraceae)植物草麻黄Ephedra sinica Stapf、中麻黄E. intermedia Schrenk et C. A. Mey. 或木贼麻黄E. intermedia equisetina Bge. 的干燥草质茎,具有发汗散寒、宣肺平喘、利水消肿等功效[1]。其可治疗风寒感冒、气喘、水肿及支气管哮喘等病。目前评价麻黄药材质量的方法主要有性状、显微及薄层鉴别、麻黄碱与伪麻黄碱定量测定、指纹图谱测定等,由于麻黄治疗作用的发挥依赖于多成分、多靶点的综合调节作用,通过控制单一指标成分的量来实现麻黄质量控制的方法不足以反映其作用特点,指纹图谱技术与单一指标成分定量测定相比,其所含信息是综合的、多层次的和具体量化的,但也存在局限,难以关联或反映中药安全性和有效性。中药与生物制剂有类似之处,将生物活性测定法引入中药质量控制和评价体系,不仅可以鉴定中药品种和控制质量,而且可以评价药效,尤其对于麻黄等化学成分复杂、理化测定不易反映其生物活性和临床疗效的中药而言,此方法更能凸显其优越性。
目前市售麻黄药材产地众多,质量参差不齐,严重影响到麻黄的临床疗效,对于形态、生药性状及化学成分等高度相似的不同产地的麻黄药材,基于麻黄宣肺平喘功效,测定不同产地麻黄对豚鼠离体气管平滑肌的解痉率,在此基础上建立不同产地麻黄平喘生物效价(potency)的质量评价方法,将麻黄药理作用与药材质量联系起来,为麻黄质量评价研究提供一种新的研究思路。
1 材料 1.1 动物健康Hartley系豚鼠80只,雄性,体质量(350±50)g,购自济南金丰实验动物有限公司,合格证号SCXK(鲁)2014-0006。
1.2 药材麻黄样品共37份,分别采自甘肃、宁夏、内蒙古、新疆、山西、陕西,由西北师范大学晏民生副教授鉴定,确定20份为草麻黄E. sinica Stapf,17份为中麻黄E. intermedia Schrenk et C. A. Mey. ,样品具体信息见表 1。麻黄对照药材为草麻黄,购自中国食品药品检定研究院(批号121051-201005),凭证标本存放于宁夏医科大学回药现代化工程技术研究中心207-1室。
| 表 1 不同产地麻黄样品信息 Table 1Information of Ephedrae Herba samples from different habitats |
氨茶碱片(太原市振兴制药有限责任公司生产,批号H14021628),K-H(Krebs-Henselei)液(用NaCl、KCl、MgSO4•7H2O、KH2PO4、NaHCO3、CaCl2、葡萄糖等分析纯试剂配制),磷酸组胺(His)为分析纯。
1.4 仪器BL-420F生物信号采集处理系统、HW200S恒温平滑肌实验系统、FT-100生物张力传感器(成都泰盟软件有限公司);Hypersil ODS2 C18色谱柱(大连依利特分析仪器有限公司);Agilent 1200高效液相色谱仪(安捷伦科技有限公司)。
2 方法 2.1 供试品与对照药材溶液的制备取生麻黄样品25 g,加10倍量水,浸泡40 min,用武火煮沸后,改用文火煎煮30 min,纱布滤过取汁;再加8倍量水,煎煮方法、时间同前,纱布滤过取汁,合并2次药液,浓缩成1 g/mL的药液[2, 3],即得供试品溶液。
麻黄对照药材同上述煎煮法制成对照药材溶液。
2.2 豚鼠离体气管条平喘模型的制备用木槌击毙豚鼠,从甲状软骨下至气管下端分叉处取整段气管,剪成宽3 mm、长30 mm的螺旋条,一端固定于盛有Kreb’s营养液的麦氏浴槽内,另一端挂于张力换能器下端金属钩上,换能器连接BL-420F生物信号采集处理系统,调节基础张力为2 g,稳定1 h。实验时取一根气管条置于麦氏浴槽内,记录一段正常曲线作基线,加入His 200 mg/mL,观察自动平衡记录仪曲线变化,当气管平滑肌张力升到最高点时,麻黄给药组采用累积剂量法滴加麻黄供试品溶液,使之终质量浓度分别为20、40 mg/mL;同理,氨茶碱(阳性对照药)组亦按照上述方法采用累积剂量法滴加氨茶碱溶液,使之终质量浓度分别为0.125、0.250 mg/mL;对照(生理盐水)组也以同法加等体积生理盐水,记录给药后3 min气管条张力变化,每个质量浓度重复4次按公式计算解痉率[解痉率=(给药前张力值-给药后张力值)/给药前张力值]。
2.3 麻黄平喘作用量效线性关系考察取麻黄对照药材,按“2.1”项方法制备对照药材溶液,按“2.2”项方法测定2.5、5.0、10、20、40、80 mg/mL对照药材溶液解痉率,以质量浓度的对数为横坐标,解痉率为纵坐标作图,考察麻黄平喘作用量效曲线,根据该曲线确定不同产地麻黄测定生物效价的供试品液质量浓度。
2.4 麻黄平喘效价测定方法将所配麻黄对照药材溶液和供试品溶液,按1∶0.5剂间距稀释,以麻黄对照药材溶液为工作对照组(S),不同产地麻黄样品溶液为供试品组(T),按“2.2”项下方法分别测定工作对照组和供试品组解痉率,平行测定4次。按照《中国药典》2010年版二部附录XIV生物检定统计法项下“量反应平行线法”(2,2)法,对麻黄对照药材进行原始效价赋值,定义麻黄对照药材效价为100 U/g,计算不同产地麻黄样品的效价(PT)和效价的可信限率(FL),并检验其可靠性[4]。
2.5 麻黄样品中麻黄碱与伪麻黄碱定量测定采用高效液相色谱法,Hypersil ODS2 C18色谱柱(250 mm×4.6 mm,5 μm),流动相A相为乙腈,B相为含0.1%磷酸和0.1%三乙胺的混合水溶液,梯度洗脱,0~15 min,98%~95% B;15~20 min,95% B;20~25 min,95%~93% B;25~45 min,93%~91% B;45~90 min,91%~85% B;运行时间90 min;体积流量1.0 mL/min;检测波长210 nm;进样量10 μL;柱温30 ℃。同时测定不同产地麻黄样品中的麻黄碱与伪麻黄碱的量,二者之和即为麻黄碱与伪麻黄碱总量。本色谱条件下得到麻黄碱回归方程为Y=19.641 X+5.940 8(R2=0.999 8),线性范围为0.004~0.800 mg/mL,伪麻黄碱回归方程为Y=20.691 X+3.562 3(R2=0.999 9),线性范围为0.006~1.800 mg/mL。
2.6 数据处理生物效价以中国药典生物检定统计程序BS2000计算,各组数据用 x±s表示,多组数据采用单因素方差分析(ANOVA)检验,应用SPSS 21.0软件进行统计学处理。
3 结果与分析 3.1 生物效价测定方法学考察 3.1.1 精密度考察取同一份麻黄供试品溶液,按“2.4”项方法测定6次生物效价值,计算麻黄平均平喘效价值为167.79 U/g,RSD 3.1%。
3.1.2 重复性考察取同一批样品分6次提取,制成供试品溶液,按“2.4”项方法测定,计算麻黄平均效价值为168.34 U/g,RSD 3.9%。
3.1.3 中间精密度考察本实验室2名不同实验人员在2个不同时间,分别按“2.4”项方法重复测定6次,计算麻黄平均效价值为166.94 U/g,RSD 4.8%,说明不同实验人员对测定结果影响较小。
3.1.4 麻黄生物效价检测可靠性检验《中国药典》2010年版二部附录XIV对量反应平行线测定法要求如下:(1)在一定剂量范围内,对照品(S)和供试品(T)的对数剂量(X)和反应或反应的特定函数(Y)呈直线关系;(2)当S和T的活性组分基本相同时,两直线平行;(3)要求回归项应非常显著(P<0.01),偏离平行应不显著(P>0.05)。
本实验对麻黄对照药材解痉作用量效关系进行了考察,结果表明,麻黄对照药材的对数剂量(X)与解痉率(Y)具有良好的线性关系,在10~80 mg/mL,回归方程Y=59.080 X-44.860(r=0.988 5)。选择麻黄剂量20与40 mg/mL对不同产地麻黄生物效价测定进行可靠性检验,结果该剂量下回归项均有极显著差异(P<0.01),偏离平行线均无显著差异(P>0.05),说明随着剂量的增加,解痉率有规律地增加,同时供试品和对照品呈平行直线关系,因而可用“量反应平行线法”(2,2)法检测不同产地麻黄药材平喘效价。
3.2 不同产地麻黄解痉率比较
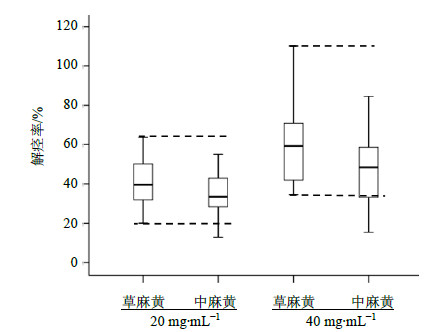
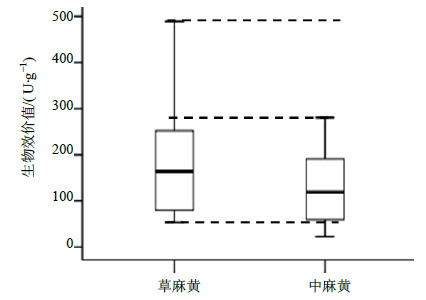
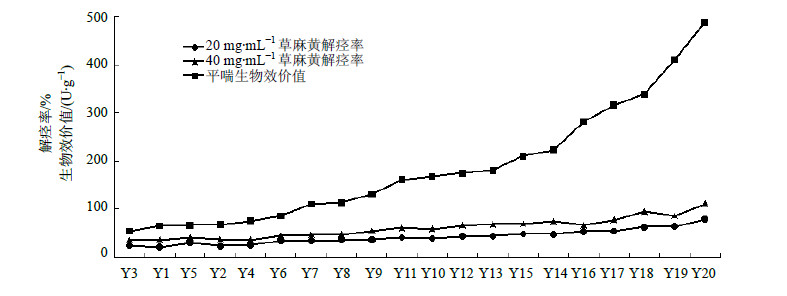
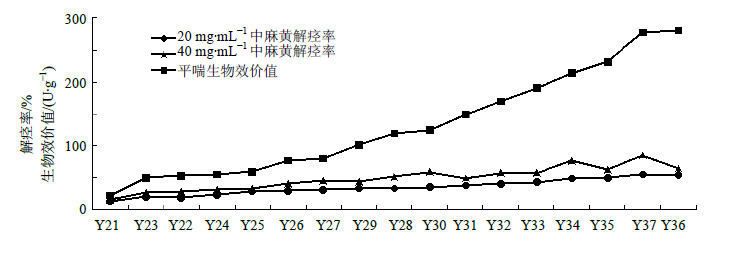
实验结果见表 2。麻黄对His引起的豚鼠离体平滑肌收缩有良好的解痉作用,与对照药材相比,20 mg/mL给药量,不同产地麻黄中有15份达显著水平(P<0.05),40 mg/mL给药量,不同产地麻黄中有20份差异达显著水平(P<0.05)。20或40 mg/mL给药量的麻黄解痉率均以甘肃泾川产中麻黄解痉率最低,以甘肃安宁草麻黄解痉率最高,二者均达显著水平(P<0.05)。同一产地不同剂量的麻黄解痉作用与麻黄质量浓度呈剂量依赖性,麻黄质量浓度增加解痉率增大,平喘作用增强。
参考文献
|
 2015, Vol. 46
2015, Vol. 46