2. 昆明道地药材可持续发展利用重点实验室, 昆明 云南 650500
2. Kunming Key Laboratory for Sustainable Development and Utilization of Genuine Medicinal Materials, Kunming 650500, China
三七是我国名贵中药材,据《本草纲目》记载,三七“止血散血定痛,金刃箭伤、跌扑杖疮、血出不止者,嚼烂涂,或为末掺之,其血即止”,表明三七外用具有显著的止血功能。在现代的中药制剂中,云南白药气雾剂、创可贴等止血功效外用制剂中均含有三七。近年来,已有大量文献针对三七的体外经皮渗透活性做出研究[1, 2, 3, 4]。三七素(dencichine,β-N-oxalyl-L-α,β-dimainopropinoieaeid)作为三七中止血活性最强的单体成分[5],能够显著影响凝血系统的凝血因子和血小板聚集,从而缩短凝血时间和出血时间[6, 7, 8, 9]。但目前针对三七素的体外透皮吸收特性研究领域尚属空白。因此本实验对三七素皮肤渗透特性做出研究,为三七素在经皮给药系统中的开发和应用提供理论基础和实验依据。
1 仪器与材料YB-P6智能透皮试验仪,天津天光光学仪器有限公司;LC-20A高效液相色谱仪,日本岛津公司;ZWY-111B恒温振荡培养箱,上海智城分析仪器制造有限公司。
三七素对照品,批号MR91890,相对分子质量为176.13,HPLC测定质量分数≥98%,上海铭睿生物有限公司;水溶性月桂氮 酮(azone,AZ),砀山县龙精细化工有限公司;N-甲基-2-吡咯烷酮(N-methyl-2-pyrrolidone,NMP),西陇化工股份有限公司;薄荷脑(menthol)、1,2-丙二醇(propylene glycol,PG),天津市致远化学试剂有限公司;色谱级甲醇,美国Sigma公司;水为超纯水;其他试剂为分析级。
酮(azone,AZ),砀山县龙精细化工有限公司;N-甲基-2-吡咯烷酮(N-methyl-2-pyrrolidone,NMP),西陇化工股份有限公司;薄荷脑(menthol)、1,2-丙二醇(propylene glycol,PG),天津市致远化学试剂有限公司;色谱级甲醇,美国Sigma公司;水为超纯水;其他试剂为分析级。
昆明种小鼠,体质量(20±2)g,雌性,昆明医科大学实验动物中心提供;猪,体质量(30±2)kg,雌性,购于当地屠宰场。
2 方法与结果 2.1 分析方法的建立2.1.1 色谱条件 岛津LC-20AB高效液相色谱仪,Thermo Scientific Hypersil GOLD C18色谱柱(250 mm×4.6 mm,5 μm);流动相为0.3%四丁基氢氧化铵(A)-甲醇(B)(磷酸调pH值为4.0),梯度洗脱:0~15 min,15%~20% A;15~25 min,20%~15% A;体积流量1 mL/min;进样量10 μL;柱温25 ℃;检测波长220 nm。
2.1.2 线性关系考察取适量三七素对照品,精密称定,用水定容于10 mL量瓶中,制成质量浓度为0.88 mg/mL的三七素对照品储备液。精密吸取储备液2、20、100、400、1 000 μL加水分别配制成质量浓度为1.76、17.60、88.00、176.00、352.00、880.00 μg/mL三七素对照品溶液。分别精密吸取上述对照品溶液10 μL,按“2.1.1”项色谱条件测定。以峰面积积分值为纵坐标(Y),质量浓度为横坐标(X)进行线性回归,得三七素的回归方程为Y=2×106 X-3 079,r=0.999 3,表明三七素在1.76~880.00 μg/mL线性关系良好。
2.1.3 供试品溶液的制备将体外经皮实验取出的接收液用0.45 μm微孔滤膜滤过,即得供试品溶液。
2.1.4 精密度试验精密称取“2.1.2”项下880.00 μg/mL对照品溶液,连续进样6次,进样体积10 μL,记录峰面积,结果三七素峰面积的RSD为0.78%,表明仪器的精密度良好。
2.1.5 重复性试验取三七素对照品溶液5份,经体外皮肤实验的接收液,按上述色谱条件测定峰面积,计算RSD值为3.58%(n=5),结果表明该方法的重复性良好。
2.1.6 稳定性试验取同一供试品溶液,按照上述色谱条件分别于0、1、2、4、8、12、24、36、48 h进样,每次10 μL,按“2.1.1”项下色谱条件测定三七素峰面积,计算其RSD为0.94%,结果表明供试品溶液中三七素在48 h内稳定性良好。
2.1.7 加样回收率试验精密称取已知质量浓度三七素供试品1 mL,分别加入88.00、35.20、17.60 μg/mL三七素对照品溶液1 mL,配制成2 mL溶液,按上述液相条件进样10 μL,测定峰面积,按回归方程计算回收率,结果平均回收率为98.4%,RSD为2.1%。
2.1.8 三七素的测定分别取三七素对照品溶液、三七素透皮接收液以及空白皮肤接收液各10 μL,按“2.1.1”项下色谱条件测定,色谱图见图 1。
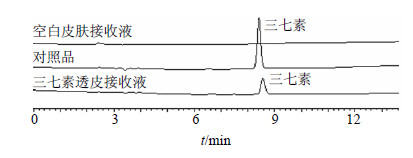 | 图 1 三七素透皮吸收HPLC对比色谱图Fig.1 Comparison on dencichine transdermal absorption by HPLC |
称取过量的三七素对照品于25 mL锥形瓶中,加入超纯水14 mL,超声30 min,配制过饱和溶液,并于36.5 ℃下350 r/min搅拌24 h后,使达到饱和状态,量取1 mL上述溶液4份,在3 000 r/min条件下离心5 min,取上清液,0.45 μm微孔滤膜滤过,按“2.1”项下方法测定。结果得到三七素表观溶解度为(981.04±17.61)mg/mL。
2.2.2 三七素油水分配系数的测定精密称取三七素过饱和溶液5 mL,加入正辛醇5 mL,摇匀,超声10 min,并于37 ℃摇床中闭光振动24 h,静置至溶液分层,取下层1 mL,过0.45 μm微孔滤膜,按“2.1.1”项下色谱条件测定三七素质量浓度。根据公式P=(C0-Cw)/Cw(其中C0为药物在水相中的原始质量浓度,Cw为萃取后药物在水相中的质量浓度)计算三七素油水分配系数为lgP=−1.66±0.04。
2.3 三七素体外经皮渗透实验 2.3.1 供试皮肤制备取昆明种小鼠剪去腹部毛发,处死后剥离腹部皮肤,去除皮下脂肪及黏液组织,用生理盐水清洗,拭干。另取猪耳背皮肤,去除皮下脂肪、组织,用生理盐水清洗,拭干。放置−20 ℃冰箱冷藏备用。实验前24 h先将小鼠皮及猪皮在室温下自然解冻,用生理盐水清洗干净,用滤纸吸干表面水分,并在实验前对皮肤完整性和均匀性进行检查。
2.3.2 供试药液制备取一定量的三七素对照品,用水溶解制成一定质量浓度的供试药液(约为0.7 mg/mL)。
2.3.3 三七素溶液经皮肤渗透实验[11]将处理好的皮肤(小鼠皮、猪皮)固定于Franz扩散池中,角质层面向供药池,并以配套的铁夹夹紧2个半池,在接收池中加入0.01 mol/L的PBS(pH 7.4)溶液15 mL,加入磁子,池内温度控制为36.5 ℃,恒温磁力搅拌,加样前平衡30 min,排除接收池中气泡。分别在实验开始的0.5、1、2、4、6、8、10、12 h时取样1 mL,每次取样完毕后,补加等体积、等温度的PBS于接收池中。将已经取好的样品过0.45 μm微孔滤膜,待HPLC液相检测。按下列公式计算单位面积累积渗透量(Q,mg∙cm−2),结果见表 1。
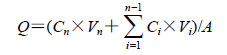
Cn、Ci为第n个和第i个取样点测得的药物质量浓度,Vn为扩散池体积(15.0 mL),Vi为每次取样的体积(1.0 mL),A为皮肤扩散面积(1.327 cm2)
| 表 1 三七素的Q(x±sn = 3) Table 1 Q of dencichine(x±sn = 3) |
对三七素在不同皮肤下不同时间点Q进行零级方程(Qt/Q∞=kt拟合)、一级方程[ln(Q-Qt)=lnQ∞-kt]以及Higuchi方程拟合(Qt/Q∞=kt1/2),结果见表 2。通过3种拟合动力学方程线性关系及相关系数可知,三七素过饱和溶液在0~12 h内小鼠皮的Qt/Q∞与t1/2拟合度最高,因此三七素溶液体外透皮吸收方程符合Higuchi方程。
| 表 2 三七素经皮渗透动力学拟合方程 Table 2 Fitting percutaneous dynamic equation of dencichine |
三七素溶液在小鼠皮和猪皮的Q、稳态流量(J,mg∙cm−2∙h−1/2)、渗透系数(Pm,cm∙h−1/2)的考察,结果见表 3。根据Higuchi曲线斜率计算J和Pm(Pm=J/C,C为供试溶液质量浓度),结果可知,三七素在小鼠皮中渗透效果高于猪皮。
| 表 3 三七素经皮渗透动力学参数 (x±s, n = 3) Table 3 |
| 表 4 促渗剂对三七素的Q的影响(x±s, n = 3) Table 4 Effect of permeation enhancers on cumulative transdermal amount of dencichine(x±s, n = 3) |
| 表 5 促渗剂经皮渗透动力学参数(x±s, n = 3) Table 5 Percutaneous penetration parameters with permeation enhancers(x±s, n = 3) |
的促渗剂NMP进行不同浓度渗透性考察[11],发现3种用量NMP促渗剂对三七素均有促渗作用,其促渗能力大小为5% NMP>3% NMP>1% NMP。对不同促渗剂和不同用量NMP促渗剂时间点Q进行Higuchi方程拟合(表 6),结果表明相关系数(r)均在0.98以上。
| 表 6 不同促渗剂的方程拟合表达式(x±s, n = 3) Table 6 Equation fitting expression with different permeation enhancers(x±s, n = 3) |
经皮给药是由皮肤吸收进入全身血液循环[13, 14, 15],而皮肤表面可视角质层是亲脂性很强的生物膜,药物的理化性质对经皮吸收能力有决定性作用。通常来说,相对分子质量小,lgP值在2~3的药物具有较好的经皮渗透特性。三七素是一种特殊的非蛋白质氨基酸,相对分子质量小,为176.13;溶解度大,表观溶解度为981.04 mg/mL;lgP值小,为−1.66±0.04,说明三七素亲水性强,对生物膜的渗透作用较弱。三七素虽然相对分子质量较小,有利于透过皮肤障碍,但是其lgP值很小,与皮肤相容性很差,因此,不易透过角质层。
皮肤的渗透系数只与药物性质和皮肤性质有关,值越大,则药物的经皮渗透越容易。小鼠皮和猪皮是药物经皮渗透研究中2种常用的皮肤模型。据文献报道,猪皮的角质层厚度约为26 μm,而小鼠皮角质层厚度仅为6 μm左右[16]。三七素在小鼠皮J为0.027 mg∙cm−2∙h−1/2,经皮Pm为0.039 cm∙h−1/2;而猪皮J仅为0.008 mg∙cm−2∙h−1/2,相对应的经皮Pm值为0.011 cm∙h−1/2,说明三七素在小鼠皮透皮能力强于猪皮。同时,猪皮表面含油脂成分高,猪皮角质层厚于小鼠皮,水溶性物质三七素难从猪皮角质层中渗透过去[17, 18, 19]。各种动物之间的解剖差异很大,不同动物的角质层厚度、单位面积汗腺数量与毛孔数量等均不同。本实验表明,三七素在小鼠皮中具有更好的经皮渗透特性。
通过考察三七素溶液体外渗透曲线,反映了三七素在皮肤的渗透特征[20]。采用零级、一级以及Higuchi方程对渗透曲线进行拟合,以相关系数作为评判标准,得出Higuchi方程>一级方程拟合>零级方程。Higuchi模型是基于Fick扩散定律的药物释放模型,是目前常见药物释放模型中应用最多的一种。皮肤是药物经皮渗透的主要屏障,药物经皮吸收速率往往被皮肤的屏障作用所限制。皮肤作为药物贮库和限速膜,三七素在其中的扩散速率和扩散行为决定了药物的经皮吸收能力[21, 22]。因此,三七素的体外经皮吸收可看作从通过皮肤限速膜的扩散与释放,三七素在皮肤中的扩散模型与Higuchi方程拟合较好。
为了增加三七素在皮肤上的通透性,选择了4种不同的促渗剂进行促渗作用评价,发现NMP对三七素的透皮吸收具有促进作用,说明NMP能够改变三七素在皮肤溶解性,促进药物在角质层的通透性。通过Higuchi方程拟合,r为0.990 4。5% NMP的Q达到0.637 mg/cm2,与对照组0.338 mg/cm2相比,增加了近1倍,Pm为0.131 cm/h1/2、J为0.187 mg∙cm−2∙h−1/2。
| [1] | 张 梅, 宋 芹, 钟 华, 等. 三七水凝胶透皮贴剂的初步研究[J]. 成都中医药大学学报, 2005, 28(3): 60-61. |
| [2] | 白志华, 方晓玲. 三七总皂苷中人参皂苷Rg1体外透皮吸收的实验研究[J]. 中成药, 2006, 28(5): 639-642. |
| [3] | 徐 白, 沈蕴琪, 方晓玲, 等. 三七总皂苷复方脂质体凝胶剂的制备及皮肤给药研究[J]. 中国临床药学杂志, 2007, 16(3): 144-148. |
| [4] | 方 蓉, 郑杭生, 陈思思. 离体皮肤渗透法测定三七总皂苷传递体经皮吸收特性[J]. 中草药, 2015, 46(4): 513-519. |
| [5] | Kosuge T, Yokota M, Ochiai A. Studies on antihemorrhagic principles in the crude drugs for hemostatics. II. On antihemorrhagic principle in Sanchi Ginseng Radix[J]. Yakugaku Zasshi, 1981, 101(7): 629-632. |
| [6] | 张玉萍, 余 琼. 三七素的止血活性及其神经毒作用实验研究[J]. 山东中医杂志, 2010(29): 43-45. |
| [7] | 王 珍, 杨靖亚, 宋书杰, 等. 三七素对凝血功能的影响及止血机制[J]. 中国新药杂志, 2014, 32(3): 356-359. |
| [8] | 郑 璐, 郑 健, 刘庆荣, 等. 红参中水溶性成分三七素的生理活性研究[J]. 中成药, 2001, 23(12): 905-906. |
| [9] | 山丽梅, 赵艳玲, 肖小河, 等. 三七止血活性与商品规格划分的相关分析[J]. 中草药, 2011, 42(9): 1779-1783. |
| [10] | 刘 然. 辣椒素理化性质及体外透皮性能的研究[J]. 中国药学杂志, 2012, 47(24): 2008-2011. |
| [11] | 胡 晓. 不同促渗剂对复方积雪草苷凝胶膏剂透皮吸收的影响[J]. 中国医院药学杂志, 2013, 33(7): 543-537. |
| [12] | 刘婷婷. 不同促渗剂对盐酸利多卡因巴布剂透皮吸收的影响[J]. 中国医院药学杂志, 2008, 28(3): 198-200. |
| [13] | 张 定, 王承潇, 韩 伟, 等. 咪唑类离子液体对三七中痕量成分人参皂苷Rh1的体外经皮促渗作用研究[J]. 中草药, 2014, 45(20): 2917-2923. |
| [14] | 许文佳, 赵修华, 祖元刚, 等. 反溶剂法制备甘草酸纳米粒的表征与体外透皮特性研究[J]. 中草药, 2014, 45(8): 1068-1071. |
| [15] | 郑 银, 王亚静. 芒果苷脂质体的理化性质和体外经皮渗透性能的研究[J]. 现代药物与临床, 2014, 29(2): 147-150. |
| [16] | 郑俊民. 经皮给药新剂型 [M]. 北京: 人民卫生出版社, 2006. |
| [17] | 王胜春. 透皮速率测定中影响透皮吸收的因素[J]. 国外医药, 1989, 10(2): 99-101. |
| [18] | 贾卫哺, 张 嫣, 李 楠. 甲硝唑经皮给药制剂的体外质量守恒研究[J]. 中药药业, 2012, 21(23): 10-12. |
| [19] | 汪 静. 卡波三醇软膏皮肤渗透研究 [D]. 长春: 吉林大学, 2013. |
| [20] | 段 红, 翟科峰, 邢建国. 雪莲巴布剂体外透皮特性的研究[J]. 时珍国医国药, 2011, 22(3): 637-638. |
| [21] | 张玲莉, 王 军, 何 文, 等. 盐酸青藤碱醇质体凝胶与脂质体凝胶体外经皮渗透动力学比较研究[J]. 中国药师, 2012, 15(12): 1678-1681. |
| [22] | 郭咸希, 何 文. 尼美舒利脂质体凝胶的研制及体外经皮渗透动力学考察[J]. 中国药学杂志, 2008, 43(1): 35-39. |
 2015, Vol. 46
2015, Vol. 46


