人参Panax ginseng C. A. Mey. 系五加科(Araliaceae)人参属Panax L. 多年生草本植物,传统用药部位主要为根和根茎,其有效成分主要为自然界中分布较少的达玛烷型(dammarane type)四环三萜,多与不同的糖基键合成苷,即人参皂苷(ginsenoside),具有独特、新颖、多样性的化学结构。迄今已从生药人参根和根茎及其商品人参中分离鉴定了70余个三萜类化合物[1],并发现报道了多种生物学活性和临床应用[2],因而,寻找人参皂苷的新资源具有重要的意义。《中国药典》2010年版一部在植物提取物项下收载了人参茎叶总皂苷提取物,研究表明人参茎叶中的人参皂苷在组成上与人参根和根茎中的人参皂苷有一定的差异[3, 4, 5, 6]。为了获得多样性的人参三萜类化合物药物先导结构并为人参茎叶皂苷的体内分析奠定基础,本实验模拟人胃内酸性条件,对人参茎叶总皂苷酸水解产物进行了研究,分离鉴定了34个化合物,代表性结构如图 1。
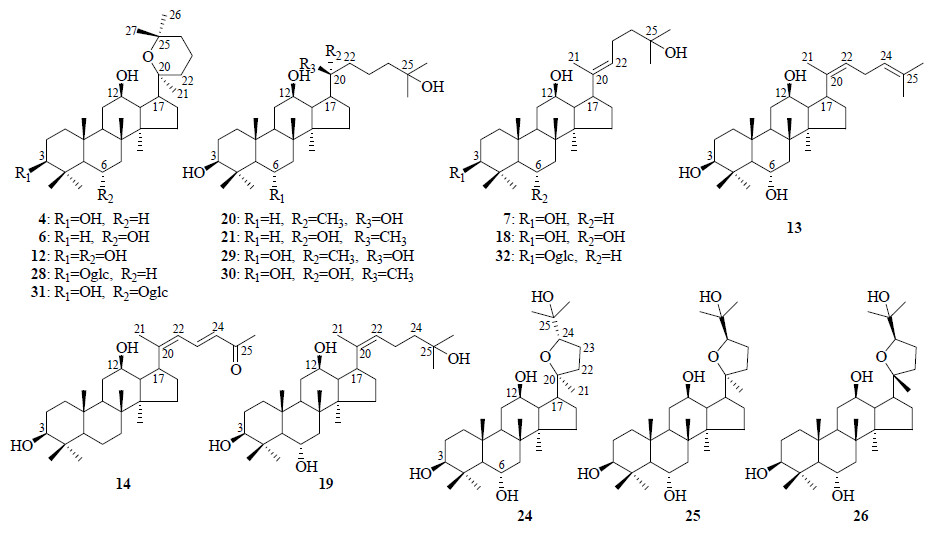 | 图 1 人参茎叶皂苷酸水解产物代表性化合物的结构Fig.1 Structures of typical compounds in acid hydrolysates from stems and leaves of P. ginseng |
Bruker AV 400型核磁共振波谱仪(Bruker BioSpin AG Facilities,Fällanden,Switzerland);MDS SCIEX API QSTAR低分辨质谱仪(Applied Biosystems/ MDS Sciex.,Foster City,CA,USA)。X-4数字显示显微熔点测定仪(北京泰克仪器有限公司);半制备型高效液相色谱(SP-HPLC)仪为CXTH 3000型(北京创新通恒科技发展有限公司),配置UV3000检测器、P3050二元泵、CXTH-3000色谱工作站、Daisogel C18色谱柱(250 mm×30 mm,10 μm),紫外检测波长为203 nm,体积流量为15或10 mL/min。柱色谱硅胶(200~300目)和薄层色谱(TLC)硅胶板GF254(0.20~0.25 mm)均为青岛海洋化工厂产品;分析纯三氯甲烷、甲醇(MeOH)均为北京化工厂产品,色谱纯MeOH和乙腈(MeCN)均为天津西华特种试剂厂产品;水为娃哈哈纯净水,用时经Millipore Milli-Q水处理系统进一步处理。
人参茎叶样品于2008年8月采自吉林省集安县,经北京大学杨秀伟教授鉴定为五加科人参属植物人参Panax ginseng C. A. Mey. 的干燥茎和叶。凭证标本(2008001)存放于北京大学药学院天然药物及仿生药物国家重点实验室。
2 提取与分离人参茎叶总皂苷按照专利方法[7]制备。主要操作流程:取干燥人参茎叶粗粉(15 kg),水煎煮3次,第1次加水量为300 L,煎煮3 h;第2次加水量为225 L,煎煮3 h;第3次加水量为150 L,煎煮1.5 h;合并煎液,滤过,浓缩至2∶1(生药∶浓缩液,折算成冻干物为2 625 g)时,加入氯化钠(使达饱和)盐析,放置6 h,滤过,冻干,得人参茎叶总皂苷(210 g)。取人参茎叶总皂苷200 g,用5%硫酸乙醇液(3 L)回流水解2 h,水解液用氢氧化钠溶液中和至中性,用等体积的醋酸乙酯萃取6次,减压浓缩后得水解产物(121.4 g)。水解产物(100 g)经硅胶柱色谱分离,石油醚-丙酮(15∶1→1∶1)梯度洗脱,TLC检测合并相同组分,得到7个流分,分别为Fr. 1(5.6 g)、Fr. 2(16.2 g)、Fr. 3(5.5 g)、Fr. 4(24.3 g)、Fr. 5(13.2 g)、Fr. 6(14.5 g)、Fr. 7(7.5 g)。
Fr. 1(5.6 g)经硅胶柱色谱分离,石油醚-丙酮(15∶1→5∶1)梯度洗脱,TLC检测合并相同的组分,得到3个流分Fr. 1-1~1-3。Fr. 1-1(670 mg)经硅胶柱色谱分离,石油醚-丙酮(15∶1→5∶1)梯度洗脱,得到化合物1(80 mg)、2(80 mg)、3(220 mg);Fr. 1-2(3.2 g)用丙酮反复重结晶得到化合物4(2.5 g);Fr. 1-3(400 mg)经SP-HPLC分离,MeCN-H2O(70∶30)洗脱,得到化合物5(tR=36 min,30 mg)和6(tR=72 min,8 mg)。
Fr. 2(16.2 g)经SP-HPLC分离,MeOH-H2O(85∶15)洗脱,得到7个流分Fr. 2-1~2-7。Fr. 2-1(1.2 g)经SP-HPLC分离,MeCN-H2O(75∶35)洗脱,得到化合物7(tR=69 min,560 mg)和8(tR=72 min,50 mg);Fr. 2-2(410 mg)经SP-HPLC分离,MeOH-H2O(70∶30)洗脱,得到化合物9(tR= 175 min,15 mg)和10(tR=195 min,120 mg);Fr. 2-3(50 mg)经SP-HPLC纯化,MeCN-H2O(55∶45)洗脱,得到化合物11(tR=89 min,10 mg);Fr. 2-4(8.1 g)用丙酮反复重结晶,得到化合物12(7.5 g);Fr. 2-5(150 mg)经SP-HPLC分离,MeCN-H2O(55∶45)洗脱,得到化合物13(tR=91 min,20 mg)和14(tR=208 min,8 mg);Fr. 2-6(150 mg)经SP-HPLC纯化,MeCN-H2O(45∶55)洗脱,得到化合物15(tR=253 min,40 mg);Fr. 2-7(220 mg)经SP-HPLC纯化,MeCN-H2O(45∶55)洗脱,得到化合物16(tR=56 min,8 mg)。
Fr. 3(5.5 g)经SP-HPLC分离,MeOH-H2O(85∶15)洗脱,得到3个流分Fr. 3-1~3-3。Fr. 3-2(450 mg)经SP-HPLC纯化,MeCN-H2O(40∶60)洗脱,得到化合物17(tR=88 min,10 mg);Fr. 3-3(2.5 g)经SP-HPLC分离,MeCN-H2O(40∶60)洗脱,得到化合物18(tR=89 min,1 g)和19(tR=98 min,48 mg)。
Fr. 4(24.3 g)经SP-HPLC分离,MeOH-H2O(75∶25)洗脱,得到4个流分Fr. 4-1~4-4。Fr. 4-1(1.5 g)经SP-HPLC分离,MeCN-H2O(50∶50)洗脱,得到化合物20(tR=149 min,60 mg)和21(tR=161 min,20 mg);Fr. 4-2(5.1 g)经SP-HPLC分离,MeCN-H2O(50∶50)洗脱,得到化合物22(tR=74 min,14 mg)和23(tR=85 min,180 mg);Fr. 4-3(2.1 g)经SP-HPLC分离,MeCN- H2O(35∶65)洗脱,得到化合物24(tR=74 min,60 mg)、25(tR=86 min,50 mg)和26(tR=95 min,40 mg);Fr. 4-4(760 mg)经SP-HPLC纯化,MeCN-H2O(22∶78)洗脱,得到化合物27(tR=9 min,180 mg)。
Fr. 5(13.2 g)经SP-HPLC分离,MeOH-H2O(75∶25)洗脱,得到4个流分Fr. 5-1~5-4。Fr. 5-1(1.05 g)经SP-HPLC纯化,MeCN-H2O(65∶35)洗脱,得到化合物28(tR=90 min,13 mg);Fr. 5-2(4.5 g)经SP-HPLC分离,MeCN-H2O(35∶65)洗脱,得到化合物29(tR=49 min,200 mg)和30(tR=60 min,1 g)。
Fr. 6(14.5 g)SP-HPLC分离,MeOH-H2O(75∶25)洗脱,得到6个流分Fr. 6-1~6-6。Fr. 6-3(450 mg)经SP-HPLC纯化,MeCN-H2O(40∶60)洗脱,得到化合物31(tR=31 min,11 mg);Fr. 6-4(2.1 g)经SP-HPLC纯化,MeCN-H2O(42∶58)洗脱,得到化合物32(tR=60 min,13 mg)。
Fr. 7(7.5 g)经SP-HPLC分离,MeOH-H2O(75∶25)洗脱,得到4个流分Fr. 7-1~7-4。Fr. 7-2(1.3 g)经SP-HPLC分离,MeCN-H2O(35∶65)洗脱,得到化合物33(tR=38 min,9 mg)和34(tR=45 min,13 mg)。
3 结构鉴定化合物1~34在TLC板上展开后喷雾10%硫酸乙醇试液均显紫色斑点;Libermann-Burchard反应阳性,提示它们均为三萜类化合物。
化合物1:白色无定形粉末(丙酮);mp 215~217 ℃;ESI-MS m/z: 503.4 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 4.68 (1H, m, H-3α), 3.78 (1H, m, H-12α), 1.32 (3H, s, H-28), 1.23 (6H, s, H-26, 27), 1.02 (3H, s, H-21), 0.91 (6H, s, H-18, 29), 0.90 (3H, s, H-19), 0.84 (3H, s, H-30);13C-NMR谱中共给出32个碳信号,4个连氧碳信号δC 81.9, 78.1, 71.4, 74.3;δ 170.6和22.4为1组乙酰基信号,δC 81.9 (C-3) 在较低场,提示乙酰基连接在C-3位;13C-NMR数据见表 1,为首次报道。参照文献报道[8],鉴定化合物1为3β-乙酰氧基-12β-羟基-20(R),25-环氧达玛烷。
| 表 1 化合物1~6、8、12、15、27的13C-NMR数据 (C5D5N) Table 1 13C-NMR data of compounds 1—6, 8, 12, 15, and 27(C5D5N) |
化合物2:白色无定形粉末(丙酮);mp 285~287 ℃;ESI-MS m/z: 583.4 [M+Na]+。1H-NMR (400 MHz, C5D5N) δ: 5.54 (1H, td, J = 11.0, 4.4 Hz, H-6β), 4.63 (1H, m, H-3α), 3.71 (1H, m, H-12α), 1.22 (3H, s, H3-28), 1.16 (3H, s, H-21), 1.15 (3H, s, H-26), 1.14 (3H, s, H-27), 1.11 (3H, s, H-18), 0.98 (3H, s, H-29), 0.88 (3H, s, H-19), 0.87 (3H, s, H-30);13C-NMR谱中共给出34个碳信号,有2组乙酰基信号δC 170.0, 21.0和170.6, 21.8,5个连氧碳信号δC 80.1, 76.8, 73.0, 70.5, 69.9;δC80.1 (C-3) 和70.5 (C-6) 在较低场,提示乙酰基分别连接在C-3和C-6位;13C-NMR数据见表 1。参照文献报道[9],鉴定化合物2为3β,6α-二乙酰氧基-12β-羟基-20(R),25-环氧达玛烷。
化合物3:白色无定形粉末(丙酮);mp 227~229 ℃;ESI-MS m/z: 519.4 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 4.70 (1H, m, H-3α), 4.28 (1H, td, J = 10.8, 3.4 Hz, H-6β), 3.70 (1H, m, H-12α), 1.57 (3H, s, H-28), 1.25 (3H, s, H-21), 1.21 (3H, s, H-26), 1.16 (3H, s, H-27), 1.15 (3H, s, H-18), 1.03 (3H, s, H-29), 0.91 (3H, s, H-19), 0.87 (3H, s, H-30);13C-NMR谱中共给出32个碳信号,5个连氧碳信号δC 81.5, 77.2, 73.4, 70.5, 67.7;1组乙酰基碳信号δC 171.0, 21.5,与化合物1相同,连接在C-3位,13C-NMR数据见表 1。参照文献报道[9],鉴定化合物3为3β-乙酰氧基-6α,12β-二羟基-20(R),25-环氧达玛烷。
化合物4:白色无定形粉末(丙酮);mp 208~210 ℃;ESI-MS m/z: 483.4 [M+Na]+。1H-NMR (400 MHz, C5D5N) δ: 3.77 (1H, m, H-12α), 3.44 (1H, m, H-3α), 1.28 (3H, s, H-28), 1.25 (3H, s, H-21), 1.24 (6H, s, H-26, 27), 1.05 (3H, s, H-18), 1.02 (3H, s, H-29), 0.92 (3H, s, H-19), 0.91 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,4个连氧碳信号δC 78.0, 76.9, 73.0, 70.2;13C-NMR数据见表 1。参照文献报道[10],鉴定化合物4为20(R)-人参二醇。
化合物5:白色无定形粉末(甲醇);mp 219~221 ℃;ESI-MS m/z: 457.6 [M-H]−;1H-NMR (400 MHz, C5D5N) δ: 4.36 (1H, m, H-6β), 3.71 (1H, m, H-12α), 3.48 (1H, m, H-3α), 1.94 (3H, s, H-28), 1.41 (3H, s, H-29), 1.18 (3H, s, H-27), 1.03 (3H, s, H-18), 0.96 (3H, s, H-30), 0.86 (3H, s, H-19), 0.80 (3H, s, H-21);13C-NMR谱中共给出30个碳信号,4个连氧碳信号δC78.5, 74.2, 71.2, 68.0;δC61.7 (C-5), 67.7 (C-6) 提示该化合物为人参三醇型皂苷元;13C-NMR数据见表 1。参照文献报道[11],鉴定化合物5为异去氢原人参三醇。
化合物6:白色无定形粉末(甲醇);mp 242~244 ℃;ESI-MS m/z: 473.5 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 4.22 (1H, m, H-6β), 3.76 (1H, m, H-12α), 1.70 (3H, s, H-28), 1.68 (3H, s, H-21), 1.29 (3H, s, H-26), 1.24 (3H, s, H-27), 1.22 (3H, s, H-18), 0.94 (3H, s, H-29), 0.94 (3H, s, H-19), 0.84 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,其中含1个羰基碳信号δC218.9,其碳谱数据与20(R)-人参三醇对比,发现仅在C-3位差异较大;13C-NMR数据见表 1。参照文献报道[12],鉴定化合物6为3-酮基-6α,12β-二羟基-20(R),25-环氧达玛烷。
化合物7:白色无定形粉末(甲醇);mp 244~246 ℃;ESI-MS m/z: 461.4 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 5.55 (1H, t, J = 7.0 Hz, H-22), 3.88 (1H, m, H-12α), 3.39 (1H, m, H-3α), 1.78 (3H, s, H-21), 1.31 (6H, s, H-26, 28), 1.19 (3H, s, H-27), 1.02 (3H, s, H-18), 1.00 (3H, s, H-29), 0.90 (3H, s, H-19), 0.85 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,包括3个连氧碳信号δC 78.3, 73.0, 69.9,1组双键碳信号δC 125.9, 139.9;δC56.8 (C-5) 提示该化合物为二醇型人参皂苷元;13C-NMR数据见表 2。参照文献报道[13],鉴定化合物7为达玛-(E)-20(22)-烯- 3β,12β,25-三醇。
| 表 2 化合物7、9、10、13、14、16、18、19、22~26的13C-NMR数据(C5D5N) Table 2 13C-NMR data of compounds 7, 9, 10, 13, 14, 16, 18, 19, and 22—26 (C5D5N) |
化合物8:白色无定形粉末(甲醇);mp 289~291 ℃;ESI-MS m/z: 517.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.62 (1H, m, H-6β), 3.70 (1H, m, H-12α), 3.40 (1H, m, H-3α), 1.52 (3H, s, H-28), 1.21 (3H, s, H-21), 1.17 (3H, s, H-26), 1.14 (3H, s, H3-27), 1.13 (3H, s, H-18), 1.12 (3H, s, H-29), 0.94 (3H, s, H-19), 0.86 (3H, s, H-30);13C-NMR谱中共给出32个碳信号,5个连氧碳信号δC 77.5, 76.8, 73.0, 71.0, 70.0;δC 170.2, 22.0为1组乙酰基信号;13C-NMR数据见表 1。参照文献报道[9],鉴定化合物8为6α-乙酰氧基-3β,12β-二羟基-20(R),25-环氧达玛烷。
化合物9:白色无定形粉末(甲醇);mp 238~240 ℃;ESI-MS m/z: 459.5 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.28 (1H, t, J = 7.2 Hz, H-24), 3.93 (1H, m, H-12α), 3.45 (1H, m, H-3α), 1.61 (3H, s, H-28), 1.59 (3H, s, H-21), 1.38 (3H, s, H-26), 1.19 (3H, s, H-27), 0.99 (3H, s, H-18), 0.97 (3H, s, H-29), 0.90 (3H, s, H-19), 0.85 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,3个连氧碳信号δC 78.3, 73.3, 71.4, δC 56.7 (C-5) 为典型的人参二醇型特征信号,δC55.2 (C-17), 27.2 (C-21), 36.3 (C-22) 为20(S) 构型的典型特征信号;13C-NMR数据见表 2。参照文献报道[14],鉴定化合物9为20(S)-原人参二醇。
化合物10:白色无定形粉末(甲醇);mp 245~247 ℃;ESI-MS m/z: 459.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.29 (1H, t, J = 7.8 Hz, H-24), 3.90 (1H, m, H-12α), 3.40 (1H, m, H-3α), 1.66 (3H, s, H-28), 1.62 (3H, s, H-21), 1.37 (3H, s, H-26), 1.20 (3H, s, H-27), 1.03 (3H, s, H-18), 1.01 (3H, s, H-29), 0.94 (3H, s, H-19), 0.88 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,由δC51.0 (C-17), 23.0 (C-21), 43.6 (C-22) 确定此化合物的C-20为R型;13C-NMR数据见表 2。参照文献报道[14],鉴定化合物10为20(R)-原人参二醇。
化合物11:白色无定形粉末(甲醇);mp 204~206 ℃;ESI-MS m/z: 505.7 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 3.89 (1H, m, H-12α), 3.39 (1H, m, H-3α), 1.37 (3H, s, H-28), 1.19 (3H, s, H-21), 1.13 (6H, s, H-26, 27), 1.02 (3H, s, H-18), 1.00 (3H, s, H-29), 0.92 (3H, s, H-19), 0.87 (3H, s, H-30);δH 1.09 (3H, t, J = 7.0 Hz) 归属为1个甲基,δH 3.30 (2H, t, J = 7.0 Hz) 归属为连氧亚甲基,提示该化合物分子结构中存在1个乙氧基。13C-NMR谱中共给出32个碳信号,羟基碳信号分别为δC78.0 (C-3), 74.3 (C-25), 71.0 (C-12), 73.2 (C-20);δC 56.8 (C-5) 为典型的人参二醇型特征信号;13C-NMR数据见表 3。参照文献报道[15],鉴定化合物11为20(S)-25-乙氧基-达玛烷-3β,12β,20-三醇。
| 表 3 化合物11、17、20、21、28~34的13C-NMR数据(C5D5N) Table 3 13C-NMR data of compounds 11, 17, 20, 21, and 28—34 (C5D5N) |
化合物12:白色无定形粉末(丙酮);mp 267~269 ℃;ESI-MS m/z: 477.5 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 3.77 (1H, m, H-12α), 3.53 (1H, m, H-3α), 4.39 (1H, m, H-6β), 1.97 (3H, s, H-28), 1.44 (3H, s, H-21), 1.27 (3H, s, H-26), 1.23 (3H, s, H-27), 1.22 (3H, s, H-18), 1.02 (3H, s, H-29), 1.00 (3H, s, H-19), 0.93 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,5个连氧碳信号δC 78.3, 76.8, 73.0, 70.0,67.6;δC 67.7 (C-6) 和61.7 (C-5) 提示该化合物为人参三醇型皂苷元;13C-NMR数据见表 1。参照文献报道[9],鉴定化合物12为20(R)-人参三醇。
化合物13:白色无定形粉末(甲醇);mp 135~137 ℃;ESI-MS m/z: 457.5 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.50 (1H, m, H-22), 5.24 (1H, m, H-24), 4.44 (1H, m, H-6β), 3.95 (1H, m, H-12α), 3.54 (1H, m, H-3α), 2.02 (3H, s, H-21), 1.84 (3H, s, H-28), 1.63 (3H, s, H-26), 1.59(3H, s, H-27), 1.47 (3H, s, H-29), 1.18 (3H, s, H-18), 1.03 (3H, s, H-30), 0.97 (3H, s, H-19);13C-NMR谱中共给出30个碳信号,δC 140.1, 123.2与δC 123.4, 131.5为2组双键信号;3个连氧碳信号δC78.8, 72.9, 68.0;δC61.8 (C-5) 的碳信号提示该化合物为人参三醇型皂苷元;13C-NMR数据见表 2。参照文献报道[16],鉴定化合物13为达玛-(E)-20(22),24-二烯-3β,6α,12β-三醇。
化合物14:白色无定形粉末(甲醇);mp 169~171 ℃;ESI-MS m/z: 441.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 7.67 (1H, dd, J = 15.4, 11.6 Hz, H-23), 6.29 (1H, d, J = 11.4 Hz, H-22), 6.19 (1H, d, J = 15.4 Hz, H-24), 3.94 (1H, m, H-12α), 3.61 (1H, m, H-3α), 2.25 (3H, s, H-27), 2.08 (3H, s, H-21), 1.25 (3H, s, H-28), 1.09 (3H, s, H-18), 1.06 (3H, s, H-29), 0.99 (3H, s, H-19), 0.92 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,1个羰基碳信号δC 198.4;δC 157.2, 123.1与δC140.8, 128.8为2组双键碳信号,δC 56.7 (C-5) 提示该化合物为人参二醇型皂苷元;13C-NMR数据见表 2。参照文献报道[17],鉴定化合物14为27-去甲基-(E,E)-20(22),23-二烯-3β,12β-二羟基达玛-25-酮。
化合物15:白色无定形粉末(甲醇);mp 211~213 ℃;ESI-MS m/z: 375.5 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 3.84 (1H, m, H-12α), 3.45 (1H, m, H-3α), 2.41 (3H, s, H-21), 1.24 (3H, s, H-28), 1.04 (3H, s, H-18), 1.00 (3H, s, H-29), 0.92 (3H, s, H-19), 0.86 (3H, s, H-30);13C-NMR谱中共给出24个碳信号,δC213.8为酮羰基碳信号,δC 56.8 (C-5) 提示该化合物为人参二醇型皂苷元;13C-NMR数据见表 1。参照文献报道[18],鉴定化合物15为3β,12β-二羟基- 22,23,24,25,26,27-六去甲达玛烷-20-酮。
化合物16:白色无定形粉末(甲醇);mp 243~245 ℃;ESI-MS m/z: 533.7 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 4.76 (1H, m, H-3α), 4.38 (1H, m, H-6β), 3.77 (1H, m, H-12α), 1.64 (3H, s, H-28), 1.46 (3H, s, H-21), 1.32 (9H, s, H3-18, H-26, 27), 1.14 (3H, s, H-29), 0.99 (3H, s, H-19), 0.95 (3H, s, H-30);13C-NMR谱中共给出32个碳信号,δC171.1, 21.5为乙酰基碳信号,δC81.5 (C-3) 在较低场,提示乙酰基连接在C-3位。参照文献报道[19],鉴定化合物16为3β-乙酰氧基-6α,12β,25-三羟基-(20S,24R)-环氧达玛烷。
化合物17:白色无定形粉末(甲醇);mp 217~219 ℃;ESI-MS m/z: 521.7 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 4.43 (1H, m, H-6β), 3.96 (1H, m, H-12α), 3.35 (1H, m, H-3α), 1.99 (3H, s, H-28), 1.45 (3H, s, H-21), 1.41 (3H, s, H-18), 1.18 (9H, s, H-26, 27, 29), 1.03 (3H, s, H-19), 0.99 (3H, s, H-30);δH1.14 (3H, t, J = 7.0 Hz) 归属为甲基峰,δH3.35 (2H, t, J = 7.0 Hz) 归属为连氧亚甲基,即该化合物分子结构中存在1个乙氧基。13C-NMR谱共给出32个碳信号,δC62.1 (C-5) 和68.1 (C-6) 为人参三醇型皂苷元的典型信号特征;13C-NMR数据见表 3。参照文献报道[15],鉴定化合物17为20(S)-25-乙氧基-达玛烷- 3β,6α,12β,20-四醇。
化合物18:白色无定形粉末(甲醇);mp 269~271 ℃;ESI-MS m/z: 475.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.61 (1H, t, J = 7.2 Hz, H-22), 4.44 (1H, m, H-6β), 3.96 (1H, m, H-12α), 3.56 (1H, m, H-3α), 2.01 (3H, s, H-21), 1.85 (3H, s, H-28), 1.47 (3H, s, H-18), 1.38 (6H, s, H-26, 27), 1.19 (3H, s, H-29), 1.04 (3H, s, H-19), 0.99 (3H, s, H-30);13C-NMR谱中共给出30个碳信号, δC 139.9和126.0为1组双键碳信号,δC 78.8, 73.0, 69.9和68.1为连氧碳信号;13C-NMR数据见表 2。参照文献报道[20],鉴定化合物18为达玛-(E)-20(22)-烯-3β,6α,12β,25-四醇。
化合物19:白色无定形粉末(甲醇);mp 275~277 ℃;ESI-MS m/z: 475.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.35 (1H, t, J = 7.2 Hz, H-22), 4.44 (1H, m, H-6β), 3.92 (1H, m, H-12α), 3.55 (1H, m, H-3α), 2.00 (3H, s, H-21), 1.95 (3H, s, H-28), 1.46 (3H, s, H-18), 1.41 (6H, s, H-26, 27), 1.18 (3H, s, H-29), 1.03 (3H, s, H-19), 0.99 (3H, s, H-30);13C-NMR数据见表 2。根据文献报道[21, 22],13C-NMR谱中,当C-20(22) 为E时,C-21的化学位移为δC 10~13,当C-20(22) 为Z时,C-21的化学位移为δC 20~30。化合物19的C-21的化学位移值为δC 19.6,其余碳谱数据与化合物18基本一致,因此确定化合物19为18的顺反异构体,即达玛-(Z)-20(22)-烯-3β, 6α,12β,25-四醇。
化合物20:白色无定形粉末(甲醇);mp 246~248 ℃;ESI-MS m/z: 477.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 3.94 (1H, m, H-12α), 3.45 (1H, m, H-3α), 1.45 (3H, s, H-28), 1.43 (3H, s, H-21), 1.42 (3H, s, H-26), 1.25 (3H, s, H-27), 1.08 (3H, s, H-18), 1.06 (3H, s, H-29), 0.96 (3H, s, H-19), 0.93 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC56.8 (C-5) 为人参二醇型皂苷元的特征性信号,δC55.1 (C-17), 27.7 (C-21) 和36.9 (C-22) 为20(S) 型人参皂苷元的特征性信号;13C-NMR数据见表 3。参照文献报道[23],鉴定化合物20为20(S)-达玛烷-3β, 12β,20,25-四醇。
化合物21:白色无定形粉末(甲醇);mp 250~252 ℃;ESI-MS m/z: 477.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 3.96 (1H, m, H-12α), 3.45 (1H, m, H-3α), 1.44 (9H, s, H-26, 27, 28), 1.26 (3H, s, H-21), 1.08 (3H, s, H-18), 1.06 (3H, s, H-29), 0.95 (3H, s, H-19), 0.93 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC56.7 (C-5) 为人参二醇型皂苷元的特征性信号,δC52.2 (C-17), 23.3 (C-21), 44.5 (C-22) 为20(R) 型人参皂苷元的特征性信号;13C-NMR数据见表 3。参照文献报道[24],鉴定化合物21为20(R)-达玛烷-3β,12β,20,25-四醇。
化合物22:白色无定形粉末(甲醇);mp 258~260 ℃;ESI-MS m/z: 475.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.25 (1H, t, J = 7.6 Hz, H-24), 4.42 (1H, m, H-6β), 3.86 (1H, m, H-12α), 3.53 (1H, m, H-3α), 2.00 (3H, s, H-28), 1.66 (3H, s, H-21), 1.63 (3H, s, H-26), 1.45 (3H, s, H-27), 1.42 (3H, s, H-18), 1.11 (3H, s, H-29), 1.00 (3H, s, H-19), 0.97 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,4个连氧碳信号δC 78.3, 73.3, 71.4, 68.0;δC 55.1 (C-17), 27.2 (C-21), 36.2 (C-22) 为20(S) 型人参皂苷元的特征性信号;13C-NMR数据见表 2。参照文献报道[25],鉴定化合物22为20(S)-原人参三醇。
化合物23:白色无定形粉末(甲醇);mp 261~263 ℃;ESI-MS m/z: 475.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.32 (1H, m, H-24), 4.44 (1H, m, H-6β), 3.97 (1H, m, H-12α), 3.53 (1H, m, H-3α), 2.00 (3H, s, H-28), 1.70 (3H, s, H-21), 1.66 (3H, s, H-26), 1.46 (3H, s, H-27), 1.41 (3H, s, H-18), 1.17 (3H, s, H-29), 1.03 (3H, s, H-19), 1.01 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC126.1 (C-24) 和130.8 (C-25) 为1组双键碳信号,δC 67.8 (C-6) 和61.8 (C-5) 为人参三醇型皂苷元的特征性信号,δC 50.7 (C-17), 22.6 (C-21), 43.3 (C-22) 为20(R) 型人参皂苷元的特征信号;13C-NMR数据见表 2。参照文献报道[25],鉴定化合物23为20(R)-原人参三醇。
化合物24:白色无定形粉末(甲醇);mp 199~201 ℃;ESI-MS m/z: 493.4 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 4.44 (1H, m, H-6β), 3.78 (1H, m, H-12α), 3.54 (1H, m, H-3α), 1.99 (3H, s, H-28), 1.45 (6H, s, H-21, 18), 1.32 (6H, s, H-26, 27), 1.17 (3H, s, H3-29), 1.06 (3H, s, H-19), 0.95 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC88.4, 87.1, 78.4, 70.9, 70.0, 67.8为6个连氧碳信号,δC61.9 (C-5), 67.8 (C-6) 提示该化合物为人参三醇型皂苷元;13C-NMR数据见表 2。参照文献报道[19],鉴定化合物24为 (20S,24S)-达玛烷-20,24-环氧-3β,6α, 12β,25-四醇。
化合物25:白色无定形粉末(甲醇);mp 198~200 ℃;ESI-MS m/z: 493.4 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 4.43 (1H, m, H-6β), 3.81 (1H, m, H-12α), 3.55 (1H, m, H-3α), 2.00 (3H, s, H-28), 1.46 (3H, s, H-21), 1.45 (6H, s, H-26), 1.35 (6H, s, H-27), 1.28 (3H, s, H-18), 1.13 (3H, s, H-29), 1.04 (3H, s, H-19), 0.98 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC 87.1, 86.1, 78.4, 70.7, 70.1, 67.7为6个连氧碳信号,δC 61.8 (C-5), 67.7 (C-6) 提示该化合物为人参三醇型皂苷元;13C-NMR数据见表 2。参照文献报道[25],鉴定化合物25为 (20S,24R)-达玛烷- 20,24-环氧-3β,6α,12β,25-四醇。
化合物26:白色无定形粉末(甲醇);mp 227~229 ℃;ESI-MS m/z: 493.4 [M+H]+。1H-NMR (400 MHz, C5D5N) δ: 4.44 (1H, m, H-6β), 3.79 (1H, m, H-12α), 3.55 (1H, m, H-3α), 2.01 (3H, s, H-28), 1.47 (6H, s, H-21), 1.46 (6H, s, H-26), 1.38 (3H, s, H-27), 1.28 (3H, s, H-18), 1.14 (3H, s, H-29), 1.04 (3H, s, H-19), 0.88 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC 86.6, 86.3, 78.8, 71.7, 70.9, 67.7为6个连氧碳信号,δC 62.2 (C-5) 和67.7 (C-6) 提示该化合物为人参三醇型皂苷元;13C-NMR数据见表 2。参照文献报道[26],鉴定化合物26为 (20R,24R)-达玛烷-20,24-环氧-3β,6α,12β,25-四醇。
化合物27:白色无定形粉末(甲醇);mp 233~235 ℃;ESI-MS m/z: 391.5 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 3.86 (1H, m, H-12α), 3.53 (1H, m, H-3α), 2.41 (3H, s, H-21), 2.00 (3H, s, H-28), 1.45 (3H, s, H-18), 1.11 (3H, s, H-29), 0.99 (3H, s, H-19), 0.95 (3H, s, H-30);13C-NMR谱中共给出24个碳信号,其中包括6个甲基碳信号,δC16.5, 17.0, 17.3, 17.7, 30.6, 32.0;δC213.3为酮羰基碳信号,δC 61.8 (C-5) 和67.6 (C-6) 提示该化合物为人参三醇型皂苷元;13C-NMR 数据见表 1。参照文献报道[16],鉴定化合物27为3β,6α,12β-三羟基-22,23,24,25,26,27-六去甲达玛烷-20-酮。
化合物28:白色无定形粉末(甲醇);mp 197~199 ℃;ESI-MS m/z: 621.8 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 4.45 (1H, m, H-3α), 3.78 (1H, m, H-12α), 1.34 (3H, s, H-28), 1.28 (3H, s, H-21), 1.23 (6H, s, H-26, 27), 1.02 (3H, s, H-18), 0.98 (3H, s, H-29), 0.94 (3H, s, H-19), 0.83 (3H, s, H-30);δH 4.63 (1H, d, J = 7.4 Hz) 归属为糖基的端基质子信号,较大的耦合常数证明该糖基为β构型;13C-NMR谱中共给出36个碳信号,δC107.4, 76.2, 79.2, 72.3, 78.8, 63.5为1组葡萄糖基的碳信号,δC56.7 (C-5) 证明其为人参二醇型人参皂苷;13C-NMR数据见表 3。参照文献报道[8],鉴定化合物28为12β-羟基-20(R), 25-环氧达玛烷-3β-O-β-D-吡喃葡萄糖苷。
化合物29:白色无定形粉末(甲醇);mp 247~249 ℃;ESI-MS m/z: 493.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 4.43 (1H, m, H-6β), 3.96 (1H, m, H-12α), 3.54 (1H, m, H-3α), 2.01 (3H, s, H-28), 1.47 (3H, s, H-21), 1.44 (3H, s, H-26), 1.41 (3H, s, H-27), 1.40 (3H, s, H-18), 1.19 (3H, s, H-29), 1.04 (3H, s, H-19), 0.98 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC 68.1 (C-6) 和62.1 (C-5) 为人参三醇型皂苷元的特征碳信号,δC 55.1 (C-17), 27.6 (C-21) 和36.8 (C-22) 为20(S) 型人参皂苷元的特征碳信号;13C-NMR数据见表 3。参照文献报道[26],鉴定化合物29为20(S)-达玛烷-3β,6α,12β,20,25-五醇。
化合物30:白色无定形粉末(甲醇);mp 258~260 ℃;ESI-MS m/z: 493.6 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 4.45 (1H, m, H-6β), 3.98 (1H, m, H-12α), 3.54 (1H, m, H-3α), 2.02 (3H, s, H-28), 1.48 (3H, s, H-21), 1.43 (9H, s, H-18, 26, 27), 1.18 (3H, s, H-29), 1.05 (3H, s, H-19), 0.98 (3H, s, H-30);13C-NMR谱中共给出30个碳信号,δC61.8 (C-5) 和67.8 (C-6) 为人参三醇型皂苷元的特征碳信号;δC51.7 (C-17), 22.8 (C-21), 44.1 (C-22) 为20(R) 型人参皂苷元的特征碳信号。参照文献报道[27],鉴定化合物30为20(R)-达玛烷-3β,6α,12β,20,25-五醇。
化合物31:白色无定形粉末(甲醇);mp 212~214 ℃;ESI-MS m/z: 637.8 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.73 (1H, m, H-6β), 3.97 (1H, m, H-12α), 3.52 (1H, m, H-3α), 1.26 (3H, s, H-28), 1.25 (3H, s, H-21), 1.22 (3H, s, H-26), 1.11 (3H, s, H-27), 1.06 (3H, s, H-18), 0.98 (3H, s, H-29), 0.87 (3H, s, H-19), 0.84 (3H, s, H-30);δH 4.69 (1H, d, J = 7.6 Hz) 为糖基的端基质子信号,较大的耦合常数证明该糖基为β构型;13C-NMR谱中共给出36个碳信号,δC106.4, 75.8, 80.3, 72.2, 78.9和63.5为1组葡萄糖基的碳信号,δC 61.8 (C-5) 证明其为人参三醇型皂苷;13C-NMR数据见表 3。参照文献报道[9],鉴定化合物31为20(R)-达玛烷-3β,6α,12β-三羟基-20,25-环氧- 6-O-β-D-吡喃葡萄糖苷。
化合物32:白色无定形粉末(甲醇);mp 159~161 ℃;ESI-MS m/z: 621.7 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.63 (1H, t, J = 7.6 Hz, H-22), 4.43 (1H, m, H-3α), 3.94 (1H, m, H-12α), 1.84 (3H, s, H-28), 1.38 (6H, s, H-26, 27), 1.34 (3H, s, H3-21), 1.04 (3H, s, H-18), 1.02 (3H, s, H-29), 0.99 (3H, s, H-19), 0.84 (3H, s, H-30);δH 4.97 (1H, d, J = 7.8 Hz) 为糖基的端基质子信号,较大的耦合常数证明糖基为β构型;13C-NMR谱中共给出36个碳信号,δC140.5和126.5为1组双键碳信号,δC 107.9, 76.7, 79.7, 72.8, 79.3和64.0为1组葡萄糖基碳信号,δC 57.3提示其为人参二醇型皂苷;13C-NMR数据见表 3。参照文献报道[28],鉴定化合物32为拟人参皂苷Rh2。
化合物33:白色无定形粉末(甲醇);mp 190~192 ℃;ESI-MS m/z 637.8 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.77 (1H, m, H-6β), 5.33 (1H, t, J = 7.8 Hz, H-24), 3.52 (1H, m, H-3α), 3.94 (1H, m, H-12α), 2.08 (3H, s, H-28), 1.68 (3H, s, H-21), 1.64 (3H, s, H-26), 1.60 (3H, s, H-27), 1.41 (3H, s, H-18), 1.21 (3H, s, H-29), 1.05 (3H, s, H-19), 0.85 (3H, s, H-30);δH 5.04 (1H, d, J = 7.4 Hz) 归属为糖基的端基质子信号,较大的耦合常数证明该糖基为β构型;13C-NMR谱中共给出36个碳信号,δC 131.4与126.7为1组双键碳信号,δC 106.1, 75.9, 80.4, 72.3, 80.0和63.5为1组葡萄糖基的碳信号;13C-NMR数据见表 3。参照文献报道[29],鉴定化合物33为20(S)-人参皂苷Rh1。
化合物34:白色无定形粉末(甲醇);mp 199~201 ℃;ESI-MS m/z: 637.8 [M-H]−。1H-NMR (400 MHz, C5D5N) δ: 5.78 (1H, m, H-6β), 5.32 (1H, t, J = 7.2 Hz, H-24), 3.99 (1H, m, H-12α), 3.55 (1H, m, H-3α), 2.09 (3H, s, H-28), 1.70 (3H, s, H-21), 1.65 (3H, s, H-26), 1.62 (3H, s, H-27), 1.41 (3H, s, H-18), 1.26 (3H, s, H-29), 1.08 (3H, s, H-19), 0.89 (3H, s, H-30);δH 5.05 (1H, d, J = 7.8 Hz) 归属为糖基的端基质子信号,较大的耦合常数证明该糖基为β构型;13C-NMR谱中共给出36个碳信号,与化合物33比较,二者仅在C-17、C-21和C-22有区别;13C-NMR数据见表 3。参照文献报道[29],鉴定化合物34为20(R)-人参皂苷Rh1。
4 结论与讨论上述34个化合物中,化合物1~3、6、8、11、17、24~26和32为首次在人参茎叶总皂苷酸水解产物中分离得到的人参三萜类化合物或其衍生物。结合本课题组对人参茎叶总皂苷组成的研究结果[3, 4, 5, 30],对上述34个化合物结构进行分析,发现人参茎叶皂苷在酸性条件下侧链易发生环合,从而生成人参二醇/三醇型皂苷元及其衍生物,并伴有构型的变化,即发生20S向20R差向异构体的转化。奥克梯隆(ocotillone)型皂苷为西洋参特有成分,除在人参叶中分离鉴定出伪人参皂苷RT5(pseudoginsenoside- RT5)[31]外,还未在人参中得到过,本实验分离得到10个奥克梯隆型三萜,即化合物1~6、8、12、28、31。近年来,对奥克梯隆型人参皂苷的研究表明其具有多种药理活性,如保护心脑血管及神经系统;拮抗吗啡身体依赖、精神依赖的形成;促智及预防老年痴呆等作用。但天然存在的奥克梯隆型三萜的量极低、分布狭窄,本研究结果为获取多样性结构的奥克梯隆型化合物并探讨其生物活性提供了一条资源途径。
人参根和根茎中的20(R/S)-原人参二醇和三醇及其皂苷,C-17侧链的C-24和C-25为双键[1, 32]。但人参茎叶中存在C-17侧链双键位置、数目变化多样的化合物[3, 4, 5, 30],其酸水解产物亦然。该类型化合物与红参[1]类似,此提示应开展人参茎叶皂苷与红参皂苷比较性研究,以发现共性问题,如生物活性异同、替代应用等。化合物18和32的C-17侧链C-20和C-22双键为E构型,而化合物19为Z构型。化合物18的C-21化学位移值为δC 13.5,化合物32的为δC13.9。化合物19的为δC 19.6,而其Z构型的为δC20.5[28]。以此为依据可相互区别。当C-17侧链为20(22),24-二烯时,2个双键未共轭,对C-21化学位移的影响不大,如化合物13的C-21化学位移值为δC 13.5。但在化合物14,C-17侧链为20(22), 23-二烯时,2个双键共轭,对C-21化学位移值有一定影响,此种情况为δC 15.2。
以具有抗癌活性的人参皂苷Rh2(32a)[33, 34, 35, 36, 37]为原料,半合成了拟人参皂苷Rh2(32)。包括32和 (Z)-20(22)-拟人参皂苷Rh2(32b)[28],在对8种人癌肿瘤细胞株SGC、HT1080、MCF-7、K562、HL-60、A375、A549、HeLa抗增殖活性实验中[28],发现32对这些肿瘤细胞株的增殖具有非常强的抑制作用,且大大强于32a和32b。对人胃癌细胞株SGC-7901抗增殖的机制之一为诱导线粒体介导的细胞凋亡[38]。本研究结果为32提供了一个新来源。同时,亦提示可通过人体消化道转化获取32,详细的研究工作正在进行中。
文献报道[39]肝微粒体和肝细胞可代谢20(S)-原人参二醇为 (20R,24R)-达玛-20(24)-环氧-3β,12β, 25-三醇,提示人参皂苷的代谢与人参皂苷的酸水解存在某种相似性。因此,本实验结果对于发现新颖结构的人参三萜类化合物并为更好地揭示人参皂苷的体内代谢过程、探索人参皂苷的代谢产物与人消化道之间的关系具有重要的指导意义。
| [1] | 杨鑫宝, 杨秀伟, 刘建勋. 人参中皂苷类化学成分的研究 [J]. 中国现代中药, 2013, 15(5): 349-358. |
| [2] | Jee H S, Chang K H, Park S H, et al. Morphological characterization, chemical components, and biofunctional activities of Panax ginseng, Panax quinquefolium, and Panax notoginseng roots: A comparative study [J]. Food Rev Intern, 2014, 30(2): 91-111. |
| [3] | Li K K, Yao C M, Yang X W. Four new dammarane-type triterpene saponins from the stems and leaves of Panax ginseng and their cytotoxicity on HL-60 cells [J]. Planta Med, 2012, 78(2): 189-192. |
| [4] | Li K K, Yang X W. Minor triterpene compounds from the stems and leaves of Panax ginseng [J]. Fitoterapia, 2012, 83(6): 1030-1035. |
| [5] | 李珂珂, 杨秀伟. 人参茎叶中1个新三萜类天然产物 [J]. 中草药, 2015, 46(2): 169-173. |
| [6] | 李珂珂, 杨秀伟. 人参茎叶化学成分的研究进展 [J]. 中国现代中药, 2012, 14(1): 47-50. |
| [7] | 李龙云, 田建明, 金 毅. 人参皂苷Rg2的制备方法, 其药物组合物及在制药中的应用: 中国, 100378119C [P]. 2008-04-02. |
| [8] | Atopkina L N, Denisenko V A. Glycosylation of panaxadiol [J]. Chem Nat Compd, 2011, 46(6): 892-896. |
| [9] | Atopkina L N, Denisenko V A. Synthesis of panaxatriol glucosides [J]. Chem Nat Compd, 2009, 45(5): 664-672. |
| [10] | Duc N M, Kasai R, Ohtani K, et al. Saponins from vietnamese ginsenoside, Panax vietnamensis HA et GRUSHV collected in central vietnam, III [J]. Chem Pharm Bull, 1994, 42(3): 634-640. |
| [11] | Wei Y, Ma C M, Hattori M. Anti-HIV protease triterpenoids from the acid hydrolysate of Panax ginseng [J]. Phytochem Lett, 2009, 2(2): 63-66. |
| [12] | Ookawa N, Aeba K, Ogawa N, et al. Anticancer substances prepared from materials extracted from medicinal plants or by organic synthesis method [P]. Jpn Kokai Tokkyo Koho, 1996, JP 08119866 A 19960514. |
| [13] | Tao L N, Meng Q, Yin J Y, et al. A new panaxadiol from the acid hydrolysate of Panax ginseng [J]. Chin Chem Lett, 2009, 20(6): 687-689. |
| [14] | 时圣明, 李 巍, 曹家庆, 等. 三七果化学成分的研究 [J]. 中草药, 2010, 41(8): 1249-1251. |
| [15] | 胡晗绯. 三七地上部分总皂苷水解产物的药学研究 [D]. 沈阳: 辽宁中医药大学, 2008. |
| [16] | Wu L J, Wang L B, Gao H Y, et al. A new compound from the leaves of Panax ginseng [J]. Fitoterapia, 2007, 78(7/8): 556-560. |
| [17] | Tran T L, Kim Y R, Yang J L, et al. Dammarane triterpenes from the leaves of Panax ginseng enhance cellular immunity [J]. Bioorg Med Chem, 2014, 22(1): 499-504. |
| [18] | Wang X H, Wang W. Cytotoxic and radical scavenging nor-dammarane triterpenoids from Viburnum mongolicum [J]. Molecules, 2013, 18(2): 1405-1417. |
| [19] | Meng Q G, Yi B, Liang W, et al. Synthesis, structural determination of a new ocotillol derivative and its epimer [J]. Lett Org Chem, 2011, 8(9): 682-685. |
| [20] | Chen G T, Yang M, Lu Z Q. Microbial transformation of 20(S)-protopanaxatriol-type saponins by Absidia coerulea [J]. J Nat Prod, 2007, 70(7): 1203-1206. |
| [21] | Baek N I, Kim D S, Lee Y H, et al. Ginsenoside Rh4, a genuine dammarane glycoside from Korean red ginseng [J]. Planta Med, 1996, 62(1): 86-87. |
| [22] | Kim S I, Park J H, Ryu J H, et al. Ginsenoside Rg5, a genuine dammarane glycoside from Korean red ginseng [J]. Arch Pharm Res, 1996, 19(6): 551-553. |
| [23] | Thoison O, Sevenet T, Niemeyer H M, et al. Insect antifeedant compounds from Nothofagus dombeyi and N. pumilio [J]. Phytochemistry, 2004, 65(14): 2173-2176. |
| [24] | Wang P, Bi X L, Xu J, et al. Synthesis and anti-tumor evaluation of novel 25-hydroxyprotopanaxadiol analogs incorporating natural amino acids [J]. Steroids, 2013, 78(2): 203-309. |
| [25] | 马双刚, 姜永涛, 宋少江, 等. 西洋参茎叶总皂苷碱降解成分 [J]. 药学学报, 2005, 40(10): 924-930. |
| [26] | 李 巍. 西洋参茎叶皂苷酸降解产物的化学成分研究 [D]. 长春: 吉林大学, 2012. |
| [27] | 赵余庆, 袁昌鲁, 傅玉琴, 等. 人参茎叶中微量三萜化合物的化学研究 [J]. 药学学报, 1990, 25(4): 297-301. |
| [28] | Qian G T, Wang Z C, Zhao J Y, et al. Synthesis and anti-cancer cell activity of pseudo-ginsenoside Rh2 [J]. Steroids, 2014, 92: 1-6. |
| [29] | 贾继明, 王宗权. 西洋参总皂苷乙酸水解产物的化学成分研究 (I) [J]. 中草药, 2009, 40(8): 1204-1207. |
| [30] | Yang X W, Li L Y, Tian J M, et al. Ginsenoside-Rg6, a novel triterpenoid saponin from the stem-leaves of Panax ginseng C. A. Mey. [J]. Chin Chem Lett, 2000, 11(10): 909-912. |
| [31] | Dou D Q, Chen Y J, Ren J, et al. Ocotilone-type ginsenoside from leaves of Panax ginseng [J]. J Chin Pharm Sci, 2002, 11(4): 119-121. |
| [32] | 王洪平, 杨鑫宝, 杨秀伟, 等. 吉林人参根和根茎的化学成分研究 [J]. 中国中药杂志, 2013, 38(17): 2807-2817. |
| [33] | Oh M, Choi Y H, Choi S, et al. Anti-proliferating effects of ginsenoside Rh2 on MCF-7 human breast cancer cells [J]. Int J Oncol, 1999, 14(5): 869-875. |
| [34] | Lee K Y, Park J A, Chung E, et al. Ginsenoside-Rh2 blocks the cell cycle of SK-HEP-1 cells at the G1/S boundary by selectively inducing the protein expression of p27kip1 [J]. Cancer Lett, 1996, 110(1/2): 193-200. |
| [35] | Kim H E, Oh J H, Lee S K, et al. Ginsenoside Rh2 induces apoptotic cell death in rat C6 glioma via a reactive oxygen-and caspase-dependent but Bcl-X (L)-independent pathway [J]. Life Sci, 1999, 65(3): 33-40. |
| [36] | Kim Y S, Jin S H, Lee Y H, et al. Differential expression of protein kinase C subtypes during ginsenoside Rh2-induced apoptosis in SK-N-BE (2) and C6Bu-1 cells [J]. Arch Pharm Res, 2000, 23(5): 518-524. |
| [37] | Fei X F, Wang B X, Tashiro S, et al. Apoptotic effects of ginsenoside Rh2 on human malignant melanoma A375-S2 cells [J]. Acta Pharmacol Sin, 2002, 23(4): 315-322. |
| [38] | Qu X R, Qu S C, Yu X F, et al. Pseudo-G-R2 induces mitochondrial-mediated apoptosis in SGC-7901 human gastric cancer cells [J]. Oncol Rep, 2011, 26(6): 1441-1446. |
| [39] | Li L, Chen X Y, Li D, et al. Identification of 20 (S)-protopanaxadiol metabolites in human liver microsomes and human hepatocytes [J]. Drug Metab Dispos, 2011, 39(3): 472-483. |
 2015, Vol. 46
2015, Vol. 46


