萝藦科(Asclepiadaceae)是双子叶植物纲、龙胆目的一个科,其模式属为马利筋属Asclepias L.,约有250属,2 000多种,主要分布于热带和亚热带地区。在中国,萝藦科有44属,243种。自有本草记载以来,萝藦科植物就具有重要的药用价值,如治疗跌打损伤、风湿关节炎、毒虫咬伤、肿瘤以及强心等。该科可以药用的属有马利筋属、牛角瓜属Calotropis R. Br.、鹅绒藤属Cynanchum L.、牛皮消属Cynanchum L.、牛奶菜属Marsdenia R. Br.、黑鳗藤属Stephanotis Thou.、杠柳属Periloca L. 等,其中药用成分主要涉及生物碱类和苷类[1]。在萝藦科植物中广泛存在的一类C21甾体苷类成分被证实在抗肿瘤、免疫调节等方面有显著的药理活性。本文着重从萝藦科植物C21甾体苷类的植物来源、骨架类型、波谱特征及生物活性进行综述。
1 萝藦科植物的C21甾体苷类的植物资源近年来萝藦科中C21甾体苷类成分主要是从马利筋属、鹅绒藤属、杠柳属、牛奶菜属、牛皮消属、黑蔓藤属植物中分离得到,具体来源和分布见表 1。
|
|
表 1 萝藦科植物C21甾体苷类成分植物来源 Table 1 Plant resources of C21 steroidal glycosides in plants of Asclepiadaceae |
近5年来国内外对萝藦科植物近10个种进行了研究,发现了40个C21甾体苷类化合物。C21甾体苷类苷元为孕甾烷衍生物,与2-去氧糖等形成苷,糖链最多的含有6个糖。苷元的C-5、6位之间有无双键,C-8、11、12、17位有无羟基,C-17、20位的不同构型等特点是区分该科C21甾体苷类的依据。其苷元结构见图 1,分得的C21甾体苷类化合物见表 2。
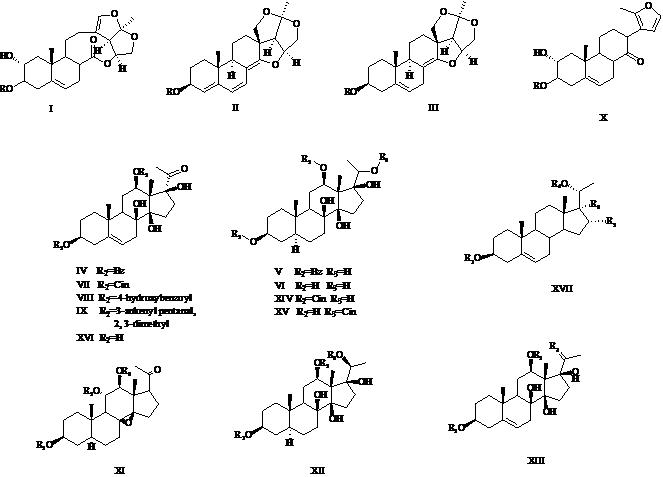 | 图 1 C21甾体苷类骨架 Fig. 1 Backbones of C21 steroidal glycosides |
|
|
表 2 萝藦科植物中分离的C21甾体苷类 Table 2 C21 steroidal glycosides from plants of Asclepiadaceae |
一般通过Libermann-Burchard反应确定化合物是甾体,Molish反应确定化合物具有糖的性质,即为苷类。总结这些化合物的13C-NMR谱可判断其苷元类型。C-20位羟基氧化成羰基后化学位移向低场移至δ 200以上,且C-17,21位相应地向低场位移δ 6~10和6~8,因此苷元骨架中C-20位的13C-NMR谱可作为区分苷元C-20位结构的依据,推断C21甾体苷的骨架类型;C-5,6位为双键时,13C-NMR数据分别为δ 139~142和117~124;而C-5、6位无双键时,C-5位δ 43~46,C-6位δ 43~46;当低场区出现较多碳信号时,苷元骨架考虑多为类似于I、II、III的结构类型[16](图 1)。
3.2 糖的连接顺序特点该科C21甾体苷的糖主要是2-去氧糖。利用苷化位移的原理,苷元与糖成苷后,苷元上的碳原子将向低场位移δ 6~10,糖上的C-1的化学位移比相应的甲基苷向高场位移大约δ 3,由此可推断成苷位置。缓和化学降解法和酶解法都可用于确定糖的连接顺序,但由于这些方法均需降解和破坏样品的结构,分数阶傅里叶变换(PRFT)技术得到普及。在苷分子结构中,由于相对于苷元远近不同,构成糖的反转自由度不一样,从而导致弛豫时间(T1)值不一致,各个糖的平均T1值将有明显的差别,末端葡萄糖>中间葡萄糖>内部磁麻糖,据此即可推测糖的连接顺序[16]。
4 生物活性 4.1 抗肿瘤陈书红等[17]研究表明杠柳苷元对MCF-7肿瘤细胞的增殖有非常强的抑制作用,其IC50为(1.006±0.013)μg/mL(远小于顺铂相应的IC50值)。
赵连梅等[18]应用MTT法检测香加皮醇提物杠柳苷对食管癌细胞TE-13、Eca-109、TE-1和TE-10增殖的影响,结果表明杠柳苷可明显抑制食管癌细胞的增殖,其作用机制可能是通过下调凋亡抑制基因的表达而诱导细胞凋亡。
王冬艳等[19]建立肝癌实体型(Heps)小鼠移植性肿瘤模型,并采用免疫荧光(AO/EB)测定肿瘤细胞凋亡情况,免疫组化染色检测bcl-2基因的表达。测得自白首乌中提取得到的C21甾体总苷(包括白首乌苷A、B、C,隔山消苷C3N、C2N、C1G、KN和白首乌新苷A,10、20、40 mg/kg)可促进肿瘤细胞的凋亡,电镜下可见凋亡的形态学改变,并出现凋亡小体;免疫组化结果显示,bcl-2基因的表达与模型组比较明显降低(P<0.01),但不同于凋亡结果的是高剂量组的阳性面积表达比中剂量略高。降低bcl-2基因表达从而促进肝癌细胞的凋亡,可能是C21甾体苷抗肝癌的机制之一。Wang等[20]和张如松等[21]也都证实从白首乌中分离得到的C21甾体苷有抑制肿瘤细胞的作用,同时不同的C21甾体苷对不同肿瘤细胞的抑制作用具有选择性。
4.2 免疫调节Li等[14]和Ye等[22]对黑鳗藤中分离得到的C21甾体苷的生物活性进行了研究,发现多具有免疫调节或免疫抑制作用,其中C21甾体苷的C-20位上的取代基对其免疫活性具有重要影响。Li等[8]用小鼠离体的脾细胞,证实从蔓剪草中分离得到的4种C21甾体化合物(其中2种为化合物17、18)对刀豆素A和脂多糖(LPS)具有抑制作用,从而说明4种化合物具有免疫抑制作用。
4.3 抗癫痫青阳参Cynanchum otophyllum Schneid. 很早就被用于治疗癫痫,青阳参苷更是被开发为临床治疗癫痫病的新药。Zhao等[15]从青阳参中分离得到5个新化合物cynanotoside A~E(41~45),以及2个已知化合物deacetylmetaplexigenin和 cynotophyllo- side H,其中化合物cynanotoside A、B和cynotophylloside H在羟基柠檬酸(HCA)诱导细胞死亡实验中表现出剂量依赖性,这可能是青阳参治疗癫痫的机制之一。
5 结语从20世纪70年代开始,萝藦科植物逐渐引起了国内外学者的普遍关注,对其成分及药理作用的研究结果表明,该科植物具有广泛的药理作用,特别是其主要成分C21甾体苷类的研究更受到重视。近几年从该科植物共分得40个新的C21甾体苷类,随着新的分离、检测技术,以及细胞生物学、分子生物学等学科的飞速发展,人们对C21甾体苷类化合物的认识必将会更加全面深入。期待对萝藦科植物的进一步研究,以便使该科植物得到更好的开发与利用。
| [1] | 中国科学院中国植物志编辑委员会. 中国植物志 (第63卷) [M]. 北京: 科学出版社, 1977. |
| [2] | Liu Y, Hu Y C, Yu S S, et al. Steroidal glycosides from Cynanchum forrestii Schlechter [J]. Steroids, 2006, 71(1): 67-76. |
| [3] | Yu J Q, Zhang Z H, Deng A J, et al. Three new steroidal glycosides from the roots of Cynanchum stauntonii [J]. Biomed Res Int, 2013, 2013: 816145. |
| [4] | Fu M H, Wang Z J, Yang H J, et al. A new C21 steroidal glycoside from Cynanchum stauntonii [J]. Chin Chem Lett, 2007, 18(4): 415-417. |
| [5] | Li J Z, Liu H Y, Lin Y J, et al. Six new C21 steroidal glycosides from Asclepias curassavica L. [J]. Steroids, 2008, 73(6): 594-600. |
| [6] | Chen G, Xu N, Pei Y H. C21 steroidal glycosides from Cynanchum wallichii Wight [J]. J Asian Nat Prod Res, 2009, 11(2): 177-182. |
| [7] | Chen G, Wang D, Pei Y H. Two new C21 steroidal glycosides from Cynanchum wallichii Wight [J]. J Asian Nat Prod Res, 2008, 10(7): 671-676. |
| [8] | Li X Y, Sun H X, Ye Y P, et al. C21 steroidal glycosides from the roots of Cynanchum chekiangense and their immunosuppressive activities [J]. Steroids, 2006, 71(1): 61-66. |
| [9] | Wang L, Yin Z Q, Zhang Q W, et al. Five new C21 steroidal glycosides from Periploca sepium [J]. Steroids, 2011, 76(3): 238-243. |
| [10] | Zhang H, Tan A M, Zhang A Y, et al. Five new C21 steroidal glycosides from the stems of Marsdenia tenacissima [J]. Steroids, 2010, 75(2): 176-183. |
| [11] | 雷勇胜, 李占林, 杨珅珅, 等. 通光散藤茎的C21甾体成分 [J]. 药学学报, 2008, 43(5): 509-512. |
| [12] | Ye L F, Wang Y Q, Yang B, et al. Cytotoxic and apoptosis inducing properties of a C21 steroidal glycoside isolated from the roots of Cynanchum auriculatum [J]. Oncol Lett, 2013, 5(4): 1407-1411. |
| [13] | Zhang R S, Liu Y L, Wang Y Q, et al. Cytotoxic and apoptosis-inducing properties of auriculoside A in tumor cells [J]. Chem Biodiv, 2007, 4(5): 887-892. |
| [14] | Li X Y, Sun H X, Ye Y P, et al. Three new immunomodulating C21 steroidal glycosides from the stems of Stephanotis mucronata [J]. Chem Biodiv, 2005, 2(12): 1701-1711. |
| [15] | Zhao Z M, Sun Z H, Chen M H, et al. Neuroprotective polyhydroxypregnane glycosides from Cynanchum otophyllum [J]. Steroids, 2013, 78(10): 1015-1020. |
| [16] | 张玉娥, 阮金兰, 丁惟培. 13C NMR在C21甾体甙结构研究中的应用 [J]. 国外医药: 植物药分册, 1992, 7(2): 51-56. |
| [17] | 陈书红, 杨峻山, 任风芝, 等. 香加皮的抗肿瘤活性成分研究 (I) [J] . 中草药, 2006, 37(4): 519-520. |
| [18] | 赵连梅, 艾 军, 张 倩, 等. 香加皮杠柳苷诱导人食管癌细胞凋亡及其作用机制的研究 [J]. 肿瘤, 2009, 29(11): 1025 -1030. |
| [19] | 王冬艳, 张洪泉, 李 心. 白首乌C21甾体苷诱导肝癌细胞凋亡的作用及其机制 [J]. 药学学报, 2007, 42(4): 366-370. |
| [20] | Wang H, Wang Q, Srivastava R K, et al. Eeffets of total glycosides from Baishouwu on human breast and prostate cancer cell prorliferation [J]. Altern Ther Health Med, 2003, 9(5): 62-66. |
| [21] | 张如松, 叶益萍, 沈月毛, 等. 白首乌体外抑制肿瘤细胞的成分研究 [J]. 药学学报, 2000, 35(6): 431-437. |
| [22] | Ye Y P, Sun H X, Li X Y, et al. Four new C21 steroidal glycosides from the roots of Stephanotis mucronata and their immunological activities [J]. Steroids, 2005, 70(12): 791-797. |
 2014, Vol. 45
2014, Vol. 45


