2. 天津药物研究院, 天津 300193
2. Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
阿哌沙班是一种新型的口服直接Xa因子抑制剂[1],由百时美施贵宝公司和辉瑞公司联合研制[2]。目前,阿哌沙班已获欧盟及美国在内的多个国家批准,用于降低非瓣膜性房颤患者中风和全身性栓塞的风险[3-4]。此外,还可用于降低已接受择期髋关节或膝关节置换手术成人患者的静脉血栓栓塞[5]、深静脉血栓或肺血栓[6]、癌症患者静脉血栓[7]形成的风险,并对血栓栓塞具有较好的治疗效果。在该原料药的合成和精制过程中,需要用到二氯甲烷、四氢呋喃、乙醇、异丙醇、甲醇、丙酮、醋酸乙酯、叔丁基甲醚、吗啉、三乙胺、DMF、原甲酸三甲酯12种溶剂。这些残留溶剂对人体健康有一定的影响,需要除去或者使其残留的量不超过2015年版《中国药典》规定的限度。因此,本实验建立了测定阿哌沙班原料药中可能残留的12种有机溶剂的气相检测方法,结果表明,该方法分离度良好,灵敏度高,在考察的浓度范围内线性关系良好,回收率符合规定,耐用性良好,可作为阿哌沙班原料药中残留溶剂的检测方法。
1 仪器与试药Agilent 7890B气相色谱仪;Agilent 7697A顶空进样器;氢火焰离子化检测器(FID);HG-Model300A色谱专用氢气发生器、AIR-Model-5L色谱专用空气压缩机(天津市色谱科学技术公司);Open LBA CDS Chem Station Edition工作站;Sartorius BP211D电子分析天平。
甲醇、乙醇、异丙醇、二氯甲烷、醋酸乙酯、四氢呋喃、DMF(分析纯,天津市康科德科技有限公司);丙酮(分析纯,天津市凯信化学工业有限公司);叔丁基甲醚(分析纯,天津市化学试剂三厂);三乙胺、原甲酸三甲酯(分析纯,天津市光复科技发展有限公司);吗啉(分析纯,天津市化学试剂批发公司)。阿哌沙班原料药由天津药物研究院化药部自制(质量分数≥99.0%),批号分别为160310、160706、160707。
2 方法与结果 2.1 色谱条件DB-624毛细管柱(30.0 m×0.53 mm×3.00 μm),升温程序为40 ℃维持6 min,以20 ℃/min升至220 ℃,维持10 min,进样口温度为250 ℃,检测器温度为250 ℃,检测器为FID,载气为高纯度氮气,体积流量2.8 mL/min,分流比5:1,顶空条件:平衡温度100 ℃,加热20 min,定量环110 ℃,传输线120 ℃,自动顶空进样,定量环1 mL。溶剂为N-甲基吡咯烷酮(阿拉丁,HPLC测 质量分数≥99.5%)。
2.2 溶液的配制 2.2.1 对照溶液的配制分别精密移取二氯甲烷、四氢呋喃、乙醇、异丙醇、吗啉、三乙胺、DMF、甲醇、丙酮、醋酸乙酯、叔丁基甲醚、原甲酸三甲酯适量至100 mL量瓶中,加溶剂稀释定容,摇匀,配制成质量浓度分别为0.6、0.72、5、5、1、0.32、0.88、3、5、5、5、1 mg/mL对照品储备液。再精密量取对照储备液5 mL,加溶剂稀释定容至100 mL量瓶中,摇匀,即得。
2.2.2 供试品溶液的制备精密称取阿哌沙班原料药100 mg,置10 mL顶空瓶中,加入2 mL溶剂,加盖密封,即得。
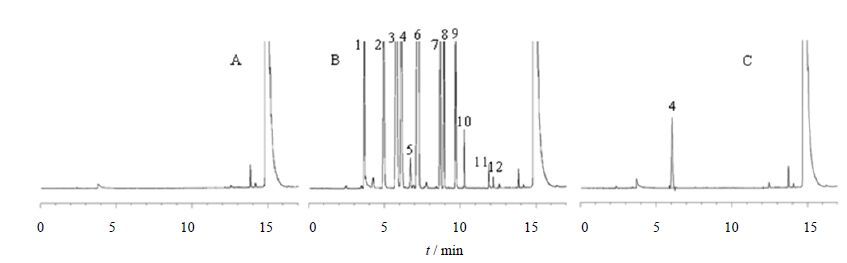
2.3 系统适用性试验取对照溶液,精密量取2 mL置10 mL顶空瓶中,加盖密封,平行配制6份,进样测定。结果各组分的分离度均大于1.5,峰面积RSD均小于10%,理论塔板数均大于5 000,符合规定。色谱图见图 1。
2.4 定量限 2.4.1 定量限的确定分别精密移取甲醇、乙醇、丙酮、异丙醇、二氯甲烷、原甲酸三甲酯、吗啉、DMF、叔丁基甲醚、醋酸乙酯、四氢呋喃、三乙胺适量至同一25 mL量瓶,加溶剂稀释定容,摇匀,作为溶液A。将溶液A用溶剂逐步稀释,直至信噪比为10,计算所测溶剂的定量限,结果见表 1。
|
1-甲醇 2-乙醇 3-丙酮 4-异丙醇 5-二氯甲烷 6-叔丁基甲醚 7-乙酸乙酯 8-四氢呋喃 9-三乙胺 10-原甲酸三甲酯 11-吗啉 12-DMF 1-methanol 2-ethanol 3-acetone 4-isopropanol 5-tert-Butyl methyl ether 6-dichloromethane 7-aceticether 8-tetrahydrofuran 9-triethylamine 10-trimethylorthoforMate 11-morpholine 12-N,N-Dimethylformamide 图 1 空白(A)、对照溶剂(B)和阿哌沙班原料药(C)的GC图谱 Fig. 1 GC chromatograms of blank solution (A),reference substance solvents (B),and Apixaban bulks drug (C) |
2.4.2 定量限精密度
平行配制6份定量限溶液,计算各成分峰面积的RSD值,结果见表 1。
2.4.3 定量限回收率取对照溶液2 mL置10 mL顶空瓶中,加盖密封,平行配制2份对照溶液;称取样品100 mg置10 mL顶空瓶中,加入2 mL溶剂,加盖密封,平行配制2份样品溶液;样品加定量限溶液:称取样品100 mg置10 mL顶空瓶中,平行3份,分别加入定量限溶液2 mL,加盖密封,对照和样品溶液分别进2针,加定量限溶液进样3针测定,使用外标法计算回收率,结果见表 1。
测得量=A1/A对×C对
质量分数=A2/ A对×C对/C2
原始量=C1×质量分数
加入量=C3
回收率=(测得量-原始量)/加入量
式中,A对为对照溶液中各溶剂峰面积;A1为样品加定量限溶液各溶剂峰面积;A2为样品溶液中含有的溶剂峰面积;C对为对照溶液中各溶剂质量浓度;C1为样品加定量限溶液质量浓度;C2为样品溶液质量浓度;C3为各溶剂定量限的质量浓度。
2.5 检出限将定量限溶液用溶剂逐步稀释,直至信噪比为3,计算所测溶剂的检出限,结果表明,二氯甲烷、四氢呋喃、乙醇、异丙醇、吗啉、三乙胺、DMF、甲醇、丙酮、醋酸乙酯、叔丁基甲醚、原甲酸三甲酯检出限分别为1.154、0.2206、0.8968、0.9448、4.002、0.1396、4.708、0.9608、0.5360、0.3428、0.1600、0.8592 μg/mL。
| 表 1 定量限考察结果 Table 1 Results of LOQ test |
2.6 线性关系考察
取对照储备液5 mL至25 mL量瓶中,加溶剂稀释定容,摇匀;分别移取1.25、2.00、2.50、3.00、6.25 mL置不同10 mL量瓶中,加溶剂稀释定容,摇匀;定量限浓度参考“2.4定量限”,进样测定。结果表明,各溶剂在一定浓度范围内线性关系良好,结果见表 2。
2.7 方法精密度试验对照溶液:取对照溶液2 mL置10 mL顶空瓶中,加盖密封,平行配制2份。
样品溶液:称取样品100 mg至10 mL顶空瓶中,加入2 mL溶剂,加盖密封,平行配制6份,结果表明,样品中只检测出异丙醇,异丙醇质量分数的RSD为2.64%。
| 表 2 线性关系考察结果 Table 2 Results of linearity test |
样品加对照溶液:称取样品100 mg至10 mL顶空瓶中,加入对照溶液2 mL,加盖密封,平行配制6份,进样测定,计算各溶剂RSD值,结果见表 3。
2.8 中间精密度配制方法同2.7,由另一人员在另外一台仪器上完成;样品溶液测定结果表明,异丙醇质量分数的RSD为2.12%,两台仪器异丙醇质量分数的RSD为4.46%。样品加对照溶液结果见表 3。
| 表 3 精密度试验结果 Table 3 Results of precision test |
2.9 回收率试验
对照溶液:取对照溶液2 mL置10 mL顶空瓶中,加盖密封,平行配制2份。
样品溶液:称取样品100 mg置10 mL顶空瓶中,加入2 mL溶剂,加盖密封,平行配制2份。
80%、100%、120%的回收率溶液配制:取对照储备液10 mL置50 mL量瓶,加入溶剂稀释定容,作为A溶液;从A溶液中分别移取2.0、2.5、3.0 mL至10 mL量瓶,加入溶剂稀释定容,摇匀,各平行配制3份;称取样品100 mg至10 mL顶空瓶,平行9份,分别加入各上述配置好的溶液2 mL,加盖密封,进样测定。结果见表 4。
2.10 耐用性试验试验表明,顶空温度、检测器温度、进样口温度、平衡时间、升温速率发生微小变化时,对照溶液中各溶剂的峰面积RSD值在2.18%~4.63%。方法耐用性良好。
2.11 稳定性试验由于样品以N-甲基吡咯烷酮为溶剂时,常温状态下50 mg/mL尚不能溶解,因此,未考察样品溶液的稳定性。
对照溶液稳定性试验:分别考察了0、1、2、4、8、20、30 d稳定性,试验表明,各溶剂30 d内稳定性良好。结果见表 5。
| 表 4 回收率试验结果 Table 4 Results of recovery test |
| 表 5 稳定性试验结果 Table 5 Results of stability test |
2.12 样品测定
分别精密称定160310、160706、160707批阿哌沙班原料药各100 mg,置10 mL顶空瓶中,加入2 mL溶剂,加盖密封,进样测定,采用外标法计算,结果见表 6。阿哌沙班原料药中有机溶剂残留限度参考2015年版《中国药典》[8]及国际人用药品注册技术协调大会(ICH)等相关指导原则和文献,最后设定控制标准:二氯甲烷、四氢呋喃、乙醇、异丙醇、DMF、甲醇、丙酮、醋酸乙酯、叔丁基甲醚、吗啉、三乙胺、原甲酸三甲酯的限度分别为0.06%、0.072%、0.5%、0.5%、0.088%、0.3%、0.5%、0.5%、0.5%、0.1%、0.032%、0.1%。结果表明,3批样品中异丙醇残留量不超过规定限度,其他溶剂均未检出。
| 表 6 阿哌沙班原料药中有机溶剂残留测定结果 Table 6 Determination of residual organic solvents in Apixaban bulks drug |
3 讨论 3.1 溶剂的选择
考察了N,N-二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)、N,N-二甲基乙酰胺、N-甲基吡咯烷酮、水5种溶剂,常温条件下,发现样品在以上溶剂中均不溶解;70℃水浴加热条件下,样品能在N-甲基吡咯烷酮中完全溶解。考虑到样品溶解性问题及各残留溶剂沸点,选择N-甲基吡咯烷酮作为溶剂。
3.2 温度的选择考察了250℃、280℃两个检测器温度,发现280℃比250℃基线噪音大;考察了40℃、45℃两个起始温度,发现40℃比45℃分离度更好。
3.3 分流比的选择考察了分流比为1:1、5:1、10:1三个条件,发现分流比为5:1时,灵敏度较高,溶剂噪音尚可接受,因此确定分流比为5:1。
3.4 体积流量的选择考察了3、2.8 mL/min两个体积流量条件,发现流速为2.8 mL/min时,各溶剂分离度更好。
3.5 测定结果分析检测结果表明,3批样品中二氯甲烷、四氢呋喃、乙醇、吗啉、三乙胺、DMF、甲醇、丙酮、醋酸乙酯、叔丁基甲醚、原甲酸三甲酯均未检出,异丙醇残留量未超过限度标准。该12种溶剂均是合成阿哌沙班原料药的工艺杂质,本次试验旨在建立一个全面的检测方法对阿哌沙班原料药予以控制。
4 结论2015年版《中国药典》四部通则0861规定,二氯甲烷、甲醇、四氢呋喃、DMF为第二类残留溶剂,限度分别为0.06%、0.3%、0.072%、0.088%,该4种残留溶剂对人体有一定的毒性,应限量使用;醋酸乙酯、叔丁基甲醚、乙醇、异丙醇、丙酮为第三类残留溶剂,危害性比第二类残留溶剂较小,因此限度均为0.5%。药典上未规定吗啉、三乙胺、原甲酸三甲酯的残留限度,并且这3种残留溶剂检测的相关文献报道较少,本实验根据ICH对阿哌沙班原料药残留溶剂的规定及项目需求,设定三者的限度分别为0.1%、0.032%、0.1%。本实验采用顶空气相色谱法对阿哌沙班原料药相关的12种残留溶剂进行检测,方法学验证证明该方法分离度良好,灵敏度高,在考察的浓度范围内线性关系良好,回收率符合规定,耐用性良好,可作为阿哌沙班原料药中残留溶剂的质量控制方法。
| [1] | Tomari S, Homma K, Noguchi T, et al. Development of Interstitial Lung Disease after Initiation of Apixaban Anticoagulation Therapy[J]. J Stroke Cerebrovasc Dis, 2016, 25:1767–1769. doi:10.1016/j.jstrokecerebrovasdis.2016.03.036 |
| [2] | 许昕, 薛晓文. 开发中的新型口服抗凝血药-Xa因子抑制剂[J]. 药学与临床研究, 2010,18(3):294–298. |
| [3] | Connolly S J, Eikelboom J, Joyner C, et al. Apixaban in patients with atrial fibrillation[J]. New Engl J Med, 2011, 364(9):806–817. doi:10.1056/NEJMoa1007432 |
| [4] | Granger C B, Alexander J H, McMurray J J V, et al. Apixaban versus warfarin in patients with atrial fibrillation[J]. New Engl J Med, 2011, 365(11):981–992. doi:10.1056/NEJMoa1107039 |
| [5] | Lassen M R, Gallus A, Raskob G E, et al. Apixaban versus enoxaparin for thromboprophylaxis after hip replacement[J]. New Engl J Med, 2010, 363(26):2487–2498. doi:10.1056/NEJMoa1006885 |
| [6] | Agnelli G, Buller H R, Cohen A, et al. Oral apixaban for the treatment of acute venous thromboembolism[J]. New Engl J Med, 2013, 369(9):799–808. doi:10.1056/NEJMoa1302507 |
| [7] | Agnelli G, Buller H R, Cohen A, et al. Oral apixaban for the treatment of venous thromboembolism in cancer patients:results from the AMPLIFY trial[J]. J Thromb Haemost, 2015, 13(12):2187–2191. doi:10.1111/jth.13153 |
| [8] | 中国药典[S]. 四部. 2015. |
 2017, Vol. 40
2017, Vol. 40


