2. 天津市第一中心医院, 天津 300192;
3. 天津药物研究院, 天津市新药设计与发现重点实验室, 天津 300193
2. Tianjin First Central Hospital, Tianjin 300192, China ;
3. Tianjin Key Laboratory of Drug Design and Discovery, Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
不宁腿综合征(restless legs syndromes,RLS)是中枢神经系统感觉运动障碍性疾病,发病机制尚不明确。该病临床主要表现为腿部难以描述的不适感,不受控制地强烈活动下肢使症状部分或全部缓解,夜间症状严重,通常在23:00~4:00最为严重,因此影响了患者的生活质量。大多数患者有原发性RLS,多种因素可能会导致继发性RLS,如铁缺乏症、帕金森病、怀孕和某些药物(抗抑郁药、抗组胺药等)[2]。RLS在老年人群中高发,女性患病率约为男性的2倍;不同人种患病率有差异,非洲、中东、亚洲、拉美和东南欧的发病率较低,北欧和北美的发病率较高。因为各地报道的患病率有所不同,其确切发病率存在争议,西方国家的流行率为4%~15%,据估计,美国成年人中有2%~3%受中度至重度RLS侵扰[3]。目前临床使用的治疗RLS药物有左旋多巴、多巴胺激动剂,如罗匹尼罗、普拉克索、培高利特等;安定类药物、阿片类药物、抗惊厥药物等,均疗效不理想或受副作用限制[4]。美国FDA于2011年4月批准加巴喷丁恩那卡比(gabapentin enacarbil,GEn,图 1)上市,临床上用于治疗中度至重度RLS,在治疗该病中发挥了较好的疗效。综述Gen的研发背景、合成、药理作用、临床研究,以期为临床应用提供依据。
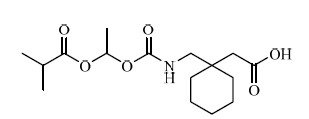
|
图 1 加巴喷丁恩那卡比的结构 Fig. 1 Structure of gabapentin enacarbil |
1 药物概况
通用名:加巴喷丁恩那卡比
化学名:(±)-1-([(1-(2-甲基-1-氧代丙氧基)乙氧基)甲酰]氨甲基)环己烷乙酸
分子式:C16H27NO6
相对分子质量:329.18
研发公司:葛兰素史克
作用靶点:电压依赖的钙离子通道
适应症:中至重度不宁腿综合征
剂型:缓释片剂
用法用量:1次/d,600 mg/次,下午5点服药
不良反应:主要有嗜睡、眩晕、头痛、恶心、呕吐等。
警告和注意事项:GEn能够显著减弱服用者的驾驶技能,因此服药后尽量不要驾驶车辆;肾功能不全者不推荐使用。
2 合成方法以1-(甲氨基)环己烷乙酸为起始原料,经三甲基氯硅烷和三乙胺处理后,与1-氯乙基氯甲酸酯进行酰化反应得到1-([(1-氯乙氧基)甲酰]氨甲基)环己烷乙酸,该化合物可以不经纯化进行下一步反应,在三乙胺和二氯甲烷中与异丁酸反应生成最终的化合物GEn,合成工艺见图 2[5]。
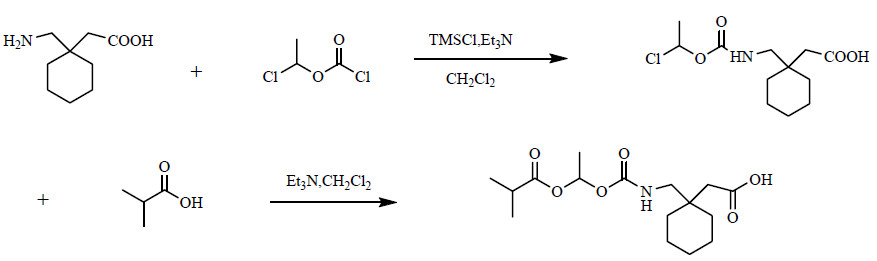
|
图 2 加巴喷丁恩那卡比的合成路线 Fig. 2 Synthesis rute of gabapentin enacarbil |
3 药理学
GEn是加巴喷丁的前药,口服吸收进入体内血液循环后经酶作用迅速水解转化为加巴喷丁而发挥药理作用,通过前药设计大大改善了加巴喷丁在人体内药动学方面的缺点,研究表明加巴喷丁的结构和神经递质γ-氨基丁酸(GABA)结构类似,但是它对GABA和受体的相互结合、相互作用没有影响,加巴喷丁治疗RLS的具体作用机制目前还没有确定[6]。研究人员对GEn和加巴喷丁进行了放射性配体结合试验,结果表明两者对其他常见的药物靶点,如受体、离子通道和酶都没有作用。在体外研究中发现加巴喷丁与电压依赖的Ca2+通道的α2δ亚基具有较高的亲和力,但是这种结合作用是否与治疗RLS有关尚不能确定[7]。
4 药动学GEn口服后在小肠被迅速吸收,经过酯酶类水解为加巴喷丁、二氧化碳、乙醛和异丁酸,该水解反应主要在肠细胞中进行,释放的加巴喷丁最终以原形药物经肾脏排出体外[8]。在进食状态下本品血浆中加巴喷丁的表观口服清除率为6.0~9.3 L/h,平均生物利用度约为75%,空腹状态下为42%~65%[9]。本品临床推荐剂量为600 mg,空腹状态下口服5 h后达到血药浓度最大值(Cmax),非空腹状态约7.3 h。口服吸收2 d后达稳态,加巴喷丁在体内的血浆蛋白结合率小于3%[10]。
一项非随机、单中心临床试验旨在研究GEn在人体内吸收、分布、代谢和消除特征[11]。用14C放射性标记GEn,6位健康受试者口服600 mg GEn,通过在尿中和粪便的总放射性、血浆和全血中Cmax、14C-GEn衍生放射性和血药浓度曲线下面积(AUC)评估药动学特征。通过不良事件报道、生命体征、临床实验室参数和心电图进行耐受性评估。结果显示,尿中和粪便放射性总回收率为99.3%(尿94.1%、粪便5.2%),血和血浆放射性比率为0.91,给药24 h内85%以上放射性剂量在尿液中回收,没有出现不良事件报告。由此可以看出,GEn口服后被广泛吸收,在血浆和全血中消除迅速。
5 临床评价为了评估GEn在中度至重度原发性RLS患者中的维持疗效和耐受性,进行了1个24周的单盲治疗和接下来立即进行12周的随机双盲治疗[12]。单盲治疗阶段,患者在每天下午5点进食时随机服用GEn(1 200 mg)或安慰剂。主要终点是在双盲阶段患者疾病复发人数的比例。在单盲治疗阶段,有221例患者参加;在双盲阶段有168例参加。结果显示GEn组患者复发率为10%,安慰剂组为23%,GEn组的复发率明显小于安慰剂组。由此可以看出,GEn(1 200 mg)在中度至重度原发性不宁腿综合征患者中表现出很好的疗效和耐受性。
一项随机、双盲、三组交叉治疗的临床研究中,旨在评估GEn和吗啡在药动学、药效学、安全性和耐受性方面是否存在相互作用[13]。研究对象随机接受吗啡安慰剂+GEn 600 mg,吗啡60 mg+GEn 600 mg,吗啡60 mg+GEn安慰剂。研究主要终点为Gen、吗啡、吗啡-6-葡萄糖醛酸的Cmax和AUC。结果表明:GEn的AUC 1.035~1.162 (mg·min)/mL,Cmax 0.920~1.126 mg/mL;吗啡的AUC1.014~1.098 (mg·min)/mL,Cmax 0.967~1.134 mg/mL;吗啡-6-葡糖苷酸的AUC 0.929~1.058 (mg·min)/mL,Cmax 0.855~1.062 mg/mL。吗啡+GEn和吗啡治疗常见的不良事件为恶心(13%,11%)、头痛(27%,28%)。由此可以看出两种药物之间没有显著药动学相互作用,当GEn和吗啡联合给药时可能会增加其不良反应的发生。
一项多中心、随机、双盲、52周临床研究中,旨在评价GEn在亚洲RLS患者长期治疗中的效果和安全性,181名受试者分别接受GEn 1 200 mg/d,以国际不宁腿综合征量表(IRLS)、研究者临床疗效总评量表(ICGI)和患者临床疗效总评量表(PCGI)进行评分[14]。结果表明,IRLS分数从24.4±0.4降低至6.3±0.6,减少了−18.0±0.6,严重不良事件发生率1.6%,该IRLS、ICGI、PCGI应答率分别为80.3%、87.1%和87.1%。从结果可以看出,GEn在亚洲中度至重度RLS患者长期治疗中,表现出良好的RLS症状改善和可接受的安全性。
在患有严重RLS成人中,进行一项2周、随机、双盲、安慰剂对照试验,旨在评估加巴喷丁的疗效和耐受性[15]。95名受试者被随机分配为3组:GEn 1 200 mg组(33例)、600 mg组(29例),安慰剂组(33例)。其中2名受试者(GEn 1 200 mg)因为不良事件中途退出。结果显示,与安慰剂比较,1 200 mg的GEn基线RLS总分平均变化显著增大(P<0.000 1);在治疗的14 d内,600 mg剂量GEn的基线RLS平均变化为−9.1(5.95),与安慰剂相似。治疗中出现的最常见的不良反多为轻度或中度的嗜睡,发生率分别为:GEn 1 200 mg组36%、600 mg组14%、安慰剂组15%;头晕的发生率分别为:GEn 1 200 mg组18%、600 mg组14%、安慰剂组3%。可以看出,与安慰剂相比,1 200 mg的GEn能显著改善不宁腿综合征的症状;剂量为600 mg的GEn疗效与安慰剂相似,两种剂量的GEn耐受性良好。
6 安全性和耐受性一项随机、双盲、安慰剂对照的临床研究,旨在评价GEn的药动学和耐受性,以及在超剂量下对心脏复极化的影响,并为未来QT/QTC的研究提供剂量参考[16]。32名健康志愿者随机口服GEn 2 400、3 600、4 800、6 000 mg或安慰剂,36 h后收集血液样本,并用液相色谱-串联质谱的方法分析。通过监控不利事件、实验室参数、测量生命体征、12导联心电图评估耐受性。结果显示,受试者中出现了轻微的眩晕和恶心不良反应,没有严重不良事件报道。实验室参数、生命体征测量和心电图也没有发生显著的变化。由此可以看出,GEn剂量高达6 000 mg受试者也表现出良好的耐受性和安全性。
美国FDA批准的GEn剂型为缓释片剂,推荐用量为1日1次600 mg,下午5点服药。对于肌酐清除率小于30 mL/min的肾功能不全患者,不推荐使用该药,因为该药的剂量不能小于600 mg[17]。服用GEn常见的不良反应主要有嗜睡、眩晕、头痛、恶心、呕吐等,特别需要注意的是,GEn能够显著减弱服用者的驾驶技能,因此服药后尽量不要驾驶车辆[18]。
7 结语RLS是一种神经系统感觉运动障碍性疾病,目前尚不能确定其发病机制,临床表现大多为夜间睡眠时“双下肢出现极度不适感”导致患者不断地移动下肢,引起患者睡眠质量下降,该病虽然不危害患者的生命,却大大降低了患者的生活质量。随着社会的不断发展,人民生活水平的提高,对生活质量要求的不断提高,RLS也逐渐引起了人们的重视。目前临床上治疗该病的一线药物为多巴胺受体激动剂,虽然这类药物在治疗中表现出较好的效果,但是在长期的临床应用中也暴露出一些缺点,如可能会出现强化现象,即药物疗效减低、症状加重。临床报告显示,有30%~50%的患者出现强化现象[12]。这些不良反应限制了它们在临床的应用,而GEn在治疗RLS中有良好的效果,临床上主要应用于中度至重度RLS,作为治疗的一线药物,其具有巨大的市场,今后还应该针对减轻其不良反应,进行结构改造,加强不良反应监测,以确保安全、合理用药。
| [1] | Imamura S, Kushida C. Gabapentin enacarbil (XP13512/GSK1838262) as an alternative treatment to dopaminergic agents for restless legs syndrome[J]. Exp Opin Pharmacother, 2010, 11 (11) :1925–1932. |
| [2] | Winkelman J W, Bogan R K, Schmidt M H, et al. Randomized polysomnography study of gabapentin enacarbil in subjects with restless legs syndrome[J]. Mov Disord, 2011, 26 (11) :2065–2072. |
| [3] | Raillard P, Zhou C X, Yao F M, et al. Methods for synthesis of acyloxyalkyl derivatives of GABA analogs[P]. US, 20040014940 A1. 2004-01-22. |
| [4] | Allen R P, Walters A S, Montplaisir J, et al. Restless legs syndromeprevalence and impact:REST general population study[J]. Arch Intern Med, 2005, 165 (11) :1286–1292. |
| [5] | Tan E K, Seah A, See S J, et al. Restless legs syndrome in an Asian population:a study in Singapore[J]. Mov Disord, 2001, 16 (3) :577–579. |
| [6] | 王钢, 程卯生. 加巴喷丁恩那卡比(gabapentin enacarbil)[J]. 中国药物化学杂志,2011,21 (5) :406. |
| [7] | Hong D, Kevin L, Subas M, et al. Synthetic approaches to the 2011 new drugs[J]. Bioorg Med Chem, 2013, 21 (6) :2811. |
| [8] | Richard K, Michel A, Cramer, M D, et al. Long-term maintenance treatment of restless legs syndrome with gabapentin enacarbil:a randomized controlled study[J]. Mayo Clinic Proc, 2010, 85 (6) :512–521. |
| [9] | Akito K. Gabapentin enacarbil for the treatment of moderate to severe primary restless legs syndrome (Willis-Ekbom disease):600 or 1200 mg dose[J]. Neuropsychiatric Dis Treat, 2014 (10) :249–262. |
| [10] | Yuichi I, Naohisa U, Kenji K, et al. Long-term efficacy and safety of gabapentin enacarbil in Japanese restless legs syndrome patients[J]. Progr Neuro-Psychopharm Biol Psy, 2012, 36 (5) :251–257. |
| [11] | Walters A S, Ondo W G, Kushida C A, et al. Gabapentin enacarbil in restless legs syndrome:a phase 2b, 2-week, randomized, double-blind, placebo-controlled trial[J]. Clinic Neuropharmacol, 2009, 32 (6) :311–320. |
| [12] | William G O. Restless legs syndrome:pathophysiology and treatment[J]. Curr Treat Opt Neurol (IF 1938), 2014, 16 (11) :1–17. |
| [13] | Bogan R K, Lee D O, Buchfuhrer M J, et al. Treatment response to sleep, pain, and mood disturbance and their correlation with sleep disturbance in adult patients with moderate-to-severe primary restless legs syndrome:Pooled analyses from 3 trials of gabapentin enacarbil[J]. Ann Med, 2015, 47 (3) :269–277. |
| [14] | Chao C, James U, Thangam A, et al. Gabapentin enacarbil and morphine administered in combination versus alone:a double-blind, randomized, pharmacokinetic, and tolerability comparison[J]. Clinic Therap, 2015, 37 (2) :349–357. |
| [15] | Ondo W G, Hermanowicz N, Borreguero D G, et al. Effect of prior exposure to dopamine agonists on treatment with gabapentin enacarbil in adults with moderate-to-severe primary restless legs syndrome:pooled analyses from 3 randomized trials[J]. J Clin Move Disord, 2015, 21 (3) :9–12. |
| [16] | Lal R, Sukbuntherng J, Ho J, et al. A phase I, single-dose study ofthe disposition of 14C-radiolabeled gabapentin enacarbil in healthy male volunteers[J]. J Clinic Pharmacol Ther, 2011, 49 (2) :109–115. |
| [17] | Ritu L, Juthamas S, Wendy L, et al. Pharmacokinetics and tolerability of single escalating doses of gabapentin enacarbil:a randomized-sequence, double-blind, placebocontrolled crossover study in healthy volunteers[J]. Clinic Ther, 2009, 31 (8) :1776–1786. |
| [18] | Avidan A Y, Lee D, Park M, et al. The effect of gabapentinenacarbil on quality of life and mood outcomes in a pooled population of adult patients with moderate-to-severe primary restless legs syndrome[J]. CNS Drug, 2016, 30 (4) :305–316. |
 2016, Vol. 39
2016, Vol. 39


