2. 河北北方学院附属第一医院心脏外科, 河北 张家口 075000
2. The first affiliated hospital cardiac surgery, Hebei North University, Zhangjiakou 075000, China
学习记忆是人类及动物重要的高级脑活动,研究表明,学习记忆过程与脑内c-fos和c-jun基因表达关系非常密切。c-fos及c-jun基因属于即刻早期癌基因[1],在脑内广泛表达,以皮层、海马较多,多种学习训练模型均可诱导脑内c-fos基因表达上调[2, 3],如回避训练、光辨别训练等。长时程增强及药物也可影响c-fos基因的表达。相关研究提示c-fos基因表达受中枢神经系统神经递质或调质的调控。谷氨酸作为中枢神经系统兴奋性神经递质可诱导c-fos基因表达上调。而非竞争性N-甲基-D-天冬氨酸(N-methyl-D-aspartate,NMDA)受体抑制剂MK801可使c-fos基因表达明显减少,并且研究提示NMDA受体激活先于c-fos基因的表达[4]。
大黄酚(Chrysophanol)具有改善学习记忆障碍,提高阿尔茨海默病(Alzheimer' s disease,AD)小鼠学习记忆和认知功能。研究表明大黄酚产生上述药理作用与其抗氧化作用有关[5]。但从分子和基因水平探讨大黄酚提高小鼠学习记忆功能的机制还未见报道。本研究从体内、外阐述大黄酚对小鼠大脑皮层c-fos、c-jun表达的影响及与学习记忆的关系。
1 材料与方法 1.1 动物昆明种健康小鼠,体质量25~30 g,由中国医学科学院实验动物中心提供,许可证编号:SCXK京2004-0001。所有实验动物在动物室适应性饲养,自由饮食、进水,分笼饲养,室温(20~25 ℃)。
1.2 药品与试剂大黄酚购自中国食品药品检定研究院(批号110796-201017),制备大黄酚单体溶液[N,N-二甲基甲酰胺(DMF)-聚山梨酯80-生理盐水(1∶1∶8)]。DMEM培养液、BSA、dBcAMP均购买于美国Sigma公司;马血清和Trizol购于美国Invitrogen公司;TaKaRa RNA PCR Kit(AMV)Ver. 3.0购自宝生物工程有限公司(中国大连);特异性引物序列合成于上海生工生物工程有限公司。
1.3 仪器DWS-2 Morris水迷宫、SBA-2程控避暗箱(中国医学科学院药物研究所);紫外-可见分光光度计(LabTech公司)。
1.4 动物分组与给药80只小鼠随机分为4组,每组20只,分别为正常对照组;大黄酚高、中、低剂量(10.0、1.0、0.1 mg/kg)组。正常对照组ip 0.1 mL/10 kg溶剂,即N,N-二甲基甲酰胺-聚山梨酯80-生理盐水(1∶1∶8);大黄酚高、中、低剂量组ip给予不同剂量大黄酚。连续给药14 d。
1.5 行为学实验 1.5.1 避暗实验用药停止后第2天进行避暗实验训练(每组取7只小鼠)。8׃30开始训练,每只小鼠训练3 min。小鼠进入暗室受电击逃往明室,记录3 min内小鼠进入暗室的次数(错误次数),及首次进入暗室的时间(避暗潜伏期)。当日14׃00,次日8׃30和第3天8׃30以同样的方法进行实验,每次实验测试3次。9次结果均值用t检验进行分析。小鼠学习记忆成绩用两个参数反映:错误次数和避暗潜伏期。
1.5.2 Morris水迷宫实验用药停止后第2天进行水迷宫实验训练(每组取7只小鼠)。实验共进行5 d,第1天小鼠自由游泳120 s。从第2天开始,每天分上、下午两段,每段训练4次,每次间隔30 min。小鼠从不同的入水点面向池壁进入池中,观察小鼠寻找并爬到平台的情况。每次小鼠到达平台后让其休息30 s,如果小鼠120 s内未能找到平台,则将其放置到平台上休息30 s。第5天最后1次训练,记录120 s内小鼠寻找并爬上平台所需时间(潜伏期),及路线图(游泳总路程),未能找到平台的小鼠,潜伏期记为120 s。小鼠空间学习记忆成绩用两个参数表示:平均逃避潜伏期和游泳总距离[6]。
1.6 取样及处理用药停止后6 h快速断颈处死小鼠(每组取6只小鼠),迅速取其大脑皮层组织,放入EP管;大脑用生理盐水冲洗干净,-80℃保存备用,用于c-fos和c-jun表达检测。
1.7 星形胶质细胞培养小鼠大脑皮层星形胶质细胞原代培养参考Hertz[7]方法。选择新生不超过1 d小鼠,断头,取出大脑置于10%马血清培养基(DMEM 8.3 g/L,Glucose 1 g/L,Glutamine 0.292 g/L,Sodium Pyruvate 0.11 g/L,NaHCO3 3.7 g/L,Phenol Red 0.015 g/L)中。在显微镜下剥离脑膜,用手术刀片将大脑切碎( < 0.4 mm)。漩涡震荡分离组织1 min。再经100 μm 和70 μm尼龙网过滤组织。用含10%马血清培养液稀释过滤后的细胞,再将含细胞的培养液分装到60 mm培养皿中。37℃、5% CO2、95% O2培养。待每皿细胞铺满整个培养皿时(>95%),加入dBcAMP(0.25 mmol/L)。
1.8 逆转录-聚合酶链反应(RT-PCR)mRNA提取:将细胞用冰的1×PBS洗涤2次,每60 mm培养皿中加入200 μL Trizol试剂。室温下孵育5 min(完全溶解)。在混合物中加入1/5 Trizol提取液剂量的氯仿。剧烈震荡,12 000×g、4℃离心15 min。将上清液转移至新的离心管中,加入1/2 Trizol提取液剂量的异丙醇,混匀。在−80℃ 孵育1 h。12 000×g、4℃离心10 min。弃去上清液,用75%乙醇洗2次。干燥,加入50 μL DEPC-H2O溶解。
使用紫外分光光度进行RNA定量:用DEPC-H2O将样品稀释80~160倍,在260 nm和280 nm条件下测量吸光度(A)值并计算RNA总质量浓度。
RNA质量浓度(μg/mL)= A260×稀释倍数×40/1 000
逆转录及cDNA扩增:根据试剂盒说明书加入各反应试剂。
RT-PCR中所使用的c-fos、c-jun和TBP引物如下:c-fos(forward: GCTGACAGATACACTCCAAGCGG,reverse: AGGAAGACGTGTAAGTAGTGCAG,542 bp)[8];c-jun(forward: AGCCTACCAACGTGAGTGCT,reverse: AGAACGGTCCGTCACTTCAC,228 bp)[9];TBP(forward: CCACGGACAACTGCGTTGAT; reverse: GGCTCATAGCTACTGAACTG,236 bp)[10]。
1.9 统计学分析采用SPSS 13.0软件进行统计学分析,实验数据以x±s 表示,组间比较采用t检验。多组资料用one-way ANOVA方法进行方差分析,LSD-t检验。
2 结果 2.1 避暗实验各实验组小鼠试验前后体质量变化无显著性差异。大黄酚对小鼠学习记忆功能的提高见表 1,大黄酚低、中、高剂量组(0.1、1.0、10.0 mg/kg)可提高小鼠学习记忆能力。中、高剂量组可使小鼠避暗潜伏期明显延长,错误次数明显减少,与对照组相比差异具有统计学意义(P < 0.01);低剂量组可轻度提高小鼠学习记忆能力,但与对照组相比差异无统计学意义。
| 表 1 大黄酚对小鼠避暗潜伏期和3 min错误次数的影响 (x±s,n=7) Table 1 Effects of Chry on error count in 3 min and latency of mice (x±s,n=7) |
大黄酚对小鼠空间学习记忆功能的改善见表 2,大黄酚可提高小鼠空间学习记忆能力,中、高剂量组可使小鼠平均逃避潜伏期和游泳总路径显著缩短,与对照组相比差异均具有统计学意义(P < 0.01);低剂量组可轻度改善小鼠空间学习记忆能力,但与对照组相比差异无显著性。
| 表 2 大黄酚对小鼠平均逃避潜伏期和游泳总路径的影响 (x±s,n=7) Table 2 Effects of Chry on swimming distance and average escape latency of mice (x±s, n=7) |
原代培养小鼠星形胶质细胞,不同质量浓度大黄酚(0.1、1.0、10.0 μg/mL)处理细胞1、2、3周。RT-PCR检测c-fos、c-jun mRNA表达。中、高浓度大黄酚上调c-fos、c-jun mRNA表达,在2周处表达增加,并长时维持此水平(P < 0.05)(图 1)。不同浓度大黄酚处理细胞1周不引起c-fos、c-jun mRNA表达改变,且低浓度大黄酚无上调作用。ip给予不同质量浓度大黄酚(0.1、1.0、10.0 mg/kg)14 d,取小鼠皮层组织,中、高浓度大黄酚上调c-fos、c-jun mRNA表达,但低浓度大黄酚无上调作用(图 2),ip给予大黄酚1周,c-fos、c-jun mRNA表达无变化。与体内实验结果相似。
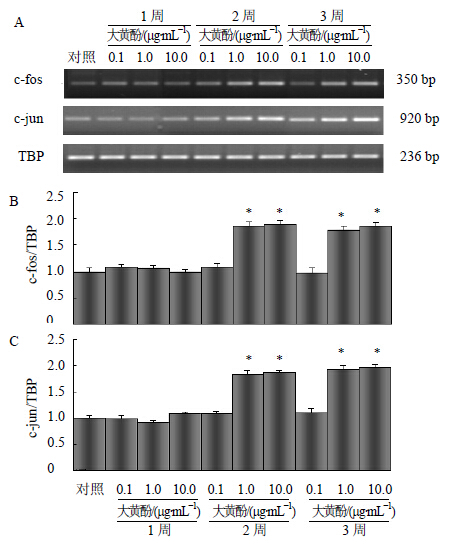 | 与对照组比较:*P < 0.05 *P < 0.05 vs control group 图 1 大黄酚(0.1、1.0、10.0 μg/mL)处理1、2、3周小鼠星形胶质细胞中c-fos和c-jun mRNA的表达Fig. 1 mRNA Expression of c-fos and c-jun in primary cultured astrocytes treated with Chry (0.1, 1.0, and 10.0 g/mL) for 1, 2, and 3 weeks |
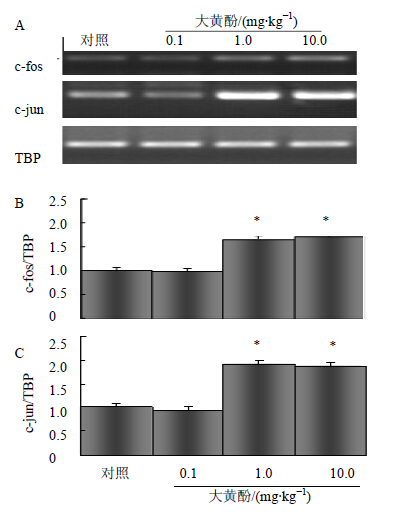 | 与对照组比较:*P < 0.05 *P < 0.05 vs control group 图 2 大黄酚(0.1、1.0、10.0 mg/kg)处理14 d小鼠脑皮层组织中c-fos和c-jun mRNA的表达Fig. 2 mRNA Expression of c-fos and c-jun in brain tissue of mice treated with Chry (0.1, 1.0, and 10.0 mg/kg) for 14 d |
为了进一步研究大黄酚上调c-fos和c-jun mRNA的机制,分别用中、高质量浓度大黄酚(1.0、10 μg/mL)、谷氨酸(50 μmol/L)和MK-801(1 μmol/L)处理细胞2周。大黄酚和谷氨酸均上调c-fos和c-jun mRNA表达,MK-801抑制上述反应(图 3)。
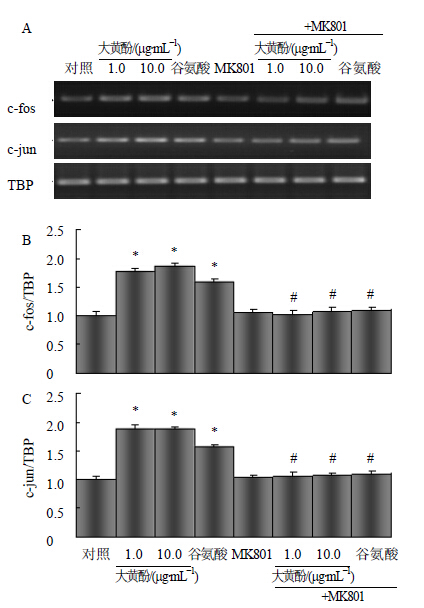 | 与对照组比较:*P < 0.05;与同组加入MK801前比较:#P < 0.05 *P < 0.05 vs control group; #P < 0.05 vs same group before MK801 图 3 非竞争性NMDA受体抑制剂MK801抑制大黄酚诱导c-fos、c-jun mRNA表达上调Fig. 3 Inhibition of noncompetitive NMDA acceptor inhibitor MK801 on upregulation of c-fos and c-jun expression induced by Chry |
学习记忆是人类和动物重要的大脑高级活动,研究表明,学习记忆过程与脑内c-fos和c-jun基因表达密切相关。c-fos属于fos蛋白家族。fos蛋白家族是一组转录因子,包括c-fos、fosB、fra-1、fra-2和delta-fosB(为fosB的剪接变体)。fos家族成员可以和jun家族成员形成一组蛋白激活因子1(activating protein-1,AP-1)蛋白二聚体,后者可以结合于目的基因启动子和增强子的TPA敏感部 位[11]。所有的AP-1蛋白均有一个亮锌部位以便二聚体形成和DNA结合。很多因素可以影响fos和jun蛋白表达,例如不同的学习训练类型、第二信使(蛋白激酶A、蛋白激酶C、钙离子等)及某些药物(谷氨酸、乙酰胆碱、人参皂苷等)。受调控后的fos和jun蛋白又可以进一步影响蛋白稳定性、蛋白结合活力、一些转录因子的间接激活潜力等[3]。
谷氨酸作为中枢神经系统兴奋性递质与学习记忆有着十分密切的关系。研究表明NMDA受体激动剂可上调脑c-fos基因表达,并且NMDA受体激活先于c-fos、c-jun等早期基因的表达。
大黄酚作为大黄有效成分之一,大量实验研究已明确其改善学习记忆的药理作用,但从分子水平探讨其改善学习记忆的机制尚未见报道。本课题采用连续ip大黄酚14 d,模型小鼠学习记忆能力及空间探索能力均出现不同程度的提高,同时c-fos和c-jun mRNA表达上调。体内实验结果显示大黄酚于2周处诱导c-fos和c-jun mRNA表达上调,且长时维持此水平。低浓度谷氨酸同样可以上调c-fos和c-jun mRNA表达,而非竞争性NMDA受体抑制剂MK801可抑制上述作用,提示大黄酚可能通过激活谷氨酸受体来诱导c-fos和c-jun基因表达。但大黄酚提高小鼠学习记忆能力是否还具有其他方面的机制有待进一步研究。
| [1] | Morgan J I, Curran T. Stimulus-transcription coupling in the nervous system: involvement of the inducible proto-oncogenes fos and jun[J]. Annu Rev Neurosci, 1991, 14: 421-451 . |
| [2] | Ohiwa N, Saito T, Chang H, et al. Differential responsiveness of c-Fos expression in the rat medulla oblongata to different treadmill running speeds[J]. Neurosci Res, 2006, 54(2): 124-132 . |
| [3] | 张玉秋, 梅俊. 学习记忆对脑内c-fos基因表达的影响[J]. 生命科学, 2000, 12(5): 228-231. |
| [4] | Chandramohan Y, Droste S K, Reul J M. Novelty stress induces phospho-acetylation of histone H3 in rat dentate gyrus granule neurons through coincident signalling via the N-methyl-D-aspartate receptor and the glucocorticoid receptor: relevance for c-fos induction[J]. J Neurochem, 2007, 101(3): 815-528. |
| [5] | 李淑娟, 李春更, 侯勇, 等. 大黄酚抗衰老作用研究进展[J]. 河北北方学院学报, 2009, 26(1): 69-70. |
| [6] | 潘陈为, 潘珍珍, 金玲湘, 等. 血氨升高对大鼠空间学习记忆能力的影响[J]. 温州医学院学报, 2009, 39(5): 462-463. |
| [7] | Hertz L, Peng L, Lai J C. Functional studies in cultured astrocytes[J]. Methods, 1998; 16(3): 293-310. |
| [8] | Elkeles A, Juven-Gershon T, Israeli D, et al. The c-fos proto-oncogene is a target for transactivation by the p53 tumor suppressor[J]. Mol Cell Biol, 1999; 19(4): 2594-2600 . |
| [9] | Asim M, Chaturvedi R, Hoge S, et al. Helicobacter pylori induces ERK-dependent formation of a phospho-c-fos·c-jun activator protein-1 complex that causes apoptosis in macrophages[J]. J Biol Chem, 2010, 285(26): 20343-20357 . |
| [10] | El Marjou M, Montalescot V, Buzyn A, et al. Modifications in phospholipase D activity and isoform expression occur upon maturation and differentiation in vivo and in vitro in human myeloid cells[J]. Leukemia, 2000, 14(12): 2118-2127. |
| [11] | 孙开宏. c-fos基因在学习记忆及运动中表达的研究进展[J]. 中国康复理论与实践, 2008, 14(6): 542-544. |
 2015, Vol. 38
2015, Vol. 38


