丹参酮ⅡA是丹参中的主要脂溶性活性成分,属于二萜醌类化合物[1],具有增加冠脉流量、抗心肌缺血、抗心律失常、抗动脉粥样硬化等作用。丹参酮ⅡA水溶性差,渗透性低,目前上市剂型为丹参酮ⅡA磺酸钠注射剂,但其存在易分解、稳定性差等问题,致使临床应用受到限制[2-3]。口服的给药方式因为相对安全、方便而更易为广大患者接受。口服给药方式的药物在胃肠道内的稳定性是其在机体内吸收、代谢和起效的一个重要环节。普通口服制剂在胃肠道中对药物成分没有保护作用,因此开发一种新型纳米给药系统,提高药物胃肠道稳定性、提高口服生物利用度是亟待解决的问题。本实验结合本研究团队新研制的纳米口服给药系统脂化乳,以丹参酮ⅡA为模型药物,制备含有稳定体系的丹参酮ⅡA脂化乳以及不含有稳定体系的脂化乳粒。以原型药物丹参酮ⅡA为对照,采用紫外分光光度法对原型药物、丹参酮ⅡA脂化乳粒、脂化乳在人工胃、肠液中的变化进行考察,以期达到改善丹参酮ⅡA胃肠稳定性,提高口服生物利用度的目的,为脂化乳作为口服制剂的合理性和可行性研究提供依据。
1 仪器与试药 1.1 仪器TU-1810APC型紫外分光光度计(北京普析通用仪器有限责任公司);CP225D、BS210S型电子天平(德国Sartorius公司);KQ-5200DE型数控超声波清洗器(昆山市超声仪器有限公司)
1.2 试药丹参酮ⅡA(宝鸡市国康生物科技有限公司,批号120428,质量分数>98%);蛋黄卵磷脂PC-98T(高纯度注射级,日本丘比株式会社);蛋黄卵磷脂(PL-100M,上海艾韦特医药科技有限公司,批号93685-90-6);大豆卵磷脂(德国Lipoid公司,质量分数>94%);氢化大豆磷脂(HSPC,上海艾韦特医药科技有限公司,批号92128-87-5);中链甘油三酸酯(MCT)、蓖麻油聚氧乙烯(医用级)、大豆油(药用级)购自西安悦来医药科技有限公司;十二烷基硫酸钠(SDS);胃蛋白酶(Sigma Vetec公司,批号V900497);胰蛋白酶(Sigma公司,批号85450C);甲醇(色谱纯,Fisher公司)。
2 方法与结果 2.1 样品的制备 2.1.1 丹参酮ⅡA混悬液的制备取适量丹参酮ⅡA,加入SDS溶液中,制成0.5 mg/mL丹参酮ⅡA混悬液。
2.1.2 丹参酮ⅡA脂化乳、脂化乳粒的制备称取处方量丹参酮ⅡA10 mg,与2.625 g油相一起溶于适量无水乙醇中,60 ℃水浴加热至完全溶解,搅拌下加入18 mL,60 ℃含有适量稳定材料聚丙烯酰胺的蒸馏水中,高压乳匀机中60 MPa循环1 min,即得丹参酮ⅡA脂化乳。所得丹参酮ⅡA脂化乳粒径为(267.8±5.66)nm,多分散系数(PDI)为0.073±0.04,电位为(−4.65±0.53)mV。
丹参酮ⅡA脂化乳粒制备方法与脂化乳相同,但水相中不加入稳定材料聚丙烯酰胺。丹参酮ⅡA脂化乳粒的粒径为(252.2±6.03)nm,PDI为0.059±0.08、电位为(−5.88±0.53)mV。
2.2 人工胃肠液的配制取稀盐酸16.4 mL,加水约800 mL与10 g胃蛋白酶摇匀后,加水稀释成1 000 mL,即得人工胃液(pH 1.0)。
取磷酸二氢钾6.8 g,加水500 mL使溶解,用0.1 mol/L NaOH溶液调节pH值至6.8;另取胰酶10 g,加水适量使溶解,将两液混合后,加水稀释至1 000 mL,即得人工肠液(pH 6.8)。
2.3 丹参酮ⅡA测定方法的建立 2.3.1 标准母液的配制精密量取干燥至恒定质量的丹参酮ⅡA 7.5 mg,置于25 mL棕色量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得300 μg/mL丹参酮ⅡA标准母液。
2.3.2 测定波长的选择将丹参酮ⅡA溶液于190~400 nm进行全波长扫描,结果丹参酮ⅡA在266 nm处有最大吸收,因此选定266 nm作为测定波长。
2.3.3 标准曲线的绘制分别精密量取丹参酮ⅡA标准母液30、50、100、200、300、500 μL,分别置于10 mL棕色量瓶中,加甲醇至刻度,分别得到质量浓度分别为0.9、1.5、3.0、6.0、9.0、15.0 μg/mL的系列溶液。以甲醇作参比,分别测定266 nm处吸光度(A),记录A值。以A值对质量浓度进行线性回归,得回归方程A=0.055 7 C+0.073 2(r=0.984 5)。结果表明,丹参酮ⅡA质量浓度在0.9~15 μg/mL与吸光度值线性关系良好。
2.3.4 精密度试验取丹参酮ⅡA适量,精密称定,配成6.0 μg/mL溶液,在266 nm处连续平行测定6次,记录A值,结果A值的RSD值为2.98%。
2.3.5 稳定性试验取丹参酮ⅡA脂化乳供试品溶液,室温条件下避光保存,分别于0、2、4、8、24、48 h测定A值,结果其RSD值为3.63%。
2.3.6 重复性试验精密吸取同一批丹参酮ⅡA脂化乳6份,制备供试品溶液,测定A值,结果其RSD值为3.19%。
2.3.7 加样回收率试验取已知含量的丹参酮ⅡA脂化乳供试品溶液6份,各0.1 mL于10 mL量瓶中,其中3份加入0.1 mL丹参酮ⅡA对照品溶液,另外3份加入0.2 mL丹参酮ⅡA对照品溶液,混匀,测定A值,计算得平均回收率为104.8%,RSD值为3.62%。
2.3.8 供试品溶液中丹参酮ⅡA的测定精密吸取丹参酮ⅡA混悬液、脂化乳粒、脂化乳各1 mL,加甲醇6 mL,摇匀,在266 nm处测定A值,计算供试样品液中丹参酮ⅡA的质量浓度。
2.4 丹参酮ⅡA混悬液、脂化乳、脂化乳粒在人工胃液中的变化精密量取丹参酮ⅡA混悬液、脂化乳、脂化乳粒各5 mL,加入适量人工胃液中,置于37 ℃水浴中以80 r/min搅拌。每隔0.5 h取样1 mL,连续取样3 h。每次取出的1 mL样品加入6 mL甲醇以灭活胃蛋白酶及破乳后,在266 nm处测定A值,计算不同制剂中丹参酮ⅡA。与供试样品液中质量浓度(100%)进行比较,计算平均剩余量,结果见图 1。
|
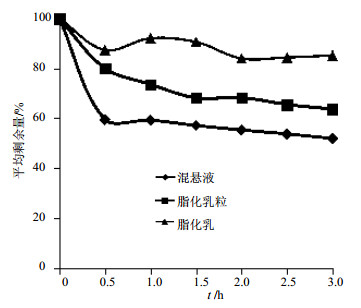
图 1 不同制剂中丹参酮ⅡA在人工胃液中的变化 Fig. 1 Changes of tanshinone ⅡA in different preparations in artificial gastric juice |
可见不同制剂中丹参酮ⅡA在人工胃液中的质量浓度均有所降低,但脂化乳、脂化乳粒均较混悬液中丹参酮ⅡA质量浓度高。在人工胃液中,3 h后混悬液中丹参酮ⅡA质量浓度比脂化乳粒少11.8%、比脂化乳少33.3%。增加稳定体系的脂化乳效果均优于不含稳定体系的脂化乳粒,说明稳定体系有助于进一步提高制剂稳定性。同时脂化乳、脂化乳粒均能提高所包载药物的稳定性。
2.5 丹参酮ⅡA混悬液、脂化乳、脂化乳粒在人工肠液中的变化精密量取丹参酮ⅡA混悬液、脂化乳、脂化乳粒各5 mL,加入适量人工肠液中。样品置于37 ℃水浴中以80 r/min搅拌。每隔1 h取样1 mL,连续取样6 h。每次取出的1 mL样品加入6 mL甲醇以灭活胃蛋白酶及破乳后,在266 nm处测定A值,计算不同制剂中丹参酮ⅡA的质量浓度。与供试样品液中质量浓度(100%)进行比较,计算平均剩余量,结果见图 2。
|
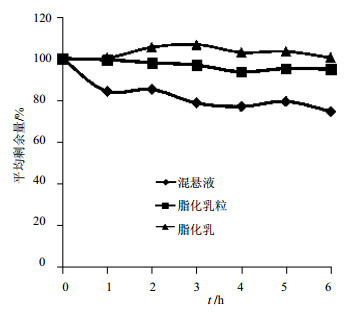
图 2 不同制剂中丹参酮ⅡA在人工肠液中变化 Fig. 2 Changes of tanshinone ⅡA in different preparations in artificial intestinal juice |
可见脂化乳粒、脂化乳在人工肠液中丹参酮ⅡA质量浓度几乎没有变化,混悬液中丹参酮ⅡA质量浓度有所降低,但较胃液中降低幅度有所缓和。在人工肠液中,6 h后混悬液中丹参酮ⅡA质量浓度比脂化乳粒少20.3%、比脂化乳少25.8%。结果说明脂化乳、脂化乳粒均能提高人工肠液中所包载药物丹参酮ⅡA的稳定性。
3 讨论药物口服吸收的主要场所在胃肠道,胃肠道的pH值和蛋白酶的消化作用会致使药物分解失活。本实验采用的模型药物丹参酮ⅡA具有较好的药理活性,但其在胃中的不稳定性影响其口服吸收,其口服绝对生物利用度低于3.5%[5]。脂化乳给药系统口服有助于提升丹参酮ⅡA胃肠道稳定性、促进吸收。丹参酮ⅡA在人工胃液的酸性环境中质量浓度随时间延长而明显降低。但在人工肠液中,丹参酮ⅡA质量浓度降低不明显,与文献报道[4]在较高pH值条件下pH值对丹参酮ⅡA的稳定性基本无影响一致。
本实验从提高药物制剂在人工胃肠液中稳定性的角度,阐释丹参酮ⅡA脂化乳口服给药的合理性。由研究结果可知,丹参酮ⅡA脂化乳、脂化乳粒均能提高人工胃、肠液中所包载丹参酮ⅡA的稳定性,且脂化乳效果优于脂化乳粒,提示稳定体系有助于进一步提高人工胃、肠液中制剂稳定性。
综上所述,丹参酮ⅡA脂化乳可提高药物胃肠道中稳定性,从而提高其口服生物利用度,具有广阔的应用前景。
| [1] |
刘海波, 徐峻, 彭勇, 等.
丹参活血化瘀活性成分的靶标[J]. 物理化学学报, 2010, 26(1) : 199–205.
( 0) 0)
|
| [2] |
张志荣, 裘福荣.
丹参酮ⅡA药理作用研究进展[J]. 医药前沿, 2016, 6(12) : 32–34.
( 0) 0)
|
| [3] |
Sun J H, Yang M, Wang X M, et al.
Identification of tanshinones and their metabolites in rat bile after oral administration of TTE-50, a standardized extract of Salvia miltiorrhiza by HPLC-ESI-DAD-MSn[J]. J Pharm Biomed Anal, 2007, 44(2) : 564–574.
DOI:10.1016/j.jpba.2006.11.003 ( 0) 0)
|
| [4] |
刘梅, 夏鑫华.
丹参酮ⅡA的化学稳定性研究[J]. 中药材, 2010, 33(4) : 606–609.
( 0) 0)
|
| [5] |
田葆萍, 袁志芳, 张兰桐.
丹参及其制剂的体内药代动力学研究概述[J]. 中国药房, 2003, 14(6) : 375–376.
( 0) 0)
|
 2017, Vol. 32
2017, Vol. 32

