2. 天津市第三中心医院 检验科, 天津 300170
2. Department of Clinical Laboratory, Tianjin Third Central Hospital, Tianjin 300170, China
依那普利为不含巯基的血管紧张素转化酶抑制剂(ACEI),作为前药在体内经脱乙酰基代谢成活性代谢产物依那普利拉,对血管紧张素转化酶起强烈抑制作用,降低血管紧张素Ⅱ的含量,舒张血管,降低血压,主要经肾脏排出体外[1]。依那普利对血管紧张素转化酶的抑制作用约为卡托普利的3倍,降压作用高效持久,在临床上应用比较广泛。依那普利不仅可以单独用于治疗高血压,还可与其他类型的抗高血压药合用物,如钙离子通道抑制剂、利尿药等,提高药物疗效,降低不良反应,发挥协同降压作用。此外,近年来研究发现,依那普利在治疗慢性肺心病、冠状动脉疾病、改善左心室功能、慢性肾小球肾炎、高胰岛素血症、糖尿病肾病、改善血管内皮、治疗神经心源性晕厥等方面效果显著[2]。但是,与钙离子通道抑制剂等相比,ACEI类降压药的不良反应较多,近年来依那普利的不良反应也有报道[3, 4]。因此,检测依那普利的活性代谢产物依那普利拉的血药浓度在临床上具有重要意义,尤其是肝肾功能减退的患者。本实验采用快速、灵敏的LC-MS/MS法,通过测定依那普利代谢产物依那普利拉的经时血药浓度,考察依那普利在大鼠体内的药动学特征。
1 材料 1.1 药品与试剂马来酸依那普利原料药(质量分数>95%)、依那普利拉对照品(批号20040815,质量分数99.5%)、贝那普利拉(批号09081001,质量分数99.1%)对照品均由山东绿因药业有限公司提供。乙腈、甲醇均为色谱纯,美国J.T. Baker公司生产;乙酸铵、氢氧化钠均购自中国医药上海化学试剂公司。
1.2 仪器Agilent 1150 series HPLC,6410 Triple Quad MS/MS(美国安捷伦科学技术公司);1 mL Sep-pak C18固相萃取小柱(美国Waters公司);梅特勒-托利多AX-205电子天平(梅特勒-托利多仪器有限公司);XW-80A型旋涡混合器(上海精科实业有限公司);ABOTT高速离心机(美国雅培公司);PK514BP超声清洗器(德国BANDEL);BHW-IV型电热恒温水温箱(北京医疗设备厂);H97-A恒温磁力搅拌器(梅颖浦仪器仪表制造有限公司)。
1.3 实验动物健康雄性Wistar大鼠6只,清洁级,体质量为(230±10)g,购自山东省实验动物中心,许可证号SYXK(鲁)2014 0010。实验鼠用配合饲料由山东省实验动物中心提供。动物房12 h/12 h明暗交替,温度(20±2) ℃,湿度(45±5)%,大鼠均自由进食饮水。
2 方法与结果 2.1 溶液的配制精密称取依那普利拉对照品10 mg,置25 mL量瓶中,用50%甲醇溶液溶解并稀释至刻度,摇匀,配成质量浓度为0.2 mg/mL。精密称取贝那普利拉对照品10 mg,置10 mL量瓶中,用甲醇溶解并加至刻度,得1.0 mg/mL母液,用流动相稀释至刻度,得5 μg/mL溶液,放入4 ℃保存,使用时放至室温。
2.2 样品处理取血浆样品200 μL,加入内标10 μg/mL贝那普利拉溶液15 μL,混匀,加入1 mol/L氢氧化钠15 μL,充分涡旋混匀后,留待上样。Sep-pak C18固相萃取小柱依次用1 mL甲醇、1 mL纯净水活化2遍,把处理好的加标血浆上样,然后用1 mL纯净水洗涤,弃去洗涤液。用1 mL甲醇洗脱,洗脱液于40 ℃水浴中用N2吹干,残渣用100 μL流动相溶解,即得。
2.3 测定条件 2.3.1 色谱与质谱条件Diamond C18色谱柱(150 mm×4.6 mm,5 μm);流动相:乙腈-5 mmol/L乙酸铵(45∶55);体积流量:0.5 mL/min;柱温:30 ℃;进样量:5 μL。
采用ESI(+)离子源;干燥气(N2)体积流量11.0 L/min,压力275.8 kPa,温度350 ℃;毛细管电压3 500 V;多级反应监测(MRM)模式,正离子模式;EMV为400 eV。依那普利拉与内标贝那普利拉的定量离子对分别为m/z 349.1→206.2,397.2→351.2。
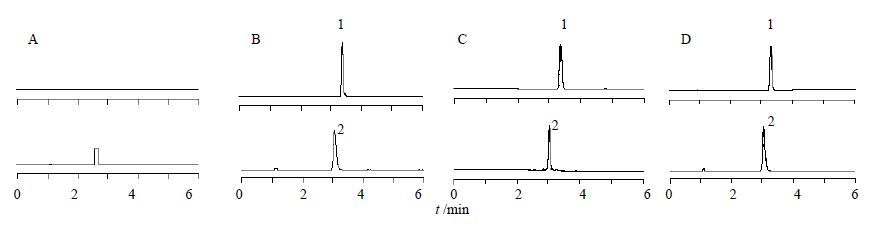
2.3.2 专属性试验大鼠空白血浆、依那普利拉和内标贝那普利拉对照品溶液、空白血浆外加依那普利拉和内标贝那普利拉、大鼠给药后血浆样本处理后进样测定,所得的色谱图见图 1。依那普利拉、内标贝那普利拉出峰时间分别为3.45、3.08 min。结果表明,各色谱峰形良好,血浆中的内源性物质不干扰测定。
|
图 1 空白血浆(A)、依那普利拉500 ng/mL和内标溶液(B)、空白血浆加依那普利拉50 ng/mL、内标溶液(C)和依那普利给药后3 h血浆样品(D)色谱图 Fig. 1 Chromatograms of blank plasma (A),enalaprilat 500 ng/mL and I.S. standard solution (B),blank plasma sample spiked with enalaprilat 50 ng/mL and I.S. (C),and plasma sample 3 h after ig administration (D) 1-依那普利拉 2-内标贝那普利拉 1-enalaprilat 2- I.S. benazeprilate |
2.3.3 标准曲线与最低定量限
取空白血浆适量,用对照品溶液配制含依那普利拉20、50、100、200、500、1 000、1 500 ng/mL的样本,每个浓度5份样本,处理后进样分析。以待测物质量浓度为横坐标,待测物与内标峰面积比值为纵坐标,用加权法(W=1/x2)进行回归运算,得回归方程Y=7.09×10-4 X-0.016 2(r=0.995),结果表明依那普利拉在20~1 500 ng/mL线性关系良好。
以信噪比(S/N)大于10确定其最低定量限。依那普利拉质量浓度为20 ng/mL时,S/N为10.3,因此,最低定量限为20 ng/mL。
2.3.4 精密度和准确度试验取空白血浆适量,用对照品溶液配制含依那普利拉50、200、1 000 ng/mL的样本,每个浓度5份样本,连续测定3 d,根据当日标准曲线回归方程计算依那普利拉的质量浓度,日内、日间RSD和RE分别表示精密度和准确度,见表 1。
| 表 1 精密度和准确度试验结果(x±s,n =5) Table 1 Results of precision and accuracy test (x±s,n =5) |
2.3.5 稳定性试验
取空白血浆适量,用对照品溶液配制含依那普利拉50、200、1 000 ng/mL的样品,置超低温冰箱-80 ℃冷冻保存。分别经提取后室温放置7 h、冻融2次以及冷冻14 d后,进行样品分析,每个浓度进行5个样本,见表 2。结果表明,血浆样本中依那普利拉经冻融2次以及长期冷冻后稳定性良好。
| 表 2 稳定性试验结果(x±s,n =5) Table 2 Results of stability test (x±s,n =5) |
2.3.6 回收率与基质效应试验
取空白大鼠血浆分别配制依那普利拉质量浓度分别为50、200、1 000 ng/mL的质控样品,进行样本处理后,测得峰面积A1;以对照品溶液配制质量浓度分别为100、400、2 000 ng/mL的标准样本,测得峰面积A2;200 μL空白血浆处理后,分别采用100、400、2 000 ng/mL标准溶液100 μL复溶,测得峰面积A3。以A1/A3表示提取回收率,A3/A2表示基质效应,见表 3。结果表明,依那普利拉的回收率大于85%,且回收率无浓度相关性。
| 表 3 提取回收率和基质效应试验结果(x±s,n =5) Table 3 Results of recovery test and matrix effect test (x±s,n =5) |
2.4 药动学试验
雄性Wister大鼠6只,适应性饲养1周。禁食12 h后,分别ig依那普利15 mg/kg。于给药前和给药后1、2、3、4、6、8、12、24 h颈静脉窦取血1 mL,立即移入肝素抗凝管中,静置,3 500 r/min低温离心5 min,取上层血浆,-80 ℃冷冻保存。整个实验过程中大鼠状态良好,进水进食情况正常,无脱落。
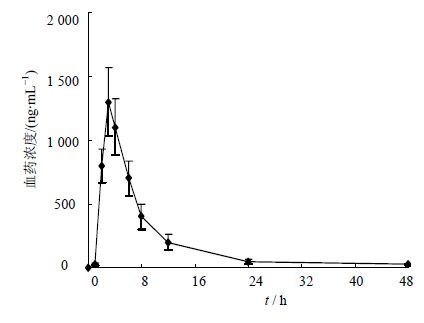
血浆样本处理后,采用HPLC-MS/MS法测定样品中依那普利拉经时血浓度。大鼠的血药浓度-时间曲线见图 2。采用DAS 2.2药动学分析软件,以非房室模型处理血浆浓度-时间数据,依那普利拉的主要药动学参数见表 4。
|
图 2 大鼠血浆中依那普利拉的浓度-时间曲线(x±s,n = 6) Fig. 2 Plasma concentration-time curve of enalaprilat in rats (x±s,n = 6 ) |
| 表 4 大鼠体内依那普利拉主要药动学参数(x±s,n =6) Table 4 Major pharmacokinetic parameters of enalaprilat in rats (x±s,n =6) |
3 讨论
目前依那普利拉的测定方法报道较多,有GC法[5]、毛细管电泳[6]、酶联法[7-8]、HPLC-MS法[9]以及LC-MS/MS法[1, 10-13]等。以上主要涉及药物制剂和人血浆样本中依那普利拉的测定。本实验建立方便可行的大鼠血浆中依那普利拉的测定方法,用于研究依那普利在大鼠体内的药动学以及相关的药物相互作用。
大鼠血浆样本的预处理方法主要有液-液萃取法和固相萃取法。本实验考察了常用的多种有机溶剂的萃取效果,如二氯甲烷、醋酸乙酯、异丙醇、氯仿,结果发现上述有机溶剂不能有效地去除大鼠血浆中内源性物质的干扰,或绝对回收率较低。采用固相萃取法进行样本预处理,并对洗脱液的组成和顺序进行了考察,结果显示Waters Sep-pak C18固相萃取小柱对大鼠血浆中依那普利拉的分离效果较好。固相萃取柱依次用1 mL甲醇、1 mL纯净水活化2遍,血浆样品上样后依次用1 mL纯净水洗涤,1 mL甲醇洗脱,能够有效地除去血浆内源性物质的干扰,降低基质效应,回收率符合要求。实验过程中对流动相的组成也进行了考察,甲醇造成测定背景不稳定并且基线较高,药物浓度-峰面积的线性关系欠佳,乙腈可改善上述现象。乙酸铵可以优化色谱峰形,降低基质效应,提高信号强度。内标对样品的测定具有至关重要,本实验也考察了包括多种ACEI类在内的的化合物。贝那普利与贝那普利拉、依那普利拉的提取方式相对一致,但是贝那普利的峰面积重现性差,可能与大鼠血浆中存在的药物代谢酶有一定关系,所以本实验采用同是ACEI类代谢产物的贝那普利拉作为内标。
综上所述,本实验所采用的血浆样品的处理方法可有效提取依那普利拉,并且无浓度相关性。LC-MS/MS法简便易行,最低定量限可达20 ng/mL,整个线性范围宽广,可适用于依那普利多种剂量的代谢产物依那普利拉的测定。本方法可以快速有效的测定大鼠血浆中依那普利拉的浓度,可用于研究依那普利在体内的代谢以及代谢物依那普利拉的血药浓度检测和药动学研究。
| [1] |
Burckhardt B B, Tins J, Laeer S. Simultaneous quantitative and qualitative analysis of aliskiren, enalapril and its active metabolite enalaprilat in undiluted human urine utilizing LC-ESI-MS/MS[J].
Biomed Chromatogr,2014, 28 (12) : 1679-1691.
( 0) 0)
|
| [2] |
Gerstein H C. Enalapril reduced the risk for developing new-onset diabetes in left ventricular dysfunction[J].
ACP J Club,2003, 139 (3) : 68.
( 0) 0)
|
| [3] |
Soejima H, Ogawa H, Suefuji H, et al. Comparison of effects of losartan versus enalapril on fibrinolysis and coagulation in patients with acute myocardial infarction[J].
Am J Cardiol,2001, 87 (12) : 1408-1411.
( 0) 0)
|
| [4] |
Spence J D. Effect of indomethacin on blood pressure in elderly people with essential hypertension well controlled on amlodipine or enalapril[J].
Am J Hypertens,2001, 14 : 835.
( 0) 0)
|
| [5] |
Shioya H, Shimojo M, Kawahara Y. Determination of enalapril and its active metabolite enalaprilat in plasma and urine by gas chromatography/mass spectrometry[J].
Biomed Chromatogr,1992, 6 (2) : 59-62.
( 0) 0)
|
| [6] |
Trapp O, Trapp G, Schurig V. Determination of the cis-trans isomerization barrier of enalaprilat by dynamic capillary electrophoresis and computer simulation[J].
Electrophoresis,2004, 25 (2) : 318-323.
( 0) 0)
|
| [7] |
Arafat T, Awad R, Hamad M, et al. Pharmacokinetics and pharmacodynamics profiles of enalapril maleate in healthy volunteers following determination of enalapril and enalaprilat by two specific enzyme immunoassays[J].
J Clin Pharm Ther,2005, 30 (4) : 319-328.
( 0) 0)
|
| [8] |
Matalka K, Arafat T, Hamad M, Jehanli A. Determination of enalapril and enalaprilat by enzyme linked immunosorbent assays: application to pharmacokinetic and pharmacodynamic analysis[J].
Fundam Clin Pharmacol,2002, 16 (3) : 237-244.
( 0) 0)
|
| [9] |
文爱东, 杨志福, 王志睿, 等. 马来酸依那普利片的人体生物等效性研究[J].
中国药学杂志,2007, 42 (7) : 524-528.
( 0) 0)
|
| [10] |
Cheregi M, Albu F, Udrescu S, et al. Greener bioanalytical approach for LC/MS-MS assay of enalapril and enalaprilat in human plasma with total replacement of acetonitrile throughout all analytical stages[J].
J Chromatogr B Analyt Technol Biomed Life Sci,2013, 927 : 124-132.
( 0) 0)
|
| [11] |
Ramusovic S, Thielking G, Läer S. Determination of enalapril and enalaprilat in small human serum quantities for pediatric trials by HPLC-tandem mass spectrometry[J].
Biomed Chromatogr,2012, 26 (6) : 697-702.
( 0) 0)
|
| [12] |
张志涛, 蒋志文. 依那普利滴丸和片剂在人体内的药动学与生物等效性[J].
中国新药与临床杂志,2008, 27 (12) : 903-907.
( 0) 0)
|
| [13] |
董淑英, 李见春, 张志涛, 等. 马来酸依那普利口腔崩解片健康人体生物等效性研究[J].
中国新药杂志,2008, 17 (9) : 782-786.
( 0) 0)
|
 2016, Vol. 31
2016, Vol. 31


