2. 天津药物研究院 天津市药物设计与发现重点实验室, 天津 300193
2. Tianjin Key Laboratory of Molecular Design and Drug Discovery, Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
达比加群酯作为最前沿的口服直接凝血酶抑制剂,主要用于预防非瓣膜性房颤患者的卒中和全身性栓塞[1]。该化合物自2002年由德国勃林格殷格翰公司研发报道至今,其理化性质、成药特性、合成工艺、制剂工艺以及药理药效作用在药物研发相关领域受到了极大关注[2-4]。其成盐化合物中的典型代表达比加群酯甲磺酸盐已在2008年研发成功并上市[5]。但是,甲磺酸盐的使用存在着一定缺陷:一方面达比加群酯甲磺酸盐的稳定性并不是非常理想,在强力破坏性条件下样品易于降解、产生较多杂质(≥5%),为制剂工艺和后期储藏运输带来挑战[6];另一方面甲磺酸盐的使用极有可能产生基因毒性杂质甲磺酸酯类,在药品使用过程中存在潜在风险[7-8]。因此,寻找更为稳定的达比加群酯新盐,同时避免基因毒性杂质的引入在抗凝药物研发中显得十分必要。
达比加群酯的结构中包括两个氨基,极易与各种酸根形成达比加群酯盐[9-12],达比加群酯及6种达比加群酯作为最前沿的口服直接凝血酶抑制剂,主要用于预防非瓣膜性房颤患者的卒中和全身性栓塞[1]。该化合物自2002年由德国勃林格殷格翰公司研发报道至今,其理化性质、成药特性、合成工艺、制剂工艺以及药理药效作用在药物研发相关领域受到了极大关注[2-4]。其成盐化合物中的典型代表达比加群酯甲磺酸盐已在2008年研发成功并上市[5]。但是,甲磺酸盐的使用存在着一定缺陷:一方面达比加群酯甲磺酸盐的稳定性并不是非常理想,在强力破坏性条件下样品易于降解、产生较多杂质(≥5%),为制剂工艺和后期储藏运输带来挑战[6];另一方面甲磺酸盐的使用极有可能产生基因毒性杂质甲磺酸酯类,在药品使用过程中存在潜在风险[7-8]。因此,寻找更为稳定的达比加群酯新盐,同时避免基因毒性杂质的引入在抗凝药物研发中显得十分必要。
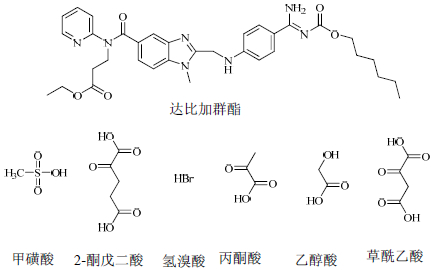
达比加群酯的结构中包括两个氨基,极易与各种酸根形成达比加群酯盐[9-12],达比加群酯及6种代表性酸根的结构见图 1。但是,其结构中多种活泼基团的存在(氨基、亚氨基和酯键等)使得该化合物在成盐状态下对热、湿及光照的稳定性表现各异。因此,选择具有代表性的酸根与达比加群酯成盐,深入研究不同种类达比加群酯盐在高温、高湿及光照下的降解产物,从分子结构层面上系统探究达比加群酯盐的稳定性根源是此类药物成盐形式研究中的关键问题,可为寻找稳定性良好的达比加群酯新盐提供理论指导和研究方向。
|
图 1 达比加群酯及6种代表性酸根的化学结构 Fig. 1 Chemical structure of dabigatran etexilate and six typical acids |
本研究拟以6种达比加群酯盐为考察对象,对比研究6种盐在高温、高湿以及光照条件下的杂质产生情况,并对各种盐的降解产物进行系统检测分析,为达比加群酯盐的降解特点探索及深入的稳定性研究提供参考。
1 仪器与试药HNP-250SD药品稳定性试验箱(重庆宇硕实验仪器有限公司);ML204和XS105DU电子天平(瑞士Mettler-Toledo公司);Waters e2695-2998系列高效液相色谱仪(美国Waters公司);Finnigan LCQ Advantage Max型质谱仪(美国Finnigan公司);Thermo Barnstead Nanopure超纯水机(美国Thermo-Fisher公司);Five Easy Plus pH计(瑞士Mettler-Toledo公司)。
本实验中的各种达比加群酯盐,包括甲磺酸盐、2-酮戊二酸盐、氢溴酸盐、丙酮酸盐、乙醇酸盐和草酰乙酸盐均为自制样品(质量分数≥99%,水分≤1.0%)。乙腈(色谱纯,美国飞世尔科学世界公司);乙醇(色谱纯,天津康科德科技有限公司);乙酸铵和硝酸钾均购于天津光复科技发展有限公司。本实验中用水均为超纯水。
2 方法与结果 2.1 色谱条件达比加群酯盐的纯度测定采用HPLC法,Waters Symmetry C18色谱柱(150 mm×4.6 mm,5 µm);以0.2%醋酸铵溶液(A)-乙腈(B)为流动相,梯度洗脱:0~18 min,10%B→60%B;18~30 min,60%B;30~35min,60%B→10%B;35~40 min,10%B;体积流量1.0 mL/min;柱温40 ℃;配置DAD检测器,主成分色谱峰检测波长为340 nm,杂质的检测波长分别为242、310、340 nm。
达比加群酯的降解产物分析采用LC-MS方法,Waters Symmetry C18色谱柱(150 mm×4.6 mm,5 µm);以0.2%醋酸铵溶液(A)-乙腈(B)为流动相,梯度洗脱:0~18 min,10%B→70%B;18~30 min,70%B;30~35 min,70%B→10%B;35~40 min,10%B;体积流量0.5 mL/min,柱温40 ℃。配置DAD检测器,采用波长分别为242、310、340 nm。质谱配备电子喷雾离子源,采集正离子信号,鞘气体积流量60 arb,扫气体积流量为10 arb,激发电压4.50 kV,毛细管温度300 ℃,毛细管电压14 V,棱镜电压10 V。
2.2 样品的处理所有达比加群酯盐样品在放样前均过5号筛(80目),分别称取过筛后样品约600 mg置扁形称量瓶中,在高温(60 ℃)、高湿(相对湿度92.5%)和光照(5 000 lx)3个条件下放置10 d。
2.3 供试品溶液的制备精密称取样品约30 mg,置100 mL量瓶中,加乙腈-乙醇-水(12∶3∶10)至刻度线,摇匀,超声使样品充分溶解,即得。
2.4 降解产物的结构确定6种达比加群酯盐在高温、高湿和光照条件下放置10 d,发现均在高温条件下产生杂质的量相对较高,见表 1。这种现象产生的原因是高温条件下可提供较多热量,使得分子键易于断裂;高湿条件仅提供水分,并不一定参与反应;光照条件可提供光能和有限的热能,而达比加群酯的结构对光相对稳定。
| 表 1 样品的杂质变化结果 Table 1 Results of change in the impuritiesof samples |
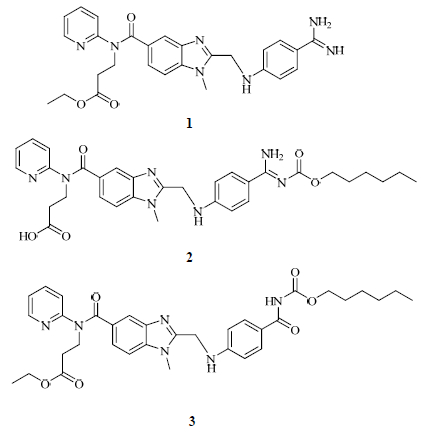
因此选用杂质含量较高的高温条件进行系统的降解产物分析。利用LC-MS法对其中代表性的样品进行测定分析,通过保留行为与相对分子质量信息综合判断,推断出3种关键的杂质,分别为N-[[2-[[[(4-氨基亚氨基甲基)苯基]氨基]甲基]-1-甲基-1H-苯并咪唑-5基]羰基]-N-2-吡啶-β-丙氨酸乙酯(1)、N-[[2-[[[4-[[[(己氧基)羰基]氨基]亚氨基甲基]苯基]氨基]甲基]-1-甲基-1H-苯并咪唑-5-基]羰基]-N-2-吡啶-β-丙氨酸(2)和N-[[2-[[[4-[[[(己氧基)羰基]氨基]羰基]苯基]氨基]甲基]-1-甲基-1H-苯并咪唑-5-基]羰基]-N-2-吡啶-β-丙氨酸乙酯(3),具体结构见图 2。
|
图 2 3种代表性降解产物的结构 Fig. 2 Structures of three typical degradation products |
2.5 降解产物的产生机制
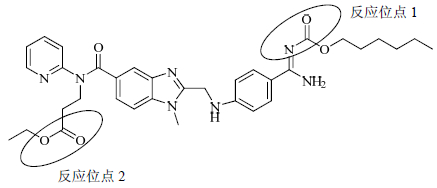
从化学结构层面推断3种杂质的产生机制,可得出杂质1是由达比加群酯结构中酰胺键断开形成,见图 3中反应位点1;杂质2是由达比加群酯结构中酯键断开形成,见图 3中反应位点2。
|
图 3 杂质1和2的产生机制 Fig. 3 Mechanism of production of impurities 1 and 2 |
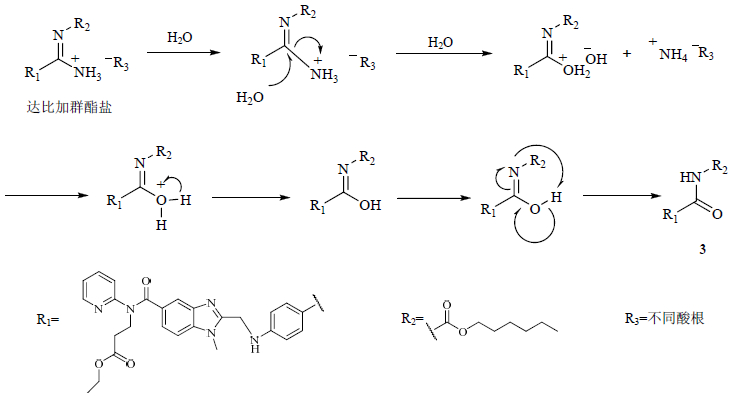
杂质3的产生机制相对较为复杂,与达比加群酯分子周边含氧基团的存在有密切关系,包括酸根中的含氧基团以及外周环境中存在的少量水分。达比加群酯结构中的脒氨基很活泼,极易在亲核基团的进攻下发生反应,产生杂质3,以水为例,具体产生机制见图 4。
|
图 4 杂质3的产生机制 Fig. 4 Mechanism of production of impurity 3 |
2.6 降解产物的测定
精密量取供试品溶液20 μL注入液相色谱仪,记录色谱图,对3D提取最大值图谱进行面积归一化定量分析,色谱图见图 5,高温条件下各杂质的量见表 2。

|
图 5 甲磺酸盐(A)、2-酮戊二酸盐(B)、氢溴酸盐(C)、丙酮酸盐(D)、乙醇酸盐(E)、草酰乙酸盐(F)的HPLC图谱 Fig. 5 HPLC chromatograms of mesylate (A), 2-ketoglutarate (B), hydrobromide(C), pyruvate (D), glycollate (E), oxalacetate (F) 1-杂质1 2-杂质2 3-杂质3 1-impurity 1 2-impurity 2 3-impurity 3 |
| 表 2 高温条件下样品中各杂质的变化结果 Table 2 Results of change in the impurities of samples under high temperature |
3 讨论
达比加群酯盐结构中酸的种类不同,导致高温条件下的降解产物也存在差异。结合现有文献报道[13-16],可初步推断出3种杂质的产生与所选酸根之间的密切联系。首先对杂质3的产生情况进行纵向分析,氢溴酸盐在高温条件下产生杂质3最少,因为氢溴酸本身结构中并无含氧基团;2-酮戊二酸盐和草酰乙酸盐在高温条件下产生杂质3的量明显高于其他酸,这种现象可归结于这两种酸结构中富含羰基和羟基(均含有3个羰基和2个羟基),其他3种盐在高温条件下产生杂质3的量并不突出。因此,杂质3的产生与酸结构中的含氧基团数目存在正相关的关系。其次,杂质1、2分别由达比加群酯结构中的酰胺键和酯键断裂产生。对表 2中数据进行分析得出:2-酮戊二酸盐和氢溴酸盐在高温降解过程中,杂质1的量远高于杂质2;而另外4种盐的降解杂质分布情况正好相反。初步推测杂质1的产生可能与酸根的还原性有直接联系。在高温条件下,酸根的还原性越强,越有利于杂质1的生成,因为氢溴酸可作为强还原剂使用,2-酮戊二酸盐在体内三羧酸循环中可充当还原剂参与谷氨酸的产生。此条件下,杂质2的产生可能与酸根的pKa有关,酸性越弱,杂质2的产生越多,反之亦然。因此,酸性较弱的乙醇酸盐和丙酮酸盐中杂质2的量明显高于其他4种盐。
综上所述,3种关键杂质的产生既与达比加群酯盐样品所处的外界环境有关,也与盐本身的结构密切相关。杂质1的产生与酸根的还原性相关,杂质2的产生与酸根的pKa相关,杂质3的产生与酸根结构中含氧基团的个数相关。但是,在同一种盐的降解过程中,杂质1、2和3的产生并不能通过酸根的单一性质来判断,需要综合所选酸根的多种结构特征进行分析判断。
通过对6种盐在高温条件下的降解产物进行深入分析,得出3种关键杂质结构,并对杂质的产生机制进行探讨。由所选酸根在3种降解杂质产生过程中的影响得出,在达比加群酯新盐的探索研究中,需要尽量选用氧化还原性弱,结构中含氧基团少及pKa值较低的酸根,减少降解杂质产生的可能性,提高达比加群酯盐的稳定性。
| [1] |
Greig S L, McKeage K. Dabigatran etexilate: a review of its use in the treatment of acute venous thromboembolism and prevention of venous thromboembolism recurrence[J].
Drugs,2014, 74 (15) : 1785-1800.
( 0) 0)
|
| [2] |
高航, 宗新杰, 刘长鹰, 等. 达比加群酯的合成工艺研究[J].
现代药物与临床,2014, 29 (12) : 1331-1333.
( 0) 0)
|
| [3] |
Hauel N H, Nar H, Priepke H, et al. Structure-based design of novel potent nonpeptide thrombin inhibitors[J].
J Med Chem,2002, 45 (9) : 1757-1766.
( 0) 0)
|
| [4] |
Mungall D. BIBR-1048 boehringer ingelheim[J].
Curr Opin Investig Drugs,2002, 3 (6) : 905-907.
( 0) 0)
|
| [5] |
Sanford M, Plosker G L. Dabigatran etexilate[J].
Drugs,2008, 68 (12) : 1699-1709.
( 0) 0)
|
| [6] |
达比加群酯胶囊(75 mg, 110 mg)使用指南 [S]. 第9版. 2013.
( 0) 0)
|
| [7] |
Evaluation of medicines for human use, guideline on the limits of genotoxic impurities [S]. 2007.
( 0) 0)
|
| [8] |
Elder D P, Teasdale A, Lipczynski A M. Control and analysis of alkyl and aryl sulfonic acids in novel active pharmaceutical ingredients (APIs)[J].
J Pharm Biomed Anal,2008, 46 (1) : 1-8.
( 0) 0)
|
| [9] |
Mihaela P, Peter S, Coen H, et al. Physiologically acceptable salts of N-[2-[4-[N-(Hexyloxycarbonyl)amidino] phenyl-aminomethyl]-1-methyl-1H-benzimidazol-5-ylcarbonyl]-N-(2-pyridyl)-beta-alanine ethyl ester [P]. WO: 2008043759, 2008-04-17.
( 0) 0)
|
| [10] |
Sieger P, Hauel N, Schmid R. Physiologically acceptable salts of N-[2-[4-[N-(Hexyloxycarbonyl)amidino]phenyl-aminomethyl]-1-methyl-1H-benzimidazol-5-ylcarbonyl]-N-(2-pyridyl)-beta-alanine ethyl ester [P]. US: 20060247278, 2006-11-02.
( 0) 0)
|
| [11] |
北京阜康仁生物制药科技有限公司. 达比加群酯新药用盐及其制备方法 [P]. CN: 102558153, 2012-07-11.
( 0) 0)
|
| [12] |
埃吉斯药物股份公开有限公司. 用于制备药物组合物的新的盐 [P]. CN: 102858762, 2013-01-02.
( 0) 0)
|
| [13] |
Guerrieri P, Jarring K, Taylor L S. Impact of counter ion on the chemical stability of crystalline salts of procaine[J].
J Pham Sci,2010, 99 (9) : 3719-3730.
( 0) 0)
|
| [14] |
Stahl P H, Wermuth C G.
Handbook of Pharmaceutical Salts Properties, Selection and Use[M]. Wcinheim: WILEY-VCH, 2002 : 265 -329.
( 0) 0)
|
| [15] |
沈芳, 苏颀, 周伟澄. 成盐药物的研究与开发[J].
药学进展,2012, 36 (4) : 151-157.
( 0) 0)
|
| [16] |
秦雪, 王成港, 兰静, 等. 新药研发中药物盐型的筛选策略[J].
现代药物与临床,2012, 27 (4) : 414-417.
( 0) 0)
|
 2016, Vol. 31
2016, Vol. 31


