2. 贵州省黔东南州人民医院 药剂科, 贵州 凯里 556000
2. Pharmaceutical Preparation Section, Qiandongnan Prefecture People's Hospital, Kaili 556000, China
银黄制剂均是由金银花提取物和黄芩提取物制成的中药复方制剂,具有清热解毒、消炎等功效,临床上主要用于治疗急慢性扁桃体炎、咽炎、上呼吸道感染等症[1-2]。市售常见剂型包括银黄片[3]、银黄口服液[4]、银黄胶囊、银黄颗粒、银黄滴丸[5]和银黄注射剂等。目前《中国药典》2015年版一部[6]收载的银黄制剂包括银黄口服液、银黄颗粒和银黄片3种剂型,且均以绿原酸及黄芩苷作为指标性成分,并均采用HPLC法对其质量进行控制。现代药理学研究表明,金银花提取物中所含有的酚酸类成分如绿原酸、异绿原酸A和异绿原酸C等具有明显的抗菌、抗炎活性[7-9],而黄芩提取物中所含有的黄酮类成分在抗菌、抗病毒、抗炎、调节免疫等方面也具有明显的药理活性[10-15]。
现有文献资料[16-19]对银黄制剂的质量控制多采用HPLC法,虽进行多指标定量测定,但检测时间均较长,检测效率较低,本实验在参考相关文献并结合前期试验的基础上,采用UPLC[20]建立了同时测定银黄制剂中的新绿原酸、绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素10种成分的方法,用于该制剂质量标准提升研究,同时本研究所建立方法亦可用于评价不同厂家银黄制剂的质量。
1 仪器和试药Acquity UPLC I-Class型超高效液相色谱仪,美国Waters公司,包括二元超高压梯度泵、真空脱气机、自动进样器、柱温箱、PDA检测器、Empower3色谱工作站;TB-215D型十万分之一天平,北京赛多利斯仪器系统有限公司;SG8200H型超声波清洗器,上海冠特超声仪器有限公司。
对照品绿原酸(批号110753-200413,质量分数96.60%)、黄芩苷(批号110715-201318,质量分数93.30%)、黄芩素(批号111595-200905,质量分数98.50%),购自中国食品药品检定研究院;对照品新绿原酸(批号15012903,质量分数99.78%)、隐绿原酸(批号15020203,质量分数99.72%)、异绿原酸A(批号14062009,质量分数99.70%)、异绿原酸B(批号15042210,质量分数99.04%)、异绿原酸C(批号14122807,质量分数99.04%),购自成都普瑞法科技有限公司;对照品汉黄芩苷(批号130603,质量分数≥98%)、汉黄芩素(批号130612,质量分数≥98%),购自四川省维克奇生物科技开发有限公司。
银黄制剂样品均为市售药品,银黄含化滴丸为贵州金宇药业有限公司产品(批号20151001、20140903),银黄含片分别为上海信宜天平药业有限公司委托上海福达制药有限公司生产(批号140616)、鲁南厚普制药有限公司产品(批号01315026),银黄胶囊分别为通化久铭药业有限公司产品(批号150321)、云南通大生物药业有限公司产品(批号150409),银黄颗粒分别为西安必康制药集团有限公司产品(批号150309)、陕西白鹿制药股份有限公司产品(批号150838)、四川升和药业股份有限公司产品(批号1502102),银黄片分别为通化金马药业集团股份有限公司产品(批号20140401)、广西鸿博药业有限公司产品(批号150301),产品共11个批次,依次标记为A~K,其中批次A(批号20151001)用于方法学研究。乙腈,色谱纯,德国Merck公司;甲醇,分析纯,国药集团化学试剂有限公司;磷酸,分析纯,重庆川东化工集团有限公司;水为娃哈哈饮用纯净水,批号20150719。
2 方法与结果 2.1 色谱条件色谱柱为Waters Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm),流动相为0.4%磷酸水溶液-乙腈,梯度洗脱:0~2.88 min,7%乙腈;2.88~3.71 min,7%~15%乙腈;3.71~6.95 min,15%~24%乙腈;6.95~11.78 min,24%~35%乙腈;11.78~16.65 min,35%~65%乙腈;16.65~20 min,65%~7%乙腈;体积流量0.4 mL/min;检测波长326 nm;柱温40 ℃;进样量1.0 μL。
2.2 供试品溶液的制备将市售银黄含化滴丸、银黄颗粒、银黄含片研细后精密称取0.2 g,银黄胶囊内容物混匀研细后精密称取0.2 g,银黄片去除包衣后研细后精密称取0.2 g,分别置100 mL量瓶中,加入80%甲醇90 mL,超声(功率260 W,频率50 kHz)提取40 min,放冷,用80%甲醇稀释至刻度,充分摇匀,进样前经0.22 μm微孔滤膜滤过。
2.3 对照品溶液的制备分别精密称取新绿原酸、绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素对照品适量,用80%甲醇定容至棕色量瓶中,配成质量浓度分别为39.912、137.172、42.680、37.886、20.996、47.539、524.346、88.200、75.254、14.504 mg/L的单一成分对照品储备液,置于4 ℃冰箱保存备用。精密量取上述各对照品储备液适量,用80%甲醇制得质量浓度分别为11.974、41.152、21.340、7.577、4.279、14.262、104.869、44.100、37.627、7.252 mg/L的混合对照品溶液。
2.4 阴性对照溶液的制备根据银黄制剂中银黄含化滴丸的处方比例及制备工艺,分别制备缺金银花提取物和缺黄芩提取物的阴性对照样品,按供试品溶液的制备方法制成阴性对照溶液。
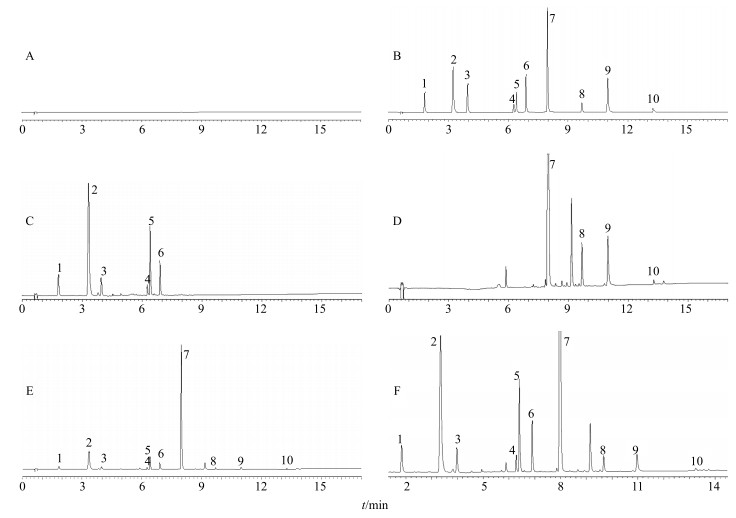
2.5 专属性考察分别精密吸取空白溶剂、混合对照品溶液、阴性对照溶液及供试品溶液1.0 μL,按“2.1”项下色谱条件进行分析,各组分与其相邻色谱峰的分离度均大于1.5,分离效果较好,空白无干扰,阴性对照在相应位置上未见色谱峰,该方法专属性良好,结果如图 1所示。
|
1-新绿原酸2-绿原酸3-隐绿原酸4-异绿原酸B 5-异绿原酸A 6-异绿原酸C 7-黄芩苷8-汉黄芩苷9-黄芩素10-汉黄芩素 1-neochlorogenic acid 2-chlorogenic acid 3-cryptochlorogenic acid 4-isochlorogenic acid B 5-isochlorogenic acid A 6-isochlorogenic acid C 7-bacicalin 8-wogonoside 9-baicalein 10-wogonin 图 1 空白(A)、混合对照品溶液(B)、缺黄芩阴性对照溶液(C)、缺金银花阴性对照溶液(D)、供试品溶液(E)的UPLC和供试品溶液局部放大图(F) Fig.1 UPLC of blank (A), standard solution (B), negative control solution without Scutellariae Radix (C) and without Lonicera Japonicae Flos (D), sample solution (E) and its partial enlarged detail (F) |
通过比较银黄制剂样品与对照品保留时间确定1~10号色谱峰分别为新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素。
2.6 线性关系考察分别精密量取上述10种单独对照品储备液,用80%甲醇依次逐级稀释成6个不同质量浓度梯度对照品溶液,按“2.1”项下色谱条件,进行测定,以对照品质量浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线并进行回归计算,得到10种对照品的标准曲线及回归方程(表 1)。
|
|
表 1 10种活性成分的回归方程、相关系数、线性范围 Table 1 Regression equation, correlation coefficient, and linear range of 10 active ingredients |
2.7 精密度试验
精密称取同一批(批号20151001)银黄含化滴丸样品,按“2.2”项下供试品溶液制备方法操作,按“2.1”项下色谱条件连续进样6次,计算峰面积的RSD值,结果新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素及汉黄芩素峰面积的RSD分别为1.18%、1.16%、1.07%、1.01%、0.62%、1.00%、0.59%、0.93%、1.18%、1.05%,表明仪器精密度良好。
2.8 重复性试验精密称取同一批银黄含化滴丸样品(批号20151001)0.2 g,按“2.2”项下方法,平行制备6份,进行分析,结果新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素及汉黄芩素平均质量分数为1.486、16.863、1.091、0.567、2.702、1.464、78.249、6.635、2.502、0.403 mg/g,RSD分别为0.88%、0.79%、1.07%、2.13%、1.36%、1.70%、0.52%、1.17%、0.33%、1.55%,表明该方法重复性良好。
2.9 稳定性试验取同一批银黄含化滴丸样品(批号20151001)溶液,分别于制备后第0、2、4、8、12、24 h进样,测定10种成分的峰面积并计算RSD,结果新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素及汉黄芩素峰面积RSD分别为1.69%、0.85%、0.71%、1.10%、0.22%、1.06%、0.42%、1.47%、0.49%、0.84%,表明供试品溶液在24 h内稳定。
2.10 回收率试验精密称取已测定的银黄含化滴丸样品(批号20151001)0.1 g,共取9份,将其分为高、中、低剂量3组,每组平行3份。分别精密加入新绿原酸0.059 mg/mL、绿原酸0.673 mg/mL、隐绿原酸0.045 mg/mL、异绿原酸B 0.023 mg/mL、异绿原酸A 0.108 mg/mL、异绿原酸C 0.059 mg/mL、黄芩苷1.484 mg/mL、汉黄芩苷0.270 mg/mL、黄芩素0.111 mg/mL及汉黄芩素0.024 mg/mL的对照品溶液2.0、2.5、3.0 mL,按“2.2”项下供试品溶液方法制备,按“2.1”项下色谱条件分析,分别计算回收率,结果新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素的平均回收率分别为98.38%、98.69%、98.86%、98.79%、99.18%、99.94%、99.50%、98.81%、98.05%、97.43%,RSD分别为0.90%、0.98%、1.30%、1.03%、0.85%、1.27%、1.31%、0.58%、0.55%、1.02%,结果表明,该方法具有较好的回收率。
2.11 样品定量测定分别精密称定10个不同厂家11批银黄制剂0.2 g,按“2.2”项下供试品溶液方法制备,按“2.1”项下色谱条件分析,根据新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素的标准曲线计算其质量分数,结果见表 2。
|
|
表 2 银黄制剂中10种成分的定量测定结果(n=3) Table 2 Determination of 10 components in Yinhuang preparations (n=3) |
3 讨论
本实验采用光电二极管阵列检测器,在190~400 nm波长范围内对10种目标组分的对照品溶液进行紫外全波长扫描,结果显示绿原酸等有机酸类成分均在326 nm处有最大吸收峰,黄芩苷和黄芩素在278 nm处有最大吸收峰,汉黄芩苷和汉黄芩素在275 nm处有最大吸收峰。银黄制剂中黄芩苷量明显高于其他组分,为提高该方法的灵敏度,本实验最终选取绿原酸等有机酸类最大吸收波长326 nm作为检测波长,汉黄芩苷、黄芩素和汉黄芩素量虽相对较低,但在该波长条件下,各成分的检测灵敏度均良好,分离度均大于1.5,符合定量测定相关要求。
目前,《中国药典》2015年版一部[6]收载的银黄制剂包括银黄口服液、银黄颗粒和银黄片,在质量控制方面也仅是以绿原酸和黄芩苷作为定量测定指标,并且采用的是不同前处理条件和检测色谱条件。本实验采用UPLC法对样品中多组分进行同时检测,在16 min内完成10种成分的检测,与《中国药典》2015年版方法和现有文献报道的HPLC测定银黄制剂多组分的方法相比[18-19, 21],不仅提高了检测效率、节约了分析成本,也减少了溶剂的使用量,更有利于环保,该方法的建立为将来银黄制剂质量标准提升提供数据参考。
从表 2测定结果可以看出,不同生产企业之间的相同剂型在绿原酸和黄芩苷量上均有较大差异,而其他组分量亦有较大差别,说明不同生产企业的原料来源、产品性状及工艺上多有差异,致使市场上银黄制剂产品质量不均一,而不同剂型的银黄制剂在给药剂量上也存在差异,更有待于在药动学和药效学方面对其质量进行考察。现行的质量控制标准难以客观反映该类中药制剂的整体质量水平,有必要对银黄制剂中多种有机酸和黄酮类成分进行测定,同时应规范该类制剂中主要成分量的上限和下限,在保证临床疗效的同时,也应关注其临床用药安全性[22-24]。
| [1] | 赵刚, 杜玮, 魏玉辉, 等. 银黄制剂的HPLC-ELSD指纹图谱研究[J]. 中草药, 2009, 40(7):1053–1056. |
| [2] | 刘文翔.二维液相色谱-质谱联用技术在复方银黄制剂成分研究中的应用[D].西安:陕西师范大学, 2011. |
| [3] | 林永强, 徐丽华, 王淑华, 等. 一测多评法同步测定银黄片中6种咖啡酰奎宁酸[J]. 中草药, 2012, 43(4):706–710. |
| [4] | 刘文翔. 二维液相色谱分离中药复方银黄口服液中的有效成分[J]. 河南化工, 2010, 27(24):41–43. |
| [5] | 彭芸, 戴德雄, 朱莹. 银黄滴丸、银黄颗粒和银黄胶囊体外溶出度比较研究[J]. 中草药, 2012, 43(6):1122–1124. |
| [6] | 中国药典[S].一部. 2015. |
| [7] | 王勖. 中药金银花药用成分及药理作用分析[J]. 亚太传统医药, 2015, 11(18):30–31. |
| [8] | 周细根, 梁生林, 胡存华, 等. 金银花乙醇提取液对急性炎症的抑制作用[J]. 实用临床医学, 2012, 13(2):12–13. |
| [9] | 杨斌, 丘岳, 王柳萍, 等. 广西山银花绿原酸体外抗炎作用及分子机制研究[J]. 中国药理学通报, 2009, 25(4):542–544. |
| [10] | 付璟, 石继和. 黄芩素体外抑菌与体内抗炎作用研究[J]. 中国药房, 2014, 25(23):2136–2138. |
| [11] | 王雅芳, 李婷, 唐正海, 等. 中药黄芩的化学成分及药理研究进展[J]. 中华中医药学刊, 2015, 31(1):206–211. |
| [12] | 于蓓蓓, 吕凌, 于宗渊, 等. 基于抑菌药效的黄芩提取物精制工艺优选[J]. 中草药, 2014, 45(3):362–366. |
| [13] | Hao H, Aixia Y, Lei F, et al. Effects of baicalin on Chlamydia trachomatis infection in vitro[J]. Planta Med, 2010, 76(1): 76–78. DOI:10.1055/s-0029-1185943 |
| [14] | 任晓东, 符伟, 张晓芸, 等. 天然产物汉黄芩素的研究进展[J]. 中国新药杂志, 2011, 20(9):777–784. |
| [15] | 朱广伟, 张贵君, 孙奕, 等. 黄芩的三种不同炮制品对感染甲型H1N1流感病毒小鼠肺指数及病毒载量的影响[J]. 中医杂志, 2016, 57(9):779–782. |
| [16] | 史国生, 林永强, 徐丽华, 等. HPLC法同时测定银黄颗粒中6个咖啡酰奎宁酸[J]. 中成药, 2015, 37(2):311–315. |
| [17] | 韩强, 陈辉, 李银洁, 等. HPLC法同时测定银黄制剂中9个成分的含量[J]. 药物分析杂志, 2013, 33(10):1686–1692. |
| [18] | 何兵, 杨世艳, 张燕. HPLC同时测定银黄含片中10个活性成分的含量[J]. 药物分析杂志, 2012, 32(10):1853–1857. |
| [19] | 杨世艳, 何兵, 张燕. HPLC同时测定银黄颗粒中7种有机酸及4种黄酮类成分[J]. 中草药, 2013, 44(3):301–304. |
| [20] | 周新, 陈会明, 白桦, 等. HPLC与UPLC色谱条件转换方法研究[J]. 分析试验室, 2008, 27(4):56–58. |
| [21] | 王荣梅, 徐丽华, 林永强. HPLC法同时测定银黄含片中6个咖啡酰奎宁酸类成分的含量[J]. 药物分析杂志, 2012, 32(1):57–60. |
| [22] | 张利平, 王平, 高燕, 等. 8批银黄颗粒及其含药血清的体外抑菌作用[J]. 中国药房, 2015, 26(7):894–897. |
| [23] | 马力.银黄颗粒成药性评价及对鸡毒支原体病治疗的初步应用[D].长春:吉林大学, 2014. |
| [24] | 冯萍, 勾忠平, 邹林玲, 等. 注射用银黄Ⅰ期临床耐受性试验[J]. 中国循证医学杂志, 2012, 12(3):278–282. |
 2017, Vol. 48
2017, Vol. 48


