2. 华润三九医药股份有限公司, 广东 深圳 518110
2. China Resources Sanjiu Medical & Pharmaceutical Co., Ltd., Shenzhen 518110, China
川芎Chuanxiong Rhizoma为伞形科(Umbelliferae)植物川芎Ligusticum chuanxiong Hort.的干燥根茎。《中国药典》2010年版记载川芎有活血行气、祛风止痛的功能,用于胸痹心痛、胸胁刺痛、跌扑肿痛、月经不调、经闭痛经、头痛、风湿痹痛等症状[1]。川芎中含有挥发油、内酯、生物碱、酚酸等多种成分[2],其中阿魏酸为川芎药材主要活性成分。研究表明,阿魏酸在抗肿瘤、抗血小板凝集和抗血栓等方面均有明显作用[3, 4, 5],吴艳华等[6]还证实了阿魏酸能够抑制人表皮黑素细胞增殖及黑素合成。
由于产地、采收季节、气候、炮制方法等各因素影响,川芎药材多种成分的量差异较大。《中国药典》2010年版对川芎药材中阿魏酸、水分和浸出物的量设定相关质量要求,其中阿魏酸、水分和浸出物的测定分别采用HPLC法、甲苯法和热浸法等传统测定方法,这些方法虽能准确测定,但一般分析周期较长,不利于满足大批量药材快速分析的需求。
近红外光谱(near infrared spectroscopy,NIRS)技术是目前发展最快和最具有应用前景的过程分析技术之一,具有样品处理简单、无损耗、分析快速、无需试剂消耗等特点,已经陆续在中药有效成分的测定[7, 8, 9]、产地鉴别[10, 11]及中药制剂生产过程的监控[12, 13, 14, 15, 16]等方面有较广泛的应用。随着NIRS技术的深入研究及化学计量学的发展,该技术将会在中药及其制剂的质量控制中发挥越来越重要的作用。本研究将NIRS技术应用于川芎药材质量的快速分析,利用偏最小二乘(PLS)法建立川芎药材中阿魏酸、水分及浸出物的定量校正模型,实现川芎药材的快速检测,以提高川芎药材的质量控制水平。
1 仪器与材料Bruker Matrix Duplex近红外光谱仪(Bruker Optic Co.,Germany),配有外置Q412A漫反射探头、光纤及OPUS数据处理软件;DFY-200摇摆式高速万能中药粉碎机(温岭市林大机械有限公司);精宏DZF-6021真空干燥箱(上海精宏实验设备有限公司);减压干燥器;FA2004电子天平(上海越平科学仪器有限公司);Agilent 1200高效液相色谱仪(Agilent,美国),含UV检测器、自动进样器、在线脱气、四元泵和Chemstation色谱管理软件;GraceSmart RP C18分析柱(250 mm×4.6 mm,5 μm);H1650-W高速离心机(长沙湘仪离心机仪器有限公司)。
样品由华润三九医药股份有限公司提供(产地主要为四川),由浙江大学药学院徐娟华副教授鉴定为川芎Ligusticum chuanxiong Hort. 的干燥根茎;甲醇为分析纯(南京化学试剂有限公司);磷酸为色谱纯(阿拉丁);超纯水(Millipore);阿魏酸对照品由成都曼思特生物科技有限公司提供(采用高效液相色谱法分析,采用峰面积归一化计算,质量分数大于98.0%)。
2 方法与结果 2.1 近红外光谱采集川芎药材经粉碎机粉碎后,过80目筛,得到粒度均匀的川芎药材粉末。在室温条件下,以空气为背景,使用Bruker Matrix Duplex近红外光谱仪采集川芎粉末样品的NIRS光谱,光谱采集条件:扫描范围为4 000~12 000 cm-1,扫描次数为32次,分辨率为8 cm-1。所得川芎药材粉末原始光谱见图 1。
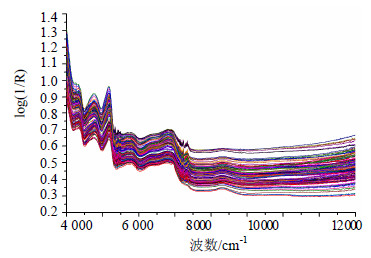 | 图 1 川芎粉末原始NIRS图Fig.1 Raw NIRS spectra of Chuanxiong Rhizoma powder |
采用减压干燥法测定川芎药材的水分量。取川芎药材1 g,置于干燥至恒定质量(连续2次质量差异小于5 mg)的扁形瓶(X0)中,精密称定药材质量(X1),打开瓶盖置于减压干燥器中(底层铺有约2 cm厚的五氧化二磷),减压至2.67 kPa(20 mmHg)以下持续干燥30 min,室温放置24 h后精密称定质量(X2)。根据减失的质量,按公式计算川芎药材中的水分量
水分=(X1+X0-X2)/X1
2.3 浸出物测定川芎药材的浸出物测定方法参照《中国药典》2010年版的热浸法,精密称定样品1 g(X1),精密加95%乙醇25 mL,密塞,称定质量,静置1 h后85 ℃回流提取1 h。放冷后用乙醇补足减失质量,摇匀,在3 800 r/min条件下离心30 min,精密量取上清液10 mL,置已干燥至恒定质量的扁形瓶(X0)中,在水浴锅上挥干溶剂后,于105 ℃干燥3 h,精密称定质量(X2)。以干燥品计算川芎药材中浸出物的量。
浸出物=(X2-X0)×2.5/X1
2.4 阿魏酸的测定 2.4.1 HPLC色谱条件色谱柱为GraceSmart RP C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-0.1%磷酸水溶液(25∶75);检测波长321 nm,体积流量为1 mL/min,进样量为10 μL。理论塔板数应不低于4 000。
2.4.2 标准曲线绘制精密称取阿魏酸对照品10.37 mg,甲醇定容至10 mL,作为储备液。精密吸取储备液1 mL,用甲醇定容至100 mL,作为对照品溶液,避光保存。取阿魏酸对照品,按“2.4.1”项色谱条件分别进样5、10、15、20、25、30 μL,以阿魏酸的质量为横坐标,峰面积为纵坐标绘制标准曲线。回归方程为Y=5 110.01 X-17.34,r为0.999 5,结果表明阿魏酸在0.051 9~0.311 1 μg线性关系良好。
2.4.3 供试品溶液的制备精密称取川芎药材粉末(过80目筛)0.5 g,精密加入70%甲醇50 mL,精密称定,90 ℃回流提取0.5 h,放冷,精密称定,70%甲醇补足减失质量,样品溶液于13 000 r/min离心10 min,取上清液,即得。
2.4.4 方法学考察(1)精密度试验:取一批样品溶液,在上述色谱条件下连续进样6次,比较阿魏酸峰面积,计算其RSD为1.71%。显示该方法精密度良好,符合定量要求。
(2)重复性试验:平行制备6份供试品溶液(2013090102),在上述色谱条件下分析,比较阿魏酸峰面积,计算其质量分数的RSD为0.96。表明该方法的重复性符合要求。
(3)稳定性试验:取同一样品溶液在室温下放置0、4、8、12、24、36 h后分别进样分析,考察方法稳定性,得阿魏酸峰面积的RSD为1.71%,表明供试品溶液在36 h内基本稳定。
(4)加样回收率试验:取已测定的川芎药材(1.481 7 mg/g)6份,每份0.25 g,分别精密加入阿魏酸对照品溶液(0.355 mg/mL),按上述色谱条件下分别进样测定,加样回收率为102.18%,RSD为1.66%,说明该方法准确可靠。
2.4.5 近红外方法学考察精密称定1 g川芎粉末,在相同光谱采集条件下重复采集同一样品光谱9次,计算光谱RSD值作为精密度评价指标;精密称定同一批次的川芎粉末9份(每份1 g),在相同光谱采集条件下分别采集得到9张光谱,计算其RSD平均值作为重复性的评价指标,光谱RSD值计算见公式,结果表明RSD平均值分别为1.42%,0.33%,说明光谱采集数据准确可靠。
| $rs{{d}_{j}}=\frac{SD}{{\bar{X}}}=\frac{\sqrt{{\sum\limits_{i=1}^{n}{{{\left( {{x}_{i,j}}\text{-}{{{\bar{x}}}_{j}} \right)}^{2}}}}/{n-1}\;}}{{{{\bar{x}}}_{i}}}$ |
| $RSD = \sum\limits_j^m {rs{d_j}} $ |
运用Bruker公司OPUS软件的PLS法建立川芎药材中阿魏酸、水分和浸出物的量3个关键质控指标的NIRS定量分析模型,随机选取样本量的1/4为验证集,以交互验证误差均方根(RMSECV)和相关系数(r)值为模型评价指标。以校正集预测误差均方根(RMSEC)和验证集预测误差均方根(RMSEP)考察模型对校正集样本和验证集样本的预测误差。当RMSEC和RMSEP较小且越接近时,表明模型具有较高的预测能力。同时以相对预测偏差(RSEP)来考察模型的预测能力,RSEP越小表明模型预测效果越好。
2.6 质控指标测定结果测定138批川芎药材中的阿魏酸、水分和浸出物的量。结果表明,药材中阿魏酸、水分和浸出物的最大量分别为0.23%、13.43%、30.24%;最小量分别为0.07%、6.02%、20.12%;均值分别为0.17%、9.66%、27.16%。药材中3个指标的量差距较大,RSD值均超过15%,其有效成分阿魏酸量的RSD值为30.58%,说明不同批次川芎药材的质量波动较大。故在投入中药制剂生产前有必要对川芎药材的关键质量指标进行控制,从而保证产品质量的均一和稳定。
2.7 NIRS模型的建立 2.7.1 异常光谱剔除测量环境的改变、仪器和性能参数的变化或者样品物理、机械的变化等许多不确定性因素均会导致异常光谱的产生。所以在建模之前,必须先排除异常光谱,以保证模型的准确性和适用性。本实验采用样品的马氏距离来判断异常光谱,马氏距离计算[14]见下列公式方法。
| ${D_m}\left( {{x_i},{x_j}} \right) = {\left[ {{{\left( {{x_i} - {x_j}} \right)}^{\,T}}X{{\left( m \right)}^ + }\left( {{x_i} - {x_j}} \right)} \right]^{1/2}}$ |
以138批光谱的平均光谱为参照光谱,在95%置信限下计算样本的马氏距离,结果见图 2。可知51号样品马氏距离超过置信限。因此在建立定量模型之前把51号剔除,模型性能相应提高。
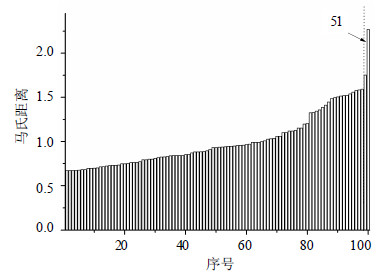 | 图 2 马氏距离异常光谱判别Fig.2 Discrimination of spectral outlier by Mahalanobis distance |
在采集光谱的过程中由于外界环境的改变(如温度、湿度)、粉末表面不平整或者颗粒不均匀等因素均会对光谱产生一定影响,导致基线漂移、信噪比降低等问题。因此在建立定量模型之前,有必要对光谱进行预处理以提高信噪比和模型的预测精度。常用的光谱预处理有导数处理、消除常数偏移量、多元散射校正(MSC)、标准正交变换(SNV)等,多种预处理方法联用可得到较好的预处理结果。
本研究选取104批校正集样本的全波长为研究对象,比较了不同预处理方法对模型性能影响,包括消除常数偏移量、一阶导数(1stD)、一阶导数+减去一条直线,一阶导数+标准正交变换(1stD+SNV)和一阶导数+多元散射校正(1stD+MSC),结果见表 1。通过比较不同的预处理方法对建模参数的影响,结果表明水分量模型选用消除常数偏移量的预处理方法,浸出物和阿魏酸模型选用1stD+标准正交变换的光谱预处理方法,所得到的模型RMSECV值最小且r相对较高,模型效果最好。2种预处理方法所得的光谱图见图 3。
| 表 1 不同光谱预处理方法对模型性能影响 Table 1 Influence of different pretreatment methods on performance of calibration models |
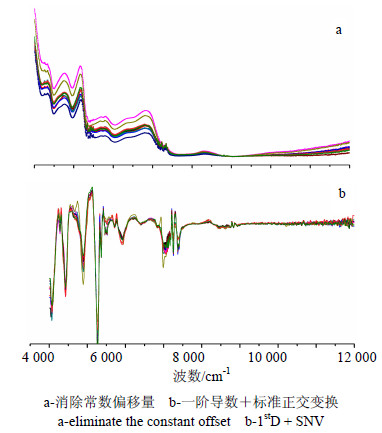 | 图 3 光谱预处理后结果图Fig.3 Results of spectral pretreatment |
NIRS全光谱除了包含有效信息外还包含噪音等冗余信息,既增加了建模的工作量,使模型复杂化,而且也会在一定程度上影响模型的精度。不同的质量指标在近红外光谱中对应的有效波段也不同,通过近红外光谱(图 1)可见,在8 500~12 000 cm-1波段吸收较少,没有特征吸收峰;在4 000~4 200 cm-1波段内,由于光纤吸收含有较多噪音,不适用于建模。参考2种光谱预处理后的光谱图可以发现,在4 500~8 500 cm-1内有明显的特征吸收峰,因此选择在4 500~8 500 cm-1波段内有选择性地建模。通过比较不同建模波段对模型性能的影响,结果见表 2,可发现水分模型在4 500~6 500 cm-1波段建模RMSECV更小,r值更大,而浸出物和阿魏酸模型的建模波段在4 500~7 500 cm-1波段建模模型效果较好。
| 表 2 光谱波段选择对阿魏酸、水分及浸出物校正模型性能的影响 Table 2 Influence of spectral band selection for PLS models performance ferulic acid, moisture, and extractum |
运用OPUS软件,剔除光谱异常点后,选择相应的光谱预处理方法和建模波段,随机选择104批为校正集。运用PLS法建立NIRS定量校正模型,校正集样品的NIRS实测值和预测值的相关性图见图 4,从图 4中可以看出,3个质控指标的r均在0.9以上,所得阿魏酸、水分和浸出物模型的r值分别为0.913 0、0.905 9和0.954 4,RMSEC分别为0.000 5、0.669和1.592,表明模型相关性较好。
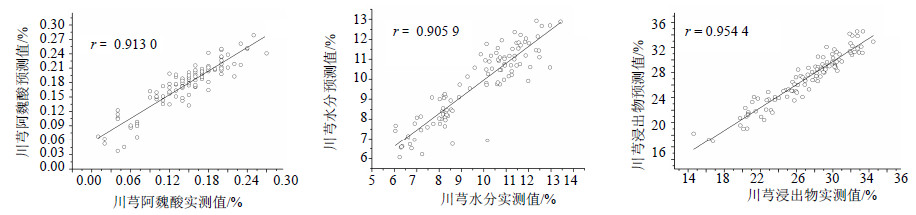 | 图 4 校正集样本NIRS预测值和实测值线性相关性Fig.4 Correlation of NIRS predicted value and measured value in calibration set |
为了进一步确定模型的预测能力,利用建立好的NIRS模型对33批验证集川芎样本中的3个指标进行外部验证,预测效果采用RSEP值评价,其计算方法见下列公式。
| $RSEP = \sqrt {\frac{{\sum\limits_{i = 1}^n {{{({X_i} - Y{}_i)}^2}} }}{{\sum\limits_{i = 1}^n {{X_i}^2} }}} $ |
33批验证集样本的NIRS预测值与参比方法实际测得值的相对趋势对比见图 5,结果表明3个指标的NIRS预测值与实际测得值都十分接近,RMSEP分别为0.000 3、0.305 6和2.209 0,RSEP分别为9.87%、5.30%、和5.69%,均控制在10%以内,基本满足中药实际生产过程中分析精度要求。
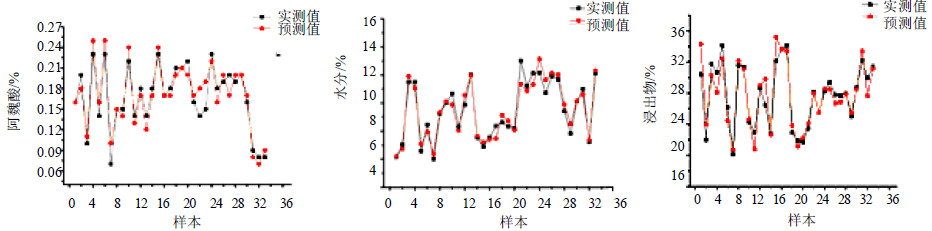 | 图 5 验证集中3个指标NIRS预测值与实测值的相对趋势Fig.5 Relative trend of NIRS predicted value and measured value of three indicators |
本研究建立了川芎药材中阿魏酸、水分和浸出物3个关键指标的NIRS快速检测方法,所建立的NIRS模型的r在0.9以上,RMSEC和RMSEP较为接近,RESP在10%以内,模型性能良好,为川芎药材的质量控制提供新方法,同时可以实现生产过程在线检测川芎药材中阿魏酸、水分及浸出物量,为中药制剂生产前原药材投料过程提供质量评价参数,从而实现中药生产过程质量在线检测。同时为NIRS技术在中药质量控制和在线检测提供新的技术支持。
| [1] | 中国药典[S]. 一部. 2010. |
| [2] | 赵文萃, 康雪莱. 川芎的有效成分鉴别与含量标准研究[J]. 中国医药指南, 2011, 33(9):288-289. |
| [3] | 洪倩. 阿魏酸抗辐射活性及其作用机制研究[D]. 北京:中国人民解放军军事医学科学院, 2012. |
| [4] | 赵润英, 郝伟, 孟祥军, 等. 阿魏酸川芎嗪抗血栓形成作用及其对血小板中性粒细胞黏附的影响[J]. 中国医科大学学报, 2012, 41(10):900-903. |
| [5] | Zhao J, Suyama A, Tanaka M, et al. Ferulic acid enhances the vasorelaxant effect of epigallocatechin gallate in tumor necrosis factor-alpha-induced inflammatory rat aorta[J]. J Nutr Biochem, 2014, 25:807-814. |
| [6] | 吴艳华, 汤楠, 蔡兰花, 等. 阿魏酸对黑素细胞增殖、黑素合成、酪氨酸酶活性及c-kit、ERK蛋白表达的影响[J]. 中华皮肤科杂志, 2014, 47(10):728-731. |
| [7] | Kim Y J, Lee H J, Shin H S, et al. Near-infrared feflectance spectroscopy as a rapid and non-destructive analysis tool for curcuminoids in turmeric[J]. Phytochem Anal, 2014, 25:445-452. |
| [8] | 张金巍, 张延莹, 刘岩, 等. 近红外光谱法在线质量监控白芍工业化提取[J]. 中草药, 2011, 42(12):2459-2461. |
| [9] | 赵艳丽, 张霁, 袁天军, 等. 近红外光谱快速鉴别不同产地药用植物重楼的方法研究[J]. 光谱学与光谱分析, 2014, 34(7):1831-1835. |
| [10] | 曲佳, 王秋珍, 王杰. 近红外光谱法快速鉴别不同厂家的天王补心丸(小蜜丸)[J]. 药物评价研究, 2014, 37(4):346-348. |
| [11] | 闫珂巍, 王福, 梅国荣, 等. 基于近红外光谱技术快速定性鉴别广陈皮模型的建立[J]. 中草药, 2015, 46(20):3096-3099. |
| [12] | 白新涛, 霍宝军, 张博, 等. 近红外光谱法快速检测黄芪注射液中黄芪甲苷和总固体量[J]. 中草药, 2012, 43(11):2189-2193. |
| [13] | Wu Y J, Jin Y, Li Y R, et al. NIRS spectroscopy as a process analytical technology (PAT) tool for on-line and real-time monitoring of an extraction process[J]. Vib Spectrosc, 2012, 58:109-118. |
| [14] | 吴莎, 刘启安, 李云, 等. 最小二乘支持向量机和偏最小二乘法在栀子中间体纯化工艺近红外定量分析中的应用[J]. 中草药, 2015, 46(7):990-997. |
| [15] | 陈乐, 张华峰, 郝淼, 等. 淫羊藿水分和灰分的近红外快速检测[J]. 中草药, 2015, 46(9):1368-1373. |
| [16] | 石雪, 蔡广生, 邵学广. 局部建模方法用于烟草样品的近红外光谱定量分析[J]. 光谱学与光谱分析, 2008, 82(11):2561-2564. |
 2016, Vol. 47
2016, Vol. 47


