2. 义乌市中心医院, 浙江 义乌 322000
2. The Central Hospital of Yiwu City, Yiwu 322000, China
芦荟Aloe是百合科多年生常绿、多肉质草本植物,其中具有重要药用价值的有库拉索芦荟Aloe vera L.、木立芦荟Aloe arborescens Mill.和中华芦荟Aloe veraL. var.chinensis Haw.[1]。芦荟多糖是芦荟凝胶的主要生物活性成分,具有杀菌、消炎、抗辐射、抗肿瘤、抗衰老、抗内毒素、免疫调节等多种药理作用,已广泛用于药品、食品、化妆品等行业[2-9]。《植物实名图考》记载芦荟“治烫火灼伤”。民间使用库拉索芦荟治疗烧烫伤时,常将成熟期库拉索芦荟去皮取叶肉直接涂烧烫伤患处。该法不符合现代药物治疗原则,更难于临床推广[10]。
为解决烧烫伤患者给药频繁,换药痛苦的问题,本实验将库拉索芦荟多糖(Aloe vera polysac-charide,AVP)制成凝胶剂,即复方AVP凝胶剂(compound AVP gel,CAVPG),考察不同基质对纳米银[11-12]、纳米锌、AVP释放度的影响,为后续AVP的开发利用奠定基础。
1 仪器与材料XS105DualRange型分析天平,梅特勒-托利多仪器(上海)有限公司;JA2003N型电子天平,上海精密科学仪器科技有限公司;NDJ-5S型数字式黏度计,上海菁海仪器有限公司;Avanti J-26XP型高效离心机,贝克曼库尔特商贸(中国)有限公司;DZF6050型真空干燥箱,上海精宏实验设备有限公司;DGG-9053A型电热恒温鼓风干燥箱,上海森信实验仪器有限公司;KH-250DB型数控超声波清洗器,昆山禾创市超声仪器有限公司;WH-861型震荡仪,淄博中惠仪器有限公司;DF-101S型集热式恒温加热磁力搅拌器,巩义市英峪于华仪器厂。
AVP,实验室自制,质量分数35.37%(以D-甘露糖计),批号20131203、20131207、20131208;纳米银(批号20130918001,粒径20 nm)、纳米锌(批号20130723003,粒径80 nm),上海超威纳米科技有限公司;硝酸(批号20130802,优级纯)、三乙醇胺(批号20120520,分析纯),广东省化学试剂工程技术研究开发中心;丙三醇(批号20110401,分析纯),浙江杭州双林化工试剂厂;卡波姆(Carbomer)-940(批号1208,47.6 Pa·s)、卡波姆-934(批号11163,38.0 Pa·s)、卡波姆-980(批号11125,7.0 Pa·s),廊坊聚通化工有限公司;羟丙基甲基纤维素(HPMC,批号27624 K4M)、羟丙基甲基纤维素(批号27668 K15M)、羟丙基甲基纤维素(批号27688 K100M)、甲基纤维素(MC,批号31537),阿拉丁试剂(上海)有限公司;羧甲基纤维素钠(CMC-Na,批号110723)、聚乙二醇(PEG)4000(批号090226),国药集团化学试剂有限公司;磷酸二氢钾(批号20130413,分析纯),成都市科龙化工试剂厂;水为去离子水。
2 方法与结果 2.1 基质筛选 2.1.1 评分标准以外观、涂展性[13]、黏度、高温稳定性[14]和低温稳定性[15]的综合评分作为考察指标,综合评分(50分)=外观评分(10分)+涂展性评分(10分)+黏度评分(10分)+高温稳定性评分(10分)+低温稳定性评分(10分),具体评分标准见表 1。
|
|
表 1 CAVPG基质筛选的评分标准 Table 1 Scoring criteria of CAVPG screening matrix |
2.1.2 磷酸盐缓冲液(PBS,pH 6.86)的配制
取0.2 mol/L磷酸二氢钾溶液250 mL,加0.2 mol/L氢氧化钠溶液118 mL,用水稀释至1 000 mL,摇匀,即得[15]。
2.1.3 不同种类凝胶基质的制备(1)Carbomer、CMC-Na和PEG 4000基质的溶胀:称取基质适量,缓慢加入PBS中,使其均匀散布于PBS表面,35 ℃搅拌15 min至基质均匀分散于水中,室温下静置12 h,即可充分溶胀,最终制备的凝胶剂中Carbomer的质量分数为0.5%、CMC-Na的质量分数为5.0%、PEG 4000的质量分数为10.0%。
(2)HPMC的溶胀:称取HPMC适量,85 ℃下缓慢加入PBS中,使其均匀散布于PBS表面,搅拌15 min,至HPMC均匀分散于水中,加入适量的PBS,使HPMC凝胶液温度降低,35 ℃搅拌15 min,室温下静置12 h,即可充分溶胀,最终制备的凝胶剂中HPMC的质量分数为2.0%。
(3)MC的溶胀:称取MC适量,70 ℃下缓慢加入PBS中,使其均匀散布于PBS表面,搅拌15 min,至MC均匀分散于水中,加入适量的PBS,使MC凝胶液温度降低,35 ℃搅拌15 min,室温下静置12 h,即可充分溶胀,最终制备的凝胶剂中MC的质量分数为5.0%。
2.1.4 基质初筛以基质的外观、涂展性、黏度为考察指标,通过高温实验(55 ℃水浴放置5 h)、低温实验(−20 ℃放置24 h)考察基质的稳定性。取“2.1.3”项所制备的凝胶基质,加入甘油约5.0 g,PBS补足至100 g,35 ℃,搅拌2 h,三乙醇胺调节pH值至7.0左右,搅拌均匀后观察凝胶基质外观,考察其涂展性、黏度、高温稳定性和低温稳定性,结果见表 2。
|
|
表 2 凝胶基质初筛(x±s, n=3) Table 2 Character results of gel screening matrix (x±s, n=3) |
根据表 2中结果,Carbomer-980为0.5%、HPMC K15M为2.0%时,其外观、涂展性、黏度、稳定性都符合凝胶剂的质量要求。因此,对Carbomer-980和HPMC K15M这2种凝胶基质做进一步的筛选。
2.1.5 基质确定(1)空白凝胶剂制备:称取凝胶基质适量,充分溶胀,加入甘油约5.0 g,PBS溶液补足至100 g,35 ℃,搅拌2 h,三乙醇胺调节pH值至7.0左右,搅拌均匀,即得。
(2)CAVPG制备:称取AVP 2 g,溶解于适量PBS中;称取凝胶基质0.5 g,充分溶胀;称取纳米银、纳米锌各1 g,与5 g甘油一起润研均匀;将三者混合,以PBS补足至100 g,一定温度下搅拌2 h,三乙醇胺调节pH至7.0左右,即得。
(3)CAVPG中纳米银、纳米锌释放度的测定:采用改良后的转篮法对药物释放度进行测定。称取CAVPG约2 g,精密称定,每个处方平行3份,置于转篮中,将转篮依次放入6个溶出杯中,以脱气去离子水250 mL作为释药介质,调节温度为(37.0±0.5)℃,转速为10 r/min,分别于2、4、6、8、10、12 h分别取样品5 mL,置于10 mL离心管中,同时补充等温、等体积的脱气释药介质。
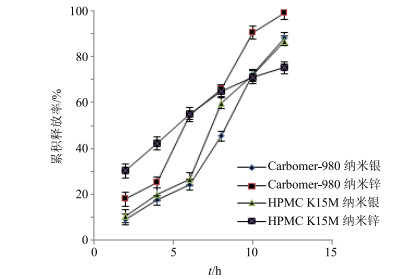
将5 mL释药介质转移到消解管中,加入5 mL硝酸,置于消解仪内,1 600 W升温5 min,于120 ℃保持2 min,1 600 W升温8 min,于185 ℃保持5 min。消解液转移至50 mL量瓶中,加去离子水稀释至刻度。使用电感耦合等离子体原子发射光谱(ICP-AES)法测定溶出液中Ag+、Zn2+的量[16-18],计算纳米银、纳米锌在各时间点的累积释放率,释放曲线见图 1。由图 1可以看出,Carbomer-980、HPMC K15M均能够起到缓释作用,Zn2+的释放速率显著高于Ag+。其中以HPMC K15M制备的CAVPG在12 h后纳米银、纳米锌的累积释放率分别为60.39%、75.31%,释放不完全;而以Carbomer-980为基质制备的CAVPG在12 h后纳米银、纳米锌的累积释放率分别为88.09%、99.01%,释放较为完全。
|
图 1 基质对CAVPG中纳米银、纳米锌累积释放率的影响(n=3) Fig.1 Cumulative release profile of diffirent screening of nano-silver and nano-zinc in CAVPG (n=3) |
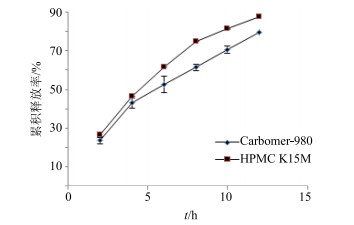
(4)CAVPG中AVP释放度的测定:参照“2.1.5(2)”项下的转篮法,称取CAVPG约2 g,精密称定,平行3份,置于转篮中,称取空白凝胶剂约2 g,精密称定,置于转篮中,将其依次放入溶出杯中,分别于2、4、6、8、10、12、24 h取样2 mL,置于25 mL试管中,立即补充同体积同温度的脱气释药介质。以空白凝胶溶出液作为空白对照,用紫外-可见分光光度法测定溶出液中AVP的量[19],计算AVP在各时间点的累积释放率,结果见图 2。由实验结果可知,Carbomer-980、HPMC K15M均能够起到缓释作用,以HPMC K15M为基质制备的CAVPG在12 h后AVP的累积释放率达到87.94%,以Carbomer-980为基质制备的CAVPG在12 h后AVP的累积释放率达到79.61%,但释放速度Carbomer-980<HPMC K15M。
|
图 2 基质对CAVPG中AVP累积释放率的影响(n=3) Fig.2 Cumulative release profile of different screening of AVP in CAVPG (n=3) |
由此可见,以Carbomer-980为基质制备的CAVPG中纳米银、纳米锌的释放更完全,AVP也能释放较完全且缓慢,因此采用Carbomer-980为基质。拟定处方为AVP 2%,纳米银1%,纳米锌1%,Carbomer-980 0.5%,甘油5%,三乙醇胺适量,PBS补足至100 g。
2.2 处方工艺优化 2.2.1 正交试验设计由预试验可知,基质用量、甘油用量、搅拌温度对CAVPG的外观、黏度、涂展性等有较大的影响,因此,以Carbomer-980用量(A)、甘油用量(B)、搅拌温度(C)为考察指标。取AVP 2 g,纳米银1 g,纳米锌1 g,三乙醇胺适量,依照表 3中各处方中基质成分的量,制成CAVPG,以外观、涂展性、黏度、高温稳定性和低温稳定性的综合评分作为指标进行L9(34)正交试验[20],因素水平及正交试验结果见表 3,方差分析结果见表 4。
|
|
表 3 正交试验设计与结果 Table 3 Design and results of orthogonal test |
|
|
表 4 方差分析(综合评分) Table 4 Analysis of variance (composite score) |
2.2.2 处方工艺优化结果
根据方差分析结果可知,3个因素对CAVPG综合评分的影响大小依次为Carbomer-980用量>搅拌温度>甘油用量,Carbomer-980的用量对结果有显著影响(P<0.05)。其中A3>A2>A1,B1>B3>B2,C1>C2>C3,最终优化后的处方工艺为A3B1C1,即Carbomer-980用量0.5%,甘油用量5.0%,搅拌温度25 ℃。
2.2.3 最佳处方工艺确定根据处方工艺优化结果,确定最佳CAVPG处方工艺为AVP 2%,纳米银1%,纳米锌1%,Carbomer-980 0.5%,甘油5.0%,三乙醇胺适量,PBS补足至100 g,搅拌温度25 ℃。
2.2.4 验证试验按照优选的最佳处方工艺制备3批CAVPG,按“2.1.1”项下方法对所制备的CAVPG进行评分,结果见表 5。3批CAVPG的综合得分分别为48.54、47.9、48.08,表明优选的处方工艺稳定可行。
|
|
表 5 验证试验 Table 5 Validation test |
2.3 CAVPG的释药特征评价[21]
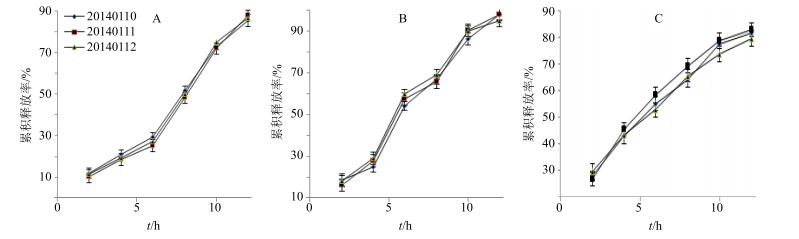
分别称取3批CAVPG约2 g,精密称定,均平行3份,参照《中国药典》2015年版“凝胶剂中药物释放度的测定”[15]项下的方法对CAVPG中纳米银、纳米锌、AVP的释放度进行测定,释药数据经零级方程、一级方程、Higuchi方程和Peppas方程4种数学模型拟合,释放曲线见图 3,数学模型拟合结果见表 6。由相关系数r2可知,其中纳米银体外释放模型拟合接近程度依次为零级方程>Peppas方程>Higuchi方程>一级方程;纳米锌体外释放模型拟合接近程度依次为零级方程>Higuchi方程>Peppas方程>一级方程;AVP体外释放模型拟合接近程度依次为一级方程>Peppas方程>Higuchi方程>零级方程。纳米银、纳米锌释放曲线符合零级方程,AVP的释放曲线符合一级方程。
|
图 3 CAVPG中纳米银(A)、纳米锌(B)和AVP (C)在各时间点的累积释放率(n=3) Fig.3 Cumulative release profile of nano-silver (A), nano-zinc (B), and AVP (C) in CAVPG at various time points (n=3) |
|
|
表 6 CAVPG中纳米银、纳米锌和AVP释放曲线的数学模型拟合结果 Table 6 Mathematical model fitting results of nano-silver release curve |
3 讨论
本实验通过对凝胶剂的外观、涂展性、黏度、高温稳定性、低温稳定性进行综合评分以及对凝胶剂中药物释放度的测定优选出Carbomer-980作为CAVPG的基质。Carbomer又名聚羧乙烯,是pH型凝胶基质,具有良好的生物相容性,以Carbomer为基质制备的凝胶剂具有无毒、对皮肤和黏膜无刺激性、易于涂布等优点。Carbomer含有52%~68%的酸性基团,在酸性条件下,聚合物链上有一小部分的羧基未和其他基团脱离而形成柔性的卷曲链;在碱性条件下,Carbomer树脂离子化并沿着聚合物的主链产生负电荷,同性电荷之间的相斥便促使分子伸直变成张开状态,形成黏稠的凝胶[22]。通常采用酸碱调节剂调节Carbomer水凝胶的pH值,常用的酸解调节剂为NaOH和三乙醇胺,由于NaOH为强碱,可能会对皮肤有局部刺激性,因此本实验选择三乙醇胺来调节pH值至7.0左右。
由于制备CAVPG时使用了PBS,含有一定的无机离子,会对Ag+、Zn2+的测定带来干扰,因此样品在进行测定前必须经过消解处理,消解液经稀释后再进行测定。同时,使用的玻璃仪器、消解管等均需要用30%的硝酸(优级纯)浸泡过夜,去离子水清洗烘干后方能使用。
凝胶剂是一类具有半固体性质的大分子网络体系,它能够与作用部位较长时间地紧密黏附,有较好的生物相容性,且制备简单,易于操作。凝胶剂吸水溶胀后所形成的水化凝胶层对药物有一定的控释作用[23]。考虑到烫烧伤患者换药时的巨大痛苦,临床上在治疗烧伤时都会选择能够缓释的药物,以此来减少给药次数及频率,减轻患者痛苦。本实验制备的CAVPG具有缓释的特点,可以为临床用药提供参考。
| [1] | Feily A, Namazi M R. Aloe vera in dermatology:a brief review[J]. Gital Dermatol Venereol, 2009, 144(1): 85–91. |
| [2] | Choi S W, Son B W, Son Y S, et al. The wound-healing effect of a glyprotein fraction isolated from Aloe vera[J]. Br J Dermatol, 2001, 145(9): 535–545. |
| [3] | 傅继华, 温涛, 徐琛, 等. 芦荟多糖对动物实验性胃溃疡的影响[J]. 中草药, 2006, 37(6):894–897. |
| [4] | Saini D K, Saini M R. Evaluation of radioprotective efficacy and possible mechanism of action of Aloe gel[J]. Environ Toxicol Pharmacol, 2011, 31(3): 427–435. DOI:10.1016/j.etap.2011.02.004 |
| [5] | Hamman J H. Composition and applications of Aloe vera leaf gel[J]. Molecules, 2008, 13(8): 1599–1616. DOI:10.3390/molecules13081599 |
| [6] | Choi S, Chung M H. A review on the relationship between Aloe vera components and their biologic effects[J]. Semin Integr Med, 2003, 1(1): 53–62. DOI:10.1016/S1543-1150(03)00005-X |
| [7] | Lee E M, Bai H W, Lee S K, et al. Gamma irradiation improves the antioxidant activity of Aloe vera (Aloe barbadensis Miller) extracts[J]. Radiat Phys Chem, 2012, 81(8): 1029–1032. DOI:10.1016/j.radphyschem.2012.02.033 |
| [8] | 王巧娥, 谢丹, 钱洁, 等. 库拉索芦荟凝胶多糖的GPC指纹图谱研究[J]. 中药材, 2015, 38(10):2070–2075. |
| [9] | 任海毅, 王巧娥, 董银卯, 等. 药用库拉索芦荟活性多糖的护肤特性研究[J]. 药物评价研究, 2012, 35(6):431–434. |
| [10] | 唐建红, 刘川玉, 何洁. 芦荟凝胶的制备及其稳定性评价[J]. 广西医学, 2015, 37(8):1138–1141. |
| [11] | 孙文杰, 陈彦, 高霞, 等. 地榆-纳米银复合物的制备与表征[J]. 中草药, 2013, 44(24):3465–3470. |
| [12] | 蔡伟, 马月, 方杰, 等. 中药材生物质还原制备银纳米颗粒及其抑菌活性研究[J]. 中草药, 2015, 46(7):977–981. |
| [13] | 赵纪峰, 王海军, 苏晶, 等. 中药多糖的提取分离工艺研究[J]. 重庆中草药研究, 2007, 1(5):29–32. |
| [14] | 翁闪凡, 庄锡伟, 杨安平, 等. 正交设计法优选元江芦荟多糖提取工艺的研究[J]. 现代医药卫生, 2009, 25(11):1675–1676. |
| [15] | 中国药典[S].二部. 2015. |
| [16] | 方彦霞, 郑省政, 王红燕. ICP-AES测定锑烟灰中铜、银、硒、碲、砷、铋方法研究[J]. 甘肃冶金, 2012, 34(4):101–103. |
| [17] | 吕培涛, 黄新敏, 陆益民, 等. ICP-AES法测定纳米银在非洲菊切花中的时空分布[J]. 光谱学与光谱分析, 2011, 31(8):2253–2255. |
| [18] | 张黄琴, 严辉, 钱大玮, 等. 不同产地百合药材中无机元素的分析与评价[J]. 中国现代中药, 2016, 18(8):960–966. |
| [19] | 陈伟, 陈俊, 林新华, 等. 库拉索芦荟多糖纯化方法研究[J]. 药物生物技术, 2004, 11(3):184. |
| [20] | 周丽, 张博雅, 张永忠. 亚临界水提取葛根中总异黄酮的研究[J]. 中草药, 2012, 43(3):492–495. |
| [21] | 张爱丽, 邵杰, 张庆芬, 等. 海蒙制酸缓释片制备工艺研究[J]. 中草药, 2015, 46(23):3514–3519. |
| [22] | 王彦, 王子娟. Carbomer在药剂学中的应用[J]. 中国药事, 2005, 19(6):361–364. |
| [23] | Meewes C, Brenneisen P, Wenk J, et al. Adaptive antioxidant response protects dermal fibroblasts from UVA-induced phototoxicity[J]. Rree Radic Bio Med, 2001, 30(3): 238–247. DOI:10.1016/S0891-5849(00)00463-9 |
 2016, Vol. 47
2016, Vol. 47


