2. 颈复康药业集团有限公司, 河北 承德 067000
2. Jingfukang Pharmaceutical Group Co., Ltd., Chengde 067000, China
苍术Atractylodis Rhizoma为我国常用中药材,药用历史悠久,始载于东汉《神农本草经》,被列为上品。目前收载于《中国药典》2010年版。其来源为菊科(Compositae)苍术属Atractylodes DC.植物北苍术Atractylodes chinensis (DC.) Koidz. 或茅苍术Atractylodes lancea (Thunb.) DC. 的干燥根茎[1]。具有燥湿健脾、祛风散寒之功效,用于湿阻中焦、脘腹胀满、泄泻、水肿、脚气痿蹙、风湿痹痛、风寒感冒、夜盲、眼目昏涩等证。现代药理研究表明苍术具有抗溃疡、抗心律失常、降血压、利尿、保肝、抗炎、抗菌、抗肿瘤等作用[2]。
北苍术分布于我国北京、河北、山西、内蒙古、辽宁、吉林、黑龙江、安徽等省、市、自治区;朝鲜、日本等国也有分布。承德是北苍术的产地之一,而且承德产北苍术苍术素量多于内蒙古、辽宁所产[2],其中颈复康药业集团有限公司已获得国家工信部批准的《北苍术规模化、规范化生产示范基地建设》-2013年中药材种植扶持项目。
目前,《中国药典》2010年版项下关于苍术的质量控制[1]是以显微、鉴别、水分、总灰分和苍术素的测定为指标进行的。王迪等[3]对大兴安岭产苍术建立了HPLC指纹图谱,陈佳等[4]对几个道地产区茅苍术建立了指纹图谱及苍术素测定。但目前北苍术药材中苍术素、苍术酮和β-桉叶醇的GC量测定及特征图谱综合研究,尚未见文献报道,本实验采集了承德地区及其他市场采购的北苍术药材,并建立了苍术素、苍术酮和β-桉叶醇3个主要成分的GC测定及特征图谱方法。同时,为科学评价北苍术质量及北苍术的规范化、规模化种植提供依据。
1 材料、仪器与试剂 1.1 材料25批北苍术样品经颈复康药业集团有限公司中药材、中药饮片高级鉴别师商春丽鉴定为北苍术Atractylodes chinensis (DC.) Koidz. 的干燥根茎,见表 1。
| 表 1 样品信息 Table 1 Information of samples |
Agilent7890A、Agilent6890 N、岛津2010气相色谱仪(FID检测器);Agilent HP-5气相毛细管色谱柱(30 m×0.32 mm,0.25 μm),DB-1701(30 m×0.32 mm,0.25 μm)毛细管柱,HP-INNOWAX(30 m×0.32 mm,0.25 μm)气相毛细管柱(安捷伦公司),AG245型电子分析天平(瑞士梅特勒-托利多集团);KQ-500DE型数控超声仪(昆山市超声仪器 有限公司);苍术素对照品,中国食品药品检定研究院,批号 111924-201303;苍术酮对照品,成都普菲德生物技术有限公司,批号 140607;β-桉叶醇对照品,成都普菲德生物技术有限公司,批号 140626;甲醇、醋酸乙酯、三氯甲烷都为国产分析纯,正己烷为进口分析纯。
2 方法与结果 2.1 定量测定 2.1.1 色谱条件Agilent7890A气相色谱仪,HP-5石英毛细管柱,配备FID检测器;进样口温度250 ℃,检测器温度250 ℃,柱温130 ℃,载气为高纯氮气,进样量2 μL,分流比10∶1;升温程序:初始温度130 ℃,保持8 min,以5 ℃/min的速率升温至145 ℃,保持8 min,以10 ℃/min的速率升温至190 ℃,保持1 min,再以5 ℃/min的速率升温至230 ℃,保持13 min。色谱图见图 1。
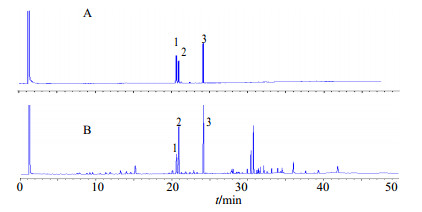 |
1-β-桉叶醇 2-苍术素 3-苍术酮 1-β-eudesmol 2-atractylon 3-atractylodin 图 1 混合对照品 (A) 和北苍术药材 (B) GC图谱 Fig.1 GC of mixed reference substances (A) andAtractylodis Rhizoma (B) |
精密称取苍术素、苍术酮、β-桉叶醇对照品适量,分别置棕色量瓶中,加正己烷,制成含苍术素39.516 μg/mL、苍术酮41.844 μg/mL、β-桉叶醇48.732 μg/mL的混合对照品储备液。
2.1.3 供试品溶液的制备取北苍术药材粉末0.5 g,置于棕色量瓶中,精密加正己烷15 mL,密塞,称定质量,超声(功率500 W,频率40 kHz)30 min,放冷,再称定质量,用正己烷补足减失的质量,摇匀,滤过,取续滤液,即得。
2.1.4 线性关系考察取“2.1.2”项下各对照品母液,按苍术素和苍术酮分别自动进样0.1、0.5、1.0、1.5、2 μL,β-桉叶醇自动进样0.1、0.2、0.3、0.5、1.0、2.0 μL,在“2.1.1”项色谱条件下测定,记录色谱峰面积,然后以进样量质量浓度为横坐标(X)对峰面积(Y)进行回归处理,计算得线性回归方程、相关系数及线性范围,结果见表 2。
| 表 2 对照品标准曲线、相关系数及线性范围 Table 2 Criteria curves, correlation coefficients, and linearity ranges of reference substances |
精密称取北苍术药材1份,按照“2.1.3”项方法制备供试品溶液,在“2.1.1”项色谱条件下重复进样6次,每次2 μL,记录各色谱峰面积,结果苍术素、苍术酮、β-桉叶醇峰面积的RSD值分别为0.67%、0.62%、0.39%,表明精密度良好。
2.1.6 重复性试验平行称取样品6份,制备供试品溶液,于“2.1.1”项下条件测定,记录色谱峰面积,结果苍术素、苍术酮、β-桉叶醇质量分数的RSD值分别为1.40%、1.30%、1.21%,表明重复性良好。
2.1.7 稳定性试验取按照“2.1.3”项方法制备供试品溶液1份,分别于0、2、4、6、8 h共进样5次,记录各色谱峰面积,计算8 h内苍术素、苍术酮、β-桉叶醇峰面积的RSD值分别为1.94%、2.71%、0.85%,表明供试品溶液在8 h内基本稳定。
2.1.8 加样回收率试验精密称取6份已测定的北苍术药材粉末0.25 g,分别加入混合对照品溶液适量,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下条件进行测定,以样品溶液中绝对质量分数计算加样回收率,结果苍术素平均回收率为100.12%,RSD为0.88%;苍术酮平均回收率为99.84%,RSD为1.29%;β-桉叶醇平均回收率为100.75%,RSD为1.17%;表明回收率良好。
2.1.9 检测限3种对照品,分别取其标准曲线工作液中最低质量浓度的溶液稀释,按“2.1.1”项色谱条件进样,记录各色谱峰面积,当信噪比值为3∶1时,取其峰面积与之相对应的进样质量浓度为检测限质量浓度。结果苍术素的检测限为0.06 ng;苍术酮的检测限为0.04 ng;β-桉叶醇的检测限为0.12 ng。
2.1.10 定量限按“2.1.1”项色谱条件,取已稀释的对照品溶液进样,并记录色谱峰面积和信噪比,当信噪比为10∶1时,取其峰面积与之相对应的进样质量浓度为定量限质量浓度。结果苍术素的定量限为0.16 ng;苍术酮的定量限为0.14 ng;β-桉叶醇的定量限为0.20 ng;
2.1.11 样品测定精密称取25批北苍术样品,分别按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件测定,测定结果见表 3。25批北苍术药材3种成分量差异明显;承德与山西样品β-桉叶醇量最高,内蒙古与黑龙江样品次之,辽宁与吉林样品中β-桉叶醇未检出;承德与黑龙江样品苍术酮量最高,内蒙古与辽宁(清源)样品量次之,山西、吉林与辽宁(凤城、海城)样品量最低;承德样品苍术素量最高,其余依次是吉林、内蒙古、辽宁、山西和黑龙江;6个不同产地3种成分量总体分析,承德地区β-桉叶醇、苍术酮、苍术素3种成分量均高于其他产地,尤其苍术素量更加明显。
| 表 3 25批北苍术药材3种成分测定结果 Table 3 Determination of three constituents in 25 batches of Atractylodis Rhizoma |
同“2.1.1”项。
2.2.2 对照品溶液制备同“2.1.2”项。
2.2.3 供试品溶液制备同“2.1.3”项。
2.2.4 精密度试验精密称取北苍术药材1份,按照“2.1.3”项下方法制备供试品溶液,在“2.1.1”项色谱条件下重复进样6次,每次2 μL,记录色谱图,以苍术素(5号峰)作为参照峰,色谱图中九个特征峰的相对保留时间和相对峰面积的RSD分别在0.001 3%~0.007 9%和0.501 6%~3.229 1%,表明仪器精密度良好。
2.2.5 重复性试验取同一批样品,按照“2.1.3”项下方法制备供试品溶液6份,将其按“2.1.1”项下色谱条件进样,记录色谱图,以苍术素(5号峰)作为参照物,色谱图中9个特征峰的相对保留时间和相对峰面积的RSD分别在0.008 1%~0.051 9%和0.087 7%~2.576 1%,表明仪器重复性良好。
2.2.6 稳定性试验取按照“2.1.3”项方法制备供试品溶液1份,分别于0、2、4、6、8 h共进样5次,记录色谱图,以苍术素(5号峰)作为参照峰,色谱图中9个特征峰的相对保留时间和相对峰面积的RSD分别在0.001 0%~0.019 1%和0.913 8%~2.082 9%,表明供试品溶液在8 h内基本稳定。
2.2.7 北苍术药材GC特征图谱的建立取承德与其他市场采购的25批北苍术药材,按照“2.1.3”项方法制备供试品溶液,在“2.1.1”项色谱条件下依次进行测定,记录色谱图。根据色谱图可知,苍术素(5号峰)的色谱峰分离良好,峰形稳定,且各样品中均含有此峰,选择苍术素(5号峰)作为参照峰。采用国家药典委员会“中药色谱指纹图谱相似度评价系统软件(2004A版)”,对25批北苍术药材生成对照图谱,结果见图 2和图 3。
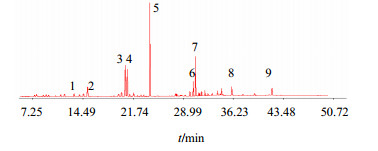 |
1-石竹烯 2-γ-榄香烯 3-β-桉叶醇 4-苍术酮 5-苍术素 6-1,2,3,4,5,6,7,8-八氢-9,10-二甲基蒽 7-4,5,6,7-四氢-3,6-二甲基-α-亚甲基-6-乙烯基-5-苯并呋喃乙酸甲酯 8-β-香树脂醇 9-2,5-双 (1-甲基-1-硅环丁基)-对-二甲苯 1-caryophyllene 2-γ-elemene 3-β-eudesmol 4-atractylon 5-atractylodin 6-1,2,3,4,5,6,7,8-octahydro-9,10-dimethylanthracene 7-4,5,6,7-tetrahydro- 3,6-dimethyl-α-methylene-6-ethenyl-5-benzofuranacetic acid methyl ester 8-β-amyrin 9-2,5-bis (1-methyl-1-silacyclobutyl)-p-xylene 图 2 北苍术药材对照图谱 Fig.2 Reference map of Atractylodis Rhizoma |
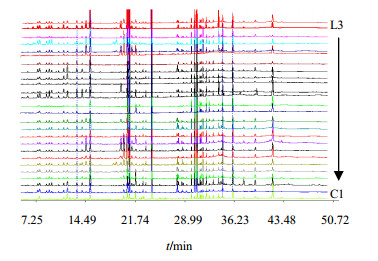 | 图 3 25批北苍术药材指纹图谱 Fig.3 Fingerprint of 25 batches of Atractylodis Rhizoma |
经承德与其他市场采购的25批北苍术药材色谱图比较后,从成分中选定了相对量较高的9个色谱峰作为特征峰。特征峰中的3、4、5号峰经与对照品对照,确定3号峰为β-桉叶醇,4号峰为苍术酮,5号峰为苍术素,其余1、2、6、7、8、9号峰是由GC-MS联用技术结合NIST11谱库匹配被指认出,1号峰为石竹烯,2号峰为γ-榄香烯,6号峰为1,2,3,4,5,6,7,8-八氢-9,10-二甲基蒽,7号峰为7-4,5,6,7-四氢-3,6-二甲基-α-亚甲基-6-乙烯基-5-苯并呋喃乙酸甲酯,8号峰为β-香树脂醇,9号峰为2,5-双 (1-甲基-1-硅环丁基)-对-二甲苯。
2.2.8 北苍术药材GC特征图谱相似度分析根据“2.1.7”项下生成的特征图谱,所得各批次样品的相似度见表 4。从表 4的北苍术药材相似度可以看出,承德地区第3、7、9、11号样品相似度最高,大于0.95;内蒙古第1号和承德第1、4、10、14~17号样品相似度次之,在0.90以上;内蒙古第2号和承德第2、5、6、8、12、13号样品相似度在0.80以上;吉林、黑龙江、辽宁样品相似度在0.75以上;山西样品的相似度最低0.68。
| 表 4 北苍术药材相似度 Table 4 Similarity of Atractylodis Rhizoma |
(1)提取溶剂:考察了甲醇、三氯甲烷、正己烷和醋酸乙酯,以成分个数和质量分数为依据,结果表明正己烷提取成分多,相对量高于甲醇、三氯甲烷和醋酸乙酯;(2)提取方法:对加热回流、提取挥发油和超声3种不同提取方式进行了比较,结果显示超声提取的结果最佳;(3)提取溶剂用量:考察提取溶剂用量(10、15、20、25 mL),经比较得出,15 mL的提取量高于10 mL的提取量,而15 mL的提取量与20、25 mL的提取量无明显差别;因此,以15 mL正己烷超声提取。(4)超声时间:考察了超声时间20、30、45、60 min,结果表明超声时间30 min的提取量略高于20 min的提取量,而30 min的提取量与45、60 min的提取量相当,因此确定提取的超声时间为30 min。(5)超声温度:考察了超声不同温度段水温(12~15、18~24、27~30 ℃),经比较得出,18~24 ℃的提取量略高于其余2个温度段的提取量,并且该温度段温度易控制,确定超声提取温度为18~24 ℃。
3.2 色谱条件的选择选用GC测定是在苍术文献报道[4, 5, 6, 7, 8, 9]的基础上,经多次重复验证和筛选对比以及北苍术自身所含化学成分的性质(挥发性、不稳定、避光)等综合考虑而确定的。所用GC色谱条件也是在文献报道[10, 11, 12]的基础上经过多次筛选、优化而确定的。其中,比较了不同的程序升温、载气流量、柱温、分流比及不同极性色谱柱等的影响,结果表明,本实验所建立的色谱条件出峰个数较多,且各峰间的分离度较好。
3.3 不同实验室与仪器的考察对所建立的色谱条件在不同实验室和不同仪器(Agilent7890A、Agilent6890N、岛津2010)上做了考察,结果表明在不同实验室和不同仪器上所测样品量和整体色谱图无明显差异。
3.4 定量测定与特征图谱结果分析由承德与其他市场采购的25批北苍术药材3个主要成分测定结果,对6个不同产地3种成分量总体分析,承德地区β-桉叶醇、苍术酮、苍术素3种成分量要高于其他产地,其中苍术素量尤为显著,平均值在其他5个产地苍术素量以上;通过方法学研究与样品测定结果表明,本实验建立的北苍术药材特征图谱方法可行,其中各样品间特征峰相对保留时间具有较好的重现性(RSD值:0.01%~0.05%);通过承德与其他市场采购的25批北苍术药材特征图谱相似度比较,承德地区17批样品平均相似度在0.90以上,高于其他市场采购的北苍术样品。综上,承德地区北苍术药材质量优于其他5个产地。
北苍术药材测定和GC特征图谱测定方法简便,精密度高,结果准确可靠,能为北苍术药材的规范化、规模化种植提供依据。另外,本实验收集的山西、辽宁、吉林、黑龙江、内蒙古的北苍术样品来源于市场采购、药材批次有限,还有待产地采挖更多批次的样品验证。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 李云霞, 李沈明, 商春丽. 承德发展苍术种植的可行性分析 [J]. 中草药, 2013, 44(9): 1215-1218. |
| [3] | 王 迪, 夏永刚, 杨炳友, 等. 大兴安岭产苍术HPLC指纹图谱研究 [J]. 中医药学报, 2013, 41(3): 14-16. |
| [4] | 陈 佳, 谢小霞, 刘合刚, 等. 几个道地产区茅苍术指纹图谱及苍术素含量测定研究 [J]. 中国实验方剂学杂志, 2013, 19(10): 125-127. |
| [5] | 葛晓郡, 张亚中, 黄丽丹, 等. 苍术药材HPLC特征指纹图谱研究 [J]. 山西中医学院学报, 2011, 12(5): 19-22. |
| [6] | 姚 佳, 刘玉强, 才 谦, 等. GC法测定不同来源苍术饮片中茅术醇和β-桉叶醇的含量 [J]. 中国药房, 2014, 25(3): 246-248. |
| [7] | 张贝贝, 方 婧, 许海玉, 等. HPLC测定道地产地和主产地茅苍术中β-桉叶醇及其他成分的含量 [J]. 中国实验方剂学杂志, 2011, 17(8): 116-118. |
| [8] | 刘佳鑫, 李古月, 才 谦, 等. 苍术麸炒后增量成分研究 [J]. 中国医药导报, 2014, 11(5): 105-108. |
| [9] | 张 铮. 不同产地苍术中茅术醇含量测定 [J]. 中国药事, 2011, 25(10): 1033-1034. |
| [10] | 张金龙, 秦昆明, 徐自升, 等. 南北苍术炮制前后特征图谱及苍术素含量研究 [J]. 科学技术与工程, 2011, 11(20): 4843-4847. |
| [11] | 冯维希, 谷 巍, 孔令婕, 等. 不同产地茅苍术HPLC指纹图谱研究 [J]. 南京中医药大学学报, 2010, 26(6): 434-435. |
| [12] | 付梅红, 方 婧, 王祝举, 等. 气相色谱法测定苍术中茅苍术醇含量的方法学研究 [J]. 时珍国医国药, 2008, 19(4): 994-995. |
 2016, Vol. 47
2016, Vol. 47



