2. 天士力控股集团有限公司研究院 现代中药开发中心, 天津 300410 ;
3. 天士力制药集团股份有限公司 创新中药关键技术国家重点实验室, 天津 300410
2. Development Center of Modern Chinese Materia Medica, Tasly Academy, Tasly Group Co., Ltd., Tianjin 300410, China ;
3. State Key Laboratory of Critical Technology in Innovative Chinese Medicine, Tianjin 300410, China
芪参益气滴丸(Qishen Yiqi Dropping Pills,QYDP)是天士力在传统经验方基础上,采用现代工艺制备而成的一种中药复方制剂,由黄芪、丹参、三七、降香油组成,广泛用于冠心病及气虚血瘀所引起的各种疾病的治疗[1],尤其在心肌梗死二级预防的基础与临床试验中显示了良好的应用前景[2-3]。目前对于该制剂非挥发性成分的研究已相当明确[4],而对于其挥发性成分的研究尚不清晰。降香以挥发油形式入方,为该方主要的挥发性成分,据文献报道降香油主要成分有反式橙花叔醇(trans- nerolidol)、氧化橙花叔醇及其异构体[5-7],此外,还有法尼醇(金合欢醇,farnesol)、E-β-金合欢烯(E-β-farnesene)、氧化石竹烯(caryophyllene oxide)、β-甜没药烯(β-bisabolene)、α-白檀油醇(α-santalol)等[8-9],具有抗血栓[7, 10]、抗血小板凝集[11-12]、抑菌[13]等药理活性。另外,中药挥发油及芳香性药物透皮吸收促进作用的研究报道日益增多[14],Han等[15]利用Caco-2细胞模型研究降香油体外促吸收作用,发现可以显著增加芪参益气方中丹参主要成分丹参素、原儿茶醛、丹酚酸D、迷迭香酸,黄芪主要成分毛蕊异黄酮苷、黄芪甲苷,及三七主要成分三七皂苷R1、人参皂苷Rb1和人参皂苷Rg1等的吸收,显示出良好的促吸收作用。因此,阐明QYDP中挥发性成分对于表征该复方全方药效及配伍合理性具有重要意义。另外,目前降香资源稀少,价格昂贵,研究者可尝试通过增加用药部位、改善工艺条件等方法尽可能使降香资源利用最大化,本实验研究也可为降香资源研究提供检测手段。
本实验对收集到的12批市售QYDP和13批生产用降香油开展GC指纹图谱研究,运用“中药色谱指纹图谱相似度评价系统2012版”软件,进行相似度评价,并对指纹图谱中共有峰进行化学指认,为QYDP和降香油的质量评价与控制奠定一定工作基础。
1 仪器与材料Agilent 7890A气相色谱仪,配FID检测器,美国Agilent公司;岛津GCMS-TQ8030气质联用色谱仪,日本Shimadzu;KQ-500DV超声波清洗器,昆山市超声仪器有限公司;XS205电子天平,瑞士Mettler Toledo公司。
N,N-二甲基甲酰胺(DMF),色谱纯,德国Merck公司;反式橙花叔醇(批号Lot#BCBP532TV,质量分数≥85%),德国Sigma公司;法尼醇(顺反异构混合对照品,批号20140106,总质量分数98.0%)、氧化石竹烯(批号20140106,质量分数98.0%)、E-β-金合欢烯(批号20140815,质量分数98.0%),天津士兰科技有限公司;12批市售QYDP(批号20120201、20130202、20130401、20130702、20140207、20140406、20140709、20140903、20140909、20150102、20150208、20150314,代号Q1~Q12)是由天津天士力制药股份有限公司提供,是先由黄芪、丹参、三七3味药材按照不同的工艺与配比制成浸膏,再与降香油混合制成,制备过程符合GMP要求,质量达到企业内控标准;13批降香油(批号20100601、20111101、20131203、20140501、20140701、20140702、20140703、20140801、20140802、20140803、20150301、20150302、20150303,代号D1~D13),由天津天士力现代中药资源有限公司提供,药材均为市场统货,经中国药科大学余伯阳教授鉴定为豆科植物降香檀Dalbergia odorifera T. Chen树干和根的干燥心材,采收季节为全年,除去边材,阴干,按照统一生产工艺流程,采用水蒸气蒸馏法,连续提取至油尽所得,制备过程符合GMP要求,质量达到企业内控标准。
2 方法与结果 2.1 GC-MS条件 2.1.1 GC条件Agilent HP-INNOWax毛细管柱(30 m×0.25 mm,0.25 μm);程序升温:柱起始温度100 ℃,保持2 min,以3 ℃/min升温至160 ℃,以1 ℃/min升温至190 ℃,以5 ℃/min升温至220 ℃,以10 ℃/min升温至250 ℃;进样口温度230 ℃,分流比5∶1,进样量1 μL;恒流模式,载气为氮气,体积流量0.5 mL/min;FID检测器温度300 ℃,氢气体积流量40 mL/min,空气体积流量400 mL/min,尾吹氮气体积流量25 mL/min。
2.1.2 MS条件EI离子源温度230 ℃,接口温度250 ℃,电离电压70 eV,扫描质量范围m/z 35~600,溶剂延迟8 min,碰撞气:氩气(纯度≥99.999%),岛津GC Solution工作站。
2.2 溶液的制备 2.2.1 QYDP供试品溶液的配制取每批QYDP 500 mg,精密称定,置于10 mL量瓶中,加入DMF 8 mL,超声处理45 min(功率500 W,频率40 kHz,温度30 ℃),放至室温,加入DMF定容,摇匀,于4 ℃冷藏2 h后,低温离心15 min(4 ℃,14 100 r/min),取上清液,即得。
2.2.2 降香油供试品溶液的配制取每批降香油20 mg,精密称定,置25 mL量瓶中,加入DMF定容,摇匀,过0.22 μm微孔有机滤膜,取续滤液,即得。
2.2.3 混合对照品溶液的配制分别称取反式橙花叔醇、法尼醇、E-β-金合欢烯、氧化石竹烯适量于10 mL量瓶中,加入DMF制成分别含反式橙花叔醇1.12 mg/mL、法尼醇1.02 mg/mL、氧化石竹烯1.17 mg/mL、E-β-金合欢烯0.48 mg/mL的混合对照品溶液。
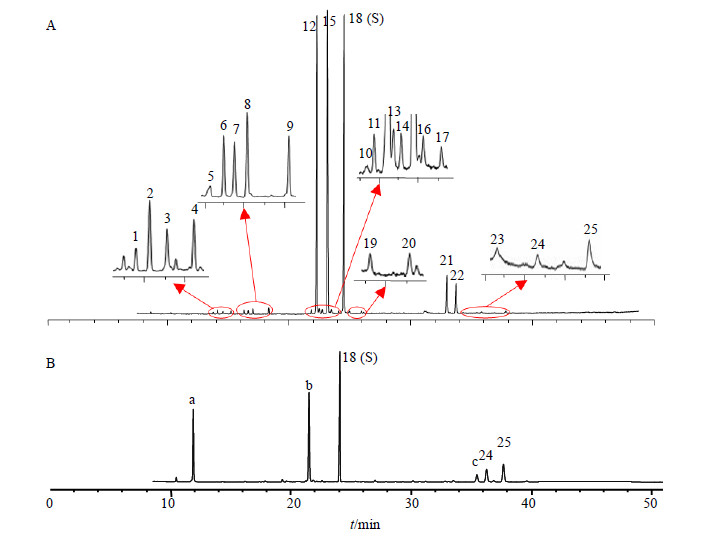
2.3 方法学考察 2.3.1 专属性考察取空白溶剂、QYDP供试品溶液、降香油供试品溶液各1份,按“2.1.1”项下色谱条件,分别进样,记录色谱图,见图 1。经考察,空白溶剂对供试品指纹图谱均无干扰,表明该方法专属性良好。

|
图 1 专属性 Fig.1 Specificity |
2.3.2 精密度试验
取同一份QYDP供试品溶液(批号20140909)和同一份降香油供试品溶液(批号20131203),按“2.1.1”项下色谱条件,各自连续进样6针,记录色谱图。以18号色谱峰反式橙花叔醇为参照峰,QYDP中33个主要色谱峰的相对保留时间(tR)RSD值≤0.01%,相对峰面积的RSD值≤2.30%;降香油中25个主要色谱峰tR的RSD值≤0.01%,相对峰面积的RSD值≤1.77%。结果表明仪器精密度良好。
2.3.3 重复性试验取同一批QYDP(批号20140909)和同一批降香挥发油(批号20131203)按“2.2”项下操作,平行制备制剂和降香油供试品溶液各6份,按“2.1.1”项下色谱条件,依次进样,记录色谱图。以18号色谱峰反式橙花叔醇为参照峰,QYDP中33个主要色谱峰tR的RSD值≤0.03%,相对峰面积的RSD值≤2.62%;降香油中25个主要色谱峰tR的RSD值≤0.01%,相对峰面积的RSD值≤1.64%。结果表明,该方法对于QYDP和降香油均具有良好的重复性。
2.3.4 稳定性试验取同一份QYDP供试品溶液(批号20140909)和同一份降香油供试品溶液(批号20131203),按“2.1.1”项下色谱条件,分别于0、2、4、6、8、12、24 h进样,记录色谱图。以18号色谱峰反式橙花叔醇为参照峰,QYDP中33个主要色谱峰tR的RSD值≤0.01%,相对峰面积的RSD值≤2.44%;降香油中25个主要色谱峰tR的RSD值≤0.01%,相对峰面积的RSD值≤2.29%。结果表明QYDP和降香油供试品溶液在24 h内均稳定。
2.4 指纹图谱分析 2.4.1 参照峰的选择在各批次样品指纹图谱中反式橙花叔醇(18号)色谱峰分离度良好,出峰时间居中,峰面积较大,且所有样品中共有,故以18号色谱峰的保留时间和峰面积为参照(S),计算各共有峰的tR和相对峰面积。
2.4.2 特征指纹图谱的建立及相似度评价将12批市售QYDP和13批生产用降香油的GC-FID图谱导入国家药典委员会“中药色谱指纹图谱相似度评价系统2012版”软件,生成QYDP和降香油指纹图谱,见图 2。QYDP指纹图谱中共有33个共有峰,其中25个与降香油指纹图谱的共有峰重合,约占总峰面积的85.2%以上,对应的共有峰见图 3,其中12、15、18、21、22号峰峰面积所占比例较大,QYDP中上述5个峰分别约占总峰面积的19.4%、21.8%、26.1%、3.9%、2.9%,降香油中上述5个峰分别约占总峰面积的25.6%、27.1%、31.3%、4.8%、3.9%,因此对多批次QYDP及降香油的GC-FID数据中这5个色谱峰进行单独积分,考察它们对相似度的贡献,见表 1,结果显示,QYDP和降香油中上述5个大色谱峰对各指纹图谱相似度贡献较大,是表征整体指纹图谱的重要特征峰。

|
图 2 QYDP (A)、降香油 (B) GC-FID指纹图谱及各自对照图谱 (R) Fig.2 GC-FID fingerprint of volatile components from QYDP (A),D. odorifera oil (B) and each reference fingerprin t (R) |

|
图 3 典型QYDP (A) 和降香油 (B) GC-FID图谱 (共有峰编号参照表 2) Fig.3 TypicalGC-FIDfingerprint of volatile components from QYDP (A) and D. odorifera oil (B) (serial numbers of common peaks refer to Table 2) |
|
|
表 1 QYDP及降香油GC-FID指纹图谱相似度 Table 1 Similarity of volatile components in QYDP and D. odorifera oil by GC-FID |
本实验将所有峰积分以中位数分别计算指纹图谱的相似度值,QYDP的相似度在0.979~0.999,降香油的相似度在0.989~1.000,表明天士力生产的QYDP和生产用降香油各批次之间相似度良好、质量稳定。
2.5 共有色谱峰的化学指认按“2.2”项下方法制备1份降香油供试品溶液,1份混合对照品溶液,按“2.1”项下条件进样,分别记录GC-MS色谱图,见图 4。通过GC Solution 4.2化学工作站数据处理系统,检索NIST 11.0质谱图库,对照品比对,并结合相关文献报道[6-7, 14]进行人工谱图解析,确定了23个共有峰的化学成分,结果见表 2。
|
图 4 降香油 (A) 和混合对照品 (B) GC-MS图谱 (共有峰编号参照表 2) Fig.4 GC-MSchromatogram of volatile components from D. odorifera oil (A) and mixed reference substances (B) (serial numbers of common peaks refer to Table 2) |
|
|
表 2 降香油的共有成分 Table 2 Common components of D. odorifera oil |
3 讨论 3.1 提取条件的优化
QYDP是将药材提取物与聚乙二醇(PEG)6000用适宜方法混匀后,滴入不相混溶的冷凝液中,收缩冷凝而制成的制剂,因此为使样品信息最大化,应选择能使PEG 6000完全溶解,使成分尽可能全部溶出且对样品测定无干扰的溶剂,故选择DMF;
采用超声提取方法对制剂进行前处理,考察了超声温度(20、30、40 ℃)、时间(30、45、60 min)对指纹图谱的影响,以色谱峰数、响应值为主要因素,同时考虑节约能源,选择超声30 ℃、45 min为最佳提取条件;另外,为减小PEG 6000对进样口的污染及图谱的干扰,超声后的提取液于4 ℃冷藏2 h后,4 ℃低温离心,使部分PEG 6000析出,取上清液进样。
3.2 色谱柱的选择根据文献报道[7, 14-18],本实验对不同极性的气相色谱柱进行筛选,包括以 (5%-苯基)-甲基聚硅氧烷为固定相的低极性毛细管柱Agilent HP-5,以 (50%-苯基)-甲基聚硅氧烷为固定相的中等极性毛细管柱Agilent DB-17,以及以PEG为固定相的强极性毛细管柱Agilent HP-INNOWax,发现仅有以PEG为固定相的强极性毛细管柱能将12、15、18、21、22号峰完全分开,故选择Agilent HP-INNOWax毛细管柱。
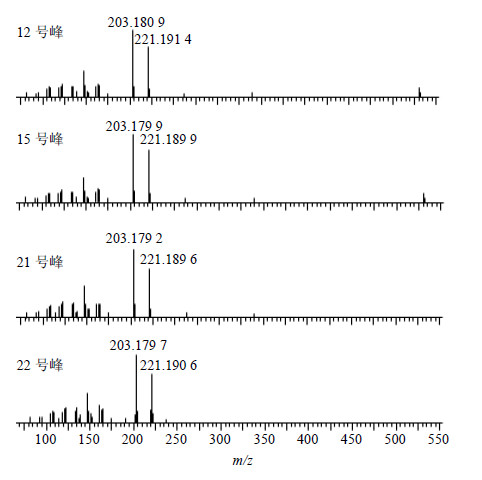
3.3 化学成分推测本实验对文献中报道较多的降香油成分,如反式橙花叔醇、法尼醇、E-β-金合欢烯、氧化石竹烯,采用对照品进行比对;对于无对照品的成分,通过检索NIST 11.0质谱图库并结合文献报道推测其结构。对照品比对结果显示,18号峰对应的成分为反式-橙花叔醇;本实验所使用的法尼醇对照品为3个顺反异构体的混合物,24、25号峰与混合对照品的2个峰重合,且质谱碎片信息一致,故推测二者为法尼醇的2个异构体;而E-β-金合欢烯、氧化石竹烯对照品与降香油样品图谱比对,均未发现重合部分,且质谱碎片信息不一致,与文献报道[6-7, 14]不一致。另外,降香油样品中量较高的12、15、21、22号峰均无对照品,GC-MS结果显示,上述4个峰均具有m/z 155、138、127、111、109、93、81、69、55、43的碎片离子,LC-ESI-MS结果(图 5)显示,上述4个峰在正离子模式下均具有m/z 221.19([M+H-H2O]+),203.17([M+H-2H2O]+)的碎片离子,与文献报道[3, 5, 11]一致,推测上述各成分为氧化橙花叔醇(3,7,11-trimethyl-3,6-epoxy-1,10-dodecadien-7-ol)的旋光异构体,但对于立体结构的确定,还需要通过核磁、红外等手段进行进一步的确认。
|
图 5 12、15、21、22号峰LC-ESI-MS正离子模式质谱碎片图谱 Fig.5 LC-ESI-MS spectrum of peaks 12,15,21,and 22 in positive ion ESI |
3.4 12批QYDP和13批降香油的质量评价
目前QYDP的质量研究主要集中在非挥发性成分上,如酚酸类、皂苷类、黄酮类等,对挥发性成分研究较少,降香以挥发油形式入方,为该方主要的挥发性成分,但目前由于缺少降香油主要成分的对照品,故本实验通过建立GC指纹图谱的方法来整体评价制剂及降香油挥发性成分的质量。本实验结果显示,12批市售QYDP相似度均大于0.979,表明该制剂批次间差异小,质量稳定;13批降香油相似度均大于0.989,表明该生产用降香油批次间差异小,质量稳定。同时,该制剂33个共有峰中有25个来自降香油,约占总峰面积的80.1%~89.2%,表明该制剂生产工艺合理,几乎保留了全部的降香油成分。
本实验建立的GC指纹图谱方法,简单、可靠,可同时用于QYDP和降香油的挥发性成分研究,为制剂全面、系统的质量评价与控制提供参考,也为生产用降香油质量评价与控制提供参考,同时为降香资源研究和工艺研究提供了有效的检测手段。
| [1] | 高晟, 周静. 芪参益气滴丸联合西药对冠心病心绞痛气虚血瘀证患者疗效的影响[J]. 现代药物与临床, 2012,27 (4) :389–392. |
| [2] | 崔佩佩, 王刚, 宋生有, 等. 芪参益气滴丸对大鼠心肌缺血Ppp3r1及Atp5d基因表达变化的影响[J]. 药物评价研究, 2010,33 (3) :191–193. |
| [3] | 商洪才. 芪参益气滴丸对心肌梗死二级预防的临床试验研究通过专家组验收[J]. 天津中医药, 2010,27 (4) :266. |
| [4] | Wang J, Wei N, Zhao H, et al. Global chemome study by LC coupled with DAD and ESI-Q-TOF MS of a composite traditional Chinese medicine Qishenyiqi Dropping Pills[J]. Chromatographia, 2010, 72 (5/6) :431–440 . |
| [5] | 谭春梅, 张文婷, 马临科, 等. GC法测定降香药材中反式苦橙油醇及4个氧化苦橙油醇异构体的含量[J]. 药物分析杂志, 2014,34 (11) :2083–2086. |
| [6] | 高阳, 金浩鑫, 魏惠珍, 等. GC测定降香油中氧化橙花叔醇I、氧化橙花叔醇II、反式橙花叔醇的含量[J]. 中国实验方剂学杂志, 2014,20 (24) :78–80. |
| [7] | Tao Y, Wang Y. Bioactive sesquiterpenes isolated from the essential oil of Dalbergia odorifera T. Chen[J]. Fitoterapia, 2010, 81 (5) :393–396 . |
| [8] | 刘洪玲. GC-MS法分析降香挥发油化学成分[J]. 中成药, 2009,31 (6) :915–917. |
| [9] | 赵祥升, 魏建和, 甘炳春, 等. 降香挥发油GC指纹图谱的研究[J]. 中国现代应用药学, 2011,28 (11) :995–999. |
| [10] | 朱亮, 冷红文, 谭力伟, 等. 降香挥发油对血栓形成、血小板cAMP和血浆纤溶酶活性的影响[J]. 中成药, 1992,14 (4) :30–31. |
| [11] | 杨超燕, 唐春萍, 沈志滨. 降香挥发油对垂体后叶素致大鼠急性心肌缺血的保护作用及急性毒性实验研究[J]. 时珍国医国药, 2011,22 (11) :2685–2686. |
| [12] | 王秀丽, 张艳秋. 降香挥发油-HP-β-CD的制备及对急性心肌缺血模型大鼠的保护作用[J]. 山东中医药大学学报, 2010,34 (3) :256–257. |
| [13] | Wang H, Dong W H, Zuo W J, et al. Five new sesquiterpenoids from Dalbergia odorifera[J]. Fitoterapia, 2014, 95 :16–21 . |
| [14] | 黄罗生, 顾燕飞, 李红. 中药挥发油及芳香性药物的研究进展[J]. 中国中药杂志, 2009,34 (12) :1605–1611. |
| [15] | Han Y Q, Wang J, Cui Q X, et al. Absorption, metabolism and effect of compatibility on absorption of qishenyiqi dropping pill[J]. Biomed Chromatogr, 2013, 28 (4) :554–563 . |
| [16] | 赵祥升, 魏建和, 甘炳春, 等. GC法同时测定降香中4个成分的含量[J]. 药物分析杂志, 2012,32 (3) :392–395. |
| [17] | 郭丽冰, 王蕾, 廖华卫. 降香CO2超临界萃取物的GC-MS分析[J]. 广东药学院学报, 2007,23 (1) :12–13. |
| [18] | 宋晓涛, 赵颖, 张文生, 等. 降香药材及其制剂指纹图谱研究[J]. 天津中医药, 2003,20 (1) :51–54. |
| [19] | 王文燕, 王靖, 张铁军. 降香挥发油的指纹图谱研究[J]. 中草药, 2007,38 (1) :66–68. |
| [20] | 刘荣霞, 王巧, 毕开顺, 等. 降香药材色谱指纹图谱的建立及其在药材鉴定中的应用[J]. 药学学报, 2005,40 (11) :48–52. |
 2016, Vol. 47
2016, Vol. 47


