肺部给药目前一直是国内外研发的热点之一[1],肺部吸入剂型也一直受到广泛关注。对于慢性肺阻塞(COPD)、哮喘、肺气肿等疾病,肺部吸入给药是理想的给药途径,避免了肝首关效应,起效快,肺外副作用小[2, 3]。对于肺部可吸入微粉而言,微粉粒径大小影响着药物在肺部的吸收,当粒径>5 μm时药物倾向沉积于上呼吸道,最后会随上皮细胞黏膜而呼出或被吞咽,而<1 μm时则到达下呼吸道,最终也会呼出体外,而只有1~5 μm才能在肺部沉积[4, 5]。生地黄低聚糖是由生地黄饮片加水煎煮浓缩后采用HPD大孔树脂进行蒸馏水洗脱后,将得到的洗脱液采用活性炭煮沸脱色后,用超滤膜(截留相对分子质量为1 000的卷式膜)和纳滤膜(截留相对分子质量为150的卷式膜)进行超滤和纳滤之后最终得到的纳滤截留液减压浓缩至少量后冷冻干燥得到的低聚糖部位。其为淡黄色疏松状固体,相对分子质量为1 000以下,在临床上对于COPD有很好的治疗和预防作用[6, 7, 8],对于肺部给药具有一定的可行性。生地黄低聚糖由水苏糖、棉子糖和甘露三糖等组成,水苏糖为其主要成分[9]。生地黄低聚糖吸湿性强,在不加入辅料的情况下无法直接制成微粉,因此前期丁礼琴等[9]采用喷雾干燥将其制成可吸入微粉,加入辅料L-亮氨酸和甘露醇改善其吸湿性,制得了载药量为20%的生地黄低聚糖微粉,收率和吸湿率分别为79%和6%,但由于载药量低,成本高,亟需提高载药量。
纳米喷雾干燥是近年来发展起来的新兴喷雾干燥技术,采用压电驱动原理,将料液从微孔中喷出形成喷雾,雾化的液滴进入热干燥气体中快速干燥,形成干粉微粒后采用高压静电装置收集微粉。与传统的喷雾干燥技术相比,它使微粉的干燥受热过程更加均匀,能够温和地干燥热敏物质,保持其活性,并且可直接得到平均粒径为0.3~5 μm的微粒,而且对于低至毫升级别的药液,产率也高达90%,避免了传统喷雾干燥时由于物料黏性太强而粘壁、结块导致的收率过低问题,尤其适合制药、生物技术、材料和纳米技术方面,对于吸入制剂也尤为适用[10]。本实验采用纳米喷雾干燥技术制备生地黄低聚糖微粉,采用单因素考察后通过正交试验设计优选最佳制备工艺,旨在提高载药量,改善生地黄低聚糖的吸湿性。
1 仪器与材料Buchi B-90纳米喷雾干燥仪、Buchi296除湿机,瑞士步琦公司;90-1双向磁力搅拌器,上海亚荣生化仪器厂;SEMKYKYSBC-12B型离子溅射仪,北京中科科仪股份有限公司;型号VEGA TS 5136 MM扫描电子显微镜,德国泰思肯公司;MS3000激光粒度测定仪,英国马尔文公司;MA35型红外快速水分测定仪,德国赛多利斯公司;药品稳定性试验箱,上海一恒科学仪器有限公司;生地黄低聚糖,曙光医院制剂室自制;乳糖inhalac70、inhalac120和inhalac230,德国美剂乐公司;木糖醇、D-海藻糖,上海格澜精细化工公司;甘露醇,青岛明月海藻集团有限公司,批号F20091029;L-亮氨酸,上海耕奔生物技术有限公司,批号100125;其他试剂均为分析纯。
2 方法与结果 2.1 纳米喷雾干燥工艺的评价指标 2.1.1 微粉粒径分布及平均粒径的测定[11]采用马尔文MS3000粒径测定仪干法测定微粉的粒径。每次取少量样品进行测定,得到d0.1、d0.5、d0.9和d(4,3),1个样品测定3次,取平均值,平均的d(4,3)值即为该样品的平均粒径。粒径分布用跨度(span)表示,span=(d0.9-d0.1)/d0.5,跨度越大,粒径分布越宽,粒子大小越不均匀。
2.1.2 微粉收率的测定以纳米喷雾干燥前称取的生地黄低聚糖和辅料总质量记为W1,纳米喷雾干燥后收集的微粉总质量记为W2,则微粉收率=W2/W1。
2.1.3 微粉吸湿率的测定称取一定量的微粉于干燥器中平衡脱湿24 h后,精密称取微粉0.5 g平摊于恒定质量的称量瓶中,置于25 ℃、相对湿度为75%的药品稳定性试验箱中,于48 h称定质量,平行3份,取平均值,计算吸湿率。
吸湿率=(吸湿48 h后样品质量-吸湿前样品质量)/吸湿前样品质量
2.2 纳米喷雾干燥单因素试验考察 2.2.1 不同辅料的考察以平均粒径、收率、吸湿率、流动性和分散性作为指标,固定纳米喷雾干燥的喷头大小为7.0 μm,气体流量为120 L/min,泵为Pump 1,进风口温度为120 ℃,喷雾干燥效率为80%,药液质量分数为2%,生地黄低聚糖与辅料比例为2∶8,分别对不同乳糖(inhalac70、inhalac120和inhalac230)、木糖醇、D-海藻糖、甘露醇和L-亮氨酸进行筛选。由表 1可知,和其他辅料相比,只有甘露醇和L-亮氨酸制备得到的微粉平均粒径较低,收率较高,并且考虑到粉体的分散性和流动性,确定甘露醇和L-亮氨酸作为制备微粉的辅料。
| 表 1 不同辅料制得的微粉性质考察 Table 1 Properties of micro powders prepared by different materials |
以平均粒径、收率和吸湿率为指标,固定纳米喷雾干燥气体流量为120 L/min,泵为Pump 1,进风口温度为120 ℃,喷雾干燥效率为80%,药液质量分数为2%,生地黄低聚糖与辅料比例为2∶8,辅料选用甘露醇和L-亮氨酸(两者比例为8∶2),分别以喷头大小4.0、5.5、7.0 μm制备微粉,考察喷头大小对粉体的影响。由表 2可知,喷头大小可显著影响微粉的平均粒径,喷头越大,平均粒径也越大,喷头为4.0 μm时平均粒径最小,但收率最低,综合考虑吸湿性和收率,确定5.5 μm喷头作为纳米喷雾干燥参数之一。
| 表 2 不同喷头制得的微粉性质考察 Table 2 Properties of micro powders prepared by different nozzles |
以平均粒径、收率和吸湿率为指标,固定纳米喷雾干燥喷头为5.5 μm,泵为Pump 1,进风口温度为120 ℃,喷雾干燥效率为80%,药液质量分数为2%,生地黄低聚糖与辅料比例为2∶8,辅料选用甘露醇和L-亮氨酸(两者比例为8∶2),分别以气体体积流量110、120、130 L/min制备微粉,考察气体体积流量对粉体的影响。由表 3可知,随着气体体积流量的提高,微粉的平均粒径和收率均得到提高,吸湿率也明显降低,因此选择气体体积流量130 L/min作为纳米喷雾干燥的参数之一。
| 表 3 不同气体体积流量下制备的微粉性质考察 Table 3 Properties of micro powders prepared by different gas flow |
以平均粒径、收率和吸湿率为指标,固定纳米喷雾干燥喷头为5.5 μm,气体体积流量为130 L/min,进风口温度为120 ℃,喷雾干燥效率为80%,药液质量分数为2%,生地黄低聚糖与辅料比例为2∶8,辅料选用甘露醇和L-亮氨酸(两者比例为8∶2),分别以Pump 1、2、3、4制备微粉,考察不同的泵对粉体的影响。由表 4可知,使用Pump3制备时无法得到微粉,其余3个泵制备的微粉中Pump 1和Pump 4制备的微粉平均粒径小,收率高,吸湿率低,但使用Pump 4制备微粉的速度很慢,综合考虑,选择Pump 1作为纳米喷雾干燥的参数之一。
| 表 4 不同泵制备的微粉性质考察 Table 4 Properties of micro powders prepared by different pumps |
以平均粒径、收率和吸湿率为指标,固定纳米喷雾干燥其他条件,分别以100、110、120 ℃制备微粉,考察不同的进风口温度对粉体的影响。由表 5可知,当进风口温度为110、120 ℃时,制备得到的微粉平均粒径小,吸湿率低,其中120 ℃时的收率更高,但考虑到温度过高可能对生地黄低聚糖的稳定性产生影响,选择进风口温度110 ℃作为纳米喷雾干燥的参数之一。
| 表 5 不同进风口温度制得的微粉性质考察 Table 5 Properties of micro powders prepared by different inlet temperature |
固定甘露醇和L-亮氨酸的比例,以平均粒径、收率、吸湿率和流动性分散性作为指标,对生地黄低聚糖和辅料的不同配比进行考察。由表 6得出,随着辅料量的提高,微粉的平均粒径减小,收率增加,流动性和分散性也得到改善,但辅料量过大,载药量降低,成本较高,综合考虑,确定生地黄低聚糖和辅料以3∶7的比例混合后进行纳米喷雾干燥。
| 表 6 生地黄低聚糖与辅料不同配比的微粉性质考察 Table 6 Properties of micro powders prepared by different RehmanniaeRadix oligosaccharides and material ratios |
以平均粒径、收率和吸湿率为指标,考察不同比例的甘露醇和L-亮氨酸对微粉性质的影响,确定两者的比例。由表 7得出,以上配比得到的微粉吸湿性均较好,收率均达到68%以上,但当甘露醇与L-亮氨酸配比为7∶3时,平均粒径较小,因此确定两者比例为7∶3。
| 表 7 甘露醇和L-亮氨酸不同配比的微粉性质考察 Table 7 Properties of micro powders prepared by different proportions of mannitol and L-leucine |
以平均粒径、收率和吸湿率为指标,考察不同的喷雾干燥效率对微粉的影响。由表 8得出,喷雾干燥效率越低,微粉平均粒径越小,收率越高,吸湿率也较好,但当喷雾干燥效率为30%时制备微粉的速度较慢,综合考虑,初步选择喷雾干燥效率50%为纳米喷雾干燥的参数之一。
| 表 8 不同喷雾干燥效率下制得的微粉性质考察 Table 8 Properties of micro powders prepared by different spray drying efficiencies |
以平均粒径、收率和吸湿率为指标,考察不同的药液浓度对微粉的影响。由表 9得出,3种药液质量分数制备得到的微粉吸湿性均较好,药液质量分数越低,微粉平均粒径越小,收率越高,因此选择药液质量分数1%为纳米喷雾干燥的参数之一。
| 表 9 不同药液浓度下制得的微粉性质考察 Table 9 Properties of micro powders prepared by different solution concentration |
根据前期的单因素实验结果,设定纳米喷雾干燥仪的喷头为5.5 μm,气体体积流量为130 L/min,泵为Pump 1,辅料选为甘露醇和L-亮氨酸(比例为7∶3),生地黄低聚糖与辅料比例为3∶7。选取进风口温度(A)、喷雾干燥效率(B)和药液质量分数(C)3个因素,各选择3个水平按L9(34) 正交表进行正交试验设计,以平均粒径、收率和吸湿率的综合评分为评价指标,其中平均粒径、收率和吸湿率的综合评分的权重系数依次为0.5、0.4和0.1,综合评分值=最小平均粒径值/平均粒径值×0.5+收率值/最大收率值×0.4+最小吸湿率值/吸湿率值×0.1。采用综合评分法进行方差分析。因素水平、正交试验安排及结果见表 10,方差分析见表 11。
| 表 10 生地黄低聚糖微粉喷雾干燥工艺优选正交试验安排及结果 Table 10 Spray drying orthogonal experimental optimization design and results of Rehmanniae Radix oligosaccharide micro powders |
| 表 11 方差分析 Table 11 Variance analysis |
由表 10可知,各因素对微粉制备工艺的影响顺序为A>B>C。方差分析表明,进风口温度、喷雾干燥效率和药液质量分数对试验结果均无显著性影响。结合预试验的结果以及制备速度和效率,确定最佳制备工艺为A2B2C3。
2.4 验证试验分别取3批处方比例的药物和辅料每份总计15 g按最佳制备工艺制备微粉,分别测定平均粒径、收率和吸湿率,对预测结果进行验证。由表 12可知最佳制备工艺得到的各指标的RSD值均小于2%,说明最佳制备工艺制备效率高,耗时短,稳定可行。
综合上述实验结果,最终确定的生地黄低聚糖微粉的制备工艺为采用纳米喷雾干燥技术,设置进风口温度为110 ℃,喷雾干燥效率为50%,泵为Pump1,使用5.5 μm喷头,气体体积流量为130 L/min,药液质量分数为1.0%。辅料采用甘露醇和L-亮氨酸(比例为7∶3),生地黄低聚糖与辅料比例为3∶7,载药量为30%。制备时称取相应比例的生地黄低聚糖、甘露醇和L-亮氨酸,加入一定量的纯水,使用磁力搅拌器搅拌使其充分溶解,然后用0.45 μm微孔滤膜滤过,将得到的溶液进行纳米喷雾干燥后,最终得到生地黄低聚糖微粉。
| 表 12 验证试验结果 (n = 3) Table 12 Results of verification test (n = 3) |
取少量纳米喷雾干燥得到的生地黄低聚糖微粉样品和喷雾干燥前的生地黄低聚糖样品进行真空离子喷金后放入扫描电镜中进行成像观察,得到扫描电镜图分别见图 1-A、B。通过电镜图片观察发现,喷雾干燥前生地黄低聚糖处于无定形的块状结构,大小不一,而纳米喷雾干燥之后呈圆球形,形态稳定,表面较光滑,利于粉体的分散,但圆球大小不一。其中喷雾干燥前的生地黄低聚糖和微粉粒径分布范围分别为0.52~11.2μm和18.9~389 μm。
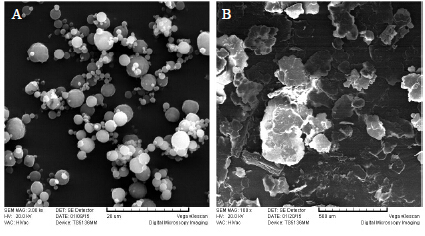 | 图 1 生地黄低聚糖纳米喷雾干燥微粉 (A) 和喷雾干燥前 (B) 电镜扫描图 Fig.1 Scanningelectron micrographs of RGOS micro powders (A) and RGOS (B) |
采用赛多利斯MA35快速红外水分测定仪测定微粉的含水量。将约2 g左右的样品放入铝箔纸上,置于水分测定仪上自室温开始升温至105 ℃,进行含水量测定。同一样品测定3次,取平均值,结果为微粉含水量为3.15%,含水量合格。
2.5.3 微粉粒径的测定按“2.1.1”项下进行微粉粒径的测定,得到粒径分布曲线见图 2,可见微粉粒径分布较窄,适合肺部给药。
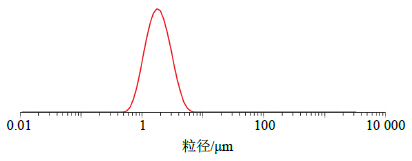 | 图 2 微粉的粒径分布图 Fig.2 Particle size distribution curve of micro powders |
微粉的密度和压缩度可以用来衡量药物制剂的流动性,密度低、压缩度高的微粉流动性好,更容易达到良好的肺部沉积[12]。采用量筒法测定微粉的堆密度和振实密度。取10 mL量筒加入微粉到5 mL量程处,记作V1,手持量筒在厚胶皮垫上敲击量筒底部将微粉振实,直至量筒中微粉体积不在变化为止,最终体积记作V2。分别称量加入微粉前后量筒的质量,两次差值为微粉质量m,微粉的堆密度(ρb)=m/V1,振实密度(ρtap)=m/V2,压缩度(C)=(ρtap-ρb)/ ρtap[11]。结果微粉的ρb为0.137g/cm3,ρtap为0.213 g/cm3,压缩度为42%。
2.5.5 微粉的吸湿性按照“2.1.3”项下的方法,分别于0、1、3、6、9、12、24、48、72、96 h称量微粉,平行3份,取平均值,吸湿率=(吸湿后样品质量-吸湿前样品质量)/吸湿前样品质量,以吸湿率为纵坐标,时间为横坐标,绘制吸湿率-时间曲线。图 3表明微粉的吸湿性良好。
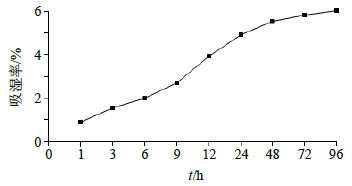 | 图 3 微粉的吸湿曲线图 Fig.3 Moisture absorption curve of micro powders |
由于生地黄低聚糖吸湿性强,接触空气后很快就变成团块,所以无法测得其ρb、ρtap和C。由表 13可知,与传统喷雾干燥制得的生地黄低聚糖微粉相比,纳米喷雾干燥制得的生地黄低聚糖微粉载药量提高到了30%,吸湿性得到了改善,收率也由79%提高到了89%,ρb和ρtap降低,C提高,表明其流动性得到了提高,说明该纳米喷雾干燥制备生地黄低聚糖微粉的工艺优于传统的喷雾干燥工艺,并且制得的微粉质量良好。
| 表 13 纳米、传统喷雾干燥生地黄低聚糖微粉和喷雾干燥前生地黄低聚糖性质对比 Table 13 Comparison on oligosaccharides properties from nano and traditional spray drying micro powders and Rehmanniae Radixbeforespraydrying |
纳米喷雾干燥工艺与传统喷雾干燥原理不同,其影响参数也不同,主要有进风口温度、喷头大小、气体流速、喷雾干燥效率、泵以及药液浓度。其中进风口温度范围为80~120 ℃;喷头有4.0、5.5、7.0 μm 3个粒径大小,分别可制得不同粒径的微粉;气体流速范围为80~160 mL/min,对微粉的干燥有着不同程度的影响;喷雾干燥效率属于自变量,范围为0~100%,可进行调节,效率越高,喷雾速度越快,也对微粉的干燥程度有着一定的影响;泵共有4个,都为蠕动泵,分别为Pump 1、Pump2、Pump 3和Pump 4,每个泵的振动频率和振动速度都不同,其中Pump 1蠕动速度较快,Pump 2蠕动较快并可以反转,Pump 3蠕动慢,可以产生液滴,使制得的微粉不易干燥,Pump 4蠕动速度缓慢,这些性质都会对制备微粉产生一定的影响[11]。
本实验采用纳米喷雾干燥工艺制备生地黄低聚糖微粉,通过单因素考察初步确定了相应的工艺参数。生地黄低聚糖对温度比较敏感,良好的进风口温度较小地影响其物理化学性质,喷雾干燥效率和药液浓度对纳米喷雾干燥的制备效率、微粉的粒径和吸湿性有着显著影响。粒径大小是影响肺部沉积效果的最主要影响因素,收率影响着微粉的制备效率和生产成本,属于第2重要因素,而吸湿性决定了微粉的流动性和分散性能,因此选择进风口温度、喷雾干燥效率和药液质量分数作为正交试验的3个因素,平均粒径、收率和吸湿性作为评价指标,根据这3个指标的重要性及查阅文献采用因子分析法最终确定权重分别为0.5、0.4和0.1,并根据单因素实验考察结果确定正交试验设计的水平。分散性也是微粉评价中的重要指标,但是吸湿性决定了分散性,因此由吸湿性替代分散性对微粉进行评价。
生地黄低聚糖具有很强的吸湿性,笔者曾尝试在不加辅料的情况下对生地黄低聚糖进行纳米喷雾干燥,喷雾干燥后得到的微粉吸湿性极强,很难保存,因此需要加入大量辅料改善其吸湿性,载药量很难提高。根据文献报道笔者也尝试在喷雾干燥时加入碳酸氢铵对最佳制备工艺进行改良,结果并不理想。笔者推测生地黄低聚糖具有吸湿性是由于其本身为无定型结构,较易发生晶型的转化,当其处于圆球形时,结构稳定,吸湿性也大大改善。该微粉为圆球形,虽然大小不一,但表面较为光滑。该圆球形状大小不一可能是由于加入的辅料本身为无定型状态,喷雾干燥后会将生地黄低聚糖包裹起来,但是包裹得并不均一,最终得到大小不一的圆球。在对微粉进行吸湿率测定时,48 h已能达到测定要求,在绘制吸湿曲线时采用96 h的数据,是为了表明该微粉吸湿性良好。
本实验在制备生地黄低聚糖微粉时曾尝试采用冷冻干燥,分别不加辅料和加入不同比例的乳糖、木糖醇、山梨醇、海藻糖、甘露醇和L-亮氨酸及不同辅料的混合物,最终得到的微粉平均粒径过大,也较易吸湿,不合格。
| [1] | 韩飞,赵志冬,王跃生,等.肺部吸入制剂评价方法的研究进展[J].中国实验方剂学杂志, 2012, 18(11):303-306. |
| [2] | 凌祥,沈雁,孙春萌,等.肺部给药研究近况[J].药学研究, 2014,(12):711-714. |
| [3] | Son Y J, McConville J T. Advancements in dry powder delivery to the lung[J]. Drug Dev ind Pharm, 2008, 34(9):948-959. |
| [4] | Bosquillon C, Preat V, Vanbever R. Pulmonary delivery of growth hormone using dry powders and visualization of its local fate in rats[J]. J Controlled Release, 2004, 96(2):233-244. |
| [5] | 缪旭,刘旭,苏健芬,等.影响干粉吸入剂雾化和沉积性能的制剂因素[J].国际药学研究杂志, 2011, 38(1):42-46. |
| [6] | 唐岚.生地黄治疗慢性阻塞性肺病药学基础研究[D].上海:上海中医药大学, 2005. |
| [7] | 刘力,张炜,徐德生,等.生地低聚糖对慢性阻塞性肺疾病大鼠外周气道病理变化的影响[J].中药材, 2013, 36(10):1678-1681. |
| [8] | 刘力,唐岚,徐德生,等.生地对大鼠肺间质成纤维细胞I、III型胶原表达的作用[J].中成药, 2008, 30(2):175-178. |
| [9] | 丁礼琴.生地治疗COPD有效部位及其吸入粉雾剂的研究[D].上海:上海中医药大学, 2009. |
| [10] | 郭静,李浩莹.纳米喷雾干燥技术在药物研究中的应用进展[J].中国医药工业杂志, 2013, 44(4):399-403. |
| [11] | 姜俊峰.硫酸沙丁胺醇纳米喷雾干燥粉雾剂配方的研究[D].沈阳:辽宁师范大学, 2013. |
| [12] | 薛艳,常明,江荣高,等.低密度多孔性颗粒在干粉吸入剂中的应用[J].中国医药工业杂志, 2008, 39(12):942-945. |
 2016, Vol. 47
2016, Vol. 47


