2. 南京中医药大学药学院, 江苏 南京 210046
2. College of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210046, China
川楝子为楝科(Meliaceae)植物川楝Melia toosendan Sieb. et Zucc. 的干燥果实(又名金铃子等),冬季果实成熟时采收,为传统理气、驱虫药,主产于四川、贵州、湖南、湖北等地,入药以四川产为道地药材,所以称川楝子。《本草纲目》记载该药性味苦寒,有小毒,并有酸味;入肝、胃、小肠经。《中国药典》2010年版记载其功能主治为疏肝泄热、行气止痛、杀虫,用于肝郁化火、胸胁、脘腹胀痛、疝气疼痛、虫积腹痛;收录有川楝子和炒川楝子2个炮制品[1]。川楝子中含有多种化学成分,包括三萜类、挥发油、黄酮类、脂肪酸、酚酸类和多糖等,而三萜类为其主要的活性成分并已被大量用于机体毒理及药理研究[2, 3]。
目前对于川楝子的化学成分分析研究中多采用甲醇、醋酸乙酯、乙醇等有机溶剂作为提取溶剂,而临床用药中是以水煎为主,因此为了更为真实反应其发挥临床疗效的化学成分群的组成,对川楝子水提后化学成分的分析就显得尤为重要。现在针对川楝子的化学成分研究仍以色谱分离为主,并通过波谱分析手段鉴定其结构[4],而液相色谱质谱联用技术已广泛应用于药动学、药效物质基础、中药化学成分分析、代谢组学等研究领域[5, 6]。为进一步明确川楝子临床上发挥抗炎、抗肿瘤等药理作用的有效成分,本实验运用UPLC-ESI-Q-TOF-MS技术对川楝子水提取物进行了分析,鉴定出了川楝子水提取物中的15个化合物,为进一步阐释其药效物质基础提供了依据。
1 仪器与试药Waters SYNAPT G2-S Q-TOF质谱仪(美国Waters公司);Waters ACQUITY UPLCTM液相色谱仪(配有在线脱气机、柱温箱、高性能自动进样器和二极管阵列检测器);Empower 3.0工作站(美国Waters公司);MassLynxV4.1分析软件;Milli-Q型纯水器(美国Millipore公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);AT201型百万分之一电子天平(瑞士Mettler公司);乙腈、甲醇(色谱纯,德国Merck公司);甲酸(色谱纯,美国Sigma公司)。
川楝素对照品(自制,经面积归一化法计算质量分数大于98%);芦丁对照品(中国药品生物制品检定所,批号10008-200306,质量分数为91.70%);川楝子生品(批号20120901,产地四川),经江苏省中医药研究院钱士辉研究员鉴定为楝科植物川楝Melia toosendan Sieb. et Zucc. 的干燥成熟果实。
2 方法 2.1 液相检测条件ACQUITY HSS T3色谱柱(100 mm×2.1 mm,1.8 μm);流动相为乙腈(A)-0.1%甲酸(B);梯度洗脱0~1 min,2% A;1~10 min,2%~95% A;10~11 min,95% A;11~12 min,95%~2% A;12~13 min,2% A;柱温35 ℃;体积流量0.4 mL/min;进样量10 μL。
2.2 质谱检测条件电喷雾离子源(ESI),正、负离子模式,多反应监测(MRM);碰撞电压(collision,CE)为20~40 V;毛细管电压(capillary voltage)2 500 V;锥孔电压(sampling cone)40 V;去溶剂温度(TEM)为450 ℃;使用高纯N2作为辅助喷雾电离与去溶剂气体,去溶剂气体积流量为800 L/h;锥孔气流(cone gas flow)为50 L/h;TOF MASSES(DA):Min=100.000 0,Max=1 200.000。
2.3 样品溶液的制备称取2.0 g川楝子生品粉末(约40目),加入100 mL水,煎煮3次,每次1.0 h;滤过,合并滤液,合并后水提液体积为240 mL;精密吸取上述提取液(未浓缩)10.00 mL蒸干、冷却,加甲醇超声溶解转移至5 mL量瓶中,定容至刻度,摇匀,过0.22 μm微孔滤膜,取续滤液,即得。
2.4 对照品溶液的制备取川楝素、芦丁对照品适量,精密称定,加甲醇超声溶解、定容,制成质量浓度分别为6.28和6.00 μg/mL的对照品溶液,于4 ℃冰箱中避光保存,备用。
3 结果 3.1 UPLC-ESI-Q-TOF-MS成分鉴定用UPLC-ESI-Q-TOF-MS对川楝子水提化学成分进行定性分析,(−) ESI-MS和 (+) ESI-MS的质谱总离子流图(TIC)见图 1。
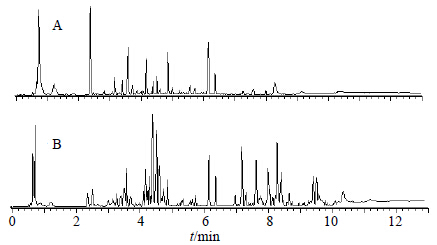 | 图 1川楝子水提取物负离子 (A) 和正离子 (B) 模式的总离子流图 Fig.1 Total ion current chromatogram in negative (A) and positive (B) ion modes for water extract of Toosendan Fructus |
通过UPLC-ESI-Q-TOF-MS检测得到川楝子水提物中各化学成分的保留时间、质谱信息,并结合提取离子流图及与对照品、相关文献数据对比进行化学成分确认,结果见表 1。
| 表 1川楝子水提物化学成分分析 Table 1Analysis on chemical constituents from water extract of Toosendan Fructus |
tR为2.84 min负离子模式下准分子离子峰为m/z 167 [M-H]−,脱去甲基后形成特征碎片m/z 152 [M-H-CH3]−,再脱去羧基形成m/z 108 [M-H-CH3-COO]−等碎片离子峰,见图 2。根据元素组成分析,该化合物分子式为C8H8O4,相对分子质量理论值为167.035 0,实测值为167.033 7,据文献报道[7]川楝子中存在香草酸,其相对分子质量168,据此推测该化合物可能为香草酸。
3.3.2 丁香酸tR为2.99 min负离子模式下准分子离子峰为m/z 197 [M-H]−,脱去甲基后形成特征碎片m/z 182 [M-H-CH3]−,再脱去1分子H2O形成m/z 164 [M-H-CH3-H2O]−;或者脱去1分子H2O形成m/z 179 [M-H-H2O]−,脱去2分子H2O形成m/z 161 [M-H-2H2O]− 等碎片离子峰,见图 3。根据元素组成分析,该化合物分子式为C9H10O5,相对分子质量理论值为197.045 5,实测值为197.044 9,据文献报道[8]川楝子中存在丁香酸,其相对分子质量198,据此推测该化合物为丁香酸。
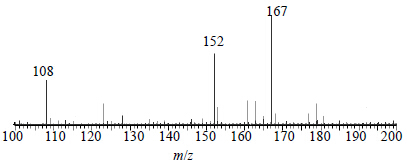 | 图 2tR 2.84 min的MS2图 (ESI−) Fig.2 MS2 spectra (ESI−) of tR at 2.84 min |
tR为3.50 min负离子模式下准分子离子峰为m/z 137 [M-H]−,脱去羟基后形成m/z 120 [M-H-OH]− 等碎片离子峰,见图 4。根据元素组成分析,该化合物分子式为C7H6O3,相对分子质量理论值为137.024 4,实测值为137.022 9,据文献报道[8]川楝子中存在对羟基苯甲酸,其相对分子质量138,据此推测该化合物可能为对羟基苯甲酸。
 | 图 3tR 2.99 min的MS2图 (ESI−) Fig.3 MS2 spectra (ESI−) of tR at 2.99 min |
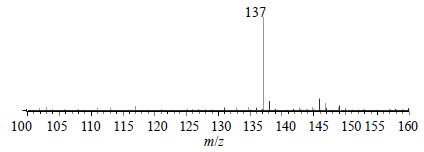 | 图 4tR 3.50 min的MS2图 (ESI−) Fig.4 MS2 spectra (ESI−) of tR at 3.50 min |
tR为4.06 min负离子模式下准分子离子峰为m/z 609 [M-H]−,脱去-Rha-Glc后形成m/z 300 [M-H-Rha-Glc]−等碎片离子峰,见图 5。根据元素组成分析,该化合物分子式为C27H30O16,相对分子质量理论值为609.146 1,实测值为609.146 5,据文献报道[8]川楝子中存在芦丁,其相对分子质量610,据此推测该化合物可能为芦丁。
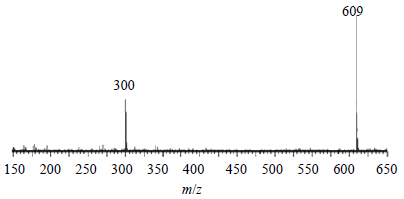 | 图 5tR 4.06 min 的MS2图 (ESI−) Fig.5 MS2 spectra (ESI−) of tR at 4.06 min |
tR为5.41 min正离子模式下准分子离子峰为m/z 553 [M+Na]+,脱去1个亚甲基后形成m/z 539 [M+Na-CH2]+等碎片离子峰,见图 6。根据元素组成分析,该化合物分子式为C28H34O10,相对分子质量理论值为553.205 0,实测值为553.207 0,据文献报道[9]川楝子中存在meliatoosenin E,其相对分子质量530,据此推测该化合物可能为meliatoosenin E。
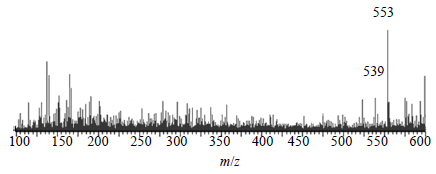 | 图 6tR 5.41 min 的MS2图 (ESI+) Fig.6 MS2 spectra (ESI+) of tR at 5.41 min |
tR为5.71 min正离子模式下准分子离子峰为m/z 515 [M+H]+,脱去1分子H2O后形成m/z 497 [M+H-H2O]+ 等碎片离子峰,见图 7。根据元素组成分析,该化合物分子式为C28H34O9,相对分子质量理论值为515.227 6,实测值为515.230 2,据文献报道[10]川楝子中存在Δ5,6-异川楝素,相对分子质量为514,据此推测该化合物可能为Δ5,6-异川楝素。
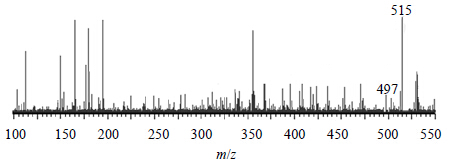 | 图 7tR 5.71 min的MS2图 (ESI+) Fig.7 MS2 spectra (ESI+) of tR at 5.71 min |
tR为6.15和6.36 min负离子模式下得到准分子离子峰为m/z 573 [M-H]−,而再脱去-OH-CH3得到m/z 531 [M-H-OH-CH3]− 等碎片离子峰,见图 8;而在正离子模式下得到准分子离子峰为m/z 597 [M+Na]+。据文献报道川楝子中存在川楝素,相对分子质量为574,且存在互变异构体异川楝素[10]。根据元素组成分析,该化合物分子式为C30H38O11,相对分子质量理论值为573.234 1,实测值为573.233 6,并与对照品中的2个色谱峰保留时间和质谱图相一致,据此推测这2个化合物可能为川楝素和异川楝素。
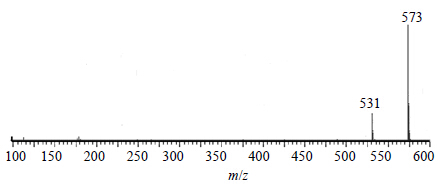 | 图 8tR 6.15 min和6.36 min的MS2图 (ESI−) Fig.8MS2 spectra (ESI−) of tR at 6.16 and 6.36 min |
tR为7.06 min正离子模式下准分子离子峰为m/z 663 [M+Na]+,再脱去-COCH3和CH3后形成m/z 605 [M+Na-C2H3O-CH3]+ 等碎片离子峰,见图 9;根据元素组成分析,该化合物分子式为C36H48O10,相对分子质量理论值为663.314 5,实测值为663.316 1,据文献报道[11]川楝子中存在meliatoosenin N,其相对分子质量为640,据此推测该化合物可能为meliatoosenin N。
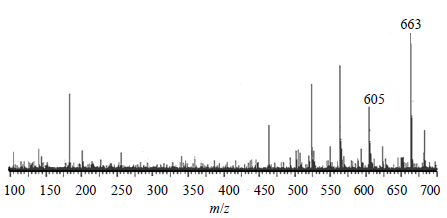 | 图 9tR 7.06 min 的MS2图 (ESI+) Fig.9 MS2 spectra (ESI+) of tR at 7.06 min |
tR为7.62 min正离子模式下准分子离子峰为m/z 547 [M+Na]+,见图 10;根据元素组成分析,该化合物分子式为C31H40O7,相对分子质量理论值为547.267 2,实测值为547.269 0,据文献报道[11]川楝子中存在meliatoosenin P,其相对分子质量524,据此推测该化合物可能为meliatoosenin P。
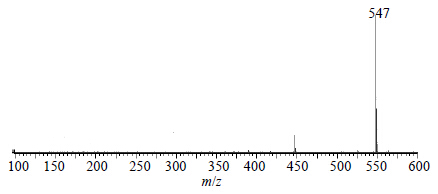 | 图 10tR 7.62 min的MS2图 (ESI+) Fig.10 MS2 spectra (ESI+) of tR at 7.62 min |
tR为8.00 min正离子模式下准分子离子峰为m/z 607 [M+Na]+,再脱去1分子后形成H2O后形成m/z 589 [M+Na-H2O]+ 等碎片离子峰,见图 11;根据元素组成分析,该化合物分子式为C33H44O9,相对分子质量理论值为607.288 3,实测值为607.290 8,据文献报道[11]川楝子中存在着1-deacetylnimbolinin B,其相对分子质量为584,据此推测该化合物可能为1-deacetylnimbolinin B。
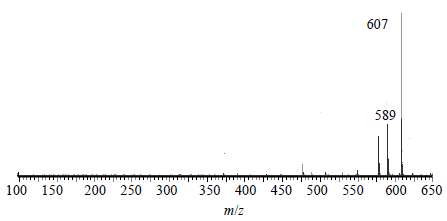 | 图 11tR 8.00 min的MS2图 (ESI+) Fig.11 MS2 spectra (ESI+) of tR at 8.00 min |
tR为8.04 min正离子模式下准分子离子峰为m/z 605 [M+Na]+,见图 12;根据元素组成分析,该化合物分子式为C33H42O9,相对分子质量理论值为605.272 7,实测值为605.273 7,据文献报道[11]川楝子中存在meliatoosenin R其相对分子质量为582,据此推测该化合物可能为meliatoosenin R。
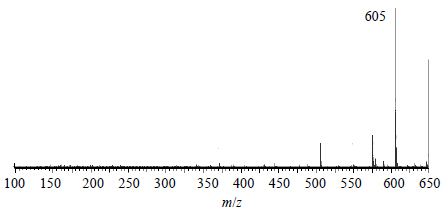 | 图 12tR 8.04 min的MS2图 (ESI+) Fig.12 MS2 spectra (ESI+) of tR at 8.04 min |
tR为8.28 min正离子模式下准分子离子峰为m/z 589 [M+Na]+,并存在m/z 567 [M+H]+,再脱去1分子C3H7OH后形成m/z 529 [M+Na-C3H7OH]+ 等碎片离子峰,见图 13;根据元素组成分析,该化合物分子式为C33H42O8,相对分子质量理论值为589.277 7,实测值为589.280 0;据文献报道[12]川楝子中存在着化合物1-O-tigloyl-1-O-debenzoylohchinal,其相对分子质量为566,据此推测该化合物可能为柠檬苦素类化合物1-O-tigloyl-1-O-debenzoylohchinal。
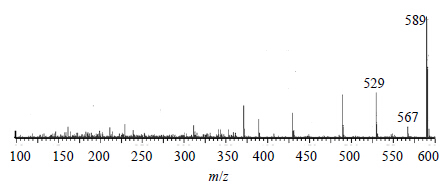 | 图 13tR 8.28 min的MS2图 (ESI+) Fig.13 MS2 spectra (ESI+) of tR at 8.28 min |
tR为8.53 min正离子模式下准分子离子峰为m/z 591 [M+Na]+,见图 14;根据元素组成分析,该化合物分子式为C33H44O8,相对分子质量理论值为591.293 4,实测值为591.295 0,据文献报道[13]川楝子中存在meliatoosenin K,其相对分子质量为568,据此推测该化合物可能为meliatoosenin K。
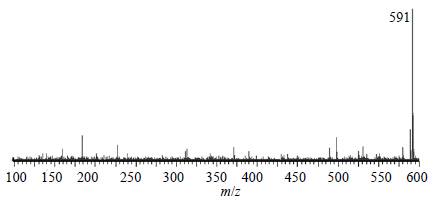 | 图 14tR 8.53 min的MS2图 (ESI+) Fig.14 MS2 spectra (ESI+) of tR at 8.53 min |
tR为9.95 min正离子模式下准分子离子峰为m/z 649 [M+Na]+,再脱去1分子CO2后形成m/z 605 [M+Na-CO2]+ 等碎片离子峰,见图 15;根据元素组成分析,该化合物分子式为C35H46O10,相对分子质量理论值为649.452 7,实测值为649.452 1,据文献报道[13]川楝子中存在nimbolinin B,其相对分子质量为626,据此推测该化合物可能为nimbolinin B。
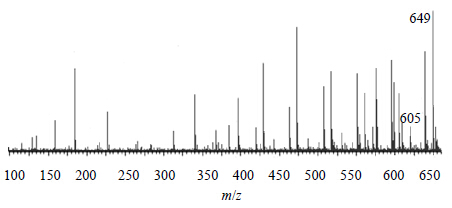 | 图 15tR 9.95 min的MS2图 (ESI+) Fig.15 MS2 spectra (ESI+) of tR at 9.95 min |
本实验运用UPLC-ESI-Q-TOF-MS联用的技术,通过获得色谱峰的准分子离子峰,对川楝子水提物进行了化学成分定性分析,并找出其水提物中可能含有的化学成分。实验中,将在正负离子模式检测到的化学成分,根据各个色谱峰在质谱中的精确相对分子质量、碎片信息、质谱裂解规律和色谱保留规律,并结合标准品的质谱信息和参考文献,最后确定了15个化合物。这15个化合物分别为香草酸、丁香酸、对羟基苯甲酸、芦丁、meliatoosenin E、川楝素、Δ5,6-异川楝素、异川楝素、meliatoosenin N、meliatoosenin P、1-deacetylnimbolinin B、meliatoosenin R、1-O-tigloyl-1-O-debenzoylohchinal、meliatoosenin R及nimbolinin B。
实验中分别考察了甲醇超声和水煎煮回流2种提取方式,结果表明,甲醇超声提取物鉴定出的化合物与文献报道的基本一致[14];而水提取物鉴定出结构的15个化合物中8个为柠檬苦素类化合物,均首次从水提物中得到。除此之外,还含3个有机酸(香草酸、丁香酸、对羟基苯甲酸),1个黄酮类化合物(芦丁),3个楝烷型三萜(川楝素、Δ5,6-异川楝素、异川楝素)。从川楝子总离子流图可以看出,色谱峰主要集中在正离子模式下,并且还有一些响应较好的色谱峰,其质谱信息未能在已有数据库中找到,表明川楝子中还有未知成分需要进一步的研究。
本实验利用UPLC-ESI-Q-TOF-MS联用技术对川楝子水提后的化学成分予以分析,为控制川楝子药材饮片质量、稳定其临床疗效及阐释其作用机制提供了科学依据;并且提示该方法也同样可用于中药复方的多成分分析,进而为中药复方的物质基础研究提供一种简单快捷、有效可靠的分析方法。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 齐双岩, 金若敏, 梅彩霞, 等. 川楝子对大鼠肝细胞色素P450诱导作用的研究 [J]. 中药药理与临床, 2011, 27(3): 62-64. |
| [3] | 时 等, 刘妍如, 杨建云, 等. 中药川楝子的最新研究进展 [J]. 中国临床药理学与治疗学, 2012, 17(3): 357-360. |
| [4] | 周 英, 王慧娟, 郭东贵, 等. 川楝子化学成分的研究 (I) [J]. 中草药, 2010, 41(9): 1421-1423. |
| [5] | 朱黎霞, 张英丰. 血液微透析法结合液质联用的丹参水煎液清醒动物多次给药药动学研究 [J]. 中草药, 2014, 45(15): 2206-2209. |
| [6] | 孟月华, 黄何松, 余黄鹏, 等. 液质联用技术鉴定预知子提取物中的主要化学成分 [J]. 中草药, 2013, 44(12): 1562-1567. |
| [7] | 陈 敏, 胡 芳, 李 丰, 等. 川楝子化学成分研究 (Ⅲ) [J]. 中药材, 2011, 34(12): 1879-1881. |
| [8] | 谢 帆, 张 勉, 张朝凤, 等. 川楝子的化学成分研究 [J]. 中国药学杂志, 2008, 43(14): 1066-1069. |
| [9] | Zhang Y, Tang C P, Ke C Q, et al. Limonoids from the fruits of Melia toosendan [J]. Phytochemistry, 2012, 73(1): 106-115. |
| [10] | 陈 琳, 穆淑珍, 晏 晨, 等. 川楝子中的化学成分研究 [J]. 中国实验方剂学杂志, 2013, 19(18): 90-95. |
| [11] | Su S, Shen L Q, Zhang Y, et al. Characterization of tautomeric limonoids from the fruits of Melia toosendan [J]. Phytochem Lett, 2013, 6(3): 418-425. |
| [12] | Xie F, Zhang M, Zhang C F, et al. Anti-inflammatory and analgesic activities of ethanolic extract and two limonoids from Melia toosendan fruit [J]. J Ethnopharmacol, 2008, 117(3): 463-472. |
| [13] | Dong S H, Zhang C R, He X F, et al. Mesedanins A-J, limonoids from the leaves and twigs of Melia toosendan [J]. J Nat Prod, 2010, 73(3): 1344-1353. |
| [14] | 聂 映, 李志裕, 姚卫峰. 基于液相色谱飞行时间质谱的炒川楝子化学成分分析 [J]. 安徽医药, 2013, 17(6): 943-945. |
 2015, Vol. 46
2015, Vol. 46


