玳玳Citrus aurantium L. var daidai Tanaka属于芸香科柑橘亚属植物,为药食同源药材,主产于福建闽北地区,福州闽侯,同安、永春等地均有栽培。《饮片新参》记载,玳玳具有破气消积、行滞化痰的功效[1]。课题组前期研究表明,玳玳果总黄酮提取物具有调血脂、清除自由基、抗氧化作用[2];为提高玳玳果总黄酮提取物的胃肠道透膜吸收,改善口服生物利用度,减少药效成分氧化,选择基于固体分散技术的原理制备玳玳黄酮滴丸剂(Daidai Flavones Dropping Pills,DFDP)[3, 4, 5, 6]。玳玳黄酮滴丸由中药有效部位玳玳果总黄酮提取物与基质PEG 6000制备而成,具有药效成分为多组分群的特点。本实验基于特征图谱具备整体性表征中药组分群的优势,采用HPLC法测定特征活性成分并结合特征图谱研究玳玳黄酮滴丸药效组分群在4种不同pH值溶出介质(pH 1.2的盐酸溶液、pH 4.5的醋酸-醋酸钠缓冲液、pH 6.8的磷酸盐缓冲液和蒸馏水)中的体外溶出行为,采用相似因子(f2)法[7, 8]对结果进行评价,更客观地评价其药效组分群的溶出及同步释药情况,探讨其溶出机制,为以中药有效部位制备的中药制剂建立针对药效组分群整体溶出及同步释药的质量评价提供可借鉴的方法。
1 仪器与材料美国Waters 2695高效液相色谱仪,美国Waters 2996光电二极管阵列检测器,Empower 3(2998)色谱工作站;XS 205十万分之一电子天平,梅特勒-托利多仪器上海有限公司;ZRS-8G智能溶出试验仪,天津大学无线电厂。
玳玳果,福建恒馨天然香料有限公司提供,经福建中医药大学药学院中药鉴定教研室范世明高级实验师鉴定为芸香科柑橘属植物玳玳Citrus aurantium L. var daidai Tanaka的干燥成熟果实;玳玳果总黄酮提取物,自制,总黄酮质量分数76.27%;玳玳黄酮滴丸,自制,批号20130808、20130810、20130812;对照品新橙皮苷(批号111857-201001,质量分数≥98%)、柚皮苷(批号110722-201111,质量分数≥98%),购于中国食品药品检定研究院;甲醇、乙腈均为色谱纯;冰醋酸为分析纯;水为重蒸馏水。
2 方法与结果 2.1 混合对照品溶液的制备分别取柚皮苷、新橙皮苷对照品适量,精密称定,加甲醇溶解并稀释为质量浓度61.5 μg/mL的柚皮苷对照品溶液及质量浓度75.1 μg/mL的新橙皮苷对照品溶液,即得。
2.2 供试品溶液的制备及测定取干燥至恒定质量的玳玳黄酮滴丸20粒,研细,精密称取玳玳黄酮滴丸粉末约100 mg,置25 mL量瓶中,加蒸馏水适量溶解并稀释至刻度,摇匀,即得。
分别精密量取混合对照品溶液、供试品溶液20 μL,注入高效液相色谱仪,按“2.6”项下色谱条件测定。
2.3 阴性对照品溶液的制备取缺玳玳果总黄酮提取物的空白处方滴丸,按玳玳黄酮滴丸制备工艺制备及“2.2”项下同法操作,即得。
2.4 样品溶出液的制备按照《中国药典》2010年版附录XC溶出度测定法第一法,取900 mL蒸馏水为溶出介质,转速为50 r/min,温度(37±0.5)℃。分别在5、10、15、20、30、60 min时,精密吸取5 mL溶出液,同时补加等体积等温溶出介质,立即用0.45 μm的微孔滤膜滤过,即得样品溶出液。取样至滤过在30 s内完成。
2.5 特征图谱相似度数据处理方法采用国家药典委员会出版的“中药色谱指纹图谱相似度评价系统”软件(2004 A版),中位数法,时间窗宽度为0.5 min生成对照图谱,以新橙皮苷色谱峰(S)为特征图谱的参照峰,评价特征图谱的相似度。
2.6 色谱条件与系统适用性试验色谱柱为Lichrocart C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-乙腈-0.2%冰醋酸水溶液,梯度洗脱;体积流量1.0 mL/min;检测波长284 nm;柱温25 ℃;进样量20 μL。梯度洗脱程序见表 1。色谱图见图 1。
| 表 1 梯度程序 Table 1 Gradient elution program |
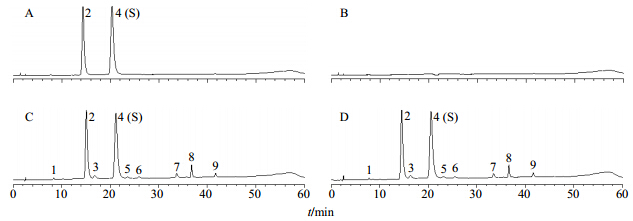 | 2-柚皮苷 4-新橙皮苷 2-naringin 4-neohesperidin图 1 混合对照品 (A)、阴性对照 (B)、玳玳黄酮滴丸 (C) 和玳玳果总黄酮提取物 (D) 的HPLC特征图谱Fig. 1 HPLC characteristics of mixed reference substances (A),blank sample (B),DFDP (C),and flavones extracts of C. aurantium var daidai (D) |
分别精密吸取混合对照品溶液、供试品溶液和阴性对照溶液各20 μL,注入液相色谱仪,记录60 min色谱图。比较玳玳果总黄酮提取物及玳玳黄酮滴丸特征色谱图保留时间和在线紫外光谱图,确定特征色谱图中的色谱峰归属,9个共有峰分别为峰1(8.332 min)、2(15.078 min)、3(16.846 min)、4(S,21.177 min)、5(23.658 min)、6(25.957 min)、7(33.713 min)、8(36.763 min)、9(41.731 min),选择其中峰面积值最大且响应稳定的4号色谱峰新橙皮苷为参照峰(S)。结果见图 1。
2.7.2 标准曲线的制备和线性关系的考察精密量取混合对照品溶液0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL置10 mL量瓶中,用蒸馏水稀释至刻度,摇匀。分别精密吸取20 μL注入高效液相色谱仪,记录色谱图。以峰面积为纵坐标(Y),对照品质量浓度为横坐标(X),绘制标准曲线。实验结果表明,柚皮苷在3.075~21.525 μg/mL线性关系良好,回归方程Y=32 700 X+331.86,r=0.999 9;新橙皮苷在3.755~26.285 μg/mL线性关系良好,回归方程Y=36 601 X+1 657.4,r=0.999 9。
2.7.3 精密度试验取同一供试品溶液,连续进样6次,计算各共有峰的相对保留时间(RRT)和峰面积比值(PAR)。实验结果表明,各供试品溶液色谱峰RRT的RSD≤2.00%,PAR的RSD≤4.88%,符合规定。
2.7.4 重复性试验分别取同一批样品6份(批号20130810),按“2.2”项下同法操作并测定,计算各共有峰的RRT和PAR。实验结果表明,各供试品溶液色谱峰RRT的RSD≤1.73%,PAR的RSD≤4.93%,符合规定。
2.7.5 稳定性试验取同一份供试品溶液,分别于0、2、4、6、8、10 h测定,计算各共有峰的RRT和PAR。实验结果表明,各供试品溶液色谱峰RRT的RSD≤1.31%,PAR的RSD≤4.86%,供试品溶液10 h内稳定性良好。
2.8 溶出介质对药物溶出行为的影响选择特征活性成分新橙皮苷和柚皮苷为指标,考察溶出介质对药物溶出行为的影响。分别以pH 1.2的盐酸溶液、pH 4.5的醋酸-醋酸钠缓冲液、pH 6.8的磷酸盐缓冲液及蒸馏水为4种不同的pH值溶出介质,测定玳玳黄酮滴丸中新橙皮苷和柚皮苷在规定时间的累积溶出度,同时采用美国食品和药物管理局(FDA)推荐的f2法对实验结果进行评价[7, 8],当50≤f2<100时,可认为2种制剂的溶出曲线相似;若f2=100,视为2种制剂的溶出曲线完全吻合。实验结果表明,pH 1.2的盐酸溶液、pH 4.5的醋酸-醋酸钠缓冲液、pH 6.8的磷酸盐缓冲液及蒸馏水的f2分别为78.14、90.60、89.45、93.64;综合f2及累积溶出度的结果,以蒸馏水为溶出介质。溶出曲线绘制结果见图 2。
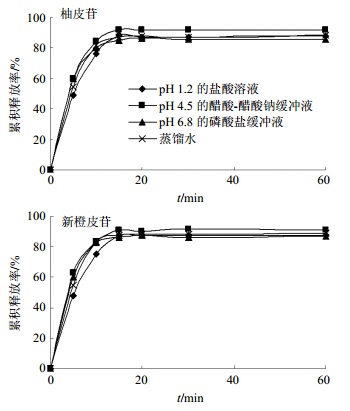 | 图 2 不同pH值溶出介质的溶出曲线Fig. 2 Dissolution curves of dissolution media with different pH values |
选择特征活性成分新橙皮苷和柚皮苷为指标,考察转速对药物溶出行为的影响。分别以50、100、150 r/min转速,蒸馏水为介质、温度为(37±0.5)℃的条件下,测定玳玳黄酮滴丸新橙皮苷和柚皮苷在规定时间的累积溶出度,并采用f2法评价。实验结果不同转速的f2分别为95.61、93.64、92.41,表明玳玳黄酮滴丸的溶出行为不受转速影响,在体内受胃肠蠕动影响较小,考虑用药人群及模拟体内的差异,故选择转速50 r/min。溶出曲线见图 3。
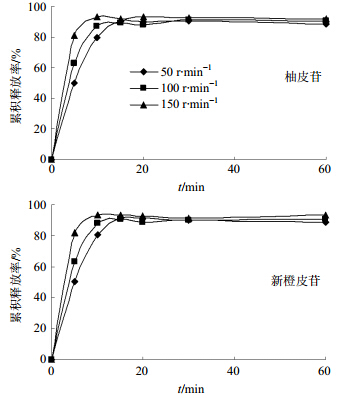 | 图 3 不同转速的溶出曲线Fig. 3 Dissolution curves of different rotational speeds |
分别取3批玳玳黄酮滴丸(批号20130808、20130810、20130812)按“2.4”项下同法操作制备样品溶出液,并在“2.6”项色谱条件下测定不同时间点的样品溶出液,同时记录特征图谱,依据“2.5”项下特征图谱相似度数据处理方法,计算3批玳玳黄酮滴丸在相同时间溶出液的特征图谱相似度。实验结果表明,3批玳玳黄酮滴丸的特征图谱相似度为1.000,基本实现玳玳黄酮滴丸组分群同步释药。结果见图 4。
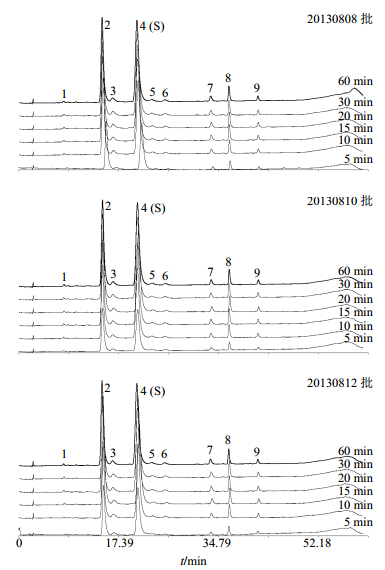 | 图 4 3批玳玳黄酮滴丸不同时间HPLC特征图谱溶出图Fig. 4 HPLC characteristic dissolution of three batches of DFDP in different times |
选取玳玳黄酮滴丸特征图谱中1~9号共有峰,记录峰面积,计算在不同时间取样的累积溶出度;根据美国FDA颁布的f2法,比较玳玳黄酮滴丸特征图谱中9个共有峰对应成分是否达到同步释药的效果。评价f2越大,表明2种制剂的体外溶出曲线差异越小;若50≤f2<100则可认为2制剂的溶出曲线相似;若f2为100,则表示2种制剂溶出度曲线完全吻合。结果表明,玳玳黄酮滴丸药效组分群9个共有峰的f2均大于50,特征药效成分柚皮苷对新橙皮苷的f2为94.86,提示该中药制剂药效部位组分群溶出曲线相似,基本实现了同步释放。结果见图 5及表 2。
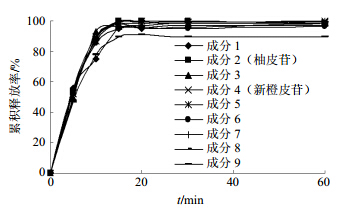 | 图 5 组分群各共有成分不同时间的溶出曲线Fig. 5 Dissolution curves of common composition in group clustering in different times |
| 表 2 特征图谱中9个共有峰成分的f2评价结果 Table 2 f2 Evaluation of nine common peak ingredients in characteristic spectrum |
采用单指数模型方程、威布尔模型方程及对数分布模型方程对玳玳黄酮滴丸共有峰各组分群成分的累积释放率进行拟合。结果表明,9个共有峰成分按各方程拟合得R2>0.800 0,其中威布尔模型方程的R2>0.980 0,特征活性成分新橙皮苷和柚皮苷的R2分别为0.999 7和0.998 7,因此,玳玳黄酮滴丸组分群整体溶出机制均较符合威布尔模型方程。结果见表 3。
| 表 3 玳玳黄酮滴丸不同成分体外溶出模型的拟合结果 Table 3 Dissolution model fitting of different ingredients in DFDP |
采用4种不同pH值介质模拟人体胃肠道不同积释放率,阐明中药制剂的体内溶出行为,进行质量控制。玳玳黄酮滴丸是以中药有效部位制备的中药制剂,具有中药多组分群作用的特点,为更全面生理环境,通过计算不同时间点特征药效成分的累地评价中药药效组分群的溶出及释药行为,本实验建立的HPLC法,结合中药特征图谱法与传统的特征成分测定法,评价玳玳黄酮滴丸溶出度,综合表征中药有效部位组分群的整体性特点,以点带面整体评价其中多组分的溶出及释药特性,提高中药制剂的内在质量评价,为中药制剂整体成分起效作用评价提供可借鉴的实验及理论依据。
建立特征图谱经色谱条件优化,曾分别比较了不同色谱柱,确定采用Lichrocart C18色谱柱结果较稳定;比较不同比例的流动相,如乙腈-0.1%磷酸水溶液、甲醇-乙腈-0.1%磷酸水溶液、甲醇-乙腈-0.2%冰醋酸水溶液等,结果甲醇-乙腈-0.2%冰醋酸水溶液梯度洗脱各色谱峰达到完全分离、基线平稳、峰形稳定,故选择甲醇-乙腈-0.2%冰醋酸水溶液梯度洗脱为流动相。
分别考察玳玳黄酮滴丸溶出行为的影响因素,提示玳玳黄酮滴丸溶出行为受转速影响较小,适合各年龄段的人群口服;4种不同pH值溶出介质对玳玳黄酮滴丸中不同成分的累积释放率综合f2及累积溶出度影响较小;玳玳黄酮滴丸中不同成分的累积溶出度在15 min时均达到85%以上,表明玳玳黄酮滴丸是一种非pH依赖型的速效中药滴丸剂。
溶出曲线相似性评价中最经典和最广泛被采用的方法,包含f2法和威布尔模型方程[9]。基于HPLC特征图谱的玳玳黄酮滴丸9个共有峰代表的药效成分组分群累积释放率曲线拟合结果,均符合威布尔模型方程溶出机制,且R2系数相近;运用f2法评价,玳玳黄酮滴丸中各药效成分溶出曲线的f2均大于50,提示玳玳黄酮滴丸药效部位组分群溶出曲线相似及同步释药的整体性作用机制。
| [1] | 新 安, 王一仁. 《饮片新参》 [M]. 上海: 上海千顷堂书局出版社, 1936. |
| [2] | 刘永静, 陈 丹, 邱洪鑫, 等. 玳玳黄酮有效部位提取物降血脂作用的研究 [J]. 中国中医药科技, 2013, 20(6): 622-623. |
| [3] | 邱洪鑫, 陈 丹, 刘永静, 等. 玳玳果黄酮滴丸对高脂血症大鼠的降血脂作用研究 [J]. 中国现代应用药学, 2011, 28(7): 597-601. |
| [4] | 刘永静, 陈 丹, 黄庆德, 等. 玳玳果中总黄酮提取工艺的研究 [J]. 中国医院药学杂志, 2009, 29(21): 1826-1828. |
| [5] | 陈 丹, 刘永静. 一种玳玳果总黄酮有效部位的制备方法: 中国, CN201010556341.9 [P]. 2011-05-18. |
| [6] | 邱洪鑫, 陈 丹, 刘永静, 等. 玳玳果滴丸的制备工艺优选 [J]. 中国医院药学杂志, 2011, 31(5): 357-361. |
| [7] | 戴 领, 申宝德, 吕青远, 等. 基于生物效价-多成分整合的中药固体制剂体外溶出度研究 [J]. 中草药, 2013, 44(19): 2666-2671. |
| [8] | 赵 燕, 李秋芬, 张忠亮, 等. 参芪麝蓉丸质量评价 [J]. 中草药, 2014, 45(7): 942-948. |
| [9] | 牛剑钊, 林 兰, 张启明. 美国和日本溶出曲线相似性判定方法介绍 [J]. 中国药物评价, 2013, 30(2): 67-69. |
 2015, Vol. 46
2015, Vol. 46


