2. 天津丹溪国药研究所, 天津 300061;
3. 天津市市场和质量监督管理委员会, 天津 300070
2. Tianjin Danxi Traditional Chinese Medicine Institute, Tianjin 300061, China;
3. Tianjin Market and quality supervision and Management Committee, Tianjin 300070, China
中药配方颗粒是以符合炮制规范的中药饮片为原料,经现代工艺提取、浓缩、干燥、制粒而成的系列产品,作为中药饮片在中医临床使用的一种补充形式,目前尚处于科研试点阶段,是中药传统汤剂的一个重大突破,具有计量准确、便于调配、服用方便、安全卫生等优点[1]。
目前中药配方颗粒的制备工艺对大多数中药而言,较传统汤剂有效成分提取更充分、药材利用率更高。但对一些含挥发性成分的中药,常规工艺挥发性成分容易损失,而这些损失的挥发性成分正是有效成分,故影响其疗效。在《中国药典》2010年版收载的500多种药材中[2],有十分之一的中药含有挥发性成分,因而对这类中药的配方颗粒进行工艺研究是十分必要的。对于这类中药,现有的技术是将挥发性成分先提取出来,再在制粒过程中加入使有效成分的量得以提高,从而保证了药效。为了进一步防止挥发性成分在放置过程中的损失,可采用β-环糊精包合技术。
本实验以牡丹皮、肉桂为代表探究其配方颗粒的制备工艺。牡丹皮含有挥发性成分丹皮酚[3];肉桂含有大量的挥发油,主要成分是桂皮醛[4]。本实验通过比较不同工艺制备的牡丹皮配方颗粒中丹皮酚的量、肉桂配方颗粒中桂皮醛的量,研究挥发性成分中药配方颗粒制备工艺的合理性。
1 仪器与材料高效液相色谱仪,包括LC-10A型高效液相色谱仪、SPD-10A紫外检测器、Anastar色谱工作站;BT-25-S型电子天平,北京赛多利斯仪器系统有限公司;HS-3120型超声波清洗仪,天津市恒奥科技发展有限公司。
对照品丹皮酚(批号110708-200506,质量分数>98%)、桂皮醛(批号110710-200915,质量分数为98.8%)均购于中国食品药品检定研究院;肉桂、牡丹皮饮片均购于天津饮片厂,均由天津市药品检验所吴贵华副主任药师鉴定,肉桂为樟科樟属植物肉桂Cinnamomum cassia Presl的干燥树皮、牡丹皮为毛茛科芍药属植物牡丹Peaonia suffruticosa Andr.的干燥根皮;甲醇、乙腈为色谱纯,水为蒸馏水,其他试剂均为分析纯。
2 方法与结果 2.1 配方颗粒的制备 2.1.1 牡丹皮配方颗粒的制备(1)工艺1:取牡丹皮饮片,加10倍量水煎煮2 h,滤过,药渣再加8倍量水煎煮1.5 h,滤过,合并2次滤液,浓缩,真空干燥,制粒,即得。每1 g颗粒相当于饮片5 g。
(2)工艺2:取牡丹皮饮片,加10倍量水,浸泡4 h,水蒸汽蒸馏,在3 h内收集3倍量蒸馏液,于蒸馏液中加入5% NaCl,冰箱(冷藏,4 ℃)放置过夜(10 h),析出白色结晶,滤过,用冷水洗涤,45 ℃以下干燥,备用;药渣再加8倍量水煎煮1.5 h,滤过,合并滤液,浓缩,真空干燥,制粒,喷入丹皮酚乙醇溶液,即得。每克颗粒相当于饮片5 g。
(3)工艺3:取牡丹皮饮片,按“2.1.1(2)”项工艺制备得到丹皮酚结晶,加适量乙醇溶解,在搅拌下缓缓滴入7倍量β-环糊精溶液(取β-环糊精加20倍量水,在50~60 ℃水浴中溶解,放置室温)中,滴毕后再搅拌30 min,冰箱(冷藏,4 ℃)放置过夜(10 h),滤过,用冷水洗涤,45 ℃以下干燥,备用;药渣再加8倍量水煎煮1.5 h,滤过,合并滤液,浓缩,真空干燥,加入包合物,混匀,制粒,即得。每克颗粒相当于饮片5 g。
2.1.2 肉桂配方颗粒的制备(1)工艺1:取肉桂饮片,加8倍量水煎煮2 h,滤过,药渣再加8倍量水煎煮1.5 h,滤过,合并2次滤液,浓缩,真空干燥,制粒,即得。每克颗粒相当于饮片5 g。
(2)工艺2:取肉桂饮片,加入8倍水提油,收集挥发油;药渣再加8倍量水煎煮1.5 h,滤过,合并滤液,浓缩,真空干燥,制粒,喷入挥发油乙醇溶液,即得。每克颗粒相当于饮片5 g。
(3)工艺3:取肉桂饮片,按“2.1.2(2)”工艺得到肉桂挥发油,加适量乙醇溶解,在搅拌下缓缓滴入6倍量β-环糊精溶液(取β-环糊精加20倍量水,在50~60 ℃水浴中溶解,放置室温)中,滴毕后再搅拌30 min,冰箱(冷藏,4 ℃)放置过夜(10 h),滤过,用冷水洗涤,45 ℃以下干燥,备用;药渣再加水8倍量煎煮1.5 h,滤过,合并滤液,浓缩,真空干燥,加入包合物,混匀,制粒,即得。每克颗粒相当于饮片5 g。
2.2 定量测定方法 2.2.1 丹皮酚测定的色谱条件[5]色谱柱为Diamonsil C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-水(55∶45);柱温35 ℃;体积流量1.0 mL/min;检测波长274 nm;进样量20 μL。理论板数按丹皮酚峰计算应不低于3 000。对照品、供试品溶液色谱图见图 1。
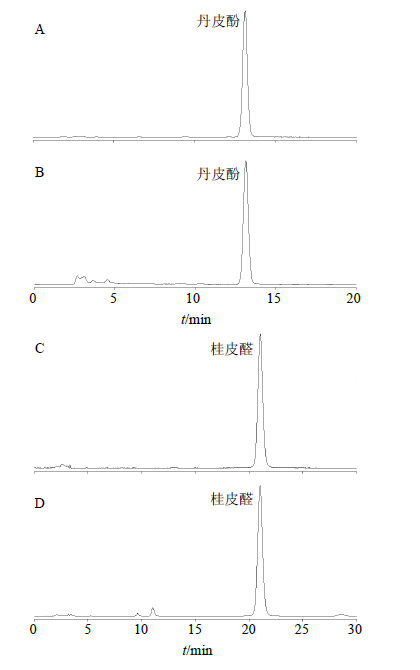 | 图 1 丹皮酚对照品 (A)、牡丹皮配方颗粒供试品溶液(B)、桂皮醛对照品 (C)、肉桂配方颗粒供试品溶液 (D) 的HPLC色谱图Fig.1 HPLC of paeonol reference substance (A), Moutan Cortex formula granule sample (B), cinnamaldehyde reference substance (C), and Cinnammi Cortex formula granule sample (D) |
色谱柱为Diamonsil C18(250 mm×4.6 mm,5 μm);流动相为乙腈-水(35∶65);柱温35 ℃;体积流量1.0 mL/min;检测波长290 nm;进样量20 μL。理论板数按桂皮醛峰计算应不低于3 000。对照品、供试品溶液色谱图见图 1。
2.2.3 对照品溶液的制备分别取丹皮酚、桂皮醛对照品适量,精密称定,加甲醇分别制成含丹皮酚168.3 μg/mL、桂皮醛129.8 μg/mL的溶液,作为储备液。再分别精密吸取3.0 mL至25 mL量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.2.4 供试品溶液的制备取牡丹皮、肉桂配方颗粒适量,研细,精密称取200 mg,置锥形瓶中,精密加入甲醇50 mL,密塞,称定质量,超声处理30 min,放凉,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密吸取续滤液1.0 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.2.5 线性关系试验取上述2种对照品储备液,分别精密吸取0.1、0.5、1.0、2.0、3.0、4.0、5.0 mL置25 mL量瓶中,以甲醇稀释至刻度,摇匀。按“2.2.1”和“2.2.2”项色谱条件分别进样,测定峰面积值。以进样量为横坐标(X),相应的峰面积值为纵坐标(Y),进行线性回归,得丹皮酚回归方程:Y=2 642 476.3 X-3 691.3,r=0.999 9;桂皮醛回归方程:Y=3 942 103.6 X-6 221.6,r=0.999 9。结果表明,丹皮酚在13.46~673.20 ng,桂皮醛在10.38~519.20 ng与峰面积值呈良好的线性关系。
2.2.6 精密度试验取质量浓度分别为丹皮酚20.196 μg/mL、桂皮醛15.576 μg/mL的对照品溶液,按“2.2.1”和“2.2.2”项色谱条件重复进样6次,测定峰面积值,其RSD值分别为0.67%和0.56%,结果表明仪器精密度良好。
2.2.7 稳定性试验分别吸取牡丹皮供试品溶液、肉桂供试品溶液,按“2.2.1”和“2.2.2”项色谱条件分别在0、1、2、4、6、8、24 h进样,测定峰面积值,RSD值分别为1.68%、1.45%。结果表明牡丹皮供试品溶液在24 h、肉桂供试品溶液在8 h内测定是稳定的。
2.2.8 重复性试验分别取牡丹皮配方颗粒、肉桂配方颗粒,按“2.2.4”项下方法操作,平行制备6份,按“2.2.1”和“2.2.2”项色谱条件测定峰面积值,计算丹皮酚平均质量分数为4.919%,RSD为1.11%;桂皮醛平均质量分数为3.846%,RSD为1.21%。
2.2.9 回收率试验精密称取已测定的配方颗粒各100 mg,分别添加丹皮酚对照品溶液(337.2 μg/mL,甲醇配制)2.0 mL、桂皮醛对照品溶液(1.321 2 mg/mL,甲醇配制)3.0 mL,按“2.2.4”项下方法操作,各平行制备6份,按“2.2.1”和“2.2.2”项色谱条件测定峰面积值,计算回收率。结果丹皮酚的平均回收率为99.50%,RSD为1.53%;桂皮醛的平均回收率为99.01%,RSD为1.41%。
2.2.10 样品的测定分别取不同工艺制备的牡丹皮、肉桂配方颗粒各3批,适量,研细,按“2.2.4”项下方法制备供试品溶液。按“2.2.1”和“2.2.2”项色谱条件测定,并计算牡丹皮、肉桂配方颗粒中丹皮酚、桂皮醛的量。结果见表 1、2。
| 表 1 牡丹皮配方颗粒中丹皮酚测定结果 Table 1Determination of paeonol in Moutan Cortex formula granule |
| 表 2 肉桂配方颗粒中桂皮醛测定结果 Table 2Determination of cinnamaldehyde in Cinnamomi Cortex formula granule |
为进一步探究含挥发性成分配方颗粒的工艺合理性,本实验选择了组方中含有牡丹皮、肉桂的桂附地黄汤为例,测定了桂附地黄汤传统饮片汤剂中丹皮酚、桂皮醛的量,对应3批结果换算成牡丹皮中含丹皮酚为3.74、5.95、4.82 mg/g;肉桂中含桂皮醛为1.93、3.00、2.36 mg/g。结果表明,常规工艺制得的配方颗粒2种成分的量远远低于传统饮片汤剂,而采用先将挥发性成分提取出来,再在制粒中加入的工艺2种成分的量均高于传统饮片汤剂,说明此工艺是合理的,按此工艺制备的配方颗粒是可以代替饮片使用的。
据文献报道[7, 8],采用β-环糊精包合丹皮酚技术,可以大大提高丹皮酚稳定性。因β-环糊精与挥发性成分的包合过程是一个物理过程,不发生化学变化,保证挥发性成分的药理作用,提高其在储存过程中的稳定性[9, 10]。因此本实验也采用先提取发性成分,再用β-环糊精包合的工艺,提高了中药配方颗粒中丹皮酚和桂皮醛的量。
| [1] | 王绍龄. 浅析中药饮片与中药配方颗粒在临床应用的优缺点[J]. 中国冶金工业医学杂志, 2012, 29(4): 477-478. |
| [2] | 中国药典 [S]. 一部. 2010. |
| [3] | 胡红宇, 杨 郁, 于能江, 等. 牡丹皮化学成分研究[J]. 中国中药杂志, 2006, 31(21): 1793-1794. |
| [4] | 袁阿兴, 覃 凌, 姜达衢. 肉桂化学成分的研究[J]. 药学通报, 1981, 16(10): 55. |
| [5] | 汪健音. 高效液相法测定六味地黄口服液中丹皮酚的含量[J]. 现代中药研究与实践, 2005, 19(5): 46-47. |
| [6] | 王 也, 裘国丽, 黄 华. 高效液相色谱法测定丁桂儿脐贴中丁香酚和桂皮醛含量[J]. 中国药业, 2011, 20(10): 43-44. |
| [7] | 张振海, 贾晓斌, 陈 彦, 等. 丹皮酚羟丙基甲基纤维素包衣颗粒的稳定性研究[J]. 中成药, 2012, 34(9): 1804-1806. |
| [8] | 董晓旭, 付 京, 尹兴斌, 等. 丹皮酚β-环糊精包合物稳定性考察[J]. 山东中医药大学学报, 2015, 39(4): 377-378. |
| [9] | 曹新志, 金征宇. 环糊精包合物的制备方法[J]. 食品工业科技, 2003, 24(10): 158-160. |
| [10] | 杨建文, 任晓亮, 戚爱棣. 环糊精及其衍生物在中药提取中的应用研究进展[J]. 药物评价研究, 2015, 38(2): 208-213. |
 2015, Vol. 46
2015, Vol. 46


