艾叶为菊科植物艾Artemisia argyi Lévl. et Vant的干燥叶,主产于湖北、安徽、山东,具有温经止血、散寒止痛、外用祛湿止痒之功效[1]。艾叶油为艾叶经水蒸气蒸馏提取出来的挥发油,具有平喘、祛痰、抗菌、抗病毒等活性[2, 3]。本实验室的前期研究表明,艾叶油能较好减轻二甲苯所致小鼠耳肿胀和角叉菜胶所致大鼠足肿胀,增加冰醋酸所致小鼠腹腔毛细血管的通透性,改善冰水浴所致大鼠急性血瘀的各项血液流变学参数。根据这些药理活性,本课题组拟开发艾叶油制剂用于防治静脉炎。
水凝胶贴膏剂是以水溶性高分子材料或亲水性物质为基质的外用贴敷剂,与传统的贴膏相比,水凝胶贴膏剂中水溶性高分子材料与皮肤有很好的亲和性,有利于皮肤角质层细胞水化膨胀,从而更有利于药物的透皮吸收[4]。根据治疗静脉炎疾病适宜经皮给药途径,本实验设计制备艾叶油乳-水凝胶贴膏剂,以初黏力、持黏力、剥离强度内聚力和渗透度作为评价手段,优化贴剂处方,并考察了其体外透皮给药特性。
1 仪器与材料JA2103N CP214电子天平,奥豪斯仪器上海有限公司;数显恒温磁力搅拌器、JJ-1精密増力电动搅拌器,金坛市科兴仪器厂;CZY-G初黏力测试仪、C2Y-S持黏性测试仪和BLD-200S电子剥离试验机,济南兰光机电技术发展中心;RYJ-6A药物透皮扩散试验仪,上海黄海药检仪器有限公司;秒表,上海晶鑫钟表有限公司;Agilent 6890N气相色谱仪、CA-1型静音无油空气泵,美国Aligent公司;CH-1高纯氢气发生器,武汉科林普丰仪器有限公司。
对照品桉油精(批号110788-201105,质量分数99.9%)、樟脑(批号110747-201008,质量分数100%)、龙脑(批号110881-201107,质量分数99.3%)购自中国食品药品检定研究院;无水乙醇、环己酮、乙二胺四乙酸二钠(EDTA)、甘油、聚山梨酯-80,国药集团化学试剂有限公司;聚乙烯吡咯烷酮K-90,阿拉丁,批号2009.08.04;聚丙烯酸钠NP-700、甘羟铝,美国国际特品公司;艾叶油,本实验室提供,批次20130509,含桉油精254.37 mg/g、樟脑51.59 mg/g、龙脑58.74 mg/g。
SPF级昆明种小鼠,雄性,18~22 g,合格证号为42000600002507,由湖北省实验动物研究中心提供。
2 方法与结果 2.1 艾叶油乳化前处理将10 g艾叶油与4 g聚山梨酯-80搅拌混匀,加入纯化水10 mL,研磨乳化制备初乳,再加入剩余水量34 mL稀释,制成艾叶油乳,备用。
采用库尔特计数器测定乳滴粒径,绘制粒径分布图,结果见图 1,所得乳滴平均粒径为(3.25±0.30)μm。
 | 图 1 艾叶油乳粒径分布Fig.1 Particle size distribution of essential oil from Artemisia Argyi Folium emulsion |
将5 g高岭土(填充剂)、1.5 g PVP-K90(增黏剂)、0.2 g酒石酸(pH调节剂)依次加入上述艾叶油乳,搅拌15 min混匀,作为乳化相。将一定量的甘羟铝(交联剂)、EDTA(交联调节剂)分散在适量甘油(保湿剂)中搅拌5 min,再加入NP-700(水凝胶骨架材料)搅拌均匀,作为甘油相。然后将乳化相缓慢加入甘油相搅拌30 min后,取4 g形成的胶体涂布于长8 cm、宽5 cm的无纺布上,贴膜,放置8 h固化[5]。
2.3 水凝胶贴膏剂的评价方法 2.3.1 外观水凝胶膏体均匀、柔软,易涂布,且剥离被衬膜时,无膜残留,被视为制备成型。
2.3.2 初黏力、持黏力、剥离强度测试[1, 6]按照《中国药典》2010年版附录XJ贴剂黏附力测定法,采用滚球斜坡停止法测定样品的初黏力,设定的评分标准为评分=10×(10-∣A-10∣),其中A表示钢球号,满分100,分数越高代表贴剂的初黏力越符合质量要求。
按照《中国药典》2010年版附录XJ贴剂黏附力测定法测定样品的持黏力,设定的评分标准为测定实验达规定时间时,供试品未脱落时样品的持黏力评分=100-5×s,其中s表示位移值,单位是cm。结果分数越高持黏力越符合贴剂质量要求,满分为100。
按照《中国药典》2010年版附录XJ贴剂黏附力测定法,采用180°剥离强度试验法测定样品的剥离强度,设定的评分标准为样品的剥离强度评分=100-∣F-100∣,其中F表示力值,单位是N。结果分数越高,剥离强度越符合贴剂质量要求,满分100。
2.3.3 内聚力和渗透度评定方法[7]将制备好的样品放置24 h,内聚力评定设为3个等级,满分为100,即当揭除贴在皮肤上的贴剂时,若膏面破坏导致基质玷污皮肤则分数在10~30,破坏程度越大分数越低;若膏面形变严重但未沾污皮肤则分数在40~70,脱离程度越大分数越低;若膏面形变较小且未沾污皮肤则分数在80~100,膏面还原性越好分数越高。
将制备好的样品放置24 h后,背衬无浸湿,渗透度即为满分100,浸湿程度越大,分数越低。分数越高,越符合贴剂要求。
2.3.4 贴膏剂评价的总分计算方法贴剂总分=(初黏力分数+持黏力分数+180°剥离强度分数)×0.7/3+(内聚力分数+渗透性分数)×0.3/2[8]。
2.4 正交试验设计优化贴膏剂处方选择影响水凝胶贴膏剂交联作用及成型性最大的4个因素即保湿剂甘油用量(A)、水凝胶贴剂骨架聚丙烯酸钠NP-700用量(B)、交联剂甘羟铝用量(C)及交联调节剂EDTA用量(D),开展正交优化实验设计,按“2.1”和“2.2”项下方法制备贴膏剂。以初黏力、持黏力、180°剥离强度、内聚力和渗透度为评价指标,按L9(34) 正交设计试验表安排试验。正交试验因素水平见表 1,表中各辅料用量以基质总量为100 g(加水至100 g)计。按各评价指标的评分方法评出正交试验的9组实验结果总分见表 1,方差分析见表 2。
| 表 1 正交试验设计与结果 Table 1Results and design of orthogonal test |
| 表 2 方差分析 Table 2Analysis of variance |
结果可知,影响因素顺序为A>C>D,此次正交实验的最佳组合为A2C2D1,其中B因素基本没有影响,在方差分析中作为误差相处理。考虑到水凝胶贴膏剂的触感软硬舒适程度,B因素选择了中间水平B2,最终选择处方最佳组合为A2B2C2D1,30%即甘油、5% NP-700、0.3%甘羟铝、0.03% EDTA。为了验证艾叶油水凝胶贴膏剂的最佳基质比,按最佳组合A2B2C2D1制备贴膏剂,重复3次,进行验证性试验。由表 3结果可知,按此处方组成制备的艾叶油水凝胶贴膏剂综合评价总分最高,膏面完整均匀,背衬干燥,初黏力、持黏力、180°剥离强度、内聚力和渗透度均符合质量标准。
| 表 3 验证结果 Table 3Results of verifying test |
选取健康的雄性昆明小鼠(18~22 g),用电动剃毛刀给其腹部脱毛,脱颈处死,立即剥离其腹部皮肤,去除干净皮下脂肪及粘连物,用生理盐水浸泡冲洗干净并检查鼠皮有无破损,将其剪成适宜的大小待用。采用改良Franz双室渗透扩散装置,将小鼠离体皮肤置于装置中间夹好固定,角质层一侧朝上面向供药室,再将裁剪好的艾叶油乳-水凝胶贴剂贴于角质层一侧鼠皮上,进行固定设定;接收室加入空白接受液(30%乙醇的生理盐水)6.5 mL,接收液与离体皮肤真皮层紧密接触不得有气泡;设置水浴温度为37 ℃,以恒速300 r/min搅拌;分别于1、2、3、4、6、8 h在接收室取样2 mL待测,并补充等体积等温的空白接受液。艾叶油水凝胶贴膏剂体外透皮性能测试,重复3次。
采用GC测定样品液中桉油精、樟脑、龙脑的量[10, 11]。色谱条件: HP-INNOWAX毛细管色谱柱(30 m×0.25 mm,0.5 μm);进样口温度250 ℃;FID检测器温度280 ℃;程序升温: 初温110 ℃(保持8 min),以25 ℃/min升至158 ℃(保持8 min),再以25 ℃/min升至230 ℃(保持9 min);载气: 氮气,体积流量0.7 mL/min(0.12 MPa);氢气体积流量40 mL/min;空气体积流量450 mL/min;分流比10∶1,进样量1 μL,内标物为环己酮。经方法学考察,空白接收液对药物测定无干扰,色谱图见图 2,各项指标均符合要求。
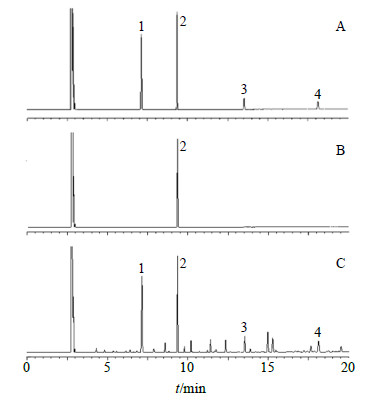 |
1-桉油精 2-环己酮 3-樟脑 4-龙脑 1-eucalyptol 2-cyclohexanone 3-camphor 4-borneol 图 2 混合对照品 (A)、阴性对照品 (B) 和艾叶油供试品 (C) 的GC图Fig.2 GC of mixed reference substances (A), negative control (B), and essential oil from Artemisia Argyi Folium sample (C) |
标准曲线的绘制: 精密称定桉油精、樟脑、龙脑对照品适量,加乙醇配制成含桉油精975.5 μg/mL、樟脑200.0 μg/mL、龙脑223.2 μg/mL的混合对照品储备液。再分别精密吸取混合对照品储备液一系列体积与内标溶液(环己酮乙醇液,1.40 mg/mL)1 mL于5 mL量瓶中,用乙醇稀释定容,摇匀即得。进样,以对照品桉油精、樟脑、龙脑的质量浓度对峰面积比值分别作标准曲线,依次得到回归方程: 桉油精Y=0.263 1 X+0.002,r=0.999 8,
线性范围为32.749~82.47 μg/mL;樟脑Y=0.246 8 X+0.000 5,r=0.999 8,线性范围为0.644~19.32 μg/mL;龙脑Y=0.237 6 X+0.000 6,r=0.999 7,线性范围为0.578~17.33 μg/mL。测量样品色谱峰面积后,根据标准曲线方程计算得到质量浓度(C),按照下式计算单位面积的药物累积透过量(Qn)。
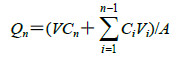
Cn和Ci分别为第n、i个取样点测得的药物浓度,V和Vi分别为接收池体积(6.5 mL)和第i次取样体积(2 mL),A为有效渗透面积(2.5 cm2)
以单位面积桉油精、樟脑、龙脑的Qn对时间(t)回归,得到桉油精、樟脑、龙脑的平均稳态透皮速率方程分别为Qn=85.216 t+6.510 5(r=0.997 6),Qn=23.775 t+3.004 9(r=0.999 6),Qn=19.401 t+1.135 6(r=0.998 0),符合零级释放过程。桉油精、樟脑、龙脑的8 h Qn为1.710、0.484、0.400 mg/cm2,稳态渗透速率分别为85.216、4.442、3.941 μg/(cm2∙h)。结果见图 3。
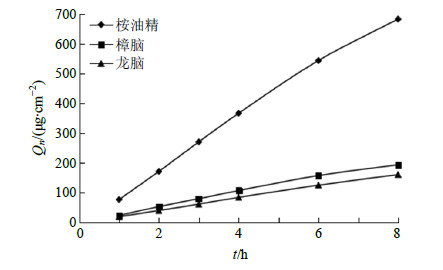 | 图 3 体外经皮渗透曲线 (n = 3)Fig.3 Cumulative penetration curves (n = 3) |
贴膏剂作为新型经皮肤给药制剂,不仅靶向性好,避免了肝脏的首过效应,提高了生物利用度,还可产生持久、恒定的血药浓度,而且贴剂外观较薄,携带、使用非常方便。艾叶油具有抗炎、抗菌、活血化瘀等活性,制成贴剂剂型用于治疗静脉炎非常适宜。在本实验中,先将艾叶油制备成乳剂,再载入基质制成贴膏剂,膏面平整,黏性适宜。《中国药典》2010年版对贴剂的黏附力测定做了要求,出于对贴剂的外观与使用舒适度的考虑,本实验在贴膏剂评价指标中加入了对内聚力与渗透性的评价,以更全面地反映贴剂的质量,保证生产应用的可行性。
水凝胶贴膏剂的制备工艺过程需严格控制,除了考察辅料的种类和用量,不同的辅料加入顺序也会影响基质的成型[12]。同时对辅料的添加方法也有要求,如骨架高分子材料若添加不当会造成溶解不完全,从而影响基质的均匀度。混匀基质时如用机械搅拌,应注意搅拌速率不宜过大,否则会使高分子材料的分子链发生断裂而使相对分子质量降低,导致基质黏性下降。另外,搅拌时间太短或太长也可能影响基质的延展性,导致难以涂布。
水凝胶贴膏剂的骨架为高分子材料,可以在一定程度上对药物起到缓释作用。《中国药典》2010年版二部附录规定透皮贴剂采用桨法测定释放度。也有研究者[13]采用改良的Franz扩散池装置考察基质的释放度。但由于水凝胶基质中高分子材料为水溶性,遇水溶胀,容易导致基质性能的改变,释放速率也会随之改变,所以上述的2种测定方法都无法准确得到水凝胶贴膏剂真实的释放数据。考虑到实际,药物透过皮肤环节才是药物释放的限速环节,所以本实验进行了体外透皮实验。艾叶油化学成分复杂,且各成分的量随产地及提取方式的不同有很大差异[14],其中桉油精、樟脑、龙脑是普遍量较高的3种主要活性成分。因此本实验将桉油精、樟脑、龙脑作为指标初步进行了体外透皮实验。实验表明3种指标成分在8 h内透皮曲线Qn-t线性良好,均以恒定速率透过皮肤,符合零级动力学模型,属于皮控型给药系统[15],其中桉油精透皮能力最强,樟脑次之,龙脑最弱。制备的凝胶贴膏剂具有较好释药性能,可以连续释放药物。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 黄学红, 谢元德, 朱婉萍, 等. 艾叶油治疗慢性支气管炎的实验研究[J]. 浙江中医杂志, 2006, 41(12): 734-735. |
| [3] | 吴朝霞, 夏天爽, 李 琦, 等. 同时蒸馏法提取艾叶挥发油及其抑菌性[J]. 食品研究与开发, 2010, 31(8): 19-22. |
| [4] | 何 文, 郭威希, 王 军. 现代药剂学 [M]. 武汉: 武汉大学出版社, 2012. |
| [5] | 崔福德. 药剂学 [M]. 第7版. 北京: 人民卫生出版社, 2011. |
| [6] | 马云淑, 刘月圆. 黄连解毒巴布剂的研制与体外透皮吸收研究[J]. 云南中医学院学报, 2002, 25(3): 31-33. |
| [7] | 任重远, 钱忠直, 王 平. 贴膏剂 (贴剂) 的粘着力及其测定方法[J]. 药物分析杂志, 2008, 28(1): 159-162. |
| [8] | 庄桂霞, 袁学勤, 胥 云. 颈舒巴布剂制备工艺研究[J]. 中医外治杂志, 2004, 13(3): 6-7. |
| [9] | 崔福德. 药剂学实验 [M]. 北京: 人民卫生出版社, 2005. |
| [10] | 刘吉金, 王晓炜, 黄服喜, 等. 气相色谱法测定菊花挥发油中桉油精、樟脑、龙脑、醋酸龙脑酯[J]. 中草药, 2006, 37(9): 1352-1353. |
| [11] | 苏健俊, 丁 野. GC测定感冒康喷雾剂中桉油精、樟脑、薄荷脑和龙脑的含量[J]. 中成药, 2006, 28(1): 39-41. |
| [12] | 徐 晖, 王绍宁, 谷 野. 巴布膏剂研制的一些问题[J]. 中医外治杂志, 2005, 14(6): 3-4. |
| [13] | 杜守颖, 陆 洋, 任晓慧. 风湿骨痛凝胶贴膏中青藤碱体外释放及透皮吸收研究[J]. 世界科学技术-中医药现代化, 2012, 14(3):1652-1655. |
| [14] | 江 丹, 洪宗国, 易 筠, 等. 不同品种艾叶挥发油的化学成分分析[J]. 中国医药生物技术, 2009, 4(5): 339-344. |
| [15] | 刘淑芝, 彭丽华, 郭春燕. 两种骨架材料的巴布剂基质体外释放度比[J]. 中医外治杂志, 2005, 14(3): 8-9. |
 2015, Vol. 46
2015, Vol. 46

