2. 江苏省中药高效给药系统工程技术研究中心, 江苏 南京 210023
2. Jiangsu Provincial TCM Engineering Technology Research Center of High Efficient Drug Delivery System (DDS), Nanjing 210023, China
双黄连口服液由金银花、连翘、黄芩3味药组成,具有清热解毒的功效[1, 2, 3],临床上主要用于治疗由上呼吸道感染引起的头痛、发热等,而发挥药效的物质基础主要为酚酸类、苯乙醇苷类和黄酮类成分[4, 5, 6, 7, 8, 9]。中药复方制剂组成复杂,杂质较多,成分的量差异较大,且双黄连口服液中不少有效成分是以同分异构体形式存在,HPLC-UV法干扰多,耗时长,只能通过测定几个指标性成分对双黄连口服液进行质量控制[10, 11]。超高效液相色谱-串联质谱联用技术(UPLC-MS/MS)具有专属性好、灵敏度高、快速等特点,可以排除复杂基质中相似化学成分的干扰,为中药及其复方制剂的多组分快速分析提供了强有力的技术支持[12, 13, 14, 15]。
本实验采用UPLC-MS/MS同时测定双黄连口服液中的17个指标性成分(6个酚酸类成分、3个苯乙醇苷类成分、8个黄酮类成分),分别主要来源于金银花、连翘和黄芩,兼顾全方,以期对该制剂的质量控制提供全面、快速、可靠的分析方法。
1 仪器与材料超高效液相色谱-TQD质谱联用仪,Acquity系统,MassLynx V4.1工作站,美国Waters公司;MicroCL 21R微量离心机,美国Thermo Scientific公司;微量移液器,上海科华实验系统有限公司;Milli-Q Synthesis 108超纯水仪,美国密理博公司;梅特勒-托利多XP6百万分之一天平,瑞士梅特勒-托利多公司。
连翘苷(批号110821-201514)、黄芩苷(批号110715-201318)、替硝唑(批号100336-200703)对照品购自中国食品药品检定研究院;连翘酯苷A(批号L-012-140730)、绿原酸(批号L-007-130130)、新绿原酸(批号X-014-130126)、隐绿原酸(批号Y-067-140116)、3,5-二咖啡酰奎宁酸(批号Y-069- 130126)、3,4-二咖啡酰奎宁酸(批号Y-068-150113)、咖啡酸(批号K-003-130501)、异连翘酯苷(批号Y-184-131108)、野黄芩苷(批号Y-012-140801)、汉黄芩苷(批号H-019-140729)、千层纸素A-7-O-β-D-葡萄糖苷(批号Q-046- 140111)、黄芩素(批号H-018-140729)、芦丁(批号L-001-130615)、汉黄芩素(批号H-029-140729)、氯霉素(批号2013091003)、千层纸素A(批号Q-020-140731)购自成都瑞芬思生物科技有限公司,质量分数均大于98%(采用色谱峰面积归一化法计算而得)。乙腈、甲醇,色谱纯,德国Merck公司;重蒸水,Milli-Q Synthesis 108超纯水仪制得。双黄连口服液,哈药集团三精制药股份有限公司提供,批号13020715、13020562、13021633、13022231、13060641,规格10 mL。
2 方法与结果 2.1 色谱条件色谱柱为Waters Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm);流动相为0.4%甲酸水溶液(A)-乙腈-甲醇(4∶1,B),体积流量0.4 mL/min,梯度洗脱程序为0~0.5 min,10%~11% B;0.5~0.75 min,11%~13% B;0.75~1.5 min,13%~15% B,1.5~2 min,15%~10% B;2~3 min,10%~30% B;3~6.2 min,30%~70% B;6.2~6.5 min,70%~10% B;6.5~7 min,10%~10% B。柱温40 ℃;进样体积5 μL。
2.2 质谱条件Waters三重四级杆串联质谱仪(TQD),离子化方式为电喷雾离子化(ESI),采用多反应监测离子扫描(MRM)模式;主要质谱参数:毛细管电压为3.5 kV,脱溶剂温度为400 ℃,脱溶剂气体积流量为800 L/h,锥孔气体积流量为50 L/h。各成分的部分质谱分析参数见表 1。双黄连口服液样品及混合对照品中17种成分及内标的提取离子流图见图 1。
| 表 1 17种成分的部分质谱分析参数 Table 1 MS parameters of 17 compounds |
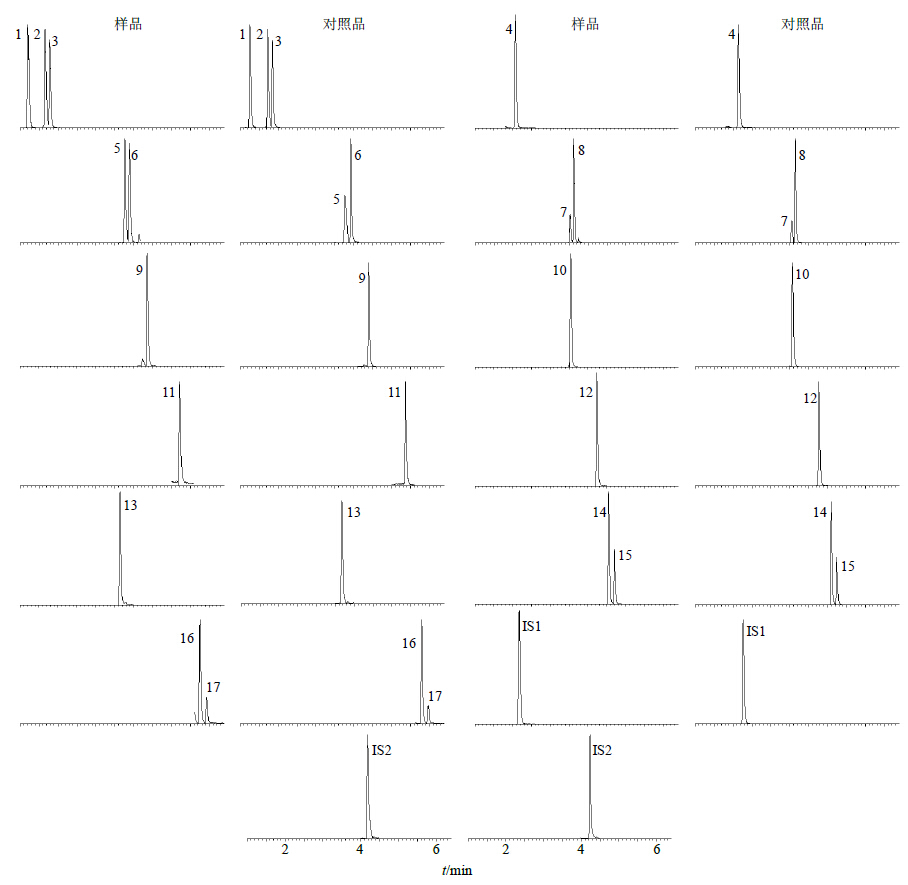 |
1-新绿原酸 2-绿原酸 3-隐绿原酸 4-咖啡酸 5-3,5-二咖啡酰奎宁酸 6-3,4-二咖啡酰奎宁酸 7-异连翘酯苷 8-连翘酯苷A 9-连翘苷 10-芦丁 11-黄芩素 12-黄芩苷 13-野黄芩苷 14-汉黄芩苷 15-千层纸素A-7-O-β-D-葡萄糖苷 16-汉黄芩素 17-千层纸素A IS1-替硝唑 IS2-氯霉素 1-neochlorogenic acid 2-chlorogenic acid 3-cryptochlorogenic acid 4-caffeic acid 5-3,5-dicaffeoylquinic acid 6-3,4-dicaffeoylquinic acid 7-isoforsythiaside 8-forsythoside A 9-forsythin 10-rutin 11-baicalein 12-baicalin 13-scutellarin 14-wogonoside 15-oroxylin A-7-O-glucuronide 16-wogonin 17-oroxylin A IS1-tinidazole IS2-chloramphenicol 图 1 双黄连口服液样品及混合对照品中17种成分及内标的提取离子流图 Fig.1 Extracting ion flow chart of 17 compounds and internal standards in Shuang-Huang-Lian Oral Liquid andmixed reference solution |
分别精密称取新绿原酸、绿原酸、隐绿原酸、咖啡酸、黄芩苷、黄芩素、汉黄芩苷、3,5-二咖啡酰奎宁酸、3,4-二咖啡酰奎宁酸、芦丁、汉黄芩素、千层纸素A-7-O-β-D-葡萄糖苷、千层纸素A、野黄芩苷、连翘酯苷A、异连翘酯苷、连翘苷对照品适量置于10 mL量瓶中,用甲醇定容至刻度,制得质量浓度分别为261、201、211、268、618、206、102、238、213、242、123、201、210、265、222、210及470 μg/mL的对照品储备液,4 ℃保存,备用。
2.4 内标溶液的制备分别精密称取替硝唑和氯霉素适量置于10 mL量瓶中,用甲醇定容至刻度,制得质量浓度分别为240 μg/mL和533 μg/mL的混合内标储备液,精密量取0.1 mL混合内标溶液至10 mL量瓶中,用甲醇定容至刻度,得含替硝唑和氯霉素质量浓度分别为2.40 μg/mL和5.33 μg/mL的混合内标溶液。
2.5 供试品溶液的制备[16, 17]精密量取1 mL双黄连口服液至100 mL量瓶中,用初始流动相乙腈-甲醇(4∶1)-0.4%甲酸水溶液(1∶9)稀释至刻度,摇匀后过0.22 μm滤膜,移取10 μL续滤液加入10 μL内标液和80 μL初始流动相,涡旋混匀,14 000 r/min离心10 min后取上清液,即得供试品溶液。
2.6 线性关系与定量限分别精密量取“2.3”项下对照品储备液适量,置于10 mL量瓶中,用初始流动相乙腈-甲醇(4∶ 1)-0.4%甲酸水溶液(1∶9)稀释至刻度,得系列质量浓度的混合对照品溶液,取10 μL混合对照品溶液加入10 μL内标液和80 μL初始流动相,涡旋混匀,14 000 r/min离心10 min后取上清液,按照“2.1”和“2.2”项下条件测定。以质量浓度为横坐标(X),对照品与内标峰面积比值为纵坐标(Y)进行线性回归,得各成分的回归方程、相关系数及线性范围,以信噪比为10确定各成分的定量限(LOQ),结果见表 2。结果表明,各成分在各自的线性范围内具有良好的线性关系。
| 表 2 17种化学成分的线性回归方程及定量限 Table 2 Linear regression equations and LOQs of 17 compounds |
取双黄连口服液(批号13021633),按“2.5”项下方法操作制备供试品溶液,按“2.1”和“2.2”项下条件测定,连续进样6次,以对照品与内标峰面积比值计算,17个成分的RSD分别为新绿原酸1.18%、绿原酸1.27%、隐绿原酸1.57%、咖啡酸0.45%、3,5-二咖啡酰奎宁酸1.25%、3,4-二咖啡酰奎宁酸1.20%、异连翘酯苷1.55%、连翘酯苷A 1.29%、连翘苷2.49%、芦丁1.09%、黄芩素1.37%、黄芩苷0.50%、野黄芩苷2.63%、汉黄芩苷0.67%、千层纸素A-7-O-β-D-葡萄糖苷1.69%、汉黄芩素2.16%、千层纸素A 0.64%,表明仪器精密度良好。
2.8 重复性考察取双黄连口服液(批号13021633),按“2.5”项下方法操作制备供试品溶液6份,按“2.1”和“2.2”项下条件测定,以对照品与内标峰面积比值计算,17个成分的RSD分别为新绿原酸1.23%、绿原酸1.41%、隐绿原酸1.96%、咖啡酸2.49%、3,5-二咖啡酰奎宁酸0.76%、3,4-二咖啡酰奎宁酸1.23%、异连翘酯苷0.67%、连翘酯苷A 1.48%、连翘苷0.27%、芦丁2.10%、黄芩素2.20%、黄芩苷2.12%、野黄芩苷0.71%、汉黄芩苷2.84%、千层纸素A-7-O-β-D-葡萄糖苷2.58%、汉黄芩素1.60%、千层纸素A 2.48%,表明该方法重复性良好。
2.9 稳定性试验取双黄连口服液(批号13021633),按“2.5”项下方法操作制备供试品溶液,分别于0、2、4、6、8、10、12 h按“2.1”和“2.2”项下条件测定,以对照品与内标峰面积比值计算,17个成分的RSD分别为新绿原酸2.10%、绿原酸2.00%、隐绿原酸1.62%、咖啡酸2.58%、3,5-二咖啡酰奎宁酸2.93%、3,4-二咖啡酰奎宁酸1.17%、异连翘酯苷1.48%、连翘酯苷A 1.08%、连翘苷1.67%、芦丁1.38%、黄芩素1.28%、黄芩苷1.61%、野黄芩苷2.13%、汉黄芩苷1.70%、千层纸素A-7-O-β-D-葡萄糖苷1.97%、汉黄芩素1.71%、千层纸素A 1.55%,表明供试品溶液室温放置12 h稳定。
2.10 加样回收率试验精密移取6份(批号13021633)1 mL双黄连口服液至100 mL量瓶中,并加入初始流动相至刻度得样品溶液,精密移取各对照品储备液适量置于10 mL量瓶中得混合对照品溶液,将样品溶液和混合对照品溶液按1∶1混合后精密移取10 μL加入10 μL内标液及80 μL初始流动相,涡旋混匀,14 000 r/min离心10 min后取上清液,即得供试品溶液,按“2.1”和“2.2”项下条件测定,计算各成分回收率,结果平均回收率及RSD分别为新绿原酸100.47%、1.11%,绿原酸96.72%、1.82%,隐绿原酸99.57%、1.24%,咖啡酸99.82%、2.69%,3,5-二咖啡酰奎宁酸102.42%、1.26%,3,4-二咖啡酰奎宁酸101.27%、2.85%,异连翘酯苷95.81%、1.25%,连翘酯苷A 101.85%、2.71%,连翘苷98.31%、2.84%,芦丁100.69%、2.30%,黄芩素101.04%、2.44%,黄芩苷97.21%、2.45%,野黄芩苷96.64%、0.91%,汉黄芩苷96.33%、1.26%,千层纸素A-7-O-β-D-葡萄糖苷99.41%、1.04%,汉黄芩素96.02%、2.51%,千层纸素A 100.70%、1.66%。
2.11 样品测定取5个批次的双黄连口服液,按照“2.5”项下方法处理,平行制得各组待测样品溶液3份,进样分析,经计算得到各成分的量,结果见表 3。
| 表 3 不同批次双黄连口服液中多组分的定量测定 Table 3 Quantitative determination of multi-components in different batches of Shuang-Huang-Lian Oral Liquid |
本实验考察了正、负离子扫描方式下待测物的响应强度,并进行比较,酚酸和黄酮类成分在正离子模式下 [M+H]+ 响应较高,而苯乙醇苷类成分在负离子模式下 [M-H]−响应较高(连翘苷为 [M+Na]+),因此采用正、负2种离子模式转换实现双黄连口服液中3类成分的同时测定,在流动相中加入不同浓度的甲酸溶液,结果发现0.4%的甲酸水溶液使正离子模式下的被测物响应增高,对负离子模式下的被测物影响较小,并且可以抑制色谱峰的拖尾,使同分异构体之间达到理想的分离效果;分别选择替硝唑和氯霉素作为正、负离子模式下的内标物,保留时间适当,峰形良好,实验过程中稳定可靠;本实验建立的同时测定双黄连口服液中酚酸类、黄酮类和苯乙醇苷类成分UPLC-MS/MS方法,17种成分在各自的质量浓度范围内,线性良好,分析时间较HPLC-UV法大大缩短,准确度、精密度、回收率、稳定性等均满足定量分析要求,并成功应用于5批双黄连口服液样品的多成分定量分析,为双黄连口服液的质量控制提供了一定的参考;所测5批样品中17种成分质量分数分别为新绿原酸782.68~1034.27 μg/mL、绿原酸786.35~1103.77 μg/mL、隐绿原酸898.00~1 238.94 μg/mL、咖啡酸82.85~115.17 μg/mL、3,5-二咖啡酰奎宁酸226.02~461.63 μg/mL、3,4-二咖啡酰奎宁酸191.59~404.21 μg/mL、异连翘酯苷243.62~298.51 μg/mL、连翘酯苷A 978.43~1 487.37 μg/mL、连翘苷351.97~435.82 μg/mL、芦丁41.19~75.65 μg/mL、黄芩素40.28~73.73 μg/mL、黄芩苷10 080.54~10 820.35 μg/mL、野黄芩苷40.88~50.51 μg/mL、汉黄芩苷187.73~204.85 μg/mL、千层纸素A-7-O-β-D-葡萄糖苷144.92~335.08 μg/mL、汉黄芩素9.30~25.58 μg/mL、千层纸素A 7.51~16.58 μg/mL,其中绿原酸、黄芩苷及连翘苷的量均符合《中国药典》2010年版双黄连口服液项下规定,且批间差异较小,而量较小的成分如汉黄芩素、千层纸素A批间的量差异较大。
| [1] | 梁业飞, 周有旺. 双黄连口服液解热抗炎作用的实验研究[J]. 临床合理用药, 2011, 4(9C): 51-52. |
| [2] | 莫红缨, 赖克方, 江永南, 等. 双黄连及其拆方抗呼吸道合胞病毒作用的药效学研究[J]. 中国中医基础医学杂志, 2005, 11(3): 194-196. |
| [3] | 莫红缨, 赖克方, 江永南, 等. 双黄连对呼吸道合胞病毒感染的气道上皮细胞炎症因子释放的影响[J]. 广州医学院学报, 2005, 33(2): 16-19. |
| [4] | 王建明, 赵楚文. 双黄连制剂中连翘苷含量与退热作用相关性研究[J]. 中国药师, 2010, 13(10): 1405-1407. |
| [5] | 于宜平, 张 艳, 李 红, 等. 黄芩苷对角叉菜胶致热大鼠解热作用的PK-PD模型研究[J]. 中草药, 2014, 45(4): 527-531. |
| [6] | 周 伟. 基于“银翘”药对的中药制剂生物有效性综合评价体系的构建与应用[D]. 南京: 南京中医药大学, 2014. |
| [7] | Ding Y, Dou J, Teng Z J, et al. Antiviral activity of baicalin against influenza A (H1N1/H3N2) virus in cell culture and in mice and its inhibition of neuraminidase[J]. Arch Virol, 2014, 159(12): 3269-3278. |
| [8] | Gao R, Lin Y N, Liang G, et al. Comparative pharmacokinetic study of chlorogenic acid after oral administration of Lonicerae Japonicae Flos and Shuang-Huang-Lian in normal and febrile rats[J]. Phytother Res, 2014, 28(1): 144-147. |
| [9] | Gao Y, Feng L, Cai R L, et al. Shuang-Huang-Lian exerts anti-inflammatory and anti-oxidative activities in lipopolysaccharide-stimulated murine alveolar macrophages[J]. Phytomedicine, 2014, 21(4): 461-469. |
| [10] | 杜英峰, 张兰桐, 靳怡然, 等. 多波长RP-HPLC法测定双黄连口服液中黄芩苷、绿原酸和连翘苷[J]. 中成药, 2009, 31(9): 1368-1371. |
| [11] | 徐大志, 张 荣, 刘启德, 等. HPLC波长转换法同时检测双黄连口服液中4种有效成分的含量[J]. 中药新药与临床药理, 2012, 23(1): 73-76. |
| [12] | 程 健, 狄留庆, 李俊松, 等. UPLC-MS/MS法同时测定通塞脉微丸中10种有效成分[J]. 中草药, 2014, 45(5): 659-664. |
| [13] | 吴 茵, 魏 欣, 张黎媛, 等. HPLC-MS/MS法同时测定参麦注射液7种主要有效成分[J]. 中草药, 2014, 45(18): 2625-2630. |
| [14] | 乔晓莉, 肖学凤, 周大铮. UPLC-MS/MS法同时测定注射用益气复脉 (冻干) 中13种成分[J]. 中草药, 2014, 45(23): 3402-3407. |
| [15] | 刘 姗, 杨 涛, 刘成海. UPLC-MS/MS法同时测定扶正化瘀胶囊中12种成分[J]. 中草药, 2014, 45(2): 214-219. |
| [16] | Zhou W, Liu S J, Ju W Z, et al. Simultaneous determination of phenolic acids by UPLC-MS/MS in rat plasma and its application in pharmacokinetic study after oral administration of Flos Lonicerae preparations[J]. J Pharm Biomed Anal, 2013, 86: 189-197. |
| [17] | He W, Liu G H, Cai H, et al. Integrated pharmacokinetics of five protober berine-type alkaloids in normal and insomnic rats after single and multiple oral administration of Jiao-Tai-Wan[J]. J Ethnopharmacol, 2014, 154(3): 635-644. |
 2015, Vol. 46
2015, Vol. 46


