2. 吉林医药学院附属医院 病理科, 吉林 吉林 132001
2. Department of Pathology, the Affiliated Hospital of Jilin Medical University, Jilin 132001, China
肝损伤是临床上常见的一类疾病,除遗传因素外,很多因素都可以诱发肝损伤。药物的护肝作用是现今研究的热点。萱草花Hemerocallis citrina Baroni,又名黄花菜,《本草纲目》中记载,有利湿热、宽胸隔、安五脏、治酒疸,安寐解郁等作用[1],中医用来治疗胸隔烦热、肝性黄疸、改善肝功能[2]。萱草花总黄酮(Hemerocallis citrina total flavonids,HCTF)是其主要成分之一。大量研究表明,HCTF具有护肝、抗抑郁、镇静催眠、抗氧化等药理作用[3, 4]。本实验在体内采用CCl4诱导小鼠肝氧化损伤模型,在体外采用H2O2诱导肝细胞损伤模型,观察肝组织病理变化及肝细胞损伤过程中肝X受体(LXR)α和脂肪酸合成酶(FAS)mRNA及蛋白表达变化,探讨HCTF对体内和体外肝氧化损伤的保护作用及其可能机制。
1 材料 1.1 实验动物昆明种小鼠65只,雄性,体质量(20±2)g,SPF级,长春市亿斯实验动物技术有限责任公司提供,合格证号SCXK(吉)-2010-0001。
1.2 细胞株人肝细胞株HL-7702,购于中国科学院上海细胞生物学研究所。
1.3 药品与试剂HCTF自制;CCl4,宜兴化学试剂三厂;博莱霉素、H2O2,美国Sigma公司;RPMI 1640培养基,美国Gibgo公司;胎牛血清、胰蛋白酶,杭州四季青生物工程材料有限公司;丙二醛(MDA)、超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)、丙氨酸转氨酶(ALT)、乳酸脱氢酶(LDH)、天冬氨酸转氨酶(AST)试剂盒,南京建成生物工程研究所;引物由上海生工生物工程有限公司提供。
1.4 主要仪器CM1900冰冻切片机,德国Leica公司;UV-6300分光光度计,上海美谱达仪器有限公司产品;DYY-11酶标仪,北京市六一仪器厂;3K30超速冷冻离心机,美国Sigma公司;双人超净工作台,上海基星生物科技有限公司;CO2培养箱,上海力申仪器有限公司;BX41TF倒置显微镜,日本Olympus公司。
2 方法 2.1 HCTF的制备萱草花药材,购于湖南祁阳,经吉林医药学院药学院雷均涛教授鉴定为萱草花Hemerocallis citrina Baroni。取粗粉适量,添加20倍量70%乙醇,加热、回流提取4 h,提取3次,冷冻干燥,得提取物粉末(得率0.94%),按照文献方法[5]测定,提取物粉末中含总黄酮5.6%。取提取物粉末加水溶解成10 g/L水溶液(总黄酮0.56 g/L),作为大孔吸附树脂纯化准备液。取预先处理好的AB-8大孔吸附树脂,按照径高比1∶6湿法装柱,取准备液6倍柱体积(BV)上样(2 mL/min),上样结束,用6 BV蒸馏水洗脱除杂(2 mL/min)。加入30%乙醇洗脱,收集3 BV洗脱液,洗脱液浓缩回收乙醇,冷冻干燥,得纯化粉末,相当于生药材28 g/g,纯化粉末含总黄酮26.5%。以蒸馏水配制成适宜质量浓度溶液,备用。
2.2 体内实验 2.2.1 分组及给药将65只昆明种小鼠按体质量随机分为5组,每组13只,分别为对照组,模型组,HCTF 25、50、100 mg/kg组。HCTF各组小鼠ig给药,给药体积20 mL/kg,每天1次,连续30 d。对照组和模型组ig等体积蒸馏水。
2.2.2 小鼠肝组织氧化损伤模型的制备除对照组外,各组末次给药2 h后,小鼠ip 3.2% CCl4的玉米油溶液5 mL/kg[6]。
2.2.3 小鼠肝组织GSH-Px、MDA水平和SOD活性检测模型制备后,禁食24 h,将小鼠脱颈椎处死,取肝组织,4 ℃生理盐水冲洗,加双蒸水冰浴匀浆,10%匀浆液离心,取上清。取10%肝组织匀浆,考马斯亮蓝法测定总蛋白浓度,按照试剂盒说明书操作,硝酸还原酶法检测GSH-Px水平[7],TBA法检测MDA水平[8],黄嘌呤氧化酶法检测SOD活性[7]。
2.2.4 小鼠肝组织HE染色[9]取小鼠肝组织3 mm×3 mm大小,10%甲醛溶液固定48 h。冲洗、脱水、透明、浸腊、包埋后,切8 μm厚度切片,脱蜡,进行HE染色,脱水封片后,用显微镜观察。
2.3 体外实验 2.3.1 HL-7702细胞体外培养及实验分组取96孔板接种5×104/mL对数生长期HL-7702细胞,无血清RPMI 1640培养液培养24 h。弃上清,对照组加入含15%胎牛血清的完全培养基;模型组加入H2O2 25 μmol/mL,给药组先加入2.5、5.0、10.0 μg/mL的HCTF作用细胞24 h,再加入终浓度为25 μmol/mL的H2O2培养12 h。
2.3.2 MTT实验将HL-7702细胞接种于96孔板,每孔5×103个细胞,接种150 μL,分组及加药处理同“2.3.1”项。加入MTT溶液(5 mg/mL)每孔20 μL,实验设4复孔,孵育4 h,弃上清,每孔加150 μL DMSO,微型震荡器震荡10 min。酶标仪检测490 nm波长各孔吸光度(A)值,考察HCTF对H2O2损伤HL-7702细胞的保护作用,结果用存活率表示。存活率=给药组A值/对照组A值。实验重复3次,取平均值。
2.3.3 HL-7702细胞上清液中GSH-Px、MDA水平和SOD活性检测取HL-7702细胞,以每孔5×104个细胞接种于24孔板,每孔150 uL体积,分组及加药处理同“2.3.1”项。各因素处理后收集细胞培养上清液,DTNB法检测GSH-Px水平,TBA法检测MDA水平,比色法检测细胞内SOD活性,分别按照试剂盒说明书操作。
2.3.4 HL-7702细胞上清液中ALT、LDH、AST水平检测细胞处理及分组给药同“2.3.3”项,ELISA法测定ALT、LDH和AST水平,按照试剂盒要求操作。
2.3.5 实时荧光定量PCR检测各组HL-7702细胞LXRα和FAS mRNA表达细胞处理及分组给药同“2.3.3”项。收集细胞,用TRIzol®试剂提取细胞的总RNA,将细胞总RNA分别稀释为1 μg/μL,以提取的总RNA为模板,反转录mRNA为cDNA。扩增引物根据Entrez Nucleotide database相关基因序列[10],应用Primer Premier 5引物设计软件设计,LXRα上游引物5’-CTGCCCAGCAACAGTGTAAC-3’,下游引物5’-CTGCTTTGGCAAAGTCTTCCC-3’;FAS上游引物5’-TTGCTAGATTATCGTCCAAAAGTGT-3’,下游引物5’-GCACTTGGTGTTGCTGGTGAGT-3’。以cDNA为模板,进行PCR扩增。电泳,凝胶分析系统进行灰度分析。
2.3.6 Western blotting检测各组HL-7702细胞LXRα和FAS蛋白表达根据文献方法[11],HL-7702细胞1×105个接种于6孔板,培养24 h,分组及加药处理同“2.3.1”项。收集细胞,提取蛋白,进行聚丙烯酰胺凝胶电泳分离,转至PVDF膜,分别加入LXRα、FAS一抗4 ℃孵育过夜,二抗室温孵育1 h,DAB显色。Imagel凝胶成像系统采集图像,SPSS 13.0软件定量分析条带净灰度值,并与内参GAPDH比较,计算比值,比较各组差异。
2.4 统计学分析数据以x±s表示,应用SPSS 13.0统计软件进行数据分析,组间计量比较采用t检验。
3 结果 3.1 对CCl4肝损伤小鼠GSH-Px、SOD活性和MDA水平的影响与对照组比较,模型组小鼠GSH-Px和SOD活性显著降低、MDA水平显著升高(P<0.05、0.01),说明CCl4引起了小鼠肝氧化损伤。HCTF 50、100 mg/kg剂量组小鼠肝组织的GSH-Px和SOD活性比模型组显著升高(P<0.05、0.01),HCTF各剂量组MDA水平与模型组比较显著降低(P<0.05、0.01)。提示,HCTF可以抑制CCl4肝损伤小鼠肝组织中脂质过氧化物的生成,提高肝组织抗氧化酶活性,对CCl4引起的肝损伤具有保护作用。结果见图 1。
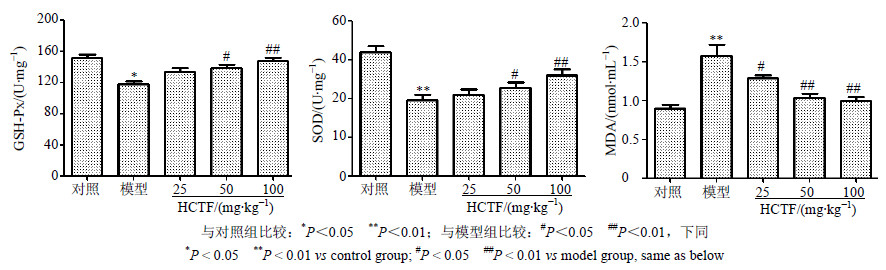 |
与对照组比较:*P<0.05 **P<0.01;与模型组比较:#P<0.05 ##P<0.01,下同 *P < 0.05 **P < 0.01 vs control group; #P < 0.05 ##P < 0.01 vs model group, same as below 图 1 HCTF对CCl4肝损伤小鼠肝组织GSH-Px、SOD活性和MDA水平的影响(x±s,n=13)Fig.1 Effect of HCTF onactivities of GSH-Px and SOD, and content of MDA in liver tissue of mice with liver injury induced(x±s,n=13) |
HE染色后,显微镜可见,对照组肝细胞整齐排列,胞浆染色均匀,无深染及空泡,细胞核均一未见融合;模型组肝细胞肿胀变形,出现空泡及大量血细胞,细胞核出现部分碎裂及溶解;HCTF 25 mg/kg组肝细胞结构基本完整,有部分细胞核出现深染或溶解;HCTF 50、100 mg/kg组肝细胞排列基本整齐,有个别空洞及深染,有极少细胞核结构改变。结果见图 2。
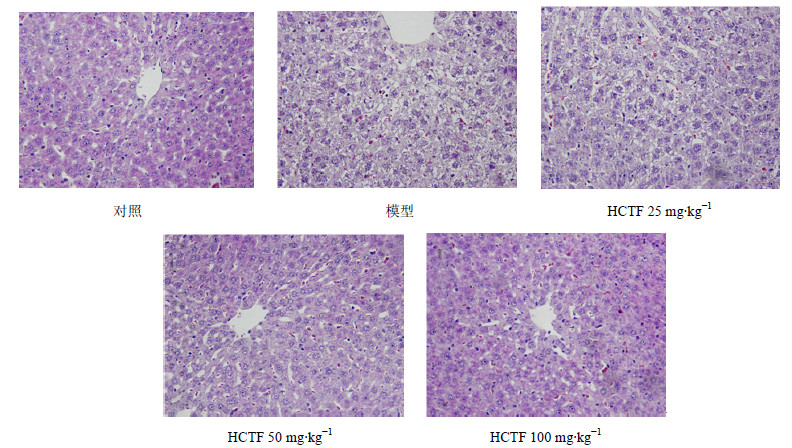 | 图 2 HCTF对CCl4肝损伤小鼠肝组织形态结构的影响Fig.2 Effect of HCTF on morphology of hepatocyte of mice with liver injury induced by CCl4 |
MTT测定结果显示,模型组细胞存活率降低,与对照组比较差异显著(P<0.01);与模型组比较,HCTF 5.0、10.0 μg/mL组细胞存活率显著提高(P<0.01)。结果见图 3。
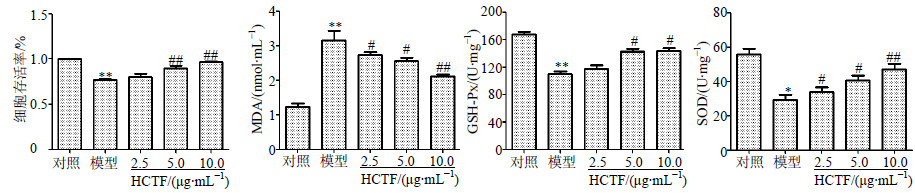 | 图 3 HCTF对HL-7702细胞存活率、MDA水平、GSH-Px和SOD活性的影响(x±s,n=5)Fig.3 Effect of HCTF on cell viability, content of MDA, and activities of GSH-Px and SOD in HL-7702 cells(x±s,n=5) |
与对照组比较,模型组细胞内MDA水平增加,不同质量浓度的HCTF孵育,可不同程度地抑制MDA水平增加,说明HCTF可抑制生物体的脂质过氧化反应,呈一定的剂量依赖性。与对照组比较,模型组GSH-Px活性显著降低(P<0.01),HCTF孵育后,各剂量组的GSH-Px活性均有所升高,2.5 μg/mL组与模型组比较差异不显著,而5.0、10.0 μg/mL组均差异显著(P<0.05),表明HCTF可以提高抗氧化酶活性。与模型组相比,HCTF各剂量组的SOD活性均显著提高(P<0.05、0.01),表明HCTF能提高HL-7702细胞SOD酶活性,并呈量效关系。以上结果提示,HCTF能够抑制H2O2对HL-7702细胞的氧化损伤。结果见图 3。
3.5 对H2O2损伤HL-7702细胞ALT、LDH、AST活性的影响H2O2损伤HL-7702细胞后,促进肝细胞内酶的释放,上清中ALT、LDH、AST活性明显增加,与对照组比较差异显著(P<0.05、0.01);HCTF 5.0、10.0 μg/mL组与模型组比较,上清中ALT、LDH、AST活性明显受到抑制(P<0.05、0.01)。提示HCTF可以改善H2O2引起的HL-7702细胞损伤。结果见图 4。
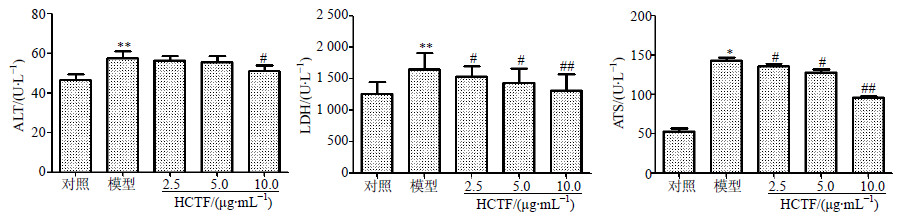 | 图 4 HCTF对HL-7702细胞ALT、LDH、AST活性的影响(x±s,n=5)Fig.4 Effects of HCTF on activities of ALT, LDH, and AST in HL-7702 cells(x±s,n=5) |
与对照组比较,模型组肝细胞LXRα、FAS mRNA表达明显增高(P<0.01),与模型组比较,HCTF 5.0、10.0 μg/mL组细胞中LXRα、FAS mRNA水平明显降低(P<0.05、0.01),提示HCTF可以下调H2O2诱导的HL-7702细胞的LXRα、FAS mRNA高表达。结果见图 5。
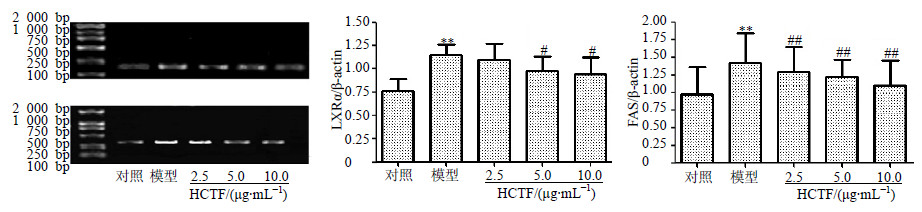 | 图 5 HL-7702细胞中LXRα和FAS mRNA表达(x±s,n=5)Fig.5 mRNA expression of LXRα and FAS in HL-7702 cells(x±s,n=5) |
与对照组比较,模型组LXRα、FAS蛋白表达增高,差异显著(P<0.01);与模型组比较,HCTF各组LXRα、FAS蛋白表达有不同程度降低,5.0、10.0 μg/mL组差异显著(P<0.05、0.01)。提示HCTF可以下调H2O2损伤肝细胞后引起的LXRα、FAS蛋白的高表达。结果见图 6。
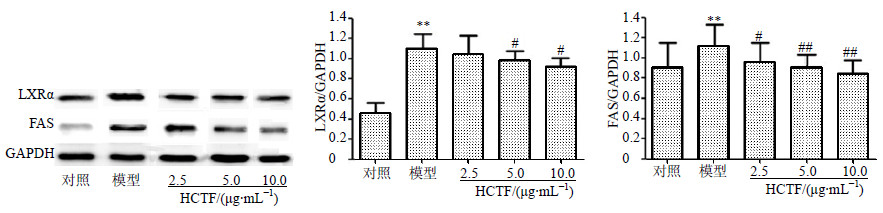 | 图 6 HL-7702细胞中LXRα和FAS蛋白表达(x±s,n=5)Fig.6 Protein expression of LXRα and FAS in HL-7702 cells(x±s,n=5) |
氧自由基(oxygen radical)与肝损伤密切相关,在酒精性肝损伤、肝纤维化等病变中,均观察到有
氧化应激的参与[12]。超氧阴离子、羟基等自由基可以间接或直接损伤肝细胞,使肝细胞膜中的脂质、蛋白质和DNA出现损伤,细胞变性坏死,引发肝疾病[13]。SOD活性及MDA水平可以反应机体抗氧化能力及脂质过氧化水平。体内实验结果显示,HCTF在CCl4引起的肝损伤小鼠模型中,明显提高了肝组织中抗氧化酶GSH-Px和SOD的活性,减少脂质过氧化物MDA的生成,减轻了CCl4对小鼠肝组织的损害。同时,体外实验结果也显示,HCTF各剂量组肝细胞的SOD活性比H2O2模型组均显著提高,不同程度地抑制MDA水平的增加,这些都表明HCTF对肝细胞具有保护作用,降低了H2O2引起的HL-7702细胞氧化损伤。综合结果提示,HCTF的肝保护作用可能是通过提高机体抗氧化能力,加强清除氧自由基能力,降低膜脂质过氧化水平而实现的。
ALT、LDH与AST是目前临床上反映肝细胞膜损伤的敏感指标[14],它们主要由肝细胞合成、分泌,ALT、LDH主要存在于肝细胞浆中,AST主要存在于肝细胞线粒体中,当炎症、氧化应激、免疫等因素使肝细胞受损时,肝细胞膜被破坏,细胞内的ALT等大量溢出,导致细胞外ALT、LDH、AST水平急剧升高。ALT、LDH、AST活性高低可以敏感地反映肝细胞损伤的程度[15]。本实验结果显示,与模型组相比,HCTF各剂量组肝细胞上清液中的ALT、LDH、AST水平降低,表明HCTF对肝细胞具有保护作用,降低了H2O2引起的HL-7702细胞氧化损伤程度。提示,HCTF的肝保护作用可能是通过提高机体抗氧化的能力,加强清除氧自由基能力,降低膜脂质过氧化水平而实现的。
有研究报道,LXR作为胆固醇代谢的感受器,可以调节细胞的增殖与分化及炎症反应[16, 17]。LXR有LXRα和LXRβ 2种亚型。LXRα是脂肪酸代谢的关键调控位点,主要表达在肝脏、脂肪组织、巨噬细胞中,在脂肪的生成、分泌、脂质过氧化等过程发挥作用[18]。FAS是脂肪合成的关键酶,LXRα直接活化FAS的转录,促进脂肪酸的合成及抑制脂酸的β氧化,从而引起三酰甘油在肝细胞内蓄积和活性氧(ROS)增加及炎症因子的生成,导致肝细胞的损伤[19]。LXR的信号传导通路参与了各种病理状态下肝功能的调节。本实验以H2O2诱导体外肝细胞氧化损伤模型,发现模型组肝细胞的LXRα、FAS mRNA及蛋白表达都高于对照组,这与相关报道相符[20, 21]。本研究显示HCTF可改善肝细胞HL-7702中LXRα、FAS的表达水平,综合HCTF在肝细胞氧化应激损伤过程中具有的保护作用,分析HCTF的抗氧化机制可能与减轻LXRα、FAS蛋白表达有关,这也是本研究下一步关注的内容之一。
综上所述,HCTF对肝细胞保护作用机制可能是通过下调LXRα、FAS mRNA基因和蛋白表达,抑制LXR信号传导通路的脂肪合成关键酶FAS的转录,加强了清除氧自由基的能力而实现的。
| [1] | 李时珍, 李炳文. 本草纲目彩图版 (上篇)[M]. 天津: 天津古籍出版社, 2006. |
| [2] | 郭冷秋, 张 颖, 张 博, 等. 萱草根及黄花菜的化学成分和药理作用研究进展[J]. 中华中医药学刊, 2013, 31(1): 74-76. |
| [3] | 王云锋, 赵丽晶, 徐 博, 等. 黄花菜的营养成分和生物活性研究进展[J]. 吉林医药学院学报, 2012, 2(33): 46-49. |
| [4] | 詹利生, 李贵荣, 李少旦, 等. 黄花菜中总黄酮的提取及其药理作用初步观察[J]. 南华大学学报: 医学版, 2005, 33(1): 112-114. |
| [5] | 周向军, 高义霞, 张 霞. 响应面法优化黄花菜总黄酮提取工艺[J]. 中国实验方剂学杂志, 2011, 17(16): 29-32. |
| [6] | 张自强, 刘玉梅, 朱雪敏, 等. 6-苄氨基嘌呤对四氯化碳致小鼠肝氧化损伤的保护作用[J]. 中国临床药理学杂志, 2015, 31(11): 928-931. |
| [7] | 茹 琴, 欧阳五庆, 张 黎. 激动素对小鼠急性四氯化碳肝损伤的保护作用[J]. 中国新药与临床杂志, 2007, 26(4): 263-267. |
| [8] | Diniz Y S, Fernandes A A H, Campos K E. Toxicity of hypercaloricdiet and monosodium glutamate: oxidative stress and metabolicshifting in hepatic tissue[J]. Food Chem Toxicol, 2004, 42(2): 313-319. |
| [9] | Ronco M T, Francés D E, Ingaramo P I, et al. Tumor necrosis factor alpha induced by Trypanosoma cruzi infection mediates inflammation and cell death in the liver of infected mice[J]. Cytokine, 2010, 49(1): 64-72. |
| [10] | 韩 莉, 杨钦河, 杨雪松, 等. 疏肝健脾方药对NASH大鼠Kupffer细胞NF-κB p65和IKKβ mRNA及蛋白表达的影响[J]. 中国病理生理杂志, 2013, 29(4): 641-646. |
| [11] | 魏 波, 杨钦河, 王文晶, 等疏肝健脾方对HASH大鼠肝组织IKK β mRNA和蛋白表达的影响[J]. 中国病理生理杂志, 2012, 28(8): 1448-1454. |
| [12] | Maki R G. Small is beautiful: insulin-like growth factors and their role in growth, development and cancer[J]. J Clin Oncol, 2010, 28(33): 4985-4995. |
| [13] | Velasco-Loyden G, Perez-Carreon J I, Aguero J F, et al. Prevention of in vitro hepatic stellate cells activation by the adenosine derivative compound IFC305[J]. Biochem Pharmacol, 2010, 80(11): 1690-1699. |
| [14] | 苑晓烨, 王 淼, 曹经琳, 等. 磷酸肌酸钠对离体大鼠肝脏 ALT/LDH指标的影响[J]. 河北医药, 2014, 36(24): 3696-3698. |
| [15] | 陈卫东. 注射用内给氧对肝缺血再灌注损伤兔血清ALT、AST、LDH和细胞凋亡的影响[J]. 中国现代医学杂志, 2008, 18(17): 2500-2502. |
| [16] | Wakade C, Kham M M, Desevilla L M, et al. Tamoxifen neuroprotection in cerebral ischemia involves attenuation of kinase activation and superoxide production and potentiation of mitochondrial superoxide dismutase[J]. Endocrinology, 2008, 149(1): 367-379. |
| [17] | Repa J J, Liang G, Ou J, et al. Regulation ofmouse sterol regulatory element-binding protein-1c gene (SREBP-1c) by oxysterol receptors, LXR alpha and LXR beta[J]. Genes Dev, 2000, 14(22): 2819-2830. |
| [18] | Adachi M, Brenner D A. High molecular weight adiponectin inhibits proliferation of hepatic stellate cells via activation of adenosine monophosphate-activated protein kinase[J]. Hepatology, 2008, 47(2): 677-685. |
| [19] | Vallim T, Salter A M. Regulation of hepatic gene expression by saturated fatty acids[J]. Prostaglandins Leukot Essent Fatty Acids, 2010, 82(4/6): 211-218. |
| [20] | 蔡 晶, 黄巧冰, 迟德彪. 五味子乙素对H2O2损伤人肝细胞Fas通路的影响[J]. 南方医科大学学报, 2012, 3(24): 583-592. |
| [21] | 卢绮萍, 吴在德, 李 东. Rxa对过氧化氢诱导人类肝细胞系Fas mRNA表达及Ca2+流变化影响的单细胞分析[J]. 中华实验外科杂志, 2000, 17(2): 155-157. |
 2015, Vol. 46
2015, Vol. 46


